CONSORT-CHM 2017 지침에 근거한 대한한의학회지 및 회원학회지에 투고된 경구투여 한약 중재를 활용한 무작위 배정 비교 임상 연구(RCT)의 양적, 질적 평가 연구
Abstract
Objectives:
This study aims to explore the current usage status of orally administered Korean herbal medicine in randomized controlled trials (RCTs) published in the Journal of Korean Medicine and member journals using the CONSORT-Chinese Herbal Medicine Formulas 2017 (CONSORT-CHM 2017) checklist.
Methods:
We searched the OASIS, RISS, and KMBASE archives as well as the websites of the Journal of Korean Medicine and 45 member journals to identify RCTs that used herbal interventions. Two independent researchers searched and categorized the RCTs and performed a quantitative evaluation by journal, study design, and target disease, as well as qualitative evaluation of the literature using CONSORT-CHM 2017.
Results:
After the search, 66 articles were selected. The quantitative evaluation resulted in 13 articles (19.6%) that were published in the Journal of Korean Medicine and 12 articles (18.1%) in the Journal of Internal Korean Medicine. In terms of study design, 62 articles (93.9%) were parallel, 4 articles (6%) were crossover, and 2-arm parallel study designs were the most common in 45 articles (68.2%). In terms of the study participants, physiological characteristics and mechanisms in healthy individuals were the most common in 21 studies (31.8%) and obesity in 9 studies (13.6%). In terms of assessing completeness in the CONSORT-CHM 2017 items, 29 articles were rated high, 31 were rated moderate, and 6 were rated low. Items 4a, 6a, and 7a had low reporting rates (≤ 30%), while items 2a, 2b, and 12a were completely reported in all studies.
Conclusion:
Future RCTs using orally administered Korean herbal medicine need to be reported completely, and the CONSORT-CHM 2017 checklist can be a helpful tool for this purpose.
Keywords: CONSORT-Chinese herbal medicine, qualitative research, randomized controlled trial, herbal medicine, journal of Korean medicine
I. 서 론
한의학은 전통의학으로서 고유의 이론 체계와 임상 경험에 기반을 둔 ‘경험중심의학’에 뿌리를 두고 발전해왔다. 그러나 1979년 영국의 역학자인 Archie Cochrane이 주장한 ‘근거중심의학(Evidence Based Medicine, EBM)’은 기존 ‘경험중심의학’이 주류를 이루던 의학계의 새로운 패러다임이 되었다 1. 이에 한의학계에서도 근거의 기반을 다지기 위한 임상연구의 중요성이 더욱 증가하였고, 그 중에서도 무작위 배정 비교 임상 시험(Randomized Controlled Clinical Trial, RCT)은 의약품 및 의료기술의 효능을 검증하고, 과학적 증거를 제시하는 가장 좋은 연구 방법이므로 그 중요성이 특히 강조되고 있다. 그러나 RCT라고 해서 반드시 근거 수준이 높은 것은 아닌데, 적절한 방법을 통해 수행된 RCT만이 치료효과에 대한 정확한 추정, 높은 재현성, 올바른 결론을 이끌어낼 수 있기 때문이다. 따라서, 의약품 및 의료기술의 유효성을 입증하기 위해서는 임상시험을 체계적으로 설계하여 치료효과를 검증해야 한다. 부적절하게 수행 및 설계된 RCT는 비뚤림을 유발할 수 있으므로, 적절한 연구 설계와 결과 기술은 전체 연구의 질을 결정하는 중요한 요인이 된다 2. RCT 연구결과보고의 질을 향상시키기 위하여 널리 사용되는 대표적인 지침은 EQUATOR (Enhancing the QUAlity and Transparency Of health Research) network에서 제공하는 CONSORT(Consolidated Standards of Reporting Trials) statement인데, 1996년 발표된 후 여러 차례의 수정을 거쳐 오늘날 의학 및 보건 계열에서 널리 사용되고 있다 3. 그러나 기존의 CONSORT 지침은 서양의학에 초점이 맞춰진 탓에 한의학 고유의 이론 체계의 특성을 충분히 반영하지 못한다 4. 이를 보완하고자 CONSORT-CHM Formula 2017 group에서 CONSORT에 부가적으로 한약연구관련 특수사항을 정리한 CONSORT-Chinese Herbal Medicine formulas(CONSORT-CHM)을 개발하였다. 이는 CONSORT와 같이 독립된 보고 가이드라인이 아닌 extension의 일종으로, 2006년 처음 개발된 CONSORT-CHM은 이후 2017년 기존 CONSORT 지침의 25가지 항목 중 7가지 항목을 더 세밀하게 다듬고, 한약 사용의 위해에 대한 설명 및 예시를 추가하는 등의 변화를 거쳐 개정되었다 4. 이를 통해 한약 중재를 활용한 RCT보고의 질을 평가할 수 있는 기반을 마련하였으나, 아직 한국어판은 개발되지 않았다. 국내 한의학 분야에서 CONSORT 및 그 확충안인 침 임상연구에서 중재 보고를 위한 표준(Revised Standards for Reporting Interventions in Clinical Trials of Acupuncture, STRICTA)을 활용하여 RCT의 질을 평가한 연구는 존재하지만 1,3,5-8, 아직까지 CONSORT-CHM 2017을 활용한 연구는 보고되지 않았다. 이에 본 연구는 2017년 갱신된 CONSORT-CHM 2017을 통해 2023년 3월까지 대한한의학회지 및 45개의 회원학회지에 게재된 경구투여 한약 중재를 활용한 RCT보고의 질을 평가하였다. 이를 통해 대한한의학회지 및 회원학회지에 보고된 RCT 문헌의 현황을 파악하고, 향후 개선 방향을 제안하여 한의학 분야에서 보다 더 높은 수준의 RCT 연구가 이뤄질 수 있도록 보탬이 되고자 한다.
II. 대상 및 방법
1. 연구대상 및 문헌 검색
2023년 3월까지 대한한의학회지 및 45개의 회원학회지에 투고된 경구투여 한약 중재를 활용한 RCT 문헌을 대상으로 하였다. CONSORT-CHM 2017을 통해 보고의 질을 평가했으며, 국내 한의학계의 한약중재 경구투여 RCT 연구보고가 신뢰할 수 있는 과정을 통해 수행되는지를 평가하고자 하였다. 전통의학정보포털(Oriental medicine Advanced Searching Integrated System, OASIS), 학술연구정보서비스(Research Information Sharing Service, RISS), 한국의학논문데이터베이스(Korean Medical Database, KMBASE)에 2023년 3월까지 수록된 문헌을 대상으로 검색어 [제목] (’무작위’, ‘대조군’, ‘임상 AND 무작위’, ‘Random’, ‘Randomized’, ‘Control’, ‘RCT’) [통합검색] (’무작위’, ‘대조군’, ‘Random’, ‘Control’) [키워드] (’무작위’, ‘대조군’, ‘Random’, ‘Control’)를 검색하였으며, 선행연구를 참고하여 누락된 문헌이 없도록 대한한의학회 및 모든 회원학회 홈페이지 자료실을 통해 동일한 검색어를 활용해 수기로 검색, 대조하였다. 대한한의학회 홈페이지에 회원학회 홈페이지 URL(Uniform Resource Locator, URL)이 수록되지 않은 경우 구글(https:// www.google.com) 검색을 통해 홈페이지를 검색했으며, 홈페이지가 없는 경우 dbpia(https://www.dbpia. co.kr/), 한국학술지인용색인(Korea Citation Index, KCI)를 활용해 문헌을 재검색하였다. ‘herbal medicine’, ‘tang’ 등 한약을 뜻하는 검색어는 검색결과가 지나치게 방대하고, 특허 처방 및 다른 제형의 결과를 포괄하지 못하여 검색어에서 배제하였다.
2. RCT 문헌의 선정 기준
사람이 대상이고, 실험군과 대조군을 설정하며, 경구투여 한약 중재가 개입되었고, 전향적인 연구 설계를 가지며, 군 배정이 무작위로 이루어진 문헌만을 분석 대상으로 선정하였다. 본초 단방 혹은 성분 추출물을 이용한 문헌은 그 본초 또는 성분이 본초학 공통 교재 9에 기재되어 있는 것일 경우에만 포함하였다. 두 명의 연구자(SM, JJ)가 독립적으로 제목과 초록을 검토해 1차로 문헌을 선별하였고, 이후 원문 전체를 확인하여 최종 평가 대상 문헌을 선별하였다. 선별한 결과가 일치하지 않은 경우 두 연구자가 충분한 논의를 거쳐 결정하였고, 합의에 이르지 못하는 경우 제3의 연구자(JL)와 논의하여 결론을 도출하였다.
3. 제외 기준
사람이 대상이 아닌 경우, 무작위 배정이 안 된 대조 임상연구, 대조연구가 아닌 경우(Case report, Case series, 후향적 연구, protocol, 중간보고 등), 중재가 경구투여 한약이 아닌 경우(외용제, 샴푸, 약침, 침 등), 투고된 학회지가 대한한의학회지 및 회원학회지가 아닌 경우 제외하였다.
4. RCT의 양적 평가
분류된 RCT 문헌을 연도별, 학회지별로 분류하여 표로 나타내었으며( Table 1) 해당 문헌들을 설계 형태, 대조군에 적용한 중재의 종류, 문헌에서 다루고 있는 질환으로 분류하여 나타내었다.
Table 1
Numbers of Randomized Controlled Clinical Trials according to Journal
|
Characteristics |
n (%) |
|
Journal |
66 (100.0) |
|
|
Journal of Korean Medicine |
13 (19.6) |
|
The Journal of Korean Oriental Internal Medicine |
12 (18.1) |
|
Korean Journal of Oriental Physiology & Pathology |
8 (12.1) |
|
The Korea Journal of Herbology |
7 (10.6) |
|
Journal of Korean Medicine Rehabilitation |
5 (7.5) |
|
Journal of Korean Medicine for Obesity Research |
5 (7.5) |
|
The Journal of Oriental Obstetrics & Gynecology |
4 (6.0) |
|
The Korean Society of Oriental Neuropsychiatry |
3 (4.5) |
|
The Journal of Korean Oriental Ophthalmology & Otorhinolaryngology & Dermatology |
2 (3.0) |
|
Journal of Sasang Constitutional Medicine |
2 (3.0) |
|
Journal of Acupuncture Research |
2 (3.0) |
|
The Institute of Korean HYUNG SANG Medicine |
1 (1.5) |
|
The Journal of the Society of Stroke on Korean Medicine |
1 (1.5) |
|
Society of Preventive Korean Medicine |
1 (1.5) |
5. RCT 문헌 보고의 질 평가 도구 및 방법
CONSORT-CHM 2017을 사용하여 RCT 문헌의 보고의 질을 평가하였다. 기존 CONSORT와 비교했을 때 CONSORT-CHM의 주요한 변경사항은 Table 2과 같다. 총 38개의 항목을 평가하였으며, 선행연구를 참조하여 지침에 맞게 보고된 경우 ‘O’, 보고가 되지 않은 경우 ‘X’, 불충분하게 보고된 경우 ‘△’, 적용할 수 없거나 해당되지 않는 경우 ‘not applicable(N/A)’로 평가하였다. 또한 원문에 ‘If any, If applicable’로 기재된 항목은 해당 기준을 충족하지 않거나 지침과 맞게 보고되지 않아도 ‘X’로 평가하지 않고 ‘N/A’로 평가하였다 4. 하나의 항목이 여러 가지의 문항으로 구성되어 있는 5b 항목(Intervention)의 경우, 각 세부 사항들의 비중을 동등하게 나눈 후 50% 미만을 충족한 경우 ‘X’, 50~80%를 충족한 경우 ‘△’, 80% 이상 충족한 경우 ‘O’로 평가하였다 10.
Table 2
Consolidated Standards of Reporting Trials Extensions for Chinese Herbal Medicine Formulas 2017 (CONSORT-CHM 2017) Checklist
|
Section/ topic |
Item number |
Standard CONSORT checklist item |
Extension for CHM formulas |
|
TITLE, ABSTRACT, and KEYWORDS |
|
|
Title and Abstract |
1a |
Identification as a randomized trial in the title |
Statement of whether the trial targets a TCM* Pattern, a Western medicine-defined disease, or a Western medicine-defined disease with a specific TCM Pattern, if applicable |
|
|
1b |
Structured summary of trial design, methods, results, and conclusions (for specific guidance, see CONSORT for abstracts [26, 27]) |
Illustration of the name and form of the formula used, and the TCM Pattern applied, if applicable |
|
|
1c |
|
Determination of appropriate keywords, including “Chinese herbal medicine formula” and “randomized controlled trial” |
|
|
INTRODUCTION |
|
|
Background and Objectives |
2a |
Scientific background and explanation of rationale |
Statement with biomedical science approaches and/or TCM approaches |
|
|
2b |
Specific objectives or hypotheses |
Statement of whether the formula targets a Western medicine-defined disease, a TCM Pattern, or a Western medicine-defined disease with a specific TCM Pattern |
|
|
METHODS |
|
|
Trial design |
3a |
Description of trial design (such as parallel, factorial), including allocation ratio |
|
|
|
3b |
Important changes to methods after trial commencement (such as eligibility criteria),with reasons |
|
|
|
Participants |
4a |
Eligibility criteria for participants |
Statement of whether participants with a specific TCM Pattern were recruited, in terms of 1) diagnostic criteria and
2) inclusion and exclusion criteria. All criteria used should be universally recognized, or reference given to where detailed explanation can be found. |
|
|
4b |
Settings and locations where the data were collected |
|
|
|
Interventions |
5 |
The interventions for each group with sufficient details to allow replication, including how and when they were actually administered |
Description (s) for different types of formulas should include the following: 5a. For fixed CHM formulas
1. Name, source, and dosage form (e.g., decoctions, granules, powders)
2. Name, source, processing method, and dosage of each medical substance. Names of substances should be presented in at least 2 languages: Chinese (Pinyin), Latin, or English. Names of the parts of the substances used should be specified.
3. Authentication method of each ingredient and how, when, where, and by whom it was conducted; statement of whether any voucher specimen was retained, and if so, where they were kept and whether they are accessible
4. Principles, rationale, and interpretation of forming the formula
5. Reference (s) as to the efficacy of the formula, if any
6. Pharmacologic study results of the formula, if any
7. Production method of the formula, if any
8. Quality control of each ingredient and of the product of the formula, if any. This would include any quantitative and/or qualitative testing method (s); when, where, how, and by whom these tests were conducted; whether the original data and samples were kept, and, if so, whether they are accessible.
9. Safety assessment of the formula, including tests for heavy metals and toxic elements, pesticide residues, microbial limit, and acute/chronic toxicity, if any. If yes, it should be stated when, where, how, and by whom these tests were conducted; if the original data and samples were kept; and, if so, whether they are accessible.
10. Dosage of the formula, and how the dosage was determined
11. Administration route (e.g., oral, external)
5b. For individualized CHM formulas
1. See recommendations 5a 1-11
2. Additional information: how, when, and by whom the formula was modified
5c. For patent proprietary CHM formulas
1. Reference to publicly available materials, such as pharmacopeia, for the details about the composition, dosage, efficacy, safety, and quality control of the formula 2. Illustration of the details of the formula, namely
1) the proprietary product name (i.e., brand name),
2) name of manufacturer,
3) lot number,
4) production date and expiry date,
5) name and percentage of added materials, and
6) whether any additional quality control measures were conducted 3. Statement of whether the patent proprietary formula used in the trial is for a condition that is identical to the publicly available reference 5d. Control groups Placebo control 1. Name and amount of each ingredient 2. Description of the similarity of placebo with the intervention (e.g.,color, smell, taste, appearance, packaging)
3. Quality control and safety assessment, if any 4. Administration route, regimen, and dosage 5. Production information: where, when, how, and by whom the placebo was produced
Active control
1. If a CHM formula was used, see recommendations 5a-5c
2. If a chemical drug was used, see item 5 of the CONSORT Statement (24) |
|
|
Outcomes |
6a |
Completely defined, prespecified primary and secondary outcome measures, including how and when they were assessed |
Illustration of outcome measures with Pattern in detail |
|
|
6b |
Any changes to trial outcomes after the trial commenced, with reasons |
|
|
|
Sample size |
7a |
How sample size was determined |
|
|
|
7b |
When applicable, explanation of any interim analyses and stopping guidelines |
|
|
|
Randomization Sequence generation |
8a |
Method used to generate the random allocation sequence |
|
|
|
8b |
Type of randomization; details of any restriction (such as blocking and block size) |
|
|
|
Allocation concealment mechanism |
9 |
Mechanism used to implement the random allocation sequence (such as sequentially numbered containers), describing any steps taken to conceal the sequence until interventions were assigned |
|
|
|
Implementation |
10 |
Who generated the random allocation sequence, who enrolled participants, and who assigned participants to interventions |
|
|
|
Blinding |
11a |
If done, who was blinded after assignment to interventions (for example, participants, care providers, those assessing outcomes) and how |
|
|
|
11b |
If relevant, description of the similarity of interventions |
|
|
|
Statistical methods |
12a |
Statistical methods used to compare groups for primary and secondary outcomes |
|
|
|
12b |
Methods for additional analyses, such as subgroup analyses and adjusted analyses |
|
|
|
RESULTS |
|
|
Participant flow (a diagram is strongly recommended) |
13a |
For each group, the numbers of participants who were randomly assigned, received intended treatment, and were analyzed for the primary outcome |
|
|
|
13b |
For each group, losses and exclusions after randomization, together with reasons |
|
|
|
Recruitment |
14a |
Dates defining the periods of recruitment and follow-up |
|
|
|
14b |
Why the trial ended or was stopped |
|
|
|
Baseline data |
15 |
A table showing baseline demographic and clinical characteristics for each group |
|
|
|
Numbers analyzed |
16 |
For each group, number of participants (denominator) included in each analysis and whether the analysis was by original assigned groups |
|
|
|
Outcomes and estimation |
17a |
For each primary and secondary outcome, results for each group, and the estimated effect size and its precision (such as 95% confidence interval) |
|
|
|
17b |
For binary outcomes, presentation of both absolute and relative effect sizes is recommended |
|
|
|
Ancillary analyses |
18 |
Results of any other analyses performed, including subgroup analyses and adjusted analyses, distinguishing prespecified from exploratory |
|
|
|
Harms |
19 |
All important harms or unintended effects in each group (for specific guidance, see CONSORT for harms [28]) |
(There is no extension for this item) |
|
|
DISCUSSION |
|
|
Limitations |
20 |
Trial limitations; addressing sources of potential bias; imprecision; and, if relevant, multiplicity of analyses |
|
|
|
Generalizability |
21 |
Generalizability (external validity, applicability) of the trial findings |
Discussion of how the formula works on different TCM Patterns or diseases |
|
|
Interpretation |
22 |
Interpretation consistent with results, balancing benefits and harms, and considering other relevant evidence |
Interpretation with TCM theory |
|
|
OTHER INFORMATION |
|
|
Registration |
23 |
Registration number and name of trial registry |
|
|
|
Protocol |
24 |
Where the full trial protocol can be accessed, if available |
|
|
|
Funding |
25 |
Sources of funding and other support (such as supply of drugs), role of funders |
|
아직 국내에 CONSORT-CHM을 활용한 질 평가 연구가 보고되지 않은 점, 개정판이 비교적 최근인 2017년에 발간되어 아직 CONSORT-CHM 2017을 이용하여 문헌을 분석한 연구가 많지 않다는 점을 고려하여, 평가 항목에 해당하는 내용이 반드시 문헌의 해당 section에 포함되어있지 않더라도 보고한 것으로 간주하여 평가하였다. 예를 들어, 13a 항목(Participant flow)에 해당하는 내용이 문헌의 연구 결과(Results) 부분이 아닌 방법(Methods)에 기재되어 있더라도, 이를 보고한 것으로 간주하여 ‘O’로 평가하였다( Table 2).
6. 질 평가 결과의 합성 및 분석
문헌의 질적 수준 평가는 각 대상 문헌별 보고율과 CONSORT-CHM 2017 세부 항목별 보고율로 나누어 평가하였으며, ‘N/A’로 평가한 항목은 보고율 산정 시 분모에서 제외하였다. CONSORT-CHM 2017을 활용한 Zuanji Liang 등의 선행연구 10를 참고하여 문헌의 보고율을 ‘O’, ‘△’, ‘X’로 평가하였고, 이를 정량화시켜 한눈에 나타내기 위해 점수로 환산하였다. ‘O’는 1점, ‘X’는 0점, ‘△’는 0.5점으로 환산하였으며, 총 38개 항목, 38점 만점을 기준으로 점수를 합계하여 보고된 항목의 총점의 비율을 환산하였다. PRISMA 2020 지침을 활용해 한방재활의학과학회지에 투고된 체계적 문헌고찰의 보고의 질을 평가한 나 등 11의 연구를 참조해 총점의 비율이 50% 미만은 ‘Low(L)’, 50% 이상 70% 미만은 ‘Moderate(M)’, 70% 이상은 ‘High(H)’로 평가하였으며, 소수점 두 자릿수에서 버림하여 표기하였다.
III. 결 과
1. 문헌 검색 및 선정 결과
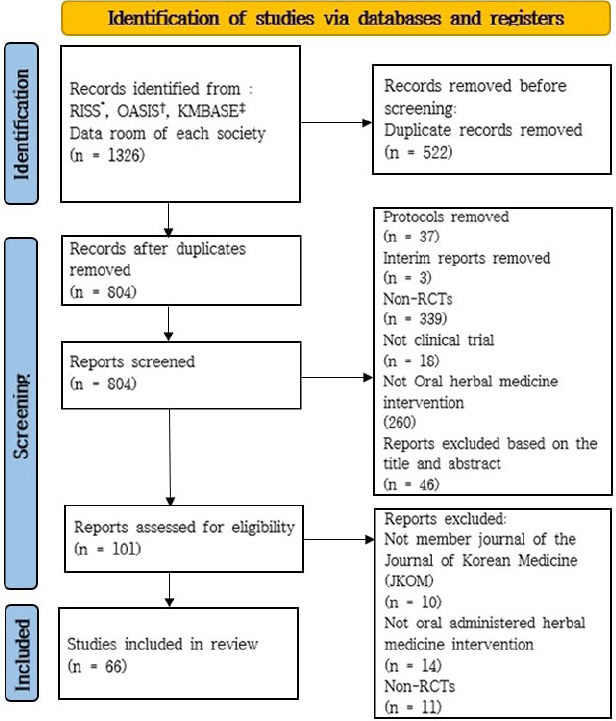
전통의학정보포털(Oriental medicine Advanced Searching Integrated System, OASIS), 학술연구정보서비스(Research Information Sharing Service, RISS), 한국의학논문데이터베이스(Korean Medical Database, KMBASE)와 대한한의학회 및 회원학회 홈페이지 자료실을 통해 2023년 3월까지의 경구투여 한약중재를 활용한 RCT 문헌을 검색한 결과 총 1,326편의 문헌이 검색되었다. 중복된 문헌 522편을 제외하고, 남은 804편의 문헌에서 프로토콜 37편을 제외하였고, 중간보고 3편, 증례보고 등 RCT문헌이 아닌 339편, 사람을 대상으로 하지 않은 문헌 18편, 경구투여 한약중재가 아닌 중재를 활용한 260편을 제외한 후, 제목과 초록을 통해 46편을 제외하였다. 1차선별 후 남은 101편의 전문을 확인하여 대한한의학회지 및 회원학회지에 투고된 문헌이 아닌 10편, 경구투여 한약중재가 아닌 14편, RCT 문헌이 아닌 11편을 제외하여 최종적으로 66편 12-77을 분석대상으로 선정하였다( Fig. 1).
Fig. 1
Flow diagram of study selection.
*RISS : Research Information Sharing Service
†OASIS : Oriental medicine Advanced Searching Integrated System
‡KMBASE : Korean Medical Database
2. 양적 분석
처음 경구투여 한약중재를 활용한 RCT가 발표된 것은 1998년도이며, 이후 1999년, 2000년, 2001년에는 발표되지 않다가 2002년부터 매해 꾸준히 발표되기 시작하였다. 한 해 평균 2.8편의 RCT 문헌이 발표되었으며, 가장 많은 수의 문헌이 발표된 해는 9편(13.6%)의 문헌이 발표된 2005년이었다( Fig. 2). 영문으로 작성된 문헌이 6편(9%), 국문으로 작성된 문헌이 60편(90.9%)이었으며, 학회지별 발간된 문헌 수는 대한한의학회지가 13편(19.6%)으로 가장 많았고, 대한한방내과학회지가 12편(18.1%)으로 뒤를 이었다. 포함된 66편의 RCT 중 연구 설계는 평행설계가 62편(93.9%), 교차 설계가 4편(6%)이었으며, 2-arm parallel study design이 45편(68.2%)으로 가장 많았다. 연구에 포함된 환자 수는 연구 당 약 75.2명(최소 10명~최대 219명), arm 당 약 31.6명(최소 5명~최대 100명)으로 나타났다. 실험군-대조군 설정에 있어서는 해당 중재와 함께 위약을 활용한 연구가 50편(75.7%)으로 가장 많았다( Table 3). 문헌의 주제로는 건강인의 생리적 특성 및 기전을 대상으로 한 연구가 21편(31.8%)으로 가장 많았고, 비만이 9편(13.6%)으로 그 뒤를 이었다. 그 외에는 근골격계 질환이 5편(7.5%), 순환기계 질환이 3편(4.5%) 등이 분포했다( Table 4).
Fig. 2
Number of randomized controlled clinical trials according to publication year. 
Table 3
Characteristics of Randomized Controlled Clinical Trials in Journal of Korean Medicine and Member Journals
|
Characteristics |
n (%) |
|
Written language |
66 (100.0) |
|
Korean |
60 (90.9) |
|
English |
6 (9.0) |
|
|
Study design |
66 (100.0) |
|
Parallel, 2-arm |
45 (68.1) |
|
Parallel, 3-arm |
12 (18.1) |
|
Parallel, 4-arm |
2 (3.0) |
|
Parallel, 5-arm |
3 (4.5) |
|
Crossover, 2-arm |
4 (6.0) |
|
|
Intervention vs. Control design |
66 (100.0) |
|
Parallel design |
62 (93.9) |
|
Main intervention vs. no treatment |
2 (3.0) |
|
Main intervention vs. placebo control |
36 (54.5) |
|
Main intervention vs. different types of same main intervention |
1 (1.5) |
|
Main intervention vs. active control (Korean medicine) |
3 (4.5) |
|
Main intervention vs. active control (Western medicine) |
1 (1.5) |
|
Main intervention vs. active control (health functional food) |
1 (1.5) |
|
Main intervention+other intervention vs. other intervention alone |
1 (1.5) |
|
Main intervention vs. other main intervention vs. placebo control |
5 (7.5) |
|
Main intervention vs. other main intervention vs. no treatment |
1 (1.5) |
|
Main intervention vs. according to dose vs placebo control |
2 (3.0) |
|
Main intervention vs. according to dose vs. according to dose |
1 (1.5) |
|
Main intervention vs. main intervention vs. main intervention vs. main intervention |
2 (3.0) |
|
Main intervention vs. main intervention vs. main intervention vs. main intervention vs. placebo control |
3 (4.5) |
|
Crossover design |
4 (6.0) |
|
Main intervention vs. no treatment |
2 (3.0) |
|
Main intervention vs. different types of same main intervention |
1 (1.5) |
|
Main intervention vs. placebo control |
1 (1.5) |
Table 4
Categories of Medical Conditions of Randomized Controlled Clinical Trials in Journal of Korean Medicine and Member Journals
|
Medical conditions |
n (%) |
|
Obesity |
9 (13.6) |
|
|
Circulatory disease |
7 (10.6) |
|
Post-stroke xerostomia |
1 (1.5) |
|
Post-stroke depression |
2 (3.0) |
|
Post-reperfusion syndrome of Arteriosclerotic Occlusive disease |
1 (1.5) |
|
Hypertension |
2 (3.0) |
|
Hyperlipidemia |
1 (1.5) |
|
|
Musculoskeletal Disease |
5 (7.5) |
|
Low back pain |
1 (1.5) |
|
Knee osteoarthritis |
4 (6.0) |
|
|
Psychologic disease |
3 (4.5) |
|
Amnesia |
1 (1.5) |
|
Hwa-byung |
2 (3.0) |
|
|
Gynecological disease |
2 (3.0) |
|
Primary dysmenorrhea |
1 (1.5) |
|
Climacteric syndrome |
1 (1.5) |
|
|
Liver dysfunction |
2 (3.0) |
|
|
Diabetes mellitus |
2 (3.0) |
|
|
Atopic dermatitis |
2 (3.0) |
|
|
Functional dyspepsia |
2 (3.0) |
|
|
Common cold |
2 (3.0) |
|
|
Heat pattern(Korean medicine pattern) |
1 (1.5) |
|
|
Cold hypersensitivity |
1 (1.5) |
|
|
Growth disorder |
1 (1.5) |
|
|
VDT(Visual Display Terminal) syndrome |
1 (1.5) |
|
|
Chronic prostatitis, chronic pelvic pain syndrome |
1 (1.5) |
|
|
Chest pain and discomfort |
1 (1.5) |
|
|
Asthma |
1 (1.5) |
|
|
Healthy subject(s) |
23 (34.8) |
3. 질 평가 결과
1) RCT문헌별 보고율
CONSORT-CHM 2017을 이용하여 문헌 검색을 통해 최종적으로 선정된 각 RCT 문헌의 보고율을 환산 점수로 평가한 결과, ‘H’로 평가된 문헌은 29편(43.9%)이었고, ‘M’으로 평가된 문헌은 31편(46.9%)이었으며, ‘L’로 평가된 문헌은 6편(9%)이었다( Fig. 3).
Fig. 3
Reporting rate of each study based on CONSORT-CHM 2017. 
모든 CONSORT-CHM 2017 기준을 완전히 충족한 RCT 문헌은 없었으며, 분석 대상 문헌 중 CONSORT-CHM 2017 보고율이 가장 높았던 논문은 91.6%, 가장 낮았던 논문은 32.1%, 전체 보고율 평균은 67.9%로 확인되었다. 3b 항목(Trial design), 6b 항목(Outcomes), 14b 항목(Recruitment)은 시험 개시 이후 방법 및 결과의 변경, 종료되거나 중단된 경우가 없어 66편의 문헌 모두에서 ‘N/A’로 평가하였다. 또한 해당하는 경우에만 평가가 요구되는 7b 항목(Sample size)과 24번 항목(Protocol)은 각각 중간평가 및 중단기준이 서술되어있지 않은 54편(81.8%)과 연구계획서의 전문에 대한 언급이 없는 62편(93.9%)의 문헌을 ‘N/A’로 평가하였다. 17b 항목(Outcomes and estimation)은 이분형 결과변수를 포함하지 않은 65편(98.4%)의 문헌을 ‘N/A’로 평가하였으며, 18번 항목(Ancillary analyses)은 하위군 분석 및 보정 분석을 실시하지 않은 55편(83.3%)의 문헌을 ‘N/A’로 평가하였다.
2) CONSORT-CHM 2017 세부 항목별 보고율 평가
CONSORT-CHM 2017의 세부 항목별로 문헌 검색을 통해 최종적으로 선정된 RCT 문헌을 평가한 결과, 보고율이 낮은 항목(≤30%)은 4a 항목(Participants), 6a 항목(Outcomes), 7a 항목(Sample size) 이었으며, 2a와 2b 항목(Background and Objectives), 12a 항목(Statistical methods)은 66편의 문헌 모두에서 온전히 보고되었다. 하기한 내용은 보고율이 절반 이하(≤50%)인 항목과, 평가 대상에 해당되지 않는 문헌을 일부 ‘N/A’로 평가한 항목을 사유와 함께 서술하였다. 전체 평가 내용은 Fig. 4, Table 5, Table 6에 표시하였다.
Fig. 4
Reporting rate of each item in CONSORT-CHM 2017. 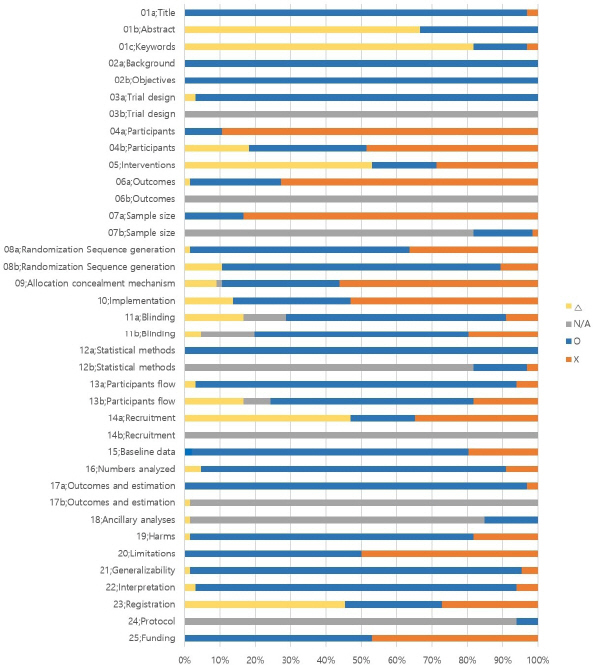
Table 5
Number of Reported Studies and Score of Journal of Korean Medicine and Member Journals
|
Section |
Topic |
Item number |
Score (number of studies evaluated as O) |
% |
|
Title, abstract, and keywords |
Title |
1a |
64/66 (64) |
96.9% |
|
|
Abstract |
1b |
44/66 (22) |
66.6% |
|
|
Keywords |
1c |
37/66 (10) |
56% |
|
|
Introduction |
Background |
2a |
66/66 (66) |
100% |
|
|
Objectives |
2b |
66/66 (66) |
100% |
|
|
Methods |
Trial design |
3a |
65/66 (64) |
98.4% |
|
3b |
0/0 |
- |
|
|
Participants |
4a |
7/66 (7) |
10.6% |
|
4b |
28/66 (22) |
42.4% |
|
|
Interventions |
5 |
29.5/66 (12) |
44.6% |
|
|
Outcomes |
6a |
17.5/66 (17) |
26.5% |
|
6b |
0/0 (0) |
- |
|
|
Sample size |
7a |
11/66 (11) |
16.6% |
|
7b |
11/12 (11) |
91.6% |
|
|
Sequence generation |
8a |
41.5/66 (41) |
62.8% |
|
8b |
55.5/66 (52) |
84% |
|
|
Allocation concealment mechanism |
9 |
25/65 (22) |
38.4% |
|
|
Implementation |
10 |
26.5/66 (22) |
40.1% |
|
|
Blinding |
11a |
47/58 (41) |
81.0% |
|
11b |
41.5/56 (40) |
74.1% |
|
|
Statistical methods |
12a |
66/66 (66) |
100% |
|
12b |
10/12 (10) |
83.3% |
|
|
Results |
Participant flow |
13a |
62/66 (61) |
93.9% |
|
13b |
43.5/61 (38) |
71.3% |
|
|
Recruitment |
14a |
27.5/66 (12) |
41.6% |
|
14b |
0/0 (0) |
- |
|
|
Baseline data |
15 |
53/66 (53) |
80.3% |
|
|
Numbers analyzed |
16 |
59/66 (58) |
89.3% |
|
|
Outcomes and estimation |
17a |
64/66 (64) |
96.9% |
|
17b |
0.5/1 (0) |
50% |
|
|
Ancillary analyses |
18 |
10.5/11 (10) |
95.4% |
|
|
Harms |
19 |
53.5/66 (53) |
81% |
|
|
Discussion |
Limitations |
20 |
33/66 (33) |
50% |
|
|
Generalizability |
21 |
62.5/66 (62) |
94.6% |
|
|
Interpretation |
22 |
61/66 (60) |
92.4% |
|
|
Other information |
Registration |
23 |
32.5/66 (17) |
49.2% |
|
|
Protocol |
24 |
4/4 (4) |
100% |
|
|
Funding |
25 |
35/66 (35) |
53% |
Table 6
Reporting Quality Assessment of Randomized Controlled Clinical Trials from Journal of Korean Medicine and Member Journals Based on CONSORT-CHM 2017
|
Authors year\Section topic |
Oh JK 1998 11
|
Park EH 2002 12
|
Seo JC (1) 2003 13
|
Seo JC (2) 2003 14
|
Kim LH 2003 15
|
Choi SM 2003 16
|
Seo JC 2004 17
|
Kim SJ 2004 18
|
Na BJ 2005 19
|
Seo BK 2005 20
|
Lee CR 2005 21
|
Jang IS 2005 22
|
Jang JB 2005 23
|
Park JM 2005 24
|
Park MJ 2005 25
|
Moon SK 2005 26
|
Park YC 2005 27
|
Choi DJ 2006 28
|
Hsing LC 2006 29
|
Hwang DS 2006 30
|
Kim SM 2006 31
|
Yang CS 2006 32
|
|
Title |
1a |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Abstract |
1b |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
△ |
O |
O |
△ |
△ |
O |
O |
△ |
△ |
△ |
△ |
|
|
Keywords |
1c |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
|
|
Background |
2a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Objectives |
2b |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Trial design |
3a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
△ |
O |
O |
|
3b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Participants |
4a |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
|
4b |
X |
X |
X |
X |
X |
X |
X |
X |
O |
X |
O |
X |
O |
X |
O |
X |
O |
O |
X |
X |
O |
X |
|
|
Interventions |
5 |
△ |
O |
△ |
△ |
X |
△ |
△ |
△ |
X |
X |
O |
O |
△ |
△ |
O |
X |
X |
X |
△ |
X |
△ |
△ |
|
|
Outcomes |
6a |
X |
X |
X |
X |
X |
X |
X |
X |
O |
X |
X |
X |
O |
O |
X |
X |
O |
O |
X |
X |
X |
X |
|
6b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Sample size |
7a |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
|
7b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
X |
O |
N/A |
N/A |
O |
|
|
Randomization Sequence generation |
8a |
X |
O |
O |
O |
X |
X |
O |
X |
X |
O |
O |
O |
O |
△ |
X |
X |
X |
X |
O |
X |
X |
O |
|
8b |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
△ |
△ |
△ |
O |
|
|
Allocation concealment mechanism |
9 |
X |
X |
O |
O |
X |
X |
O |
O |
X |
O |
X |
O |
X |
N/A |
X |
X |
X |
X |
X |
X |
X |
X |
|
|
Implementation |
10 |
X |
X |
O |
O |
X |
X |
O |
X |
X |
△ |
X |
X |
X |
X |
X |
X |
X |
X |
O |
X |
X |
△ |
|
|
Blinding |
11a |
N/A |
O |
O |
O |
O |
O |
O |
O |
X |
O |
N/A |
△ |
△ |
△ |
N/A |
X |
O |
N/A |
O |
X |
N/A |
O |
|
11b |
N/A |
X |
O |
O |
O |
O |
O |
O |
X |
O |
N/A |
O |
X |
X |
N/A |
X |
O |
N/A |
O |
X |
N/A |
O |
|
|
Statistical methods |
12a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
12b |
N/A |
O |
O |
O |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Participants flow |
13a |
O |
O |
O |
O |
O |
X |
O |
O |
O |
X |
O |
O |
O |
O |
X |
O |
O |
O |
O |
△ |
O |
O |
|
13b |
X |
O |
N/A |
N/A |
X |
△ |
N/A |
△ |
△ |
X |
△ |
O |
O |
O |
X |
X |
△ |
X |
O |
X |
O |
O |
|
|
Recruitment |
14a |
△ |
X |
O |
O |
O |
X |
O |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
X |
O |
△ |
X |
△ |
△ |
X |
|
14b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Baseline data |
15 |
X |
O |
X |
X |
X |
X |
X |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
X |
O |
O |
O |
|
|
Numbers analyzed |
16 |
X |
O |
O |
O |
O |
X |
O |
O |
O |
X |
O |
O |
O |
O |
X |
X |
O |
O |
O |
△ |
O |
O |
|
|
Outcomes and estimation |
17a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
|
17b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Ancillary analyses |
18 |
N/A |
O |
O |
O |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Harms |
19 |
X |
X |
X |
X |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
X |
X |
X |
O |
O |
O |
O |
O |
|
|
Limitations |
20 |
X |
X |
X |
X |
X |
X |
X |
O |
O |
O |
X |
O |
O |
O |
X |
O |
O |
X |
O |
X |
X |
O |
|
|
Generalizability |
21 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Interpretation |
22 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Registration |
23 |
X |
X |
X |
X |
X |
X |
X |
△ |
X |
X |
△ |
△ |
△ |
△ |
X |
X |
X |
O |
△ |
X |
X |
△ |
|
|
Protocol |
24 |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Funding |
25 |
X |
O |
O |
O |
O |
X |
O |
O |
X |
O |
O |
X |
X |
O |
X |
O |
O |
X |
X |
X |
X |
X |
|
|
Authors year\Section topic |
Hsing LC 2007 33
|
Lee SG 2007 34
|
Shin SH 2007 35
|
Son DH 2007 36
|
Yang CS 2007 37
|
Yeo JJ 2007 38
|
Bae HH 2008 39
|
Park SW 2008 40
|
Song MK 2008 41
|
Lee TH 2009 42
|
Cho SI 2010 43
|
Cho YJ 2010 44
|
Kim YM 2010 45
|
Lee JE (1) 2010 46
|
Lee JE (2) 2010 47
|
Yoon EH 2010 48
|
Choi IH 2011 49
|
Kwon DH 2011 50
|
Lee DH 2011 51
|
Lee JS 2011 52
|
Park JH 2011 53
|
Jeong HS 2012 54
|
|
|
Title |
1a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Abstract |
1b |
O |
△ |
O |
△ |
△ |
△ |
O |
△ |
△ |
O |
△ |
△ |
O |
△ |
O |
△ |
O |
O |
△ |
△ |
O |
△ |
|
|
Keywords |
1c |
△ |
O |
△ |
△ |
O |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
X |
△ |
△ |
O |
△ |
△ |
△ |
△ |
|
|
Background |
2a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Objectives |
2b |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Trial design |
3a |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
3b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Participants |
4a |
X |
X |
O |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
O |
X |
O |
X |
X |
X |
X |
X |
|
4b |
X |
X |
O |
X |
X |
O |
O |
O |
O |
X |
X |
△ |
X |
△ |
△ |
△ |
X |
X |
X |
X |
△ |
X |
|
|
Interventions |
5 |
△ |
O |
△ |
△ |
△ |
△ |
O |
△ |
O |
O |
△ |
X |
△ |
△ |
X |
O |
△ |
△ |
△ |
△ |
X |
△ |
|
|
Outcomes |
6a |
O |
X |
O |
X |
X |
X |
O |
X |
X |
O |
X |
X |
O |
X |
O |
X |
△ |
O |
X |
X |
O |
X |
|
6b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Sample size |
7a |
X |
O |
X |
X |
X |
X |
O |
X |
O |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
X |
|
7b |
O |
N/A |
N/A |
N/A |
O |
O |
N/A |
O |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
O |
|
|
Randomization Sequence generation |
8a |
X |
O |
X |
O |
O |
X |
O |
X |
O |
O |
X |
X |
X |
O |
O |
X |
O |
O |
O |
O |
O |
O |
|
8b |
O |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
△ |
O |
O |
X |
X |
O |
X |
O |
O |
△ |
O |
O |
|
|
Allocation concealment mechanism |
9 |
X |
O |
X |
X |
X |
X |
O |
X |
O |
X |
X |
X |
X |
△ |
O |
X |
X |
X |
X |
X |
O |
△ |
|
|
Implementation |
10 |
△ |
X |
X |
△ |
△ |
△ |
O |
X |
X |
△ |
O |
X |
O |
O |
X |
X |
O |
O |
O |
X |
O |
O |
|
|
Blinding |
11a |
O |
△ |
X |
O |
O |
O |
O |
△ |
△ |
O |
O |
O |
O |
O |
△ |
△ |
O |
O |
O |
O |
O |
O |
|
11b |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
X |
O |
X |
O |
O |
O |
O |
△ |
X |
O |
|
|
Statistical methods |
12a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
12b |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
O |
X |
N/A |
O |
X |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Participants flow |
13a |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
13b |
O |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
△ |
O |
|
|
Recruitment |
14a |
△ |
X |
△ |
X |
X |
△ |
O |
△ |
O |
X |
△ |
△ |
△ |
△ |
△ |
△ |
X |
△ |
X |
X |
△ |
X |
|
14b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Baseline data |
15 |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
X |
O |
O |
O |
|
|
Numbers analyzed |
16 |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Outcomes and estimation |
17a |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
17b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Ancillary analyses |
18 |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
O |
N/A |
N/A |
△ |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Harms |
19 |
△ |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
|
|
Limitations |
20 |
O |
O |
X |
X |
X |
X |
O |
O |
O |
O |
X |
O |
X |
X |
X |
O |
O |
O |
O |
X |
O |
X |
|
|
Generalizability |
21 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
|
|
Interpretation |
22 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
|
|
Registration |
23 |
△ |
△ |
X |
△ |
△ |
△ |
X |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
|
|
Protocol |
24 |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Funding |
25 |
X |
X |
O |
X |
X |
X |
X |
X |
O |
X |
X |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
|
|
Authors year\Section topic |
Park JH 2012 55
|
Kim WC 2013 56
|
Park SW 2013 57
|
Park SJ 2013 58
|
Kim HN 2014 59
|
Lee IS 2014 60
|
Park SW 2014 61
|
Jung HL 2015 62
|
Jang WS 2016 63
|
Shin SM 2017 64
|
Yoo SJ 2017 65
|
Jeon SH 2018 66
|
Ha KC 2019 67
|
Shin HR 2019 68
|
Sun woo YY 2019 69
|
Choi WC 2020 70
|
Kim SH 2020 71
|
Kwon NY 2020 72
|
Yoon Y 2020 73
|
Ha KC 2021 74
|
Kong HJ 2022 75
|
Hong CY 2023 76
|
|
|
Title |
1a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
|
|
Abstract |
1b |
△ |
△ |
△ |
O |
O |
△ |
△ |
△ |
O |
△ |
O |
O |
△ |
O |
△ |
O |
△ |
O |
△ |
△ |
△ |
△ |
|
|
Keywords |
1c |
O |
△ |
△ |
△ |
△ |
△ |
O |
△ |
△ |
△ |
O |
△ |
X |
△ |
△ |
O |
△ |
O |
△ |
△ |
△ |
△ |
|
|
Background |
2a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Objectives |
2b |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Trial design |
3a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
3b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Participants |
4a |
X |
X |
X |
O |
X |
X |
X |
X |
X |
X |
O |
O |
X |
X |
X |
X |
X |
O |
X |
X |
X |
X |
|
4b |
△ |
△ |
X |
△ |
△ |
O |
O |
X |
O |
X |
O |
△ |
O |
O |
△ |
O |
X |
O |
△ |
O |
O |
X |
|
|
Interventions |
5 |
△ |
X |
X |
X |
X |
△ |
△ |
X |
X |
X |
△ |
△ |
X |
△ |
O |
O |
△ |
△ |
X |
△ |
△ |
O |
|
|
Outcomes |
6a |
X |
X |
X |
O |
X |
X |
X |
X |
X |
X |
O |
O |
X |
X |
X |
O |
X |
X |
X |
X |
X |
X |
|
6b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Sample size |
7a |
X |
X |
X |
O |
X |
O |
X |
X |
X |
X |
X |
O |
X |
O |
X |
O |
X |
O |
O |
X |
O |
X |
|
7b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Randomization Sequence generation |
8a |
O |
O |
O |
O |
O |
O |
O |
X |
X |
X |
O |
O |
O |
O |
O |
X |
O |
O |
X |
O |
O |
O |
|
8b |
O |
△ |
O |
O |
O |
O |
O |
X |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
|
|
Allocation concealment mechanism |
9 |
O |
△ |
△ |
O |
O |
O |
O |
X |
X |
X |
X |
O |
O |
△ |
X |
X |
O |
O |
X |
△ |
O |
O |
|
|
Implementation |
10 |
X |
X |
△ |
O |
X |
O |
O |
X |
X |
△ |
X |
O |
O |
X |
X |
O |
O |
O |
X |
O |
X |
X |
|
|
Blinding |
11a |
O |
△ |
O |
O |
O |
O |
O |
X |
N/A |
N/A |
△ |
O |
O |
N/A |
△ |
O |
O |
O |
△ |
O |
O |
O |
|
11b |
X |
O |
O |
O |
O |
O |
O |
△ |
N/A |
N/A |
X |
O |
X |
N/A |
N/A |
O |
N/A |
O |
△ |
O |
O |
O |
|
|
Statistical methods |
12a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
12b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
|
|
Participants flow |
13a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
13b |
O |
O |
O |
O |
X |
O |
O |
N/A |
X |
X |
O |
△ |
△ |
X |
N/A |
△ |
O |
O |
O |
O |
O |
△ |
|
|
Recruitment |
14a |
△ |
△ |
O |
X |
X |
X |
△ |
X |
X |
X |
O |
△ |
X |
X |
△ |
△ |
X |
△ |
O |
O |
△ |
X |
|
14b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Baseline data |
15 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
X |
|
|
Numbers analyzed |
16 |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
△ |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Outcomes and estimation |
17a |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
17b |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
△ |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
|
|
Ancillary analyses |
18 |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
O |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
N/A |
|
|
Harms |
19 |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Limitations |
20 |
X |
O |
X |
X |
O |
O |
O |
O |
X |
X |
X |
O |
X |
X |
O |
O |
O |
O |
X |
X |
O |
X |
|
|
Generalizability |
21 |
O |
O |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Interpretation |
22 |
O |
O |
O |
△ |
O |
△ |
O |
X |
O |
O |
O |
O |
O |
X |
O |
O |
O |
O |
O |
O |
O |
O |
|
|
Registration |
23 |
△ |
△ |
O |
O |
O |
O |
O |
X |
△ |
O |
O |
△ |
O |
O |
O |
O |
X |
△ |
O |
O |
O |
O |
|
|
Protocol |
24 |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
N/A |
O |
O |
N/A |
N/A |
N/A |
N/A |
O |
N/A |
|
|
Funding |
25 |
O |
X |
X |
O |
X |
O |
O |
X |
O |
O |
O |
O |
X |
X |
X |
O |
X |
O |
O |
O |
O |
X |
4a 항목(Participants)은 7편(10.6%)의 문헌에서 온전히 보고되었으며, 4b 항목(Participants)은 22편(33.3%)의 문헌에서 온전히, 12편(18.1%)의 문헌에서 불충분하게 보고되었다. 여러 문항으로 구성되어있는 5번 항목(Interventions)의 경우 12편(18.1%)의 문헌에서 문항의 80% 이상을 충족하여 온전히 보고된 것으로 평가하였으며, 35편(53%)의 문헌에서 문항의 50% 이상, 80% 미만을 충족하여 불충분하게 보고된 것으로 평가하였다. 6a 항목(Outcomes)은 17편(25.7%)의 문헌에서 온전히, 1편(1.5%)의 문헌에서 불충분하게 보고되었다. 7a 항목(Sample size)은 11편(16.6%)의 문헌에서 온전히 보고되었으며, 7b 항목(Sample size)은 중간 평가나 중단 기준이 언급되지 않은 54편의 문헌을 제외한 12편의 문헌 중 11편(91.6%)에서 온전히 보고되었다. 9번 항목(Allocation concealment mechanism)은 배정을 은폐하지 않은 1편의 문헌을 제외한 총 65편의 문헌 중 22편(38.4%)의 문헌에서 온전히, 6편(9.2%)의 문헌에서 불충분하게 보고되었다. 10번 항목(Implementation)은 22편(33.3%)의 문헌에서 온전히, 9편(13.6%)의 문헌에서 불충분하게 보고되었다. 11a 항목(Blinding)은 눈가림이 시행되지 않은 8편의 문헌을 제외한 총 58편의 문헌 중 41편(70.6%)의 문헌에서 온전히, 12편(20.6%)의 문헌에서 불충분하게 보고되었으며, 11b 항목(Blinding)은 위약이 아닌 중재만을 활용한 10편의 문헌을 제외한 총 56편의 문헌 중 40편(71.4%)의 문헌에서 온전히, 3편(5.3%)의 문헌에서 불충분하게 보고되었다. 12b 항목(Statistical methods)은 하위군 분석 등 추가적 분석을 실시하지 않은 54편의 문헌을 제외한 총 12편의 문헌 중 10편(83.3%)에서 온전히 보고되었다.
13b 항목(Participant flow)은 탈락과 제외가 일어나지 않은 5편의 문헌을 제외한 총 61편의 문헌 중 38편(62.2%)의 문헌에서 온전히, 11편(18%)의 문헌에서 불충분하게 보고되었다. 14a 항목(Recruitment)은 12편(18.1%)의 문헌에서 온전히, 31편(46.9%)의 문헌에서 불충분하게 보고되었다. 17b 항목(Outcomes and estimation)은 이분형 결과변수를 포함하지 않는 65편의 문헌을 제외한 총 1편의 문헌 중 1편(100%)에서 불충분하게 보고되었다. 18번 항목(Ancillary analyses)은 추가적 분석을 실시하지 않은 55편의 문헌을 제외한 총 11편의 문헌 중 10편(90.9%)의 문헌에서 온전히, 1편(9%)의 문헌에서 불충분하게 보고되었다.
20번 항목(Limitation)은 33편(50%)의 문헌에서 온전히 보고되었다. 23번 항목(Registration)은 17편(25.7%)의 문헌에서 온전히, 31편(46.9%)의 문헌에서 불충분하게 보고되었다. 24번 항목(Protocol)은 연구계획서를 언급하지 않은 62편의 문헌을 제외한 총 4편의 문헌 중 4편(100%)에서 온전히 보고되었다( Fig. 4)( Table 5, 6).
IV. 고 찰
RCT는 여러 종류의 중재에 대한 효과를 검증하는 과학적 연구 설계로, 근거중심진료를 지향하는 임상현장에서도 가장 중요하게 여겨지고 있다 3,9. 그러나 RCT 연구가 적절하지 않게 수행될 경우, 비뚤림 위험이 높은 결과를 도출할 수 있고 이는 의료 관계자 및 정책 입안자가 치료 및 정책의 근거로 삼기에 어려움이 따른다 1. 이에 연구결과보고의 질을 향상시키기 위해 EQUATOR Network에서 RCT의 보고 지침인 CONSORT를 개발하였다. 하지만 CONSORT는 변증, 처방, 한약재 등 한의학 고유의 특성을 충분히 고려하지 못했다는 아쉬움이 있었다. 따라서 2006년에 이를 보완하기 위해 CONSORT-CHM 2017 group에서 한의학 고유의 특성을 평가하는 항목이 추가된 CONSORT-CHM 2006을 개발했으며, 이를 개선 및 보완한 CONSORT-CHM 2017이 2017년에 개발되었다 4. CONSORT-CHM 2017에서는 기존 CONSORT-2010의 25개 항목 중 Title and abstract(items 1a and 1b), Background and objectives(items 2a and 2b), Participants (item 4a), Interventions(item 5), Outcomes(item 6a), Generalizability(item 21), Interpretation(item 22) 7개를 수정하고, 1개의 새로운 항목(item 1c)을 추가하였다. 또한 처방의 의심되는 유해성을 한의학 이론이나 생의학적인 관점에서 보고할 것을 명시하는 등 ‘위해’ 항목에 대한 설명을 한약 처방에 적합하게 개정하였고(item 19), EQUATOR 그룹에서 발간한 중재의 기술 및 복제를 위한 템플릿(Template for Intervention Description and Replication, TIDieR)을 혼합하여 한의학 RCT 결과보고 질평가의 발판을 마련하였다 4. 본 연구에서는 아직 한국어판이 보급되지 않은 CONSORT-CHM 2017의 국내 연구 접근성을 높이기 위해, Lee 등의 연구 77 등을 참조하여 번역본을 완성하였다( Appendix I). 국내 한의학 분야에서 CONSORT 지침 및 그 확충안인 STRICTA를 활용하여 RCT 문헌을 평가한 문헌은 Kwon 등의 한방재활의학과학회지에 대한 연구 6와 Lee 등의 한방재활의학과학회지에 대한 연구 1, Cho 등의 척추신경추나의학회지에 대한 연구 3, Park 등의 아토피 피부염 RCT 문헌에 대한 연구 5, Shin 등의 경도인지장애의 침 치료에 대한 RCT 논문 7 등이 존재하나, 아직까지 CONSORT-CHM 2017을 활용한 연구는 보고되지 않았다. 이에 저자는 CONSORT-CHM 2017을 이용하여 2023년 3월까지 발간된 대한한의학회지 및 회원학회지에 수록된 66편의 경구투여 한약 중재를 이용한 무작위 대조군 비교임상시험(Randomized Controlled clinical Trial, RCT)의 보고의 질적, 양적 평가를 실시하였다.
양적 평가의 결과를 살펴보면, 문헌에서 다루고 있는 질환으로는 비만에 대한 약물의 효과를 분석하는 논문이 9편(13.6%)으로 가장 많았다. 2022년 보건복지부의 한방 의료 이용 실태에 따르면 ‘건강증진 및 미용’ 항목은 국내의 한방의료 이용 목적 중 2위에 해당하는 항목이며 79, 점차 증가하는 비만 유병율에 비추어 보았을 때 80, 대한한의학회지 및 회원학회지에 수록된 RCT에서도 비만과 같이 시의성을 가진 질환에 대한 관심도가 높음을 알 수 있었다. 이를 제외하면 건강한 정상 성인에 대한 약물의 효과를 검증하는 논문이 23편(34.8%)으로 다수를 차지했다. 이는 한약의 치료효과에 대한 관심뿐만 아니라 한약의 안전성 및 건강증진 효능에도 관심이 높아지고 있는 것으로 풀이되며, 이로 미루어보아 한약 사용의 위해 관련 설명을 추가한 CONSORT-CHM 2017이 기존 CONSORT 지침보다 사회적 관심을 더 잘 반영하여 RCT 문헌을 평가할 수 있을 것으로 사료된다. 또한 위약 대조군을 설정하는 것은 그 중재의 효과를 가장 정확하게 보여줄 수 있으므로 이상적인 연구 설계라고 할 수 있는데 1, 대한한의학회지 및 회원학회지에 투고된 경구 투여 한약 중재를 이용한 66편의 RCT는 위약을 대조군으로 포함한 논문이 46편(69.6%)으로 상당수를 차지한다. 이는 대한한의학회지 및 회원학회지에 투고되는 경구투여 한약중재를 활용한 RCT 논문의 설계가 비교적 이상적으로 이루어지고 있음을 시사한다. 다만 경구투여 한약 중재를 활용한 RCT가 꾸준히 발간되고는 있지만, 동일 기간 동안 대한한의학회지 및 회원학회지에 투고된 전체 30,764편의 문헌 중 66편밖에 존재하지 않는 만큼 여타 다른 연구 설계를 따른 논문들에 비해 그 수가 현저히 적다고 할 수 있다. 이는 아마도 RCT를 수행하는 데에 따르는 인적, 경제적 부담 때문인 것으로 보이나, RCT는 근거중심의학의 핵심이며 의료 정책 및 임상 진료의 중요한 의학적 결정권의 바탕이 되는 만큼 81 추후 한의계의 발전을 위해서 더욱 많은 RCT가 필요할 것으로 사료된다. 질적 평가의 결과를 살펴보면, CONSORT-CHM 2017 보고 지침에 따라 대한한의학회지 및 회원학회지에 실린 RCT 문헌의 보고의 질을 평가한 결과 ‘H’로 평가된 문헌은 29편(43.9%)이었고, ‘M’으로 평가된 문헌은 31편(46.9%)이었으며, ‘L’로 평가된 문헌은 6편(9.0%)으로, 평균적으로 약 67.9%의 보고율을 보였다. CONSORT-CHM 2017의 각 항목별로 살펴보면, 전반적으로 보고율이 낮은(≤30%) 항목은 4a 항목(Participants), 6a 항목(Outcomes), 7a 항목(Sample size)이었다. 그 중 4a 항목(Participants ; ‘진단 기준, 포함 및 배제 기준에서 특정 한의학적 변증을 가진 참가자를 모집) 및 6a 항목(Outcomes ; 결과의 기술에서 변증의 세부 사항을 표기한 설명)은 한의학적 변증(TCM pattern)에 대한 기술을 요하는 항목이다. 해당 항목들의 보고율이 낮은 이유를 분석해보면, 한의학 처방을 중재로 사용하였으나 변증을 활용하지 않고 특정 질병을 대상으로 처방을 적용한 경우, 혹은 건강인을 대상으로 약물의 효능을 실험하는 연구의 경우 지침을 준수하는 데 있어 구조적인 어려움을 지닌다. 그리고 변증을 활용하지 않고 일괄적으로 환자들에게 처방을 투여하는 설계의 연구는 만약 특정 한의학적 변증을 가진 참가자만을 모집하는 것이 특정한 경향성을 갖는 참가자들을 모집하여 결과의 비뚤림을 야기할 수 있고, 건강인을 대상으로 한 경우에는 변증에 필요한 증상 등의 근거가 부족할 수 있다. 이 같은 문제를 해결하기 위해서는 위 두 지침의 세부 사항에 ‘If applicable’의 단서를 달아 해당하는 연구만을 대상으로 보고율을 산출하게 하는 등의 개선이 필요할 것으로 사료된다.
표본 수의 산출 근거(7a ; sample size)에 대한 기술은 11편(16.6%)의 문헌에서만 찾아볼 수 있었다. 적절한 표본 수 산정은 연구 결과의 타당성 확보에 필수적인데, 연구대상자의 수가 너무 적을 경우 두 군 간의 차이가 통계적으로 의미를 갖지 못하고, 연구대상자의 수가 필요 이상으로 많을 경우 연구의 기간이 길어지고 소요되는 비용이 증가하며 임상에서는 의미 없는 작은 차이도 통계적 의미를 갖게 되는 비뚤림을 가질 수 있기 때문이다 1. 따라서 후속으로 발표될 연구들의 경우 적절한 근거를 바탕으로 표본 수를 산출하는 과정을 통해 연구 결과의 타당성을 확보하고, 이를 논문에 명시할 필요가 있다. 3b(Trial design), 6b(Outcomes), 14b 항목(Recruitment)은 모든 문헌에서 ‘N/A’로 평가되었는데, 이는 시험 개시 이후 방법 및 결과의 변경, 종료되거나 중단된 경우가 없었기 때문이다. 7b 항목(Sample size)과 24번 항목(Protocol)은 해당하는 경우에만 평가를 요구하여, 7b 항목의 경우 중간 평가나 중단기준에 대한 언급이 없는 54편(81.8%)을, 연구계획서 전문에 대한 언급이 없는 62편(93.9%)의 문헌을 ‘N/A’로 평가하였다. 17b 항목(Outcomes and estimation)은 이분형 결과변수를 포함하지 않은 65편(98.4%)의 문헌을 ‘N/A’로 평가하였으며, 18번 항목(Ancillary analyses)은 하위군 분석 및 보정 분석을 실시하지 않은 55편(83.3%)의 문헌을 ‘N/A’로 평가하였다.
본 연구에는 다음과 같은 한계가 존재한다. 첫째, CONSORT-CHM 2017을 활용하는 과정에서 아직 국내에 아직 CONSORT-CHM 2017을 기반으로 작성된 문헌이 많지 않다는 점을 고려하여, 평가 항목에 해당하는 내용이 반드시 문헌의 해당 section에 포함되어있지 않더라도 보고한 것으로 간주하여 평가하였다. 이는 평가항목에 해당하는 내용이 논문의 다른 section에 기재되어 있는 경우가 상당수 존재하여 지나치게 보고율이 낮아지는 비뚤림을 막고자 내린 결정이었으나, 이와 같은 결정으로 인해 전체적인 문헌들의 CONSORT-CHM 2017의 보고율이 상승하였음을 주지할 필요가 있다. 둘째, CONSORT-CHM 2017 한국어판이 아직 보급되지 않아 저자들이 원문을 자체적으로 번역하여 이를 기반으로 평가를 진행하였는데, 번역의 과정에서 원문의 의미가 왜곡되었거나 비뚤림이 생겼을 가능성이 있다. 추후 저자들이 번역한 한국어판의 신뢰도, 타당도에 대한 후속 연구를 통해 이를 보완해야 할 것으로 보인다.
그러나 국내 한의학 분야 최초로 한의학의 특성을 반영한 평가기준인 CONSORT-CHM 2017으로 대한한의학회지 및 회원학회지의 RCT 보고의 질 평가를 시도하였다는 점에서 이는 기존 연구에서 활발하게 사용된 CONSORT 등의 평가기준보다 한약 중재를 활용한 RCT 문헌의 보고의 질을 더 세밀히 평가할 수 있다는 점에서 유의한 차이를 가진다. 이처럼 향후 발표될 한약 중재를 활용한 RCT의 작성에 도움이 되는 지침을 도입하였으며, 한국어판을 제공해 접근성을 높였다는 점에서 본 연구는 의의를 갖는다. 분석결과 전반적으로 대한한의학회지와 회원학회지에 투고된 경구투여 한약 중재 RCT의 경우 표본 수 산출에 대한 근거 언급, 변증의 세부 사항에 대한 언급이 미비하였으며, 다른 종류의 연구 설계에 비해 문헌의 수가 적다는 문제점을 발견하였다. 추후 발표될 문헌들의 보고의 질을 향상시키기 위해서는 CONSORT-CHM 2017을 참고해 적절한 표본 수 산출 및 변증을 실시하고 세부사항을 기술하는 등의 노력이 필요하다. 또한 더 많은 수의 RCT가 발표되어 한약 처방에 대한 질 높은 근거를 제시할 수 있기를 희망한다.
V. 결 론
본 연구는 대한한의학회지 및 회원학회지에 2023년 3월까지 출판된 한약 중재를 활용한 RCT 연구 66편을 대상으로 CONSORT-CHM 2017에 근거한 질 평가를 실시해 다음과 같은 결론을 얻었다.
RCT 문헌별로 보고율을 평가한 결과, ‘H’(High) 로 평가된 문헌은 29편(43.9%)이었고, ‘M’(Moderate)으로 평가된 문헌은 31편(46.9%)이었으며, ‘L’ (Low)로 평가된 문헌은 6편(9.0%) 이었다. 66편의 RCT 중 보고율이 가장 높은 문헌은 91.6%의 보고율을, 가장 낮은 보고율을 보인 문헌은 32.1%의 보고율을 보였으며, 평균적으로 67.9%의 보고율을 보였다. CONSORT-CHM 2017 세부 항목별 보고율을 평가한 결과, 66편의 RCT 문헌 중 모든 CONSORT-CHM 2017 평가기준을 완전히 충족한 RCT는 없었다. 보고율이 낮은 항목(≤30%)은 4a 항목(Participants), 6a 항목(Outcomes), 7a 항목(Sample size) 이었으며, 이를 보완하기 위해서는 4a, 6a 항목에 ‘If applicable’ 등의 단서를 다는 등 지침을 보완하고, 근거를 바탕으로 표본 수를 추출하는 과정이 필요할 것으로 사료된다. 보고지침 중 2a와 2b 항목(Background), 12a 항목(Statistical methods)은 모든 문헌에서 보고되었으며, 3b 항목(Trial design), 6b 항목(Outcomes), 14b 항목(Recruitment)은 모든 문헌이 평가 대상에 해당되지 않았다. 한약중재를 활용한 RCT의 보고의 질을 향상시키기 위해서는 차후 수행되는 연구에서 CONSORT -CHM 2017 점검표를 바탕으로 보고율이 낮거나 누락된 항목을 보완하여 질 높은 RCT를 수행하도록 권장할 필요가 있다.
참고문헌
1. Lee HY, Heo KH, Cho HW, Hwang EH, Shin MS, Shin BC. Randomized Controlled Clinical Trials in the Journal of Oriental Rehabilitation Medicine :A Quantitative and Qualitative Analysis (1). Journal of Korean Medicine Rehabilitation 2013:23(1):87–100.
2. Park BK, Cho JH, Son CG. Randomized Clinical Controlled Trials with Herbal Acupuncture (Pharmacopuncture) in Korea - A Systematic Review. Journal of Korean Medicine 2009:30(5):115–26.
3. Cho HW, Lee HY, Heo KH, Hwang EH, Shin MS, Shin BC. Randomized Controlled Clinical Trials in the Journal of Korean Society of Chuna Manual Medicine for Spine and Nerves:A Quantitative and Qualitative Analysis. Journal of Korean Society of Chuna Manual Medicine for Spine and Nerves 2012:7(2):15–23.
4. Cheng CW, Wu TX, Shang HC, Li YP, Altman DG, Moher D, et al. CONSORT Extension for Chinese Herbal Medicine Formulas 2017:Recommendations, Explanation, and Elaboration. Ann Intern Med 2017:167(2):112–21.   5. Park HJ, Kwon JH, Yoo JH. Quantity and Quality Assessment of Randomized Controlled Trials in the Atopic Dermatitis. The Journal of Korean Medicine Ophthalmology and Otolaryngology and Dermatology 2014:27(4):45–57.  6. Kwon DH, Nam JK, Jung MK, Kim HJ, Lee MJ. Quantity and Quality Assessment of Randomized Controlled Trials in the Journal of Oriental Rehabilitation Medicine. Journal of Korean Medicine Rehabilitation 2010:20(4):91–103.
7. Shin YO, Heo WY, Lee I. Quality Assessment of Studies on Randomized Controlled Trials (RCTs) of Acupuncture Treatment for Mild Cognitive Impairment:Based on the STRICTA and CONSORT Guidelines. Journal of Internal Korean Medicine 2019:40(6):1101–11.   8. Hyun JY, Shin JE, Im CJ, Park JY. A Systematic Review on the Reporting Quality of Acupuncture Treatment for Carpal Tunnel Syndrome. Korean Journal of Acupuncture 2020:37(3):131–44.  9. 전국한의과대학 본초학공동교재 편찬위원회. 본초학 4판. 서울: 영림사: 2020. p. 1–767.
11. Na HU, Park SH, Woo HJ, Han YH, Geum JH, Lee JH, et al. Reporting Qualitative Research of Systematic Review in the Journal of Korean Medicine Rehabilitation According to Preferred Reporting Items for Systematic Reviews and Meta-Analyses 2020 Guidelines. Journal of Korean Medicine Rehabilitation 2022:32(3):85–107.  12. Oh JK, Lee MJ. The Effects of Bo-Jung-Chi- Seub-Tang Administration on Body Composition, Blood Biochemistrical Factors and Hormonal Changes during 2 weeks Weight Reduction in TaekwonDo Athletes. Journal of Korean Medicine 1998:19(2):391–400.
13. Park EH. Clinical Study for YMG-1,2's Effects on Learning and Memory Abilities. Journal of Physiology &Pathology in Korean Medicine 2002:16(5):976–88.
14. Seo JC, Han SW, Byun JS, Ha ID, Leem KH, Heo ZJ, et al. The Effects of Korean Ginseng and American Ginseng on Body Temperature in Koreans and Chineses -Double-blind Randomized Controlled Trials. Journal of Physiology &Pathology in Korean Medicine 2003:17(3):837–41.
15. Seo JC, Han SW, Byun JS, Ha ID, Leem KH, Heo ZJ, et al. Double-blind Randomized Controlled Trials on Superficial Body Temperature of Korean Ginseng and American Ginseng in Koreans and Chineses. The Korea Journal of Herbology 2003:18(2):71–86.
16. Kim LH, Jang IS, Kim JY, Song JM. A Clinical Trial about Anti-anxiety and Anti-stress Effect of a modified formula consisted with Several Herbs. Journal of Physiology &Pathology in Korean Medicine 2003:17(6):1533–7.
17. Choi SM, Kim SH, Ahn SK, Sung HJ, Yoon YS. Clinical study on the effects of a composition containing oriental medicine for eye symptoms of VDT syndrome. Journal of Korean Medicine 2003:24(2):109–20.
18. Seo JC, Lee SY, Lee KM, Leem SC, Jeong TY, An HD, et al. Double-blind Randomized Controlled Trials on Blood Pressure and Pulse Rate of Korean Ginseng and American Ginseng in Koreans and Chineses. Journal of Physiology &Pathology in Korean Medicine 2004:18(2):606–11.
19. Kim SJ, Kim HJ, Ko BP, Kim HD, Kim JA, Park JM, et al. Effect of Ephedra Sinica and Evodia Rutaecarpa on Resting Metabolic Rate in Obese Premenopausal Women during Low-calorie Diet:A Randomized Controlled Clinical Trial. Journal of Korean Medicine for Obesity Research 2004:04(01):45–54.
20. Na BJ, Jung JH, Choi CM, Hong JW, Kim TH, Lee CR, et al. Effects of Banhahubak-tang (Banxiahoupotang) on patients with poststroke depression. Journal of Internal Korean Medicine 2005:26(3):563–74.
21. Seo BK, Ryu SR, Kang JW, An KE, Lee SH, Choi DY, et al. Clinical Study of the Efficacy and Safety of Jetongdan on Patients with Osteoarthritis of the Knee. Journal of Korean Medicine 2005:26(02):231–40.
22. Lee CR, Lee SH, Rhe JW, Na BJ, Kim TH, Jung WS, et al. The Effect of Korean, Chinese and American Ginseng on Blood Pressure of Hypertensive Patients. Journal of Korean Medicine 2005:26(03):228–38.
23. Jang IS, Ko CN, Lee I, Park JM, Kim SH, Kim SW, et al. Effect of Cardiotonic Pills on Chest Pain and Discomfort:A Multi-center Double-blind Randomized Controlled Trial. Journal of Korean Medicine 2005:26(02):95–104.
24. Jang JB. Clinical Study on the Efficacy and Safety of Chiljehyangbuhwan according to Hyungsang Remedy in the Treatment of Primary Dysmenorrhea. The Institute of Korean HYUNG SANG Medicine 2005:06(01):494–524.
25. Park JM, Kim HJ, Kim JA, Kim SJ, Ko BP. The Effects of Evodia Rutaecarpa and Ephedra sinica on the Resting Metabolic Rate and Body Composition of Obese Women on a Low-Calorie Diet:A Double-blinded Randomized Controlled Clinical Trial. Journal of Korean Medicine 2005:26(03):249–62.
26. Park MJ, Seo JW, Sung IH, Kim NO, Sung SM, Chung AK, et al. The Clinical Study on the Effect of Sulguanjul-bang No.1 According to Formulation. Journal of Internal Korean Medicine 2005:13(2):193–206.
27. Moon SK, Kim YS, Park SU, Jung WS, Ko CN, Cho KH, et al. Effect of Gastrodia Elata BL water extract on human cerebral blood flow using transcranial doppler. Journal of Korean Medicine 2005:26(1):115–22.
28. Park YC. Effect of Socheongryong-tang on Punghan and Pungyeol Type Common Cold :A Double Blind, Placebo Controlled Study. Journal of Physiology &Pathology in Korean Medicine 2005:19(02):524–9.
29. Choi DJ, Cho KH, Jung WS, Park SU, Han CH, Lee WC. Clinical Effects of Korean Ginseng, Korean Red Ginseng, Chinese Ginseng, and American Ginseng on Blood Pressure in Mild Hypertensive Subjects. Journal of Korean Medicine 2006:27(4):198–208.
30. Hsing LC, Lee TH, Son DH, Yeo JJ, Yang CS, Seo ES, et al. Adverse Effects of Ma-huang according to Dose :A Randomized Double-Blind Placebo-Controlled Pilot Study. Journal of Internal Korean Medicine 2006:27(1):188–96.
31. Hwang DS, Park MW, Chun HN, Yun SS, Lee IS, Cho JH, et al. Effects of Mokhyangsaenghwa-tang beverage on Postpartum Recovery and Lactation. The Journal of Oriental Obstetrics & Gynecology 2006:19(4):216–24.
32. Kim SM, Shin SM, Kim EI, Lee JE, Yoo DY. A Clinical Study on the Effect of Daejo-hwan (DJH) on Climacteric Syndrome. The Journal of Oriental Obstetrics & Gynecology 2006:19(4):225–44.
33. Yang CS, Hsing LC, Yeo JJ, Seo ES, Jang IS. Effects of Ephedra on Weight Loss and Heart Rate Variability:A Double-Blind Randomized Controlled Pilot Study. Journal of Internal Korean Medicine 2006:27(4):836–44.
34. Hsing LC, Yang CS, Lee TH, Kim LH, Kwak MJ, Seo ES, et al. Short-Term Effects of Mahuang on State-Trait Anxiety According to Sasang Constitution Classification :A Double- Blind Randomized Controlled Trial. Journal of Internal Korean Medicine 2007:28(1):106–14.
35. Lee SG, Cho YH, Kang TG, Yang HY, Yoo BC, Cho CK, et al. Analysis of Plasma Proteome before and after Oral Administration of Acidic Polysacharide from Panax Ginseng, Double-blind, Placebo-controlled, Randomised Trial. Journal of Physiology &Pathology in Korean Medicine 2007:21(5):1185–93.
36. Shin SH, Kim JH, Kim MB, Yoon HJ, Lyu SA, Lee SY, et al. A Clinical Research about the Effects of Seunggaltang on Patients with Atopic Dermatitis. The Journal of Korean Medicine Ophthalmology &Otorhinolaryngology &Dermatology 2007:20(2):199–212.
37. Son DH, Hsing LC, Kim LH, Jeong SI, Seo ES, Jang IS. Effect of Mahuang on Heart Rate Variability in Adults :a Double-Blind, Placebo -Controlled, Randomized Trial. Journal of Korean Medicine 2007:28(1):105–16.
38. Yang CS, Hsing LC, Jeong HS, Kim LH, Kwak MJ, Seo ES, et al. Effects of Ephedra on the State-Trait Anxiety in Female Adults:A Double-Blind Randomized Controlled Study. Journal of Internal Korean Medicine 2007:28(2):346–53.
39. Yeo JJ, Hsing LC, Yang CS, Jeong SI, Seo ES, Jang IS. Effects of Mahuang for Weight Loss in Healthy Adults :A Double-Blind, Controlled, Randomized, Clinical Trial. Journal of Korean Medicine 2007:28(1):63–71.
40. Bae HH, Kang WC, Park YC. Effectiveness of a Yeonkyopaedok-san Extract in the Treatment of The Common Cold :Results of a Community -based, Double Blind, Randomized Placebo Controlled Trial. Journal of Physiology &Pathology in Korean Medicine 2008:22(1):234–45.
41. Park SW, Shin YC, Ko SG. The Improvement of Mixed Extracts of Fructus Aurantii and Mulberry Leaves on Lipid Metabolism. Society of Preventive Korean Medicine 2008:12(1):135–47.
42. Song MK, Kang JS, Kang CH, Ahn YM, Ahn SY, Doo HK, et al. The Clinical Effect of Bosingunyang-tang on Chronic Non-bacterial Prostatitis/Chronic Pelvic Pain Syndrome :Randomized Double-blind, Placebo-controlled Clinical Trial. Journal of Internal Korean Medicine 2008:29(3):800–9.
43. Lee TH, Hsing LC, Yang CS, Kim LH, Seo ES, Jang IS. Adverse Effects of Ephedra According to Sasang Typology in Healthy Adults :A Double-Blind Randomized Controlled Trial. Journal of Internal Korean Medicine 2009:30(1):144–52.
44. Cho SI, Son MW, Hong KE. Glycemic Control Effects of Sanyak (Dioscoreae rhizoma) extract in Prediabetic Stage Patients. Journal of Korean Medicine 2010:31(5):146–66.
45. Cho YJ, Kim EJ, Yang YJ, Song MY. Effects of I-razin in Overweight Children. Journal of Korean Medicine for Obesity Research 2010:10(2):17–25.
46. Kim YM, Park YC, Jo JH, Kang WC, Son MW, Hong KE. Effect of Herb Medicine Treatment for Functional Dyspepsia:A Randomized Placebo- Controlled and Compared Standard Treatment Trial. Journal of Korean Medicine 2010:31(1):1–13.
47. Lee JE, Song YK, Lim HH. Clinical Trial of Taeeumjowui-Tang(Taiyintiaowei-tang) on Obese Patients - Randomized, Double Blind, Placebo- Controlled Study. Journal of Korean Medicine Rehabilitation 2010:20(4):197–213.
48. Lee JE, Song YK, Lim HH. Randomized, Double Blind, Placebo-Controlled Study of Bofu-tsusho -san on Obese Patients. Journal of Korean Medicine for Obesity Research 2010:10(1):1–16.
49. Yoon EH, Jang MG, Hwang JH, Lee SH, Jeong WJ, Lee JD, et al. Adverse Event Study on Ojeok-san Extract Powders RCT in Low Back Pain Patients. Journal of Acupuncture Research 2010:27(4):195–202.
50. Choi IH, Kim SH, Kim YC, Yun YH. A Clinical Study of Shi Ho Cheong Gan-San on Blood Heat Pattern Atopic Dermatitis:a randomized, double-blind clinical trial. The Journal of Korean Medicine Ophthalmology &Otorhinolaryngology &Dermatology 2011:24(1):96–110.
51. Kwon DH, Lee MJ, Lim CY, Shambhunath B, Lee SJ, Kim HJ. Efficacy of Red Ginseng by Oriental Medical Obesity Syndrome Differentiation on Obese women :Randomized, Double-blind, Placebo-controlled Trial. Journal of Korean Medicine for Obesity Research 2011:11(1):1–13.
52. Lee DH, Han HJ, Kim LH, Kang SY, Jang IS. Effect of Saengmaeg-san Extract on Xerostomia in Stroke Patients :A Double-Blind Randomized Controlled Study. Journal of Internal Korean Medicine 2011:32(4):542–9.
53. Lee JS, Do EJ, Kwak MA, Park HJ, Ha ID, Sung KJ, et al. Clinical Trial to Evaluate the Efficacy of Extract of Citri Pericarpium on Serum Lipid Profiles in Subjects:a Randomized, Double-blind. The Korea Journal of Herbology 2011:26(1):125–32.
54. Park JH, Lee MJ, Kim HJ, Hong SW, Lee DK, Yoo JW, et al. Efficacy and Adverse Events of Bangpungtongseong-san(Bofutsusho-san) and Bangkihwangki-tang(Boiogiot-tang) by Oriental Obesity Pattern Identification on Obese Subjects :Randomized, Double Blind, Placebo-controlled Trial. Journal of Korean Medicine Rehabilitation 2011:21(2):265–78.
55. Jeong HS, Kang SY, Han HJ, Jang IS. The Effects of SBD-1 on Hangover Syndrome :a Randomized Double-blind Crossover Preliminary Study. Journal of Internal Korean Medicine 2012:33(4):511–9.
56. Park JH, Shambhunath B, Lim CY, Kim HJ. Impact of GNB3, ADRB3, UCP2, and PPARγ-Pro12Ala polymorphisms on Boiogito response in obese subjects :A randomized, double-blind, placebo-controlled trial. Journal of Korean Medicine for Obesity Research 2012:12(2):28–43.
57. Kim WC, Jeong JK, Kim JS, Kim KO. The Verify of Memory Improvement by Gastrodia Elata Blume. The Korean Society of Oriental Neuropsychiatry 2013:24(1):27–44.  58. Park SW, Kwon YB, Kim KT, Shin SM, Leem KH, Ko H, et al. A Randomized, Double-blind, Placebo-controlled Study to the efficacy and Safety of NMED-01 and NMED-02 in Mild Alcoholic Liver Subjects. The Korea Journal of Herbology 2013:28(6):31–8.  59. Park SJ, Choi NR, Kim K, Yoo JH, Lee SW, Joo JC. Clinical Trial of Herbal Medicine Formula Mahwangjeongcheon-tang on Patients with Asthmatic Symptom:A Preliminary Study. Journal of Sasang Constitutional Medicine 2013:25(4):373–83.  60. Kim HN, Kim JE, Jeong JK, Kim JS, Kim KO. The Verify of Memory Improvement by Gastrodia Elata Blume Depends on the Amount. The Korean Society of Oriental Neuropsychiatry 2014:25(3):243–52.  61. Lee IS, Kim MS, Lee SK. Study of Efficacy and Safety of Tianwangbuxin-dan for Poststroke Depression:A Randomized, Double Blinded, Non-inferiority Trial. Journal of Internal Korean Medicine 2014:35(2):145–56.
62. Park SW, Kim YS, Lee DH, Kwon YB, Park JY, Lee SY, et al. Efficacy and safety of HT008 and glucosamine sulfate in the treatment of knee osteoarthritis :a randomized double-blind trial. The Korea Journal of Herbology 2014:29(4):45–52.  63. Jung HL, Na HJ, Kim PS, Ryu HS, Kang HY. The Effects of Licorice Supplementation on Muscle Injury, Cortisol, Testosterone and Insulin Sensitivity After High Intensity Resistance Exercise. The Korea Journal of Herbology 2015:30(2):37–42.  64. Jang WS, Kwak MA, Park KH. The Effects and Safety of Cardiotonic Pills with Pletaal on Post-Reperfusion Syndrome of Arteriosclerotic Occlusive Disease(Pilot Study). Journal of Korean Medicine 2016:37(4):30–5.  65. Shin SM, Park SY, Kim TY. Effects of SM-2015 on Blood Alcohol Clearance and Hangover. Journal of Internal Korean Medicine 2017:38(1):20–31.   66. Yoo SJ, Ko SK, Kim HJ. Clinical Trial for the Heat-Rising Action of Ginseng and Cultivated Wild Ginseng to The Subject Diagnosed as Heat Pattern by Cold-Heat Patternization. The Journal of Oriental Obstetrics & Gynecology 2017:30(4):45–58.
67. Jeon SH, Kim JW. Effects of a Herbal Medicine, Yukgunja-Tang Extract Granule, on Functional Dyspepsia Patients by Sasang Constitution:Placebo-Controlled, Double-Blind, Randomized Trial. Journal of Sasang Constitutional Medicine 2018:30(2):42–54.
68. Ha KC, Baek HI, Kim HM, Kim YM, Jeong DY, Hong SJ, et al. Clinical Study on Child's Height Growth of Mixtures of Cynanchum wilfordii and Phlomis umbrosa Extract. Journal of Korean Medicine Rehabilitation 2019:29(1):75–83.  69. Shin HR, Park KT, Yeom SR, Kwon YD. Safety of Ojeok-san Extract Powder and Soft Extract in Healthy Male Volunteers, Single Center, Randomized Controlled, Cross-over Study. Journal of Korean Medicine Rehabilitation 2019:29(1):63–73.  70. Sunwoo YY, Kim HJ, Kim JY, Yang NR, Lee JH, Park TY. Hematologic and Serological Investigation of Effect on Gyeongokgo in Healthy Individuals :a Randomized, Subject- assessor-blind, Placebo-controlled, Single-center Pilot Study. Journal of Physiology &Pathology in Korean Medicine 2019:33(4):239–48.  71. Choi WC, Lee HS, Kim JY, Kang WC, Park YC, Kim GW, et al. Effect of Sihogayonggolmoryeo -Tang on Hwa-byung:A Multicenter, Randomized, Double-Blinded, Placebo-Control Trial. The Korean Society of Oriental Neuropsychiatry 2020:31(3):135–47.
72. Kim SH, Seo YN, Bae IH, Cho KH, Moon SK, Jung WS, et al. Effects of Dangui-jakyak-san on Common Carotid Artery Elasticity in Healthy Subjects ;A Randomized controlled crossover study. The Journal of the Society of Stroke on Korean Medicine 2020:21(1):21–31.
73. Kwon NY, Yoo JS, Kim HJ, Lee DN. Effect of Onkyung-tang on Cold Hypersensitivity on Feet:A Multi-center Double-blind Randomized Controlled Trial. The Journal of Oriental Obstetrics & Gynecology 2020:33(3):149–74.
74. Youn Y, Baek HI, Jin HY, Jeong DY, Shen L, Joo JC, et al. Randomized Double-blind Human Trial to Evaluate Efficacy and Safety of Rhus verniciflua Stokes (Lacca Sinica Exsiccata) and Eucommia ulmoides Oliver (Eucommiae Cortex) Extract Combination (ILF-RE) on Improvement of Liver Function. The Korea Journal of Herbology 2020:35(1):45–55.
75. Ha KC, Kim HM, Baek HI, Jeong DY, Kim E, Lee KH, et al. Effects of Unripe Rubus Coreanus Extract on Upper Body Obesity:A Randomized, Double-Blind, Placebo-Controlled Clinical Trial. Journal of Korean Medicine Rehabilitation 2021:31(4):117–27.  76. Kong HJ, Kang JH, Lee H. Efficacy and Safety of Cheong-A-Won Gagambang (JCE003) on Knee Osteoarthritis:Randomized Controlled Pilot Trial. Journal of Acupuncture Research 2022:39(3):202–12.   77. Hong CY, Seo SG, Na SG, Cho HS, Lee MK, Jin MH, et al. Study on the Anti-stress Effect of Chenwangbosim-Dan Extract∘Fermented Rice Extract (GABA ː gamma-aminobutyric acid 30%) Complex :A double-blind, randomized, placebo-controlled study. The Korea Journal of Herbology 2023:38(2):1–7.
78. Lee JS, Ahn S, Lee KH, Kim JH. Korean translation of the CONSORT 2010 Statement:updated guidelines for reporting parallel group randomized trials. Epidemiol Health 2014:36:e2014029doi:10.4178/epih/e2014029.   79. 보건복지부. 2022년 한방 의료 이용 실태 조사 2023:46.
80. Jeong SH, Kim HS, Shin WC, Cho JH, Chung WS, Song MY. Trend of Pharmacopuncture Treatment on Obesity:Recent 10 Years. Journal of Korean Medicine for Obesity Research 2022:22(2):147–57.  81. Kim YY, Yoo JH, Lee SK, Lee SW. Quality Assessment of Randomized Controlled Trials using Herbal Remedies in Korea. Journal of Physiology &Pathology in Korean Medicine 2011:25(5):927–33.
Appendices
【Appendix Ⅰ】
Korean Translation of CONSORT-CHM 2017
|
대주제/소주제 |
항목 번호 |
2010 CONSORT 지침의 점검 항목 |
한약 치료를 위한 CONSORT 확충안의 부가항목 |
|
제목과 초록, 핵심어 (TITLE, ABSTRACT, and KEYWORDS) |
|
|
제목과 초록 (Title and Abstract) |
1a |
제목에 무작위 임상시험임을 밝힘 |
시험이 한의학적 변증, 서양 의학에서 정의한 질병, 또는 특정 한의학적 변증을 가진 서양의학에서 정의한 질병을 대상으로 하는지 여부에 대한 설명 (해당되는 경우) |
|
|
1b |
시험 설계, 방법, 결과, 결론을 구조적으로 요약(구체적인 지침을 위해, 초록을 위한 CONSORT 참고) [4,5] |
사용된 처방의 이름과 구성 및 적용된 한의학적 변증의 설명(Illustration)(해당되는 경우) |
|
|
1c |
|
“한약 처방” 및 “무작위 대조 시험”을 포함한 적절한 핵심어(keyword) 결정 |
|
|
서론 (INTRODUCTION) |
|
|
배경과 목적 (Background and Objectives) |
2a |
과학적 배경과 근거에 대한 설명 |
생체의학적 접근(approach) 및/또는 한의학적 접근(approach)에 대한 설명 |
|
|
2b |
구체적 목적 또는 가설 |
처방이 서양의학에서 정의한 질병, 한의학적 변증 또는 특정 한의학적 변증을 가진 서양의학에서 정의한 질병을 대상으로 하는지 여부에 대한 설명 |
|
|
방법 (METHODS) |
|
|
시험 설계 (Trial design) |
3a |
배정비율을 포함한 시험설계 서술 (예 : 평행설계, 요인설계) |
|
|
|
3b |
시험 개시 이후의 방법의 중대한 변화를 원인과 함께 기술 (예 : 적격기준) |
|
|
|
참가자 (Participants) |
4a |
참가자의 적격 기준 |
1) 진단 기준 2) 포함 및 배제 기준의 측면에서 특정 한의학적 변증을 가진 참가자가 모집되었는지 여부에 대한 설명. 사용된 모든 기준은 보편적으로 인정되는 것이거나, 자세한 설명이 포함되어 있는 참조문헌을 기재해야 함. |
|
|
4b |
자료가 수집된 조건과 장소 |
|
|
|
개입 (Interventions) |
5 |
각 군에 대한 개입에 대한 재현이 가능하도록 세부사항을 기술, 언제 그리고 어떻게 개입이 실제적으로 시행되었는지를 포함 |
다른 유형의 처방에 대한 설명에는 다음이 포함되어야 함 :
5a. 기존에 존재하는 처방을 그대로 활용하는 경우(for fixed CHM formulas)
1. 명칭, 출처
2. 각 약물의 명칭, 출처, 가공 과정, 용량. 약물의 명칭은 최소 2개 언어로 표시되어야 함 : 중문, 라틴어 또는 영어. 약재의 사용 부위(parts of the substances)의 명칭은 반드시 명료하게 표현되어야 함.xyb3. 각 성분의 인증 방법, 어떻게, 언제, 어디서, 그리고 누가 제조(conducted) 하였는지 ; 바우처 표본이 확보되었는지(retained), 확보된 경우 보관 위치 및 접근 가능 여부를 나타나는 문구
4. 처방을 구성하는 원리, 논거 및 해석
5. 처방의 유효성에 대한 참조(있는 경우)
6. 처방의 약리학적 연구 결과(있는 경우)
7. 처방의 생산 방법(있는 경우)
8. 각 재료 및 처방 제품(product)의 품질관리(있는 경우) 여기에는 정량적 및/또는 정성적 테스트 방법 ; 언제, 어디서, 어떻게, 누구에 의해 이러한 연구들이 수행되었는지; 원본 데이터와 샘플이 보관되었는지, 보관된 경우 접근 가능한지 등이 포함됨.
9. 처방의 안전성평가 ; 중금속 및 독성 성분, 잔류 농약, 미생물 한계기준(microbial limits) 및 급/만성 독성(있는 경우) 만약 독성이 있다면 이러한 연구가 언제, 어디서, 어떻게 그리고 누구에 의해 수행되었는지 ; 원본 데이터와 샘플이 보관되어 있는지 ; 보관되었다면 접근 가능한지를 명시해야 함.
10. 처방의 용량과 그 용량이 어떻게 결정되었는지
11. 투여 경로(예. 경구, 외용) 5b. 개별 한약 처방(for individualized CHM formulas)
1. 5a 1-11 참고
2. 추가 정보 : 어떻게, 언제 그리고 누가 처방을 수정(modified)하였는지
5c. 특허가 출원된(patent proprietary) 한약 처방
1. 공개적으로 사용 가능한 물질에 대한 참조(reference), 처방의 약리학, 조성, 용량, 효능, 안정성, 품질관리 등
2. 처방의 세부 사항에 대한 설명(Illustration) 즉
1) 제품명 (예 : 브랜드 명)
2) 제조사
3) 롯 번호(lot number)
4) 생산 날짜 및 유통 기한(expiry date)
5) 첨가된 성분의 명칭 및 함량(백분율) 또한
6) 추가적인 품질 관리 조치가 수행되었는지 여부
3. 시험에 사용된 특허 소유 처방이 공개적으로 사용 가능한 처방과 동일한 조건인지에 대한 진술
5d. 대조군 플라시보 대조군
1. 명칭과 각 성분의 용량
2. 위약과 개입의 유사성에 대한 설명(예 : 색상, 냄새, 맛, 외관, 포장)
3. 품질관리 및 안전성 평가(있는 경우)
4. 투여 경로, 투여과정/레지맨(regimen), 용량
5. 생산 정보 : 위약이 어디서, 언제, 어떻게, 누구에 의해 생산되었는지 능동 대조군
1. 한약 처방을 사용한 경우 권장 사항 5a-5c 참조
2. 화학 약품이 사용된 경우, CONSORT의 5번 항목 참조 |
|
|
결과 (Outcomes) |
6a |
미리 지정되고 완전히 정의된 일차결과와 이차결과, 어떻게 그리고 언제 평가되는지를 포함 |
변증의 세부 사항을 표기한 결과와 측정에 대한 설명(Illustration) |
|
|
6b |
시험이 개시된 후의 시험 결과의 변경을 원인과 함께 기술 |
|
|
|
대상수 (Sample size) |
7a |
어떻게 대상수가 결정되었는지 |
|
|
|
7b |
필요하다면, 중간평가나 중단기준에 대한 설명 |
|
|
|
무작위 배정 서열 생성 (Randomization Sequence generation) |
8a |
무작위배정서열을 생성하기 위해 쓴 방법 |
|
|
|
8b |
무작위배정방법의 종류; 제한사항을 구체적으로 기술(예를 들어 블록 여부와 블록 크기) |
|
|
|
은폐 방법 (Allocation concealment mechanism) |
9 |
무작위배정서열을 시행하기 위해 쓴 방법(예를 들어 연속적으로 숫자가 기입된 봉투), 개입에 배정되기까지 서열을 은폐하기 위해 시도한 조치를 기술함 |
|
|
|
시행 (Implementation) |
10 |
무작위배정서열을 생성하는 주체, 참가자를 등록하는 주체, 그리고 참가자를 개입에 배정하는 주체 |
|
|
|
눈가림 (Blinding) |
11a |
만약 눈가림이 행해졌다면, 개입에 배정 후 누구에게 눈가림이 유지되었으며(예 : 참가자, 의료 관계자, 결과 분석자) 그리고 어떻게 |
|
|
|
11b |
필요하다면, 개입의 유사성을 기술 |
|
|
|
통계적 방법 (Statistical methods) |
12a |
일차 결과와 이차 결과를 위해 군들을 비교하기 위한 통계적 방법 |
|
|
|
12b |
하위군 분석, 보정 분석과 같이 추가적 분석을 위한 방법 |
|
|
|
연구 결과(RESULTS) |
|
|
참가 흐름도 (그림을 그릴 것을 강하게 권고) (participants - a diagram is strongly recommended) |
13a |
각 군당, 무작위배정된 참가자 수, 의도한 치료를 받은 참가자 수, 일차 결과를 위해 분석된 참가자 수 |
|
|
|
13b |
각 군당, 무작위배정 후 탈락과 제외를 원인과 함께 기술 |
|
|
|
모집 (Recruitment) |
14a |
모집 기간과 추적관찰 기간의 시작 날짜와 종료 날짜 |
|
|
|
14b |
시험이 종료되거나 중단된 이유 |
|
|
|
시작지점 자료 (Baseline data) |
15 |
각 군의 시작 시점에서의 인구학적, 임상적 특성을 보여주는 표 |
|
|
|
분석된 수 (Numbers analyzed) |
16 |
각 군당, 각 분석에 포함된 참가자 수를 기술하고 처음 배정된 군에 따라 분석되었는지 여부를 기술 |
|
|
|
결과와 추정 (Outcomes and estimation) |
17a |
각 일차 결과와 이차 결과에 대해, 군당 연구결과와 추정된 유효크기와 정밀도(예를 들어 95% 신뢰구간)를 기술 |
|
|
|
17b |
이분형 결과변수의 경우, 절대적인 유효크기와 상대적인 유효크기를 표현할 것을 권고 |
|
|
|
부차적 분석 (Ancillary analyses) |
18 |
하위군 분석과 보정 분석을 포함한 추가적 분석에 대한 연구결과를 기술하고 사전에 미리 지정된 분석인지 탐색적 분석인지 구분할 것 |
|
|
|
위해 (Harms) |
19 |
군별로 모든 중대한 위해나 의도치 않은 부작용을 기술(구체적인 지침을 위해, 위해를 위한 CONSORT 참고 [6] |
(이 항목에는 해당되는 확장안이 존재하지 않음) |
|
|
고찰 (DISCUSSION) |
|
|
한계 (Limitations) |
20 |
시험의 한계, 잠재적인 바이어스나, 비정밀도, 필요하다면 다중분석의 문제 |
|
|
|
일반화 (Generalizability) |
21 |
시험의 발견이 일반화 가능한지(외적 타당성, 응용가능성) |
처방이 한의학적 변증이나 질환에 어떻게 작용하는지에 대한 논의 |
|
|
해석 (Interpretation) |
22 |
결과와 일치하고, 편익과 위해가 균형을 유지하며, 관련 있는 다른 증거들을 고려하고 있는 해석인지 |
한의학 이론 해석 |
|
|
다른 정보(OTHER INFORMATION) |
|
등록 (Registration) |
23 |
등록번호와 시험등록명 |
|
|
|
연구계획서 (Protocol) |
24 |
필요하다면, 어디서 연구계획서 전문을 확인할 수 있는지 |
|
|
|
연구비 (Funding) |
25 |
연구비의 출처와 다른 지원(예를 들어 약제의 조달) 및 재정지원자의 역할 |
|
|
|















