I. 서 론
천식은 여러 세포 및 세포인자가 작용하여 생긴 기도의 만성 염증질환이다1. 대부분의 기류 장애는 가역적이나 천식이 적절히 치료되지 않고 오래 지속되면 폐기능이 저하되고, 비가역적인 기도폐쇄가 발생할 수 있다2,3.
나라별 천식의 유병률은 1-18%로 다양하나, 전 세계적으로 2억 3천만명 이상이 천식으로 고통 받고 있으며 2015년 천식으로 인한 사망자가 38만 여명에 이를 정도로 천식은 전 세계적으로 중요한 공중 보건 문제가 되고 있다4,5.
한의학적으로 천식은 발작적으로 호흡이 喘促하고, 喉間에서 哮鳴이 나는 哮喘證과 유사한 질환으로 분류되며 寒冷, 痰, 心因, 素因, 과민성 반응 등이 그 원인이 된다. 哮喘證은 外感風寒과 痰濕內盛의 實證과 肺虛, 心腎虛損, 上實下虛의 虛證으로 辨證하여 祛風散寒, 燥濕化痰, 養肺定喘, 補益心腎 등의 치법을 사용한다6.
厚朴麻黃湯(Hubakmawhang-tang, HMT)은 ≪金匱要略≫에서 “咳而脈浮者 厚朴麻黃湯主之”라고 기술되었으며7, ≪千金要方≫에서도 “咳而大逆上氣 胸滿 喉中不利 爲水鷄聲 氣脈浮者 厚朴麻黃湯方”이라 하여 風寒邪로 인해 脈이 浮하고 咳嗽하며 上氣되고 가슴이 답답하며 목이 불편하며 水鷄聲이 들리는 증상에 사용되었다8. 상기 증상은 哮喘證의 ‘呼吸促急 喉中有聲響’한 특징과 유사하며 外感風寒으로 인해 심한 기침 증상을 보이는 哮喘證에 HMT을 처방한 것을 유추해 볼 수 있다9.
최근 다양한 單味10,11 및 處方12,13을 사용하여 동물 천식 모델에 대한 염증반응이나 면역기능의 변화를 관찰하는 실험이 이루어지고 있다. HMT의 구성 약재 중 半夏14, 麻黃15, 杏仁16, 細辛17, 五味子18는 이전의 동물 실험에서 천식에 대한 효과가 확인되었다. 각 약재의 약리작용을 기반으로, HMT은 교감신경 흥분을 통한 기관지 확장, 부종 완화 및 진해작용을 한다고 알려져 있고, 완고한 기침 및 기관지 천식에 사용되고 있다19. HMT에 대한 기존 연구로 서20의 厚朴麻黃湯 및 그 성분인 magnolol이 인간 폐암 세포주에 미치는 항암 활성 실험이 있으며 현재까지 천식에 대한 HMT에 대한 연구는 미비한 실정이다.
이상과 같이 사람의 천식에 사용되는 처방인 HMT에 대하여 생쥐에 유발된 천식의 각종 지표들을 개선해 줄 수 있을 것이라는 가설을 세우고 본 실험을 진행하였다.
II. 재료 및 방법
1. 재 료
1) 동 물
7주령된 수컷 48마리 Balb/c 생쥐를 샘타코(오산, 한국)에서 구입하였다. 일주일 동안 실험실 환경에 적응시킨 후 온도와 습도가 조절되는 환경(24±3 °C, 12-hr light-dark cycle)에서 고형 사료와 물을 자유로이 섭취하게 한 생쥐를 사용하였다.
2) 약재의 준비
HMT는 ≪金匱要略≫7의 처방 구성에 준하여 조제하여 사용하였으며, 모든 약재는 동신대학교 목포 한방병원에서 구입하여 사용하였다.
Table 1
Prescription of Hubakmahwang-tang (HMT)
3) 시약 및 기기
천식을 유발하기 위한 난황(OVA, Ovalumin, Grade V)은 Sigma(St. Louis, USA)에서 구입하였으며, aluminum hydroxide(Alum, Imject Alum, Pierce)은 진텍(광주, 한국)을 통해 구입하였다. 항원 특이 전체 항체를 측정하기 위한 Goat anti-mouse polyvalent immunoglobulin은 Sigma(St. Louis, USA)를 통하여 구입하였고, IgE, IgG1, IgG2a에서 항원특이 항체를 검출하기 위한 Rat anti-mouse IgE antibody, Goat anti-mouse IgG1 antibody와 Goat anti-mouse IgG2a antibody는 Southern Biotech(Birmingham, USA)를 통하여 구입하였다. 기관지 폐포 세척액과 혈청 내 Cytokine을 측정하기 위한 mouse IL-4와 mouse IFN-g detection Kit는 eBioscience(San Diego, USA)를 통하여 구입하였다20. Optical Density(OD) 값의 측정하기 위해 microplate reader(Bio-rad, CA)를 사용하였고, 폐조직의 조직병리학적 소견 관찰을 위하여 광학 현미경(Olympus, Japan) 100x를 사용하였다.
2. 방 법
1) 약물의 준비
정선된 약재 98 g을 70% 에탄올 1,000 ml에 浸漬시킨 후, 15분간 초음파로 진탕하고, 히팅 멘틀(LKLab Korea, 한국)을 이용하여 60도에서 3시간 동안 추출하여 추출액을 얻었다. 얻어진 추출액은 거즈와 와트만지(No. 20)로 거른 다음 감압증류기(EYELA, Japan)를 이용하여 감압 증류하고 동결건조기(일신, 한국)를 이용하여 동결건조 하였다. 이렇게 하여 얻어진 추출물(HMT)은 6.3 g으로 수율은 6.42%였다.
2) 천식 유발과 군 분리
100 μg의 난알부민(OVA, Sigma)과 2 mg의 aluminium hydroxide을 용매 100 μl(PBS, phosphate buffer saline)에 녹여서, 3일간 생쥐의 복강에 주사하여 감작(Sensitization)시켰다. 2주 뒤 생쥐를 럼푼(10 mg/kg)과 졸레틸(100 mg/kg)으로 마취시키고 난 후, 비강 내 점적(Intra-nasal instillation) 방법20,21으로 천식을 유발하였다. 비강 내 점적시키기 위하여 25 μg의 난알부민을 30 μl의 PBS에 녹인 다음, 2일 간격으로 1회씩 총 4일간 비강 내 점적을 시행하였다. CO2 가스를 이용해 쥐를 희생시켰으며 자세한 실험의 스케줄은 Fig. 1에 제시하였다. HMT는 구강투여를 위하여 증류수에 4, 8, 16 mg/ml 농도로 녹인 다음, 7일간 100, 200, 400 mg/kg 농도로 투여하였다. 투여 농도는 인간(60 kg)의 1일 투여 용량, 수율 그리고 생쥐의 체중을 감안하여 결정하였다. 각각의 실험군을 정리하면 아래와 같다.
(1) 정상군(Normal group, NOR) : 천식을 유발하지 않고 용매(증류수)만 경구 투여한 군
(2) 천식 대조군(Asthma control group, CTL) : 천식을 유발시키고, 용매(증류수)만 경구 투여한 군
(3) 저농도 투여군(100 mg/kg treated group, LOW) : 천식을 유발시키고 100 mg/kg 농도의 HMT를 경구 투여한 군
(4) 중농도 투여군(200 mg/kg treated group, MID) : 천식을 유발시키고 200 mg/kg 농도의 HMT를 경구 투여한 군
(5) 고농도 투여군(400 mg/kg treated group, HIG) : 천식을 유발시키고 400 mg/kg 농도의 HMT를 경구 투여한 군
(6) 프레드니솔론 투여군(prednisolone treated group, PRE) : 천식을 유발시키고 10 mg/kg 농도의 prednisolone을 경구 투여한 군
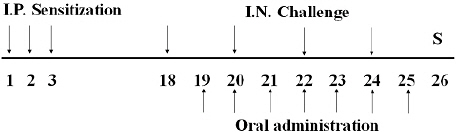
Fig. 1
Experimental schedule.
All experimental groups, except normal control group, were sensitized intra-peritoneally on days 1, 2 and 3 and challenged intra-nasally at days 18, 20, 22 and 24. Animals were treated with HMT from days 19 until 25. All animals were sacrificed on day 26. I.P. : intra-peritoneal, I.N. : intra-nasal, S. : sacrifice
3) 체중 변화 및 비장 무게 측정
실험 첫 날 생쥐의 체중을 측정하고, 이후 5일 간격으로 체중을 측정하였다. 각 군의 평균 체중은 첫 날 측정한 체중에 대한 백분율로 나타내었다. 비장 무게 측정을 위하여 실험 마지막 날 CO2 가스를 이용해 생쥐를 희생시키고, 복강에서 비장을 절제 하였다. 미량저울(Sartorius, 한국)을 이용하여 절제된 비장의 무게를 측정하고, 이를 체중에 대한 비장의 무게비로 나타내었다.
4) 기도 과민성 측정
Methacholine에 대한 기도 과민성은 실험 마지막 날 whole body plethysmograph(Allmedicus, Korea)를 이용하여 측정되었다. 실험 과정을 간단히 요약하면 nebulizer(HARVARD73-1963, HARVARD, Massachusetts, USA)를 이용하여 PBS에 0, 12.5, 25, 50 mg/ml 농도로 녹인 methacholine을 생쥐에 150초간 노출 시킨 다음, 즉시 chamber로 이동하여 150초 동안 생쥐의 호흡 양상을 모니터링 하였다. Penh(enhanced pause)값은 150초 동안 측정된 expiration time, relaxation time, peak expiratory flow rate, peak inspiratory flow rate를 이용하여 계산하였으며, 계산식은 아래와 같다21.
Penh = (Te/RT-1)×PEF/PIF
Te : expiration time (sec)
RT : relaxation time (sec)
PEF : peak expiratory flow rate (ml/s)
PIF : peak inspiratory flow rate (ml/s)
5) 폐 조직의 조직병리학적 소견 관찰
7일간의 HMT 투여가 끝나고 기관지폐포 세척액을 얻은 다음, 폐 조직을 적출하였다. 10% 포르말린에 적출된 폐조직을 3일간 담가둔 후, Xylen을 이용하여 탈수시켰다. 탈수된 조직으로 파라핀 블록을 만들고, 그 블록을 다시 박절하여 슬라이드 글라스에 부착시켰다. Hematoxylin과 eosin으로 염색하여 광학 현미경(Olympus, Japan) 100x로 관찰하였다.
6) 기관지폐포 세척액(BALF) 회수 및 면역 세포 계산
실험 마지막 날 생쥐를 희생시켜서 경부를 절개하고 기관지의 연골사이를 절개하여 개방하였다. 도관(Insyte, BD)을 연골사이로 삽입하여 기관지폐포 세척액(BALF)을 얻었다. 1회 세척당 PBS 1.5 ml를 조심히 밀어 넣어 최소 1 ml 이상의 세척액을 채취한 것만을 data로 사용하였다. 얻어진 세척액은 염증세포의 수를 측정하는데 사용되었다. BALF 내에 존재하는 각종 면역 세포의 개수를 확인하기 위하여 cyto-spin(Thermo, USA)을 이용하여 면역 세포들을 슬라이드 글라스에 부착시킨 후 hematoxylin과 eosin으로 염색하여 광학 현미경 (Olympus, Japan) 100x로 관찰하였다.
7) 항체의 측정
심장 천자로 얻은 혈청으로부터 IgE, IgG1 및 IgG2a의 함량을 측정하기 위해 ELISA 방법을 사용하였다. 심장 천자로 얻은 혈액을 5,000 rpm에서 10분간 원심분리하였다. 남은 찌꺼기는 버리고 혈청을 얻었으며, ELISA 방법을 사용하기 위하여 Mouse IgE, IgG1, IgG2a ELISA Kit(abcam, 한국)를 이용하였다. 방법을 간단히 정리하면 kit와 함께 제공된 96-well plate를 비특이적인 결합을 방지하기 위하여 1%의 탈지 분유(Skim milk)를 섞고 Blocking을 시행하였다. 세척용 완충액으로 혈청을 10배로 희석한 후, 각 well당 100 μl씩 분주하여 4 °C에 하룻밤 동안 방치하였다. 하룻밤 동안 1차 항체 결합이 끝나면 완충용 세척액으로 세 번 수세하고, 2차 항체를 부착시켰다. 결과 값(OD, Optical density)은 Microplate spectrophotometer(Bio-rad, CA)를 사용하여 405 nm에서 측정하였다.
8) Cytokine 측정
천식이 유발된 생쥐로부터 떼어 낸 폐 조직을 조직 분쇄기(인트론, 한국)를 이용하여 분쇄하였으며, lysis buffer(Sigma, USA)를 이용하여 단백질을 분리하였다. 분리된 단백질을 정량하는데 bicinchoninic Acid(BCA) 방법을 이용하였다. 정량이 끝난 단백질에서 IL-4과 IFN-g의 함량은 ELISA 방법을 이용하여 측정하였다. Cytokine 함량은 mouse IL-4 detection kit(eBioscience, USA)와 mouse IFN-g detection Kit (eBioscience, USA)를 사용하여 측정하였고, kit와 함께 제공된 지침에 따라 실험을 진행하였다.
III. 결 과
1. 체중 변화에 미치는 영향
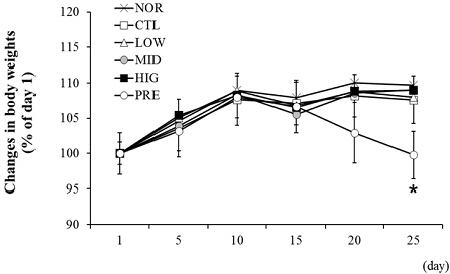
재료 및 방법에서 논술한 것과 같이 천식 유발 당시부터 1주간의 약물투여가 끝날 때 까지 체중 변화를 관찰한 결과 천식 대조군(CTL)과 HMT 투여군 모두에서 정상군(NOR)과 특별한 체중의 변화를 관찰할 수 없었다. 반면 프레드니솔론 투여군(PRE)에서 체중이 감소하였다(P<0.05)(Fig. 2).
Fig. 2
Effects of HMT on changes in body weights.
Body weights were measured from the beginning (day 1) to day 25 of experiment. Changes on body weights were represented as ratio of average weights indicated days to weight on day 1. Results are presented as mean±SD (n=8). *P<0.05 vs. CTL NOR : normal group, CTL : Asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group
2. 기도 과민성에 미치는 영향
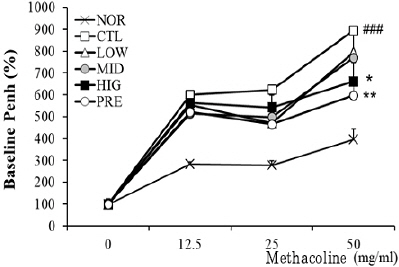
재료 및 방법에서 서술한 것과 동일하게 methacholine에 대한 기도 과민성을 측정하였으며, 그 결과 천식 대조군에서 methacholine의 농도에 의존적으로 Penh 값이 증가하였다. 고농도 투여군(HIG)에서 Penh 값이 감소하였으며(P<0.05), 프레드니솔론 투여군에서도 감소하였다(P< 0.01)(Fig. 3).
Fig. 3
Effects of HMT on Penh value in asthmatic mice.
Penh values were measured using whole body plethysmograph on day 25. Results are presented as mean±SD (n=8). ###P<0.001 vs. NOR, *P<0.05 and **P<0.01 vs. CTL NOR : normal group, CTL : Asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group
3. 폐 조직의 조직병리학적 소견에 미치는 영향
실험 마지막 날 생쥐를 희생시키고 기관지폐포 세척액을 얻은 다음 폐 조직의 일부를 적출하여 육안적으로 관찰한 결과 천식 유발군에서 면역 세포 침윤을 위주로 하는 염증 소견이 발견되었고, 고농도의 HMT 투여는 이러한 염증 소견을 억제하는 경향성을 보였다. 정상군에서는 염증세포가 기관지 및 혈관 주변을 침윤하고 조직을 손상시키는 염증 소견이 관찰되지 않았으며, 기관지 벽의 비후도 관찰되지 않았으나, 천식 대조군에서는 기관지벽의 비후가 관찰되었다. HMT의 투여는 이러한 기관지 벽의 비후 역시 억제하는 경향을 보였다. 양성 대조군으로 쓰인 프레드니솔론 군의 혈관 주위로 소량의 면역 세포 침윤이 관찰되었으며, 기관지 벽의 비후 현상은 관찰되지 않았다(Fig. 4).
Fig. 4
Effects of HMT on histopathological changes of the lung tissue in asthmatic mice.
The lung tissues were stained with hematoxylin and eosin. Sections were examined under the light mircoscope. (A) NOR : normal group, (B) CTL : Asthma control group, (C) LOW : 100 mg/kg of HMT treated group, (D) MID : 200 mg/kg of HMT treated group, (E) HIG : 400 mg/kg of HMT treated group, (F) PRE : 10 mg/kg of prednisolone treated group (×100).

4. 기관지폐포 세척액 내 세포수에 미치는 영향
생쥐의 기관지를 세척하여 얻은 세척액(BALF) 내에 존재하는 각종 면역 세포의 수를 확인한 결과 대조군에서 유의한 수준의 세포수 증가가 관찰되었는데, 대표적으로 대식세포(macrophage), 호중구(neutrophil), 호산구(eosinophil) 그리고 분류되지 않는 림프구(Lymphocyte) 등이었다. 고농도의 HMT 및 프레드니솔론 투여는 대식세포, 호중구, 호산구 및 총 세포수를 감소시켰으며(P< 0.05), 중등도 HMT 투여는 총 세포수와 대식세포의 수를 감소시켰다(P<0.05)(Fig. 5).
Fig. 5
Effects of HMT on cell count in BALF.
Cells in BALF were counted based on morphological characteristics. Results are presented as mean±SD (n=8). ###P<0.001 vs. NOR, *P<0.05 vs. CTL NOR : normal group, CTL : Asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group

5. 혈청 내 IgE, IgG1, IgG2a 함량에 미치는 영향
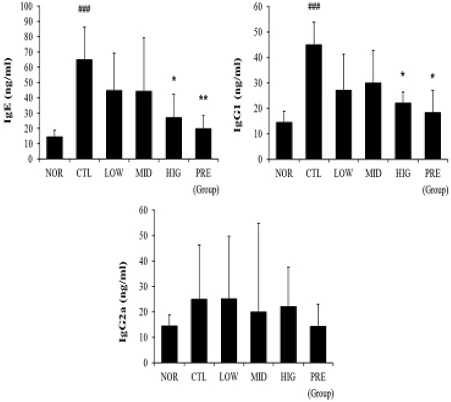
생쥐로부터 얻은 혈액에서 분리한 혈청 내 IgE 항체, 항원 특이 IgG1 항체, IgG2a 항체의 함량 변화를 측정하였다. 천식 유발군에서 정상군에 비하여 유의한 IgE 항체 함량 증가가 있었다. 이러한 증가는 고농도 HMT 투여에 의해 감소하였으며(P<0.05) 프레드니솔론 투여에 의해서도 감소하였다(P<0.01). 천식 유발군에서 항원 특이 IgG1 항체 함량 또한 정상군에 비하여 유의한 증가가 관찰되었다. 이러한 증가는 고농도 HMT 투여와 프레드니솔론 투여에 의하여 감소하였다(P<0.05). 그러나 모든 실험군에서 IgG2a 항체에 대한 유의할만한 변화가 관찰되지 않았다(Fig. 6).
Fig. 6
Effects of HMT on IgE, IgG1, IgG2a level in serum.
IgE, IgG1, IgG2a level in serum were measured using ELISA methods. Results are presented as mean±SD (n=8). ###P<0.001 vs. NOR, *P<0.05 and **P<0.01 vs. CTL NOR : normal group, CTL : asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group
6. 폐 조직 내 IL-4 수준에 미치는 영향
천식이 유발된 생쥐의 폐 조직에서 IL-4 수준의 변화를 측정한 결과, 천식 유발군에서 정상군에 비하여 유의한 IL-4 함량의 증가가 관찰되었고, 이러한 증가는 고농도 HMT와 프레드니솔론 투여에 의하여 감소하였다(P<0.05)(Fig. 7).
Fig. 7
Effects of HMT on IL-4 level and IFN-g level in lung tissue.
IL-4 level and IFN-g level in serum were measured using ELISA methods. Results are presented as mean±SD (n=8). ###P<0.001 vs. NOR, *P<0.05 vs. CTL NOR : normal group, CTL : asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group
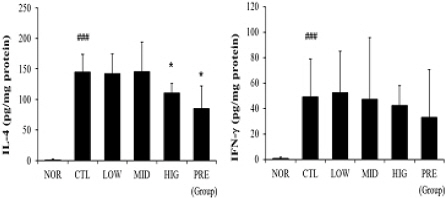
7. 폐 조직 내 IFN-g 수준에 미치는 영향
천식이 유발된 생쥐의 폐 조직에서 IFN-g 수준의 변화를 관찰한 결과 대조군에서 유의한 수준의 IFN-g의 증가가 관찰되었으며, HMT 및 prednisolone은 IFN-g 수준에 유의한 차이를 보이지 않았다(Fig. 7).
8. 비장/체중의 무게 비율에 미치는 영향
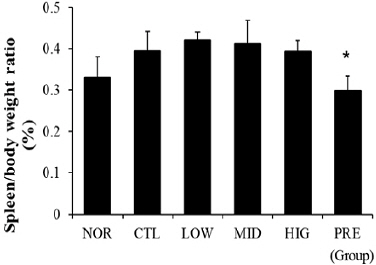
실험 마지막 날 비장을 적출하여 비장/체중의 무게 비율을 측정하였더니 천식 유발군에서 경미한 비장/체중의 무게 비율의 증가가 관찰되었다. HMT의 투여는 이러한 비장/체중의 무게 비율에 특별한 영향을 미치지 않았지만 prednisolone군에서는 비장/체중의 무게 비율이 감소되었다(P<0.05)(Fig. 8).
Fig. 8
Effects of HMT on spleen body weight ratio in asthmatic mice.
Spleen body weight ratio was calculated based on body weight measured on day 25 and spleen weight measured on day 26. Results are presented as mean±SD (n=8). *P<0.05 vs. CTL NOR : normal group, CTL : asthma control group, LOW : 100 mg/kg of HMT treated group, MID : 200 mg/kg of HMT treated group, HIG : 400 mg/kg of HMT treated group, PRE : 10 mg/kg of prednisolone treated group
IV. 고 찰
천식은 여러 세포 및 세포인자가 작용하여 발생한 기도의 만성 염증질환으로1, 조기에 적절한 약물치료와 적극적인 관리를 시행하면 질병 이환율 및 사망률을 감소시킬 수 있어 증상을 조절하고 유지하는 것이 천식의 치료 목표이다24.
기침은 水寒射肺로 인한 것으로 停水挾風한 자에게 厚朴麻黃湯을 처방한다고 ≪醫宗金鑑≫에 기술되어 있으며25, 이에서 HMT의 止咳平喘 효능은 風寒과 水飮을 發散시키고 降逆하여 나타난다고 해석할 수 있다. 구성 약재의 작용은 다음과 같다. 麻黃, 厚朴, 杏仁은 그득 찬 것을 풀어내고, 숨이 차고 上逆하는 기운을 내린다. 乾薑, 細辛, 五味子, 半夏는 寒飮을 제거하고 기침을 멈추게 하며 石膏는 수반된 煩熱을 식히고 小麥은 脾胃의 氣를 조화시키며 바르게 하는 작용을 한다7.
각 약재의 약리적인 작용을 살펴보면, 半夏와 麻黃 추출물은 천식과 관련된 염증세포와 사이토카인을 억제하여 Th2 반응을 저하시킨다고 보고되었으며14,15 杏仁은 호산구 생성과 IL-8에 대한 억제효과가 있고 細辛은 IL-4 등의 mRNA 발현을 억제하며, 五味子는 세포점착과 염증성 사이토카인을 억제하여 항천식 효과가 있다고 보고되었다16-18. 또한 厚朴의 함유물 중 magnolol과 honokiol이 기관지평활근에 대한 수축을 억제하며 乾薑의 정유 주성분도 기관지 염증 반응을 억제한다고 알려져 있다. 그 외에 황산칼슘수화물(CaSO4·2H2O)로 이루어진 石膏는 신경이나 근육의 흥분성을 억제하는 진정 및 진경작용을 하고 浮小麥은 단백질, lecithin, 전분, vitamin B 등이 영양분과 미네랄이 함유되어 있다26.
이와 같이 HMT는 문헌적으로 천식에 효험이 있다고 기술되고 천식 치료에 응용되어진 처방으로, 구성 약재 및 그와 유사한 처방에 대한 연구는 시행되었으나 아직까지 HMT의 천식에 대한 연구는 미비한 상황이다. 따라서 본 연구에서는 HMT의 천식 생쥐에 대한 기도과민성, 기도조직, BALF 내 면역세포, 면역 글로불린, cytokine 등의 변화를 살펴보았다.
본 연구에서는 비교적 최근에 알려진 비강 내 점적법(Intra-nasal instillation)을 활용하여 천식을 유발하였다. 비강 내 점적법은 종래의 분무법으로 각각의 동물에게 일정한 양의 항원을 전달할 수 없는 한계를 보완하여 고안된 방법이다22,23.
체중 변화로 실험동물의 전반적인 상태를 유추할 수 있으며, 동물을 이용한 여러 연구에서 체중 변화는 부작용으로 간주된다27,28. 본 연구의 결과에서 HMT의 투여는 체중 증가량에 특별한 영향을 미치지 않았다. 그에 반해 prednisolone은 마지막 체중 측정에서 유의한 수준의 체중 증가 억제 현상을 보였다(Fig. 2).
AHR(airway hyperresponsiveness)은 기도 과민성을 말하는 것으로 병리적으로 기도의 가역적 폐쇄와 폐 조직의 만성적인 호산구성 염증 소견을 대변하여 천식의 진단, 경과, 치료 결과 판정에 흔히 이용되는 지표이다29-31. 흔히 천식이 의심되는 환자에게 methacholine에 의한 AHR을 측정한다32. 본 연구의 결과에서 반복되는 난알부민의 처리로 methacholine에 대한 기도 과민성이 농도 의존적으로 증가하였다. HMT의 투여는 이러한 기도 과민성 증가를 농도 의존적으로 억제하였으며, 고농도 투여군에서 통계적으로 유의한 수준을 보였다(Fig. 3). 이러한 결과는 HMT가 천식 환자에게 사용되어 기도 과민성을 억제할 가능성이 있음을 시사한다.
천식환자 폐의 조직병리학적 소견의 특징은 혈관 주위 면역세포의 침윤을 대표적으로 하는 염증 소견과 기도 재형성(airway remodeling)의 주요 지표인 기관지 벽의 비후이다33. 본 연구의 결과를 살펴보면 대조군에서 혈관 주위로 많은 면역세포 침윤이 관찰되었으며, 기관지 벽의 비후 또한 관찰되었다(Fig. 4B). HMT는 이러한 면역세포 침윤 및 기관지벽 비후에 대해 농도 의존적인 개선효과를 보였으며 Prednisolone 군에서는 경미한 면역세포 침윤만이 관찰되었다(Fig. 4). 이러한 결과는 HMT가 폐 조직 내에서 항염증 작용을 통하여 면역세포 침윤과 기관지 비후를 방지한다는 근거로 볼 수 있다.
보다 정확한 면역세포 현황을 살펴보기 위해 기관지폐포 세척액(BALF) 내에 존재하는 면역 세포를 측정한 결과, 대조군에서 고농도의 HMT는 유의하게 증가한 대식세포와 호산구의 침윤에 대해 유의한 수준의 억제 효과를 발휘하였다(Fig. 5). 이러한 결과는 Fig. 4의 결과와 동일하게 HMT가 폐 조직 내에서 면역세포 침윤을 전반적으로 억제하였음을 시사한다.
항원 특이 항체(Antigen specific antibody)의 함유량과 기능성은 체액성 면역 기능 평가에 주요한 요소 중 하나이다34. IgE의 생성 레벨은 천식의 악화 및 호전의 주요 인자로서 천식의 중요한 치료 목표로 간주되었다35. 본 연구에서 고농도의 HMT 투여는 천식 유발로 인해 상승된 혈중 IgE 수준을 유의하게 감소시켰다(Fig 6). 이를 통해 HMT가 천식의 치료에 중요한 역할을 할 가능성을 유추할 수 있다.
천식은 Th2 반응에 의해 만성 염증 상태가 지속되는 질환이다36. 천식과 관련된 가장 중요한 항체는 IgE로 환자의 상당수에서 IgE가 상승되어 있으나, 천식의 유발과 악화에 관여하는 또 다른 항체들이 있다. 그 중 대표적인 것은 IgG 계열의 항체들이다. 특히 IgG1과 IgG2a는 T 세포 면역 반응의 Th1, Th2의 반응과 관련성이 있는 항체로 IgG1은 Th2 반응과, IgG2a는 Th1 반응과 관계가 깊다34. 본 연구에서, IgG1은 천식 유발로 인해 유의한 상승을 보였으나 IgG2a는 특별한 변화가 보이지 않았다. 상승된 IgG1은 HMT 투여에 의하여 유의하게 감소하였다(Fig. 6). 이러한 결과는 HMT의 항염증 반응은 Th2 반응을 억제하는 경향이 있으며, 이를 통해 천식 치료 효과를 보일 수 있음을 시사한다.
천식 환자에서 채취한 가래, 기관지 폐포 세척액에서 Th 2 driven cytokine인 IL-4 레벨은 정상인에 비해 상승되어 있다37-39. IL-4는 IgE의 생성을 촉진하고 Th2 반응을 진행하며 기도의 과민반응을 유발한다고 알려져 있는 인자이다40,41.
본 연구에서 천식 유발에 의해 폐 조직 내의 IL-4가 유의하게 상승하였으며, 이러한 상승은 HMT 투여로 효과적으로 억제되었다(Fig. 7). 그러나 유의하게 상승한 폐 조직 내 IFN-g 레벨에는 영향을 미치지 않았다(Fig. 7). 이 결과로부터 HMT는 IL-4 생성을 감소시켜 Th2의 반응을 억제시킴으로서 천식을 치료한다고 유추할 수 있다. 위의 결과는 항원 특이 항체 중에서 IgG1(Th 2 related antibody isotype)에 대한 영향과 일치한다.
비장 내에서 활성화된 B세포는 형질세포(plasma cell)가 되어 항체(antibody)를 생산한다. 따라서 일부 체액성 면역 기능 항진성 질환 및 이를 반영하는 실험 모델에서 비장종대로 인한 비장의 무게 증가를 관찰할 수 있다42,43. 본 연구에서는 천식 유발로 인해 비장/체중의 무게 비율이 증가하는 경향을 보였으나, 유의하지는 않았다. 또한 HMT를 투여해도 비장/체중의 무게 비율에 특별한 영향을 미치지 않았다. 그러나 prednisolone 투여군에서 유의한 수준의 비장/체중의 무게 비율의 감소가 관찰되었다(Fig. 8).
이를 종합하면 HMT가 천식 생쥐의 주요 병리가 되는 폐 조직 내의 염증세포의 침윤과 기관지 비후 등의 구조적 손상을 억제하고 기관지 과민성을 억제하며, 주요 면역반응 경로가 되는 Th2 반응에 관여하는 IgE, IgG1, IL-4를 감소시켜 천식의 염증 반응에 효과를 나타낼 수 있으리라 생각된다.
V. 결 론
생쥐에 난알부민(Ovalbumin)의 비강 내 점적(Intra-nasal instillation)21,22으로 천식을 유발하고 HMT을 투여한 후 생쥐의 체중 변화, 기도 과민성의 지표인 Penh value(enhanced pause), 조직병리학적 이상 소견, 기관지폐포세척액(BALF, Bronch- oalveolar lavage fluid)에서의 면역 세포수 변화, 면역 글로불린 함량과 cytokine 함량에 미치는 영향 그리고, 비장/체중의 무게 비율에 미치는 영향을 관찰하여 다음과 같은 결론을 얻었다.
1. 고농도의 HMT 투여는 50 mg/ml의 methacholine 농도에서 천식에 대한 Penh 값을 유의한 수준으로 감소하였다.
2. 고농도의 HMT 투여는 폐 조직 내에서 염증세포 침윤 및 기관지 비후를 억제하는 경향을 보였다.
3. 중등도의 HMT 투여는 기관지폐포세척액 내의 대식세초와 총세포수를 유의한 수준으로 감소시켰으며, 고농도의 HMT 투여는 대식세포, 호중구, 호산구 및 총 세포수를 유의한 수준으로 감소시켰다.
4. 고농도의 HMT투여는 혈청 내 IgE, IgG1 함량을 유의한 수준으로 감소시켰다.
5. 고농도의 HMT 투여는 폐 조직 내의 IL-4 함량을 유의하게 감소시켰다.
6. HMT투여로 인해 생쥐의 체중, 비장/체중의 무게 비율, 혈청 내의 IFN-g 함량에 유의성 있는 변화는 관찰되지 않았다.











