통합암치료를 적용한 난소암 뇌, 척추전이 환자의 5년 추적관찰 증례보고
Abstract
Objectives:
This long-term case report presents the case of an ovarian cancer patient with brain, cervical lymph node, and vertebral metastasis suppressed by traditional Korean medicine in combination with cytokine-induced killer (CIK) cell-based immunotherapy.
Methods:
The patient received acupuncture, moxibustion, GunChil-go, Hangam-dan, and CIK cell-based immunotherapy. The Eastern Cooperative Oncology Group and tumor markers were used to evaluate the treatment effects.
Results:
Integrative cancer treatment suppressed the progression of cancer, and the patient achieved eight-year survival. The performance status improved, and the tumor marker level was maintained.
Conclusions:
We suggest that an integrative cancer treatment that includes traditional Korean medicine can be a meaningful treatment option for advanced ovarian cancer.
Keywords: case report, integrative cancer treatment, ovarian cancer, traditional Korean medicine
I. 서 론
난소암은 치사율이 가장 높은 부인암으로, 5년 생존율이 64.7%로 유방암(93.8%), 자궁경부암(80.1%)에 비해 훨씬 낮은 것으로 보고되고 있다 1. 난소암의 약 15.7%는 국소 단계에서 진단되며, 약 58%는 전이된 단계에서 진단된다 2. 난소암은 증상이 특이하지 않아서 초기에 쉽게 놓칠 수 있고, 대부분의 경우에 진행된 단계에서 진단되어 예후가 나빠지는 경향이 있다 3,4. 5년 생존율은 초기에는 92.6%이나 전이된 단계에서는 30.2%로 감소한다 2. 난소암 4기는 5년 생존율이 11%에 불과하다고 알려져 있다 1. 난소암의 기본 치료 원칙은 수술과 항암화학요법이다. 수술을 통해 난소암의 진단과 병기 설정, 치료가 이루어지기 때문에 일부 예외적인 경우를 제외하고는 난소암 환자는 모두 수술을 받게 된다 5,6. 진행성 난소암에서는 일반적으로 최대한 종양감축술을 시행하고, 이후 platinum+taxane 항암치료를 시행한다 7. 난소암의 한방치료 관련한 국내 연구로는 옻나무 추출물이 세포 단위 연구에서 암세포의 사멸을 유발한다는 연구가 발표되었고 8, 동충하초 추출물이 세포 단위 연구에서 암세포의 성장을 억제한다는 연구가 보고되었다 9. 하지만 난소암의 재발 및 전이 억제를 목적으로 통합암치료를 적용하여 장기간 관찰한 증레보고는 현재까지 보고된 바가 없었다. 이에 전이성 난소암 환자가 본원에서 통합암치료를 통해 암세포의 진행을 억제하고, 8년 생존에 도달한 사례가 있어 이를 보고하는 바이다.
II. 증 례
본 연구는 대전대학교 천안한방병원 기관생명윤리위원회(IRB)에서 심의 면제 승인을 받았다(DJUMC –2023-BM-16).
1. 환 자 : ⃝⃝⃝(1967년, 여)
2. 진단명 : Ovarian cancer stage 4a
3. 진단일 : 2015년 8월(당시 48세)
4. 주소증 : Dyspepsia, oral take poor, general weakness, constipation
5. 과거력 : None
6. 가족력 : None
7. 현병력
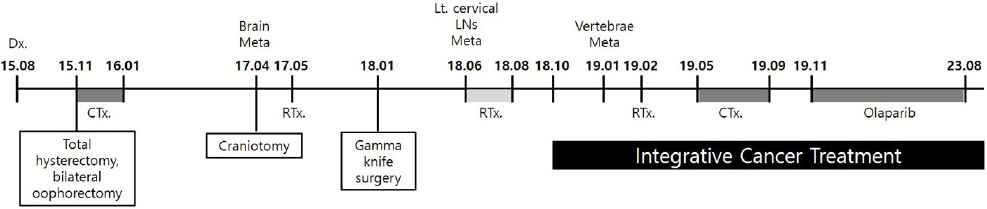
48세 여환 2015년 8월 천안 소재의 3차 의료기관에서 난소암 진단받고, 2015년 11월 서울 소재의 3차 의료기관에서 양측 난소 및 자궁 절제술을 받고, 항암치료를 8차까지 받았다. 2017년 4월 뇌전이 진단받은 후, 2017년 4월 개두술, 2017년 5월 방사선치료를 10차까지 받고, 2018년 1월 감마나이프 수술을 받았다. 2018년 6월 좌측 경부 림프절 전이를 진단받고 2018년 6월부터 8월까지 방사선치료를 30차 받았다. 2019년 1월 척추 전이를 진단받고 2019년 2월 방사선치료를 10차 받고, 2019년 5월부터 9월까지 항암치료를 6차 받았다. 그 후, 2019년 11월부터 2023년 11월까지 표적항암제인 올라파립 복용 및 중단을 반복했다( Fig. 1).
Fig. 1
Timeline of treatments and outcome.
Dx : diagnosis, CTx : chemotherapy, Meta : metastasis, RTx : radiotherapy, LN : lymphnode
8. 초진 검사소견
1) 혈액검사(2018년 10월 10일)
(1) Chemistry : Total protein 6.4(g/dL)/Na 134(mmol/L)
(2) CBC : WBC 3.23(10^3/μl)/RBC 3.76(10^6/μl) /Hemoglobin 12(g/dL)/ESR 30(mm/hr)
2) 소변검사 : 정상
3) 방사선검사
(1) Chest X-ray : 정상
4) EKG : 정상
9. 망문문절
1) 식욕 및 소화 : 방사선 치료 후 식욕저하로 일반식 1/2 2끼 섭취, 오심, 속쓰림
2) 대 변 : 1회/2일, 용력과다, 경변
3) 소 변 : 정상
4) 수 면 : 양호
5) 복용 약물 : 케프라정 500 mg 1T qd(B/pc)
10. 통합암치료 내용
본 증례의 환자는 2018년 10월 10일부터 2023년 11월까지 총 48회에 걸쳐 입원치료를 받았다.
1) 한의학 치료 : 침구 치료 및 면역세포 활성화를 위한 한방 면역 약물 치료(건칠정, 항암단)을 복용하였다.
(1) 침 치료 : 0.20 mm×0.30 mm 1회용 스테인리스 호침(동방메디컬, 한국)을 이용하여 입원 기간 동안 1일 1-2회 족삼리(ST36), 합곡 (LI4), 관원(CV4), 천추(ST25), 중완(CV12), 하완(CV10), 태충(LR3) 등에 15-20분간 유침하였다.
(2) 뜸 치료 : 신궐(CV8)을 중심으로 지름 25 cm인 4구 별뜸(힐링선, 한국)을 1일 1회, 30~60분 시행하였다.
(3) 항암단 : 2018년 10월부터 2023년 11월까지 입원기간 중 1일 3회 아침, 점심, 저녁 식후에 복용하였다( Table 1).
Table 1
Composition of Hangam-dan (1 Capsule 500 mg)
|
Herb |
Botanical name |
Amount (mg) |
|
三七根 extract |
Root of Panax notoginseng
|
246.875 |
|
冬蟲夏草 extract |
Cordyceps sinesis Sacc
|
246.875 |
|
牛 黃 |
Bos taurus Linné var. domesticus Gmeli
|
1.25 |
(4) 건칠고 : 2018년 10월부터 2019년 1월까지 입원기간 중 1일 2회 아침, 저녁 식후에 총 2번 복용하였고, 2019년 7월부터 2023년 11월까지 입원기간 중 1일 3회 아침, 점심, 저녁 식후에 복용하였다( Table 2).
Table 2
Composition of Gunchil-go (1 Pack 10 g)
|
Herb |
Botanical name |
Amount (g) |
|
乾漆 extract |
Rhus verniciflua stok
|
4 |
|
沈香 |
Aquilariae Agallochae Lignum Resinatu
|
0.05 |
2) 이뮨셀-엘씨주(Immuncell-LC, 지씨셀, 한국) : 환자에게서 약 100-150 ml의 혈액을 채혈하여 2-3주 동안 항암면역세포 중 cytotoxic T cell (CTL)과 cytokine induced killer cell(CIK)을 선택적으로 배양한 후 극대화된 면역 세포를 다시 환자에게 투여하는 치료법으로 총 40회 주입하였다.
11. 치료경과
2018년 10월 내원 당시 난소암 진단으로 수술, 항암화학요법, 뇌전이로 수술, 방사선 치료, 이후 경부 림프절 전이로 방사선 치료 후 상태였다. 2018년 12월 CT 검사상 이상소견 없었으나( Fig. 2), 2019년 1월 척추전이 발견되어 방사선치료와 항암화학요법 시행하였다. 2019년 9월경 영상검사상 육안적으로 확인되는 종괴 및 전이 없었으며 2023년 8월까지 상태 유지되어 올라파립 복용 중단 후 경과관찰하기로 하였다.
Fig. 2
2018.12.25 CT total hysterectomy, bilateral oophorectomy. 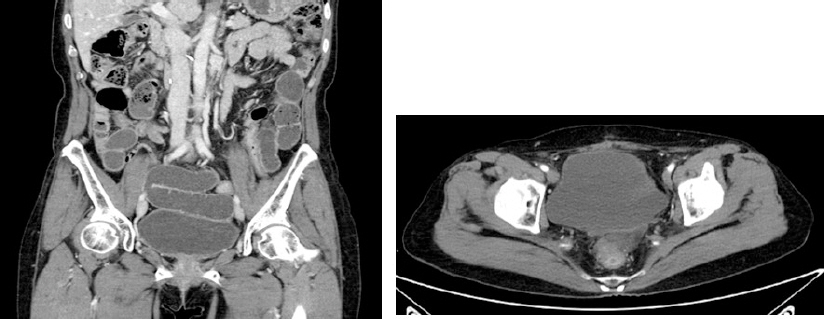
1) 종양표지자 검사 : 난소암 종양표지자인 Cancer Antigen 125(CA125)와 Carbohydrate antigen72-4 (CA72-4)를 측정하여 치료에 대한 변화를 관찰하였다. CA125는 처음 시행한 2019년 7월 15일 8.3 U/mL에서 2022년 12월 13일 8.3 U/mL으로 수치를 유지하였다. CA72-4는 처음 시행한 2019년 7월 15일 1.6 U/mL에서 2022년 4월 20일 5.6 U/mL으로 증가하였으며, 소폭 증가와 감소를 반복하다가, 2022년 5월 27일 87.8 U/Ml로 수치가 증가하였으나 영상 검사를 참조하여 재발 소견은 아닌 것으로 확인되었으며 2022년 12월 13일 4.6 U/mL으로 정상 수치 내로 감소하였다( Table 3).
Table 3
Change of Tumor Marker Level
|
2019 |
2021 |
2022 |
Normal range |
|
|
07.15 |
08.08 |
06.02 |
07.08 |
07.22 |
01.05 |
03.03 |
04.20 |
05.20 |
05.27 |
12.13 |
|
CA125 |
8.3 |
9.6 |
7.5 |
7.4 |
7.4 |
8.1 |
7.5 |
8.6 |
7.5 |
7.9 |
8.3 |
0-35 |
|
CA72-4 |
1.6 |
8.0 |
1.4 |
2.6 |
6.5 |
19.5 |
4.7 |
5.6 |
54.0 |
87.8 |
4.6 |
0-6.9 |
2) Eastern Cooperative Oncology Group Performance Status(ECOG PS) : 암 환자의 일상생활 활동 수준과 증상을 평가하기 위한 측정도구로 환자의 상태를 0~5점으로 구분하는 ECOG PS를 통해 환자의 전신수행상태를 평가하였다. 최초 내원 당시 거듭된 수술과 방사선 치료, 항암화학요법 후 생긴 기력저하 및 동반 증상들에 의해 ECOG Grade 2로 자가 보행은 가능하나 일상생활은 정상 활동수준의 50% 정도로 저하된 상태로 입원하였으나 통합 암 치료 후 ECOG Grade 1으로 일상 활동이 가능한 수준으로 호전되었다.
12. 부작용
치료 기간 중 여러 차례 시행한 간기능 수치인 AST와 ASL는 2018년 12월 21일 소폭 상승하였으나 이후 정상 범위 내를 유지하였다. BUN과 Creatinine 수치 또한 정상 범위 안에서 유지되어 신독성을 나타내지 않았다. WBC와 ANC, Hb와 PLT는 항암화학요법 시행에 따라 변화하였으나 그 외엔 처음 입원 시와 비슷하게 정상 범위 내, 또는 그 보다 약간 낮은 상태를 유지하였다( Table 4).
Table 4
|
2018 |
2019 |
2021 |
2022 |
Normal range |
|
|
10. 10 |
11. 27 |
12. 21 |
07. 15 |
08. 08 |
08. 26 |
12. 03 |
06. 02 |
07. 08 |
07. 22 |
01. 05 |
03. 03 |
04. 20 |
05. 20 |
12. 13 |
|
AST |
24 |
31 |
46 |
22 |
20 |
22 |
19 |
20 |
20 |
20 |
26 |
26 |
23 |
20 |
29 |
0-31 |
|
ALT |
20 |
17 |
38 |
20 |
19 |
17 |
15 |
15 |
16 |
13 |
21 |
16 |
14 |
13 |
22 |
0-34 |
|
BUN |
14.8 |
10.1 |
10.7 |
17.0 |
18.6 |
12.3 |
9.0 |
16.1 |
11.2 |
9.7 |
12.2 |
11.5 |
15 |
10.7 |
8.3 |
7-20 |
|
Cr |
0.70 |
0.74 |
0.80 |
0.80 |
0.79 |
0.74 |
0.84 |
0.73 |
0.68 |
0.75 |
0.63 |
0.72 |
0.80 |
0.80 |
0.77 |
0.7-1.1 (~2019.12) 0.51-0.95 (2020.1~) |
|
WBC |
3.23 |
3.10 |
2.94 |
14.06 |
6.81 |
0.47 |
1.48 |
2.17 |
2.31 |
2.10 |
2.65 |
2.20 |
2.27 |
1.89 |
2.76 |
4-10 |
|
ANC |
1.96 |
1.80 |
1.55 |
13.01 |
6.37 |
0.08 |
0.65 |
1.02 |
0.94 |
0.93 |
1.20 |
1.09 |
0.96 |
0.70 |
1.45 |
1.57-5.95 |
|
Hb |
12.0 |
12.7 |
13.0 |
11.1 |
9.8 |
8.2 |
11.3 |
12.5 |
11.9 |
11.4 |
11.9 |
12.5 |
12.4 |
12.0 |
11.4 |
12-16 |
|
PLT |
191 |
225 |
211 |
147 |
221 |
31 |
97 |
130 |
171 |
140 |
147 |
141 |
155 |
99 |
162 |
150-450 |
III. 고 찰
2020년 국가 암 등록 통계에 따르면, 난소암 발생자 수는 10만 명 당 2016년에 2,690명, 2017년에 2,758명, 2018년에 2,953명, 2019년에 2,929명, 2020년에 2,947명으로 꾸준히 증가하는 추세이다 1. 대부분의 난소암은 발견 시 진행된 병기에서 확인되며, 종양의 완전한 절제를 위해 광범위한 수술이 흔히 시행된다 10,11. 이때 잔여 종양의 존재는 예후와 생존에 있어서 가장 중요한 인자로 작용한다 12. Paclitaxel은 난소암의 일차 항암 화학요법에서 사용되며, 골수억제 증상, 말초신경 독성, 과민증 및 탈모 등을 유발할 수 있다. 또한, carboplatin 또는 cisplatin은 투여 직후부터 48시간 이내에 심한 메스꺼움과 구토, 골수억제로 인한 호흡기 감염 증상, 기관지 분비물 증가, 설사, 피부 발진 및 구강점막 궤양 증상이 나타날 수 있다 13. 2018년 미국 FDA가 BRCA 돌연변이의 진행성 난소암의 1차 치료제로 표적 항암 치료제인 올라파립을 승인하는 등, 난소암에 대한 치료 옵션이 많이 나타나고 있지만, 난소암의 재발율은 초기 난소암 환자에게서 25%, 진행성 난소암 환자에게서 80% 이상에 이른다 14-16. 난소암의 한의학 치료로는, 항암치료를 받는 난소암 환자에서 한약이 골수억제를 포함한 부작용을 완화하며, 삶의 질을 개선하고 생존기간을 늘릴 수 있는 효과가 있다고 보고된 바 있다 17-19. 난소암 치료에 대한 한의 임상 가이드라인 20이 2016년에 발표되었으며, 이에 따르면 난소암의 한방치료는 ‘扶正祛邪’의 원칙을 기반으로 한방면역치료, 한방항암치료, 전이재발 억제치료, 유지치료가 필요하다. 본 증례의 환자는 2015년 8월 난소암 진단으로 수술 후 뇌전이와 경부 림프절 전이를 진단받고, 수술과 항암화학요법, 방사선치료를 시행하고 2018년 10월부터 재발 및 전이 억제를 목적으로 한방병원에 내원하여 면역세포의 활성도를 증가시키고 미세 암세포의 괴사를 유도할 수 있는 통합 암 치료를 시행하였다. 2019년 1월 척추전이 진단 후 방사선치료와 항암화학요법 시행 후 육안적으로 확인되는 종괴 및 림프절 전이는 제거되었으며, 표적항암제인 올라파립을 재발 및 전이 방지 목적으로 복용하였다. 최초 진단 후 8년이 지난 현재에도 생존해 있으며, 혈액학적 독성이나 부작용이 관찰되지 않았고 ECOG도 Grade 2에서 1으로 뚜렷한 호전을 보였다.
한의 약물치료로 투약한 항암단은 동충하초, 삼칠근, 우황 추출물을 주성분으로 하는 약물로 신생혈관형성인자 중 섬유아세포 성장인자 차단을 통해 세포자멸사를 유도하고 암의 전이 재발을 억제하며 고형암의 성장을 억제한다는 연구 보고가 있다 21. 또한, 임상적으로도 다양한 종류의 암의 재발을 억제하는 유의미한 효능이 보고되었다 22-24. 건칠고는 건칠 및 침향의 추출물로 이루어져 있으며 옻 추출물에서 알러지 성분인 Urushiol을 제거한 한약으로 신생혈관생성을 억제하여 여러 고형 암종의 생성 억제 및 전체 생존율 향상의 효과가 있는 것으로 발표되었다 25. 또한, 건칠은 실험적 연구에 의해 다양한 항암효능이 있는 것으로 밝혀졌고 26,27, 이는 건칠 추출물들의 항산화, 항염증, 면역력 증진, 신생혈관 억제 작용 등에 의한 것으로 추정된다 28. 침구치료는 환자의 주소증인 소화기 증상 완화 및 항암 효과를 가지는 혈위가 이용되었으며, 족삼리(ST36), 합곡(LI4)을 기본으로 하여 중완, 하완, 관원, 태충 등을 추가하고 증상에 따라 혈위를 가감하여 침치료를 시행하였다. 복부의 뜸 치료 또한 주소증인 변비를 포함한 소화기 증상 완화 및 면역력 증진을 위해 시행하였다.
본 증례에서 사용된 침치료와 뜸치료는 항암화학요법의 부작용 완화 29뿐만 아니라 종양인자의 감소, 생존 기간 연장, 그리고 종양 크기의 감소와 같은 직접적인 항암 효과가 있는 것으로 연구를 통해 확인된 바 있다 30. 이뮨셀-엘씨주는 암 환자의 혈액에서 단핵구를 분리하여, 항-CD3와 IL-2에 의한 동시 자극을 통해 2주 이상 동안 배양하는 과정을 거쳐 생산된다. 이 과정을 통해 활성화된 T-림프구와 싸이토카인 유도 살해세포(CIK)를 생성하며, 이러한 면역세포는 환자 자신의 체내에서 암 세포를 탐지하고 제거하는 데 기여한다. 이 방식은 암 환자에게 극대화된 항암 기능을 가진 면역세포를 공급하여 치료하는 기전으로 작용한다. 이뮨셀-엘씨주 치료로 암 환자의 전체 생존기간이 연장되었고, 재발 또는 무진행 생존 기간이 연장됨을 보여주는 여러 실험들이 보고되었다 31. 본 증례는 다음과 같은 한계를 가진다. 단일 증례라는 한계와 더불어 양방의 표준치료 후 일시적인 중단이 있었지만, 지속적으로 올라파립을 복용하였으며 통합암치료의 복합적인 중재가 장기간 적용되었기 때문에 특정 중재의 효과를 논의하기 어렵다. 또한 입원 기간 중에만 통합암치료가 시행되어, 한약치료에서 꾸준한 투약이 이루어지지 않았다는 점이다. 따라서 전이성 난소암 환자들에게 통합암치료가 적용할 수 있는 치료법인지 효과와 안전성을 검증하기 위해 다수의 환자들을 대상으로 한 임상연구들이 추가로 필요할 것으로 사료된다.
V. 결 론
본 증례는 항암화학요법의 발전에도 불구하고, 생존율이 낮은 전이성 난소암 환자에게서 통합 암 치료를 시행하며 암세포의 추가적인 진행을 억제하여 최초 진단 후 8년 생존을 확인하였고, 혈액학적으로 안전하며 활동도 개선 효과가 있어 보고하는 바이다.
감사의 글
이 연구는 대한민국 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구임(RS-2023-00246351).
참고문헌
1. The Korea Central Cancer Registry, National Cancer Center. Annual report of cancer statistics in Korea in 2021. Ministry of Health and Welfare 2023:
2. Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin 2020:70(1):7–30.    3. Modugno F, Edwards RP. Ovarian cancer:Prevention, detection, and treatment of the disease and its recurrence. Molecular mechanisms and personalized medicine meeting report. Int J Gynecol Cancer 2012:22(8):1–22.    4. Lheureux S, Gourley C, Vergote I, Oza AM. Epithelial ovarian cancer. Lancet 2019:393(10177):1240–53.   5. No JH, Park YS, Kim SM, Chung HH, Kim JW, Park NH, et al. Pattern of care:epithelial ovarian cancer in case of incomplete previous surgery. Korean J Gynecol Oncol 2007:18(3):195–200.   6. Le T, Adolph A, Krepart GV, Lotocki R, Heywood MS. The benefits of comprehensive surgical staging in the management of early-stage epithelial ovarian carcinoma. Gynecol Oncol 2002:85(2):351–5.   7. Lim MC, Park SY. Chemotherapy for ovarian cancer. J Korean Med Assoc 2016:59(3):175–9.   8. Kang SH, Hwang IH, Son EJ, Cho CK, Choi JS, Park SJ, et al. Allergen-Removed Rhus verniciflua Extract Induces Ovarian Cancer Cell Death via JNK Activation. Am J Chin Med 2016:44(8):1719–35.   9. Jang HJ, Yang KE, Hwang IH, Huh YH, Kim DJ, Yoo HS, et al. Cordycepin inhibits human ovarian cancer by inducing autophagy and apoptosis through Dickkopf-related protein 1/β- catenin signaling. Am J Transl Res 2019:11(11):6890–906.   10. Baiocchi G, Cestari LA, Macedo MP, Oliveira R, Fukazawa E, Faloppa C, et al. Surgical implications of mesenteric lymph node metastasis from advanced ovarian cancer after bowel resection. J Surg Oncol 2011:104(3):250–4.    12. Chéreau E, Ballester M, Rouzier R, Coutant C, Daraï E. Advanced ovarian cancer:criteria of resectability. Bull Cancer 2009:96(12):1189–97.  13. Choi JH, Suh MJ, Park DT. The correlation of clusterin binding affinity to chemotherapeutic agents with chemoresistance in ovarian cancer cells. Korean J Obs Gynecol 2008:51(7):738–43.
14. Salani R, Backes FJ, Fung MFK, Holschneider CH, Parker LP, Bristow RE, et al. Posttreatment surveillance and diagnosis of recurrence in women with gynecologic malignancies:Society of Gynecologic Oncologists recommendations. Am J Obstet Gynecol 2011:204(6):466–78.   15. Armstrong DK, Bundy B, Wenzel L, Huang HQ, Baergen R, Lele S, et al. Intraperitoneal cisplatin and paclitaxel in ovarian cancer. N Engl J Med 2006:354(1):34–43.   16. Trimbos JB, Parmar M, Vergote I, Guthrie D, Bolis G, Colombo N, et al. International Collaborative Ovarian Neoplasm trial 1 and Adjuvant ChemoTherapy In Ovarian Neoplasm trial:two parallel randomized phase III trials of adjuvant chemotherapy in patients with early-stage ovarian carcinoma. J Natl Cancer Inst 2003:95(2):105–12.   17. Chan KKL, Yao TJ, Jones B, Zhao JF, Ma FK, Leung CY, et al. The use of Chinese herbal medicine to improve quality of life in women undergoing chemotherapy for ovarian cancer:a double-blind placebo-controlled randomized trial with immunological monitoring. Ann Oncol Off J Eur Soc Med Oncol 2011:22(10):2241–9.   19. Wang R, Sun Q, Wang F, Liu Y, Li X, Chen T, et al. Efficacy and Safety of Chinese Herbal Medicine on Ovarian Cancer After Reduction Surgery and Adjuvant Chemotherapy:A Systematic Review and Meta-Analysis. Front Oncol 2019:9:730.    20. Kim KS, Choi HS, Kim SM, Yoo HS. Clinical Practice Guideline for Korean Medicine for Ovarian Cancer. J of Kor Traditional Oncolog 2016:21(2):37–50.
21. Lee NH, Yoon DH, Yoo HS, Cho JH, Son CG, Lee YW, et al. Changes of Serum VEGF, bFGF levels and platelet counts in 100 Cancer Patients treated with Hang-Am-Dan. The Journal of Internal Korean Medicine 2005:26(4):753–60.
22. Yoo HS, Lee YY, Song KC, Choi BL, Seo SH, Cho JH, et al. The Effects of HangAmDan(HAD) on Anti-Metastasis and Preventing Relapses, Administered to 69 Cancer Patients. The Journal of Internal Korean Medicine 2002:23(2):165–73.
23. Yoo HS, Son CG, Cho CK. Antitumor effects of HangAmDan (HAD) on 55 patients with advanced gastric cancer. J Korean Med 2001:2(1):77–88.
24. Lee YY, Seo SH, Yoo HS, Choi WJ, Cho JH, et al. The Clinical study in 83 cases for colorectal cancer patients on the effects by Hangamdan(抗癌丹). Journal of Korean Traditional Oncology 2000:6(1):165–80.
27. Jin UH, Lee DY, Kim DS, Lee IS, Kim CH. Induction of mitochondria-mediated apoptosis by methanol fraction of Ulmus davidiana Planch (Ulmaceae) in U87 glioblastoma cells. Environ Toxicol Pharmacol 2006:22(2):136–41.   28. Baek I, Im LH, Park C, Cho YH. Anti-cancer Potentials of Rhus verniciflua Stokes, Ulmus davidiana var. japonica Nakai and Arsenium Sublimatum in Human Gastric Cancer AGS Cells. J Life Sci 2015:25(8):849–60.  29. Kim JY, Kim JY, Kim NS, Kim SJ, Oyungerel M, Kim YS, et al. Review on Clinical Trials of Chemotherapy Induced Toxicity with Acupuncture in PubMed Database. Journal of Korean Acupuncture &Moxibustion Medicine Society 2013:30(2):43–53.  30. Yoon HC, Kang JY, Kim JY, Joung JY, Son CG, Lee NH, et al. Trends in Treatment with and Mechanism of Moxibustion in Cancer Patients:A Review. J Int Korean Med 2015:36(3):361–79.
31. Zhang Y, Schmidt-Wolf IGH. Ten-year update of the international registry on cytokine-induced killer cells in cancer immunotherapy. J Cell Physiol 2020:235(12):9291–303.   
|
|













