I. 서 론
인체에서 뼈가 약해지는 것은 노화에 수반되어 나타나는 현상으로 인간 수명이 길어짐에 따라 유병률도 증가하고 있다. 골절은 노인성 사망의 주요한 원인으로 알려져 있는데 뼈가 약해진 골다공증 환자에서 많이 발생한다. 뼈의 대사과정에는 골조직에서 칼슘을 녹여내는 기능이 있는 파골세포와 칼슘을 이용하여 골을 형성하는 기능을 가진 조골세포의 작용이 균형을 이루고 있다. 건강한 사람의 뼈에서는 두 세포가 균형적으로 작용하여 골 조직이 일정하게 유지되도록 작동하고 있다1.
골다공증은 조골세포 기능이 약물들에 의해 저해되어 뼈의 생성이 억제되거나, 호르몬 분비의 변화로 파골세포 기능이 증가하여 골 손실이 증가할 때 나타난다2. 따라서, 골다공증을 억제하여 뼈를 튼튼히 하기 위해서는 파골전구세포들이 파골세포로 분화하는 과정을 차단하거나 파골세포 작용을 억제하는 방법을 우선적으로 고려할 수 있으며, 조골세포 기능 활성화를 통한 골형성을 촉진하는 것도 유익한 방법이다.
파골세포는 파골세포전구세포의 표면에 존재하는 receptor activator of nuclear factor kB(RANK)에 조골세포에서 분비하는 receptor activator of nuclear factor kB ligand(RANKL)이 결합하여 분화된다. 이 과정에 면역관련 인자인 macrophage colony-stimulating factor(M-CSF) 등이 작용한다3. 파골세포로의 분화는 RANKL로 활성화된 수용체로부터 NF-kB 신호전달과정에 신호를 전달하여 시작되는데, 이러한 과정에 extracellular signal-regulated kinase(ERK), c-Jun N-terminal kinase(JNK)와 p38와 같은 mitogen-activated protein kinases(MAPKs)이 활성을 나타내면서 분화한다4. 이와 함께 nuclear factor of activated T cell cytoplasmic 1(NFATc1)이 활성화되어, 파골세포가 골흡수에 직접적으로 작용하는데 필요한 단백질인 tartarate-resistant acid phosphatase(TRAP), cathepsin K, matrix metalloproteinases-9(MMP-9) 등의 생합성을 촉진하게 된다5.
치자는 치자나무(Gardenia jasminoides) 및 동속 식물의 열매로서 凉血解毒, 淸熱利濕, 瀉火除煩의 효능이 있어서 한의학적으로 열병이나 불면, 황달, 소갈이나 결막염, 출혈이 수반된 다양한 증상을 완화하는데 사용되었다6. 또한, 음식의 색깔을 좋게 하여 식욕을 촉진하기 위한 식품 원료로 사용되고 있다.
주성분으로는 flavonoid 성분인 gardenin을 비롯하여 genipin, pectin, tannin, crocin, nonacosane, b-sitosterol 등이 보고되었고7, 배당체로 gardenoside, geniposide, genipin-1-b-d-gentiobioside와 choline, ursolic acid 등이 보고되었다8.
최근 연구보고에 의하면, 치자는 항염증작용9과 간보호작용10, 멜라닌생성 억제작용11, 혈전생성 억제작용12, 위염 및 위궤양 억제 작용13, 항당뇨작용14, 기억력증진 작용15 등이 보고되었다. 특히, 치자 추출물이 NF-kB 를 억제하여 MMP-9의 작용을 억제한다는 보고가 있었다16. 이에 저자들은 치자 추출물이 파골세포 분화 또는 기능을 억제할 가능성이 있을 것으로 추정하였다. 따라서, 본 저자들은 뼈를 강화하여 노년기의 활력을 증진시키기 위하여 파골세포 기능을 억제하여 골을 강화시키는 한약재를 찾는 연구 목적으로 치자가 파골세포 형성 및 골 흡수에 미치는 영향을 평가하고자 하였다. 이를 위하여 RANKL로 자극한 RAW264.7 cell에서 TRAP(+) 형성능을 측정하였으며, 관련 유전자인 cathepsin K, TRAP, MMP-9, NFATc1, Dendritic Cell-Specific Transmembrane Protein(DC-STAMP), osteoclast stimulatory transmembrane protein (OC-STAMP), calcitonin receptor(CTR) 등의 유전자 발현을 측정하였으며, 인공 골조직에 파골세포를 첨가하여 나타나는 골 흡수에 미치는 영향을 측정하였다.
II. 방 법
1. 재 료
2. 방 법
1) RAW264.7 Cell 배양
DMEM(Dulbecco’s modified eagle medium)/10% FBS(Fetal bovine serum)/PC-SM 배지에 RAW 264.7 cell을 96 well plate에 5×103 cells/well가 되도록 맞춘 후, CO2 세포배양기에서 배양하였다. 24시간 동안 배양기에서 배양한 후 배양액을 제거하고, 다시 50 ng/mlRANKL, 10% FBS, 1 ng/ml TGFβ가 첨가된 α-MEM 배지로 교환하여 세포를 배양하였다. 배양액에는 약물처리를 위해 다양한 농도별로 GJ가 함유되도록 하였다. 동일한 배지인 α-MEM 용액으로 이틀 간격으로 교환해 주면서 총 6일간 배양하였다.
2) 약물처리
실험군은 RANKL이 함유되지 않은 배양군(Normal), RANKL이 함유된 배양군(Control), RANKL과 75 μg/ml의 GJ 추출물이 함유된 배양군(GJ 75), RANKL과 150 μg/ml의 GJ 추출물이 함유된 배양군(GJ 150), RANKL과 300 μg/ml의 GJ 추출물이 함유된 배양군(GJ 300)으로 나누어 실험하였다.
3) 파골세포 생성 측정
파골세포 분화는 RAW264.7 cell에 RANKL을 처리하여 유도시켰으며, 분화한 파골세포에서 발현되는 분화 marker로 tartrate-resistant acid phosphatase (TRAP)를 염색하고 발색되는 TRAP-positive 세포(TRAP(+) MNC)를 확인하여 평가하였다. 분화시킨 세포는 PBS(Phosphate buffered saline)로 2번 세척하였으며, 이후 10분 동안 3.7% formaldehyde -citrate-acetone 용액으로 고정시키고 다시 증류수로 2번 세척하였다. 2% TRAP fast garnet GBC base 용액과 NaNO3 용액을 각각 동일한 양을 넣어 만든 혼합용액을 고정시킨 세포에 처리하였다. 다시 고정된 세포에 5% naphtha AS-BI phosphoric acid, 2% 주석산, 4% 초산이 포함된 용액을 처리하고 30분 동안 상온에 방치하였다. 파골세포 생성을 관찰하기 위하여 광학현미경을 이용하여 계수하였으며, 3개 이상의 핵이 염색된 다핵세포(TRAP(+) MNCs)를 파골세포로 판정하는 생성지표로 하였다.
4) 파골세포 유전자 발현 측정
(1) Total RNA 분리
RNA 분리는 실험군 별로 배양세포의 배지를 완전히 제거한 plate를 4 °C PBS로 3번 세척한 세포를 시용하였다. 각 plate에서 세포를 떼어내어 모은 다음, 750×g에서 10분간 원심 분리하여 침전된 세포를 냉각된 PBS로 2번 더 세척하였다. 상층액을 버리고 침전된 세포에 lysis buffer를 가하고 흔들어 용해시킨 다음, 12,000×g에서 10분간 다시 원심 분리하고 상층액을 얻었다. 얻어진 용액을 1 M sucrose가 함유되도록 제조한 tris buffer 윗부분에 조심스럽게 loading한 다음, 36,000 rpm으로 160분 동안 원심분리기로 분리하였다. 침전물을 SDS buffer에 녹인 후, 37 °C 배양기에 30분 간 incubation 하였다. 여기에 Sod. Acetate buffer를 가하고 phenol/CsKl3 용액을 사용하여 추출하였다. NaCl 농도가 최종적으로 0.2 M이 되도록 만든 다음, EtOH를 가한 후 -20 °C 냉장고에 12시간 방치하여 얻은 침전물을 75% EtOH로 2번 세척하고 건조시켰다. 유전자 발현에 필요한 RNA양을 각 실험군 별로 mRNA 양이 동일하게 맞춘 후, 전기영동으로 확인하고 사용하였다.
(2) cDNA 제조
각각의 실험군으로 부터 분리한 total RNA액 10 μl(10 μg RNA 함유)에 oligo dT 1 μl(2 μg/μl)를 가한 후 조심하여 혼합한 후, 90 °C에서 5분간 가온하였다. Primer의 annealing을 위해 약 10분간 실온으로 방치한 후, 아래 시약을 가하는 동안 얼음 상에서 작업하였다. 5×cyscript buffer 4 μl, 0.1 M DTT 2 μl, dUTP nucleotide mix 1 μl, dUTP Cydye-labelled nucleotide 0.1 μl, Cyscript reverse transcriptase 1 μl, H2O 0.9 μl를 첨가하여 총 20 μl로 한 후, tipping 하는 방법으로 조심하면서 혼합하였다. 이 후, 42 °C에서 90분간 가온한 다음, 얼음 상에 방치하였다. 여기에 2.5 M NaOH을 2 μl씩 가한 후 37 °C로 15분 동안 유지시켰으며, 2M 농도의 HEPES buffer(free acid) 10 μl를 섞어 중화시켰다. 사용된 시약은 Amersham Bioscience에서 구매하였다.
(3) Real time PCR
각각의 optical tube(MicroAmp® Optical 96-Well Reaction Plate with Barcode and Optical Adhesive Films, Applied Biosystems, Cat.No. 4314320)에 3배의 SybrGreen Mix 2.5 μl(Sigma-Aldrich, Cat.No. S9430), (2)에서 만든 cDNA 1 μl, 10 pmol/μl primer pair mix 1 μl, 각각 2.5 mM의 dNTP 2 μl, 10× Tag polymerase buffer 2.5 μl, Tag Polymerase 0.3 μl와 14.7 μl H2O를 가했다. 이후 95 °C에서 5분 1 cycle, 95 °C에서 30초, 45 °C에서 30초, 72 °C에서 60초 40 cycles, 95 °C에서 20분 1 cycle로 증폭시켰다. Primer는 RT-PCR에 사용한 것을 이용하였다. PCR을 수행한 후 증폭기에서 tube를 꺼내고, 반응액 5 μl를 사용하여 3% agarose gel 상에서 PCR specificity를 측정하였다. ABI PRISM® 7000 Sequence Detection System (Applied Biosystems, Cat. No. 4349157)를 사용하여 Real time PCR 결과를 분석하였다. PCR 반응에 사용한 primer는 Table 1에 표시하였다.
Table 1
Primer
5) Bone resorption Assay
파골세포로 분화하여 작용한 결과 나타나는 골 흡수에 미치는 영향을 평가하기 위하여, plate 상에 calcium-collagen을 코팅하여 제조한 인공 뼈 모델을 사용하여 측정하였다. collagen이 코팅된 plate를 phenol-red-free MEM 배지로 세척해 준 다음, 파골세포 전구세포가 1×103 cells/well이 되도록 분주하고 24시간 배양한 후, 100 ng/ml 농도의 RANKL로 처리하였다. 1시간 지난 후 GJ 추출물을 농도별로 가한 다음 10일 동안 배양하였다. 배지는 2일 간격으로 교체해 주었다. 배양을 마친 plate는 5% sodium hypochlorite를 이용하여 파골세포를 제거하고 증류수로 세척하였다. 건조한 다음 역상현미경으로 400배 확대하여 골 흡수로 인해 형성되는 pit를 관찰하였고 사진을 촬영하였다.
III. 결 과
1. 파골세포 생성에 미치는 영향
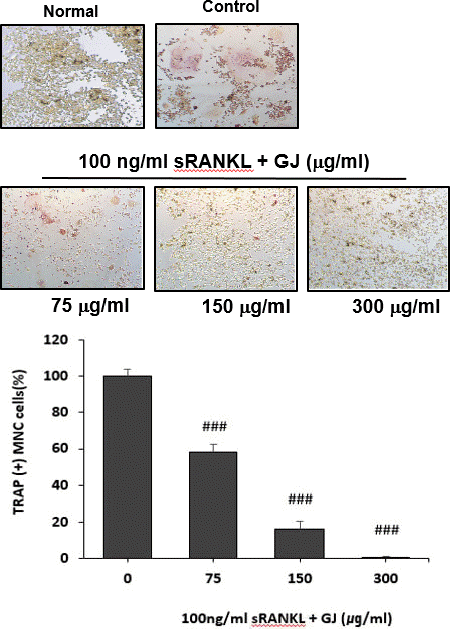
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화가 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 TRAP(+) MNC의 출현 빈도가 정상군에 비해 유의성 있게 증가하여 파골세포로 분화가 잘 유도된 것이 확인되었다. 치자 추출물(이하 GJ)은 75 μg/ml의 농도에서 대조군에 비해 TRAP(+) MNC가 유의성(p<0.001) 있게 감소(약 43.9%)하였고, 150 μg/ml의 농도와 300 μg/ml의 농도에서도 대조군에 비해 각각 유의성(p<0.001) 있게 감소(약 82.9%, 99.9%) 하였다(Fig. 1).
Fig. 1
Effects of GJ on the formation of TRAP (+) MNCs in RANKL stimulated osteoclast.
Normal : vehicle
0 (Control) : RANKL (100 ng/ml)
75 : RANKL (100 ng/ml)+75 μg/ml of GJ
150 : RANKL (100 ng/ml)+150 μg/ml of GJ
300 : RANKL (100 ng/ml)+300 μg/ml of GJ
Each bar represents Mean±SD of 5 tests.
### : p<0.001 vs Control
3. TRAP 유전자 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 TRAP 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 TRAP 발현이 정상군에 비해 유의성 있게 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 52%, 150 μg/ml의 농도에서는 약 85%, 300 μg/ml의 농도에서는 약 99.7% 억제 효과를 나타내었다(Fig. 3(A)).
Fig. 3
Effects of GJ on the expressions of TRAP (A), MMP-9 (B), and Cathepsin K (C) in RANKL stimulated osteoclast.
Normal : vehicle
0 (Control) : RANKL (100 ng/ml)
75 : RANKL (100 ng/ml)+75 μg/ml of GJ
150 : RANKL (100 ng/ml)+150 μg/ml of GJ
300 : RANKL (100 ng/ml)+300 μg/ml of GJ
Each bar represents Mean±SD of 5 tests.
*** : p<0.01 vs NC
### : p<0.01 vs Control

4. MMP-9 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 MMP-9 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 MMP-9 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 9%, 150 μg/ml의 농도에서는 약 32%, 300 μg/ml의 농도에서는 약 86% 억제 효과를 나타내었다(Fig. 3(B)).
5. Cathepsin K 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 Cathepsin K 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 Cathepsin K 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 59%, 150 μg/ml의 농도에서는 약 83%, 300 μg/ml의 농도에서는 약 99.8% 억제 효과를 나타내었다(Fig. 3(C)).
6. NFATc1 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 NFATc1 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 NFATc1 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 150 μg/ml의 농도에서는 약 45%, 300 μg/ml의 농도에서는 약 83% 억제 효과를 나타내었다(Fig. 4(A)).
Fig. 4
Effects of GJ on the expressions of NFATc1 (A), c-Fos (B), and MITF (C) in RANKL stimulated osteoclast.
Normal : vehicle
0 (Control) : RANKL (100 ng/ml)
75 : RANKL (100 ng/ml)+75 μg/ml of GJ
150 : RANKL (100 ng/ml)+150 μg/ml of GJ
300 : RANKL (100 ng/ml)+300 μg/ml of GJ
Each bar represents Mean±SD of 5 tests.
*** : p<0.001 vs NC, * : p<0.05 vs NC
### : p<0.01 vs Control, ** : p<0.01 vs Control, * : P<0.05 vs Control
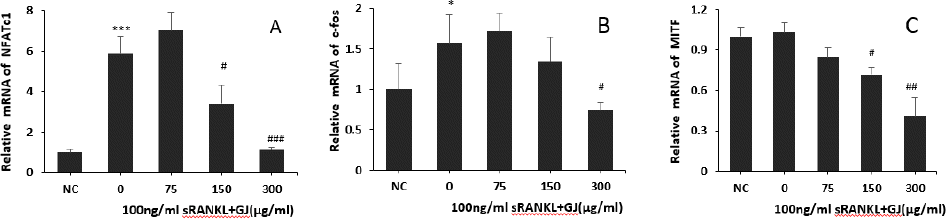
7. c-Fos 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 c-Fos 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 c-Fos 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 150 μg/ml의 농도에서는 약 13%, 300 μg/ml의 농도에서는 약 54.8% 억제 효과를 나타내었다(Fig. 4(B)).
8. MITF 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 MITF 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 MITF 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 150 μg/ml의 농도에서는 약 29.4%, 300 μg/ml의 농도에서는 약 61.8% 억제 효과를 나타내었다(Fig. 4(C)).
9. OC-STAMP 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 OC-STAMP 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 OC-STAMP 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 26.4%, 150 μg/ml의 농도에서는 약 65.9%, 300 μg/ml의 농도에서는 약 95.3% 억제 효과를 나타내었다(Fig. 5(A)).
Fig. 5
Effects of GJ on the expressions of OC-STAMP, DC-SRTAMP, and CTR in RANKL stimulated osteoclast.
Normal : vehicle
0 (Control) : RANKL (100 ng/ml)
75 : RANKL (100 ng/ml)+75 μg/ml of GJ
150 : RANKL (100 ng/ml)+150 μg/ml of GJ
300 : RANKL (100 ng/ml)+300 μg/ml of GJ
Each bar represents Mean±SD of 5 tests.
*** : p<0.001 vs NC
### : p<0.01 vs Control

10. DC-STAMP 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 DC-STAMP 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 DC-STAMP 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 29.3%, 150 μg/ml의 농도에서는 약 39.1%, 300 μg/ml의 농도에서는 약 83.2% 억제 효과를 나타내었다(Fig. 5(B)).
11. CTR 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 CTR 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 CTR 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 63.7%, 150 μg/ml의 농도에서는 약 87.8%, 300 μg/ml의 농도에서는 약 99.9% 억제 효과를 나타내었다(Fig. 5(C)).
12. ATP6vOd2 발현에 미치는 영향
실험 결과, RANKL이 함유되지 않은 정상군에서는 파골세포로의 분화시 나타나는 ATP6vOd2 발현이 거의 나타나지 않았으며, RANKL 만을 처리한 대조군은 ATP6vOd2 발현이 정상군에 비해 현저히 증가하였다. 치자 추출물(이하 GJ) 처리시 75 μg/ml의 농도에서는 약 74.1%, 150 μg/ml의 농도에서는 약 97.6%, 300 μg/ml의 농도에서는 약 99.9% 억제 효과를 나타내었다(Fig. 5(D)).
13. 염증관련 인자 발현에 미치는 영향
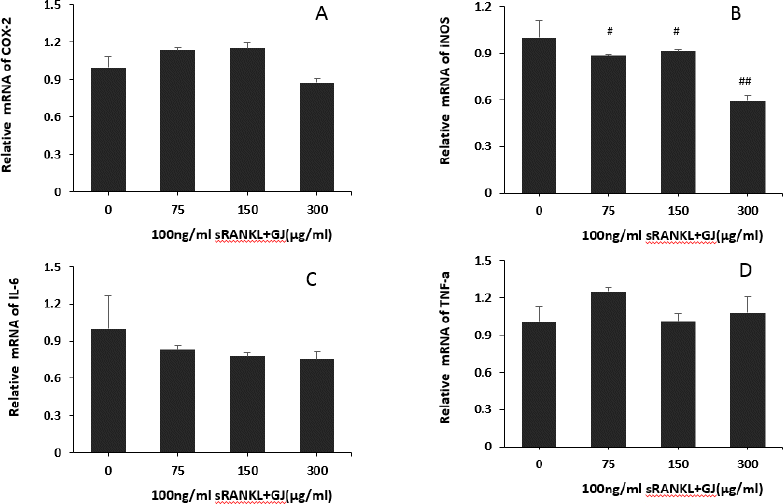
실험 결과, 치자 추출물(이하 GJ) 처리시 iNOS 발현을 75 μg/ml의 농도에서는 약 14%, 150 μg/ml의 농도에서는 약 11.2%, 300 μg/ml의 농도에서는 약 42.3% 억제 효과를 나타내었다(Fig. 6(B)). 그러나, GJ는 COX-2, IL-6, TNFα 발현에는 영향을 주지 못했다(Fig. 6(A, C, D)).
Fig. 6
Effects of GJ on the expressions of COX-2 (A), iNOS (B) and IL-6 (C), and TNFα (D) in RANKL stimulated osteoclast.
0 (Control) : RANKL (100 ng/ml)
75 : RANKL (100 ng/ml)+75 μg/ml of GJ
150 : RANKL (100 ng/ml)+150 μg/ml of GJ
300 : RANKL (100 ng/ml)+300 μg/ml of GJ
Each bar represents Mean±SD of 5 tests.
### : p<0.001 vs Control, ## : p<0.01 vs Control, # : p<0.05 vs Control
IV. 고 찰
골다공증은 노인층의 중요한 사망 원인인 골절의 실질적 원인으로 작용하고 있는데, 내분비 호르몬의 이상, 약물의 부작용, 영양소 결핍, 유전적 요인들에 의해 유발될 수 있다. 골다공증은 골 대사를 담당하는 골세포의 이상으로 골 기질물질의 손상이 빠르게 나타나는 현상으로, 골조직에서 칼슘과 결합한 결체조직을 파괴하여 칼슘의 유리를 촉진하는 파골세포가 칼슘을 이용하여 골을 형성하는 기능을 가진 조골세포 보다 활성이 우세하여 나타난다2.
파골세포는 조혈모세포로부터 유래되는 단핵구/대식세포계의 다핵성세포로 파골세포전구세포가 분화하여 형성되면 골 조직을 파괴하는 역할을 한다17. 파골세포로의 분화는 RANKL과 같은 분화자극 인자의 작용으로 시작되는데, RANKL은 Tumor necrosis factor(TNF) 계열의 싸이토카인으로 주로 조골세포에서 macrophage-colony stimulating factor(M-CSF)와 마찬가지로 분비된다3. 조골세포 기능이 활발해지면 항상성을 유지를 이해 파골세포의 기능이 함께 활성화되는 것이다. 파골세포전구세포 표면에는 RANKL과 결합하는 RANK가 존재한다. RANK는 Tumor necrosis factor receptor(TNFR) superfamily에 속하는 수용체로 RANKL이 결합하면 JNK, Extracellular signal-regulated kinase(ERK), p38 등을 포함한 Mitogen-activated proteinkinase(MAPK) 신호경로가 활성화된다4. 이 과정을 통하여 파골세포로 분화되는데 필수적인 nuclear factor of activated T cells, cytoplasmic 1(NFATc1), NF-κB, c-Fos, MITF와 같은 전사인자가 발현된다5. 이들의 작용으로 TRAP, Cathepsin K, MMP-9 과 같은 골기질 물질을 파괴하는 단백질분해효소들이 발현되어 실질적인 작용을 하게 된다18,19. 한편, Extracellular signal-regulated kinase (ERK) 계열의 신호전달계통의 활성화는 파골세포의 아폽토시스를 억제하여 파골세포의 기능을 증가시키는데, macrophage-colony stimulating factor(M-CSF)은 파골세포의 분화를 촉진하는 RANKL과 상호작용을 하여 아폽토시스를 억제하고 세포능을 유지하게 한다20.
본 연구에서는 치자가 파골세포의 분화를 억제하는 것을 관찰하고 분화관련 인자들의 발현에 미치는 영향을 평가한 것이다. TRAP은 분화하여 성숙한 파골세포에서 발현되는 단백질로 파골세포의 분화 여부와 기능의 활성 여부를 판단하는 기준 지표물질이 될 수 있다. 실험결과, 치자 추출물은 TRAP 양성인 다핵성 세포(TRAP(+) MNCs) 생성을 억제하여 파골세포의 분화과정을 통한 활성세포 형성을 억제하는 것으로 나타났다(Fig. 1).
TRAP은 골의 흡수에 관여하고 있어 파골세포의 활성화로 인한 골 흡수 과정은 세포에서 발현되는 TRAP의 mRNA 유전자 발현을 지표로 삼아 측정하였다. 실험 결과, RANKL은 파골세포에서 TRAP 발현을 증가시켰으며, GJ는 RANKL에 의해 발현이 증가된 TRAP 발현을 유의성(p<0.001) 있게 억제하여 GJ가 파골세포의 골 흡수 역할을 하는 저해할 수 있음을 확인하였다(Fig. 3(A)). 이러한 GJ의 작용은 파골세포의 골흡수를 담당하는 또 다른 골 흡수 인자인 MMP-9, Cathepsin K 발현에도 같은 양상으로 나타났다(Fig. 3(B, C)). 이를 통해 GJ가 RANKL로 유도된 파골세포의 단백질 합성을 억제하여 골흡수를 억제할 것으로 판단되었는데, 이는 실제로 골흡수를 측정한 실험결과(Fig. 7)에서 관찰한 그림에서 확인할 수 있었다. 또한, 이러한 GJ의 효과는 TRAP, OSCAR, cathepsin K와 같이 파골세포 특이 유전자의 발현을 조절하는 NFATc1 발현을 GJ가 억제하기 때문에 나타난 결과로 판단되었다.
한편, 파골세포로 분화되는 과정에 작동되는 신호전달체계에 대한 영향과 Fig. 1 확인된 TRAP(+) MNC 형성과정의 연관성을 확인하기 위하여 파골세포 분화과정에 관여하는 전사인자들의 발현에 미치는 영향을 평가하고자 하였다. 이러한 파골세포의 분화를 유도하는 핵심 전사인자로는 NF-kB, c-Fos와 NFATc1, MITF 등이 알려져 있다21. NFATc1는 RANKL이 수용체에 결합하여 활성화되는 TNF receptor associated factors(TRAF)를 통하여 c-Fos와 Calmodulin activated kinases(CaMKs) 계열의 신호전달과정을 거쳐 발현이 증가하며, 이는 파골세포 분화과정에 필요한 인자들의 발현에 중요한 역할을 하는 전사인자이다5. 실험 결과, GJ는 NFATc1 발현을 억제하여(Fig. 4(A)) 파골세포 분화과정에 필요한 인자들의 발현이 억제될 것으로 추측되었으며, 이는 Fig. 1에서 나타난 결과와 상관성이 있으며, 또한, GJ가 NFATc1에 의해 발현이 조절되는 TRAP과 cathepsin K 발현을 억제한 결과(Fig. 3(A, C))를 보였기 때문에 발현이 억제될 것으로 예측했던 바와 같이 억제되는 결과를 나타내었다. 이와는 별도로 TNF receptor associated factors (TRAF)를 통하여 전달되는 TAK1, MKK6, p38의 신호전달 결과 나타나는 microphthalmia-associated transcription factor(MITF)는 활성화되어 파골세포의 분화를 촉진하는 전사인자이다22. 실험 결과, GJ는 RANKL에 의해 증가된 MITF 발현을 감소시켰고, c-Fos 발현도 억제하여(Fig. 4(B, C)), 파골전구세포로부터 파골세포로의 분화를 억제할 것으로 판단되었다. 이러한 결과는 Fig. 1에서 보이는 바와 같이 분화가 억제되는 결과로 나타났다.
한편, NFATc1는 파골세포의 작용점으로의 이동, 골기질 물질에 대한 부착, 흡수부위의 산성화, 골기질의 파괴 등에 관여하는 파골세포 특이 단백질 유전자인 dendritic cell-specific transmembrane protein(DC-STAMP), osteoclast-stimulatory transmembrane protein(OC-STAMP), Atp6v0d2, calcitonin receptor (CTR)과 CtsK들의 발현을 조절하는 것으로 알려져 있다23,24. 이들은 RANKL 자극되어 활성화되는 MITF의 작용으로 분화된 전구세포가 세포융합을 통하여 완벽한 파골세포 형질세포로 변환하는데 중요한 역할을 한다. 이들은 파골세포의 분화과정과 파골세포의 활성화를 조절하는 NFATc1에 의해 조절되는 것으로 알려져 있다. 따라서, NFATc1 활성이 억제되면 DC-STAMP, OC-STAMP의 발현도 억제될 것으로 추측되었다. 실험결과, GJ는 예측한 대로 RANKL에 의해 발현이 증가된 DC-STAMP, OC-STAMP, Atp6v0d2, CTR의 발현을 억제하였다(Fig. 5(A, B, C, D)).
NO는 nitrite oxide synthase(NOS)에 의해 생성되는 물질로 eNO, nNO, iNO 등이 존재한다. 주로 대식세포에서 유래하는 iNO는 RANKL이나 같은 계열인 TNFα 같은 염증 유발 사이토카인에 의해 활성화된 iNOS 의해 생성된다. 생성된 iNO는 면역반응을 포함한 염증반응에 관여하는데, IL-6, TNF-a의 생합성을 증가시켜 파골세포 활성을 증가시킨다25. 이들은 세포막에 존재하는 수용체와 결합하여 활성화된 phospholipase A2(PLA2) 작용을 통해 유리되는 arachidonic acid(AA)를 이용한 prostaglandin(PG) 류의 생합성에 관여한다. Cyclooxygenase-2(COX-2)는 AA를 이용하여 PGG2를 생합성하는 효소로서 이후 PGD2, PGE1, PGI2, TXA2 등의 다양한 prostaglandin 류를 합성하여 염증반응에 관여한다26. 최근, 파골전구세포에서 NO가 증가하는 경우 파골세포로의 분화가 촉진된다고 보고되었다27. 이러한 파골세포분화가 촉진되어 골흡수가 증가하는 데는 염증반응 인자들의 세포내 증가가 관찰되었다. 따라서, COX-2 또는 iNOS를 차단하는 것은 파골세포 분화를 억제할 수 있는 또다른 경로일 수 있다28. 실험 결과, GJ는 파골세포 분화과정에서 COX-2 발현을 억제하지는 못했지만, iNOS 발현은 억제하였다(Fig. 6(B)). 이러한 결과는 치자 추출물이 다른 염증세포를 억제한다는 보고와는 효과 면에서 약간의 차이를 보이고 있다9. 그러나, GJ는 iNOS 발현을 억제하여 세포내 NO 농도를 저하시켜 파골세포 분화 관련 인자들의 억제효능에 기여하는 것으로 추측되었다.
이러한 실험결과를 바탕으로, GJ가 골흡수에 미치는 영향을 평가하여 위해 인공뼈를 이용하여 파골세포에 의해 생성되는 bone-pit 생성을 관찰하였다. 실험결과, GJ는 bone-pit 형성을 억제하여 골흡수를 억제하는 것으로 나타났다(Fig. 7).
결론적으로, 치자 추출물은 RANKL 유도된 파골세포의 분화, 세포 융합 및 이동, 골흡수 활성에 관여하는 다양한 유전자의 발현을 조절하여 파골세포 분화 및 활성을 억제하고 이를 통해 골흡수를 억제하는 것으로 나타났다.
V. 결 론
치자 추출물(GJ)이 파골세포의 분화과정과 세포활성을 억제하여 골의 재흡수를 억제할 수 있는지 평가하기 위해, RANKL 처리하여 유도되는 파골세포 분화와 관련 인자들의 유전자 발현에 미치는 영향, 골의 pit 생성에 미치는 영향을 측정하여 다음과 같은 결론을 얻었다.
1. GJ는 RANKL 유도 TRAP(+) MNCs 생성을 억제하였다.
2. GJ는 RANKL 유도 파골세포에서 TRAP, MMP-9, cathepsin K의 발현을 억제하였다.
3. GJ는 RANKL 유도 파골세포에서 NFATc1, c-Fos, MITF의 발현을 억제하였다.
4. GJ는 RANKL 유도 파골세포에서 OC-STAMP, DC-STAMP, Atp6v0d2, CTR의 발현을 억제하였다.
5. GJ는 RANKL 유도 파골세포에서 염증관련 iNOS 의 발현을 억제하였다.
6. GJ는 파골세포의 골흡수 활성을 억제하였다.
결론적으로, GJ는 RANKL로 유도되는 파골세포에서 분화를 조절하는 인자들의 발현을 조절하고, 파골세포의 골흡수 활성을 조절하는 유전자들의 발현 조절을 통하여 골흡수를 억제하는 것으로 나타났다. 따라서, 치자가 골다공증 치료 및 예방목적에 사용이 가능할 것으로 사료된다.













