통합암치료를 적용한 폐전이 동반 췌장암 환자의 장기간 추적관찰 증례보고
Long-Term Follow-up of Pancreatic Cancer Patients with Lung Metastasis Using Integrated Cancer Treatment: A Case Report
Article information
Abstract
ABSTRACT
Objective:
This long-term case report details a case of pancreatic cancer with lung metastasis suppressed by integrative cancer medicine (IMT).
Methods:
A 64-year-old woman diagnosed with pancreatic cancer visited a Korean medicine hospital complaining about the side effects of chemotherapy for lung metastasis. She received IMT involving Korean traditional medicine and Western immunotherapy from May 2017 to June 2023. Tumor dimensions were assessed through computed tomography (CT) and positron-emission tomography/CT scans, while tumor markers and safety were monitored by laboratory tests.
Results:
IMT suppressed the progression of cancer, as observed by imaging and laboratory tests. The patient achieved 5-year survival, even after discontinuing chemotherapy.
Conclusion:
This case presents a potential therapeutic alternative for patients who are ineligible for chemotherapy or surgical interventions.
I. 서 론
췌장암은 췌장을 구성하는 세포에 종양이 발생한 것으로 90% 이상이 외분비 세포에서 발생하여 췌장 선암이라고도 한다. 초기 증상이 분명하지 않아 진행이 많이 된 상태에서 진단이 되어 예후가 좋지 않은 경우가 많으며, 폐를 포함한 신체의 다른 부분으로 전이되는 경향을 보인다. 미국의 통계정보에 따르면 췌장암 진단 당시 단계별 비율은 국소화 췌장암이 13%, 국소 림프절 전이가 29%, 원격 전이는 51%로 보고하고 있다1. 국내 기준으로는 2022년도에 발표한 통계자료에 따르면 발생 암 중 8번째로 흔하며, 사망원인으로 봤을 때 4번째에 해당한다2. 또 다른 2017년 발표된 보고서에 따르면 5년 생존율의 경우 12.2%로 주요 10대 암 중 최하위를 차지하고 있다3. 췌장암의 치료는 근치적 절제술이 완치율을 높일 수 있지만 실제 수술이 가능한 환자는 20% 미만으로 국소화 및 경계성 종양인 경우만 해당된다.
2022년 발표된 국내 췌장암 치료 가이드라인에 따르면, 전이성 췌장암의 경우 항암요법만 권고되며 2차 항암치료는 항암치료 병력 및 수행능력을 고려한 조건부 권고사항으로 제시되어 있다4. 전이성 췌장암 환자 대상 고식적 항암요법에 사용할 수 있는 1차 항암제로 FOLFIRINOX 또는 gemcitabine과 nab-paclitaxel의 병합치료가 일반적으로 권고된다. FOLFIRINOX는 5-Fu/leucovorin, irinotecan 그리고 oxaliplastin으로 구성된 복합 항암치료로 gemcitabine 단독 치료에 비해 전이성 췌장암 환자의 생존 기간을 연장시킨다는 연구가 발표되었고5, gemcitabine과 nab-paclitaxel 복합 치료 또한 gemcitabine 단독치료보다 생존 기간 연장에 통계적 유의성이 있다고 보고한 바 있다6. 그러나 진단 당시 원격 전이가 확인된 췌장암의 경우 5년 생존율은 3.2%로1 생존 기간 연장을 위한 항암요법에 대한 연구가 활발함에도 불구하고 전이성 췌장암의 5년 생존율에 미치는 영향은 미미하며, 항암요법 진행 과정에서 발생하는 부작용도 환자들이 치료를 지속하는데 걸림돌이 되고 있다. 실제 전이성 췌장암의 5년 생존율은 또한 같은 항암요법을 시행해도 환자마다 다른 반응을 보이는 경우가 많아 추가적인 연구들이 필요한 실정이다.
췌장암의 한방치료 관련한 국내 임상연구로는 한방약물치료, 대사활성치료, 항암식이치료 등을 결합한 통합암치료가 NK cell 및 염증 인자에 긍정적 영향을 주었다는 후향적 분석 연구가 있었으며7, 건칠 추출물 제제, 항암플러스, 항암단, 진세노사이드 추출물 등이 췌장암 환자의 치료에 있어서 증상 개선 및 삶의 질 개선에 효과가 있었다는 증례보고들이 있었다8-10. 그러나 통합암치료를 적용하여 장기간 관찰한 증례보고는 현재까지 보고된 바가 없었다.
이에 항암화학요법을 중단하였음에도 불구하고 폐 전이를 동반한 췌장암 환자가 본원에서 통합암치료를 통해 암세포의 진행성 변화를 억제하고, 5년 생존에 도달한 사례가 있어 이를 보고하고자 한다.
II. 증례보고
본 증례는 환자동의서와 ○○한방병원 기관생명윤리위원회(Institutional Review Board, IRB)의 심의 면제를 획득하였다(HR-2305-05).
1. 환 자 : ⃝⃝⃝(1951년생, 여)
2. 진단명 : Pancreatic tail cancer stage IV
3. 진단일 : 2015년 3월(당시 64세)
4. 주소증 : abdominal pain, cough, oral take poor, general weakness, constipation
5. 과거력 : Hypertension
6. 가족력 : None
7. 현병력
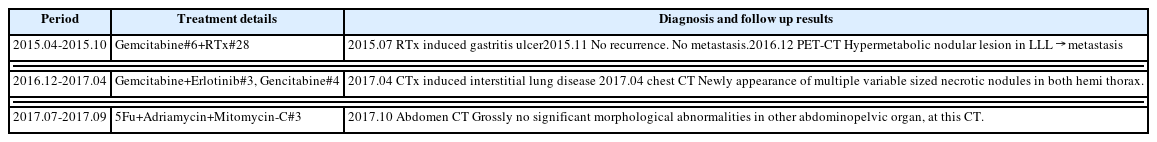
64세 여환 2015년 3월 초 폐렴으로 부산소재 모 병원에서 입원 치료 중 computed tomography(CT)상 pancreas tail cancer 소견, pancreatic magnetic resolution image(MRI) 및 positron emission tomography(PET) CT상 pancreatic cancer 확인(Fig. 1 A-1, A-2). 4월 1일 모대학병원에서 subtotal pancreatectomy, left adrenalectomy, splenectomy 시행, 조직검사 상 ductal adenocarcinoma 및 left adrenal gland metastatic adenocarcinoma 진단됨. 2015년 4월부터 10월까지 Gemcitabine을 항암요법으로 시행하였고 2016년 11월 chest CT 상 left lower lobe(LLL)에 이상 소견 있어 LLL wedge resection 시행 후 확인한 조직검사 상 metastatic adenocarcinoma 진단됨. 2016년 12월부터 4월까지 Gemcitabine, Erlotinib 병행항암요법 시행하던 중 Chemo induced interstitial lung disease 진단받아 Gemcitabine mono로 시행했으나 pneumonia로 중단, 2017년 4월에 시행한 chest CT 상 양측 폐엽에 다발성 necrotic nodule이 확인됨. 2017년 7월부터 9월까지 5-Fu, Adriamycin, Mitomycin으로 3차 시행했으나 기력저하, 식이불량, 호흡불편감으로 추가적인 항암화학요법 거부함(Fig. 2, Table 1). 2017년 5월부터 항암제 부작용 완화 및 컨디션 관리 위해 내원하셨으며 항암화학요법 중단 이후 지속적인 통합암치료 희망함.
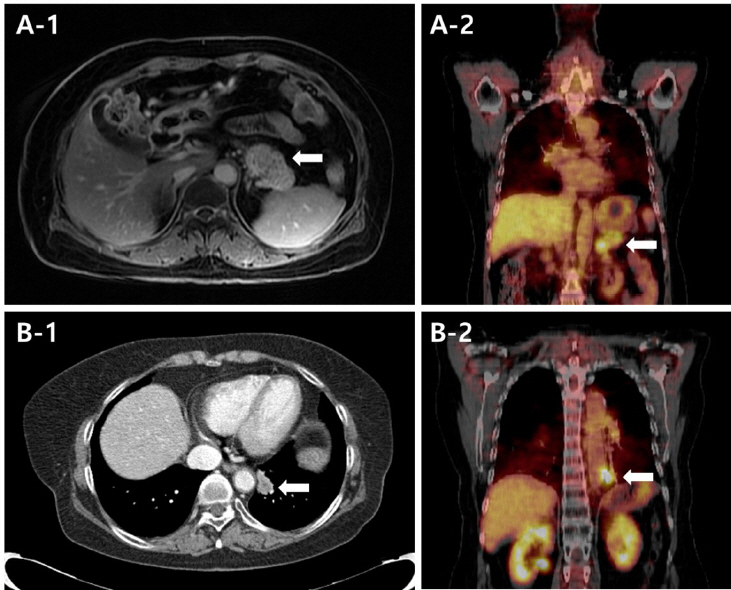
Image studies of the diagnosis.
In both A-1 (magnetic resolution image) and A-2 (PET-CT), white arrows indicate the hypermetabolic mass of pancreatic cancer observed in 2015.03. In B-1 (CT) and B-2 (PET-CT), white arrows point to lung metastases identified in 2016.12.
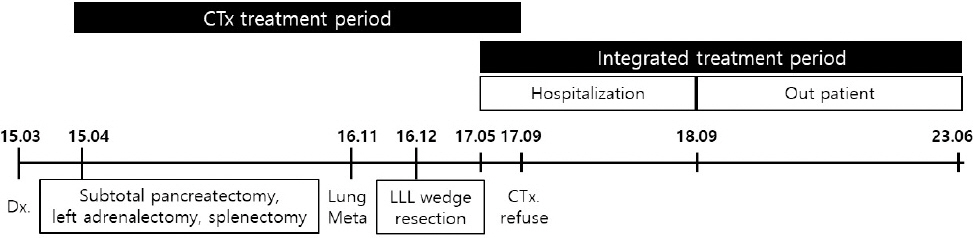
Time table of the patient.
CTx : chemotherapy, Dx : diagnosis, Meta : metastasis, LLL : left lower lobule
8. 통합암치료 과정
2017년 5월부터 2018년 9월까지 총 7회 입원 및 2018월 10월부터 현재까지 월 1-5회 외래치료 진행함(Table 2). 입원기간 : 2017년 05월 25일-2017년 06월 01일, 2017년 07월 18일-2017년 07월 25일, 2017년 08월 05일-2017년 08월 08일, 2017년 08월 16일-2017년 08월 26일, 2017년 09월 18일-2017년 10월 03일, 2017년 10월 13일-2017년 10월 21일, 2018년 09월 15일-2018년 09월 20일
1) 한방치료 : 한방 초진은 2015년 7월이었으나 본격적인 치료는 2017년 5월 25일부터 2018년 9월 20일까지 총 7회 입원하여 집중치료 하였고, 그 후 2023년 6월 현재까지 주 1회 외래로 내원하여 치료를 시행. 한방치료는 입원 기간 동안 매일 침치료, 복부 뜸치료, 산삼면역약침치료를 시행하였고, RGS, 진세노필 복용을 추가하였음. 필요시 증상에 따라 삼출건비탕, 육군자탕, 독활지황탕, 십전대보탕을 투약함. 외래 방문 시 침치료, 복부 뜸치료를 시행하였고, 2018년 9월 28일부터 2020년 7월 10일까지 기간 중 총 105일간 십전대보탕을 투약하였음.
(1) 침치료 : LI4, LI6, ST42, ST40, PC7, HT7, LR3, KI3, LU8에 1일 2회, 0.2×30 mm(동방침, 동방메디컬, 한국)의 호침을 사용하여 15분 유침함.
(2) 뜸치료 : 지름 25 cm인 7구 별뜸(힐링선, 한국)의 중심을 GV8에 위치시켜 1일 1회, 60분 시행함.
(3) 산삼면역약침 : 산양산삼미세분말 400 g과 정제수 12 L 초고속 진공 저온 농축 추출기로 85도로 72시간 전탕 후 얻어진 증류추출액을 NaCl을 첨가하여 0.9%로 농도를 조절한 후 세척 멸균 처리한 약침제재를 5 ml씩 1일 1회 ST25에 주입.
(4) 진세노필 : 산양산삼을 동결건조한 후 20 μm 이하(600매쉬 필터)로 분쇄해서 얻은 산삼분말 3 g에 봉밀 2 g을 가하여 5 g으로 제환함. 1일 1환씩 아침 공복시에 복용함.
(5) RGS : 산양산삼 분말 6.6 g을 증류수에 전탕한 액상 한약제 50 ml를 식후 1시간에 복용함.
(6) 항암플러스 : 삼칠근, 동충하초, 산자고, 인삼, 우황, 진주분, 유향, 몰약 8가지 약제를 300 mesh로 분쇄하여, 캡슐에 담아 1T 500 mg을 1일 3회 복용함.
2) 양방치료
(1) Thymosin α1 : 헤리주사(Thymosin-α1 1.6 mg)를 주 2회씩 피하 또는 근육 주사함.
(2) Mistletoe : 압노바비스쿰Q(Viscum Album 0.02 mg/ mL)을 주 2회 피하주사 시행함.
(3) 글루타치온 : 루치온주(Glutathione 600 mg) 1앰플을 생리식염수 100 ml에 혼합하여 주 2회 정맥주사 시행함.
(4) 고용량 비타민C 주사 : 생리식염수 750 ml에 비타민C 60 g을 혼합하여 주 2회 정맥주사 하였는데, 매번 진코발(Ginkgo Leaf Dried Ext. 3.5 mg/mL) 1앰플, 비콤헥사(비타민 B1 B2 B3 B6 B12 덱스판 테놀) 1앰플을 혼합하여 사용하였음.
9. 치료경과
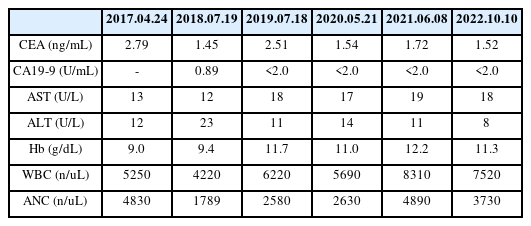
2017년 9월 지속적인 호흡 불편감 및 기력 저하를 호소하며 항암화학요법을 거부한 뒤 2017년 11월에 촬영한 흉부 CT상에서는 2017년 4월에 촬영한 영상(Fig. 3-A)에 비해 both lung necrotic nodule size는 감소되었지만 pulmonary edema 및 pericardial effusion이 확인되었다(Fig. 3-B). 통합암치료만 적용했던 2018년 4월의 chest CT상에서도 유의한 크기 변화 없는 stable state of lung metastasis 소견이었고(Fig. 3-C) 이후 2019년 7월, 2020년 5월, 2020년 12월, 2021년 6월, 2022년 7월, 2022년 10월 촬영한 chest CT상에서도 stable state 상태를 확인하였다(Fig. 3D-I). 암의 진행 여부를 확인하기 위한 CA19-9, CEA상에서도 뚜렷한 상승 소견은 관찰되지 않았으며, 항암화학요법 이후 저하된 골수기능으로 낮아졌던 헤모글로빈 수치도 2017년 4월 24일에는 9.0에서 2022년 10월 10일에는 11.3으로 수치가 회복되었다. CBC 및 absolute neutrophil count (ANC)에서도 회복경향을 보였다. 간기능 관련 지표인 AST와 ALT도 정상범위를 유지하였다(Table 3). 항암화학요법과 한방치료를 병행했던 2-4차 본원 입원 치료 기간(2017년 07월 18일~2017년 08월 26일) 당시 위염으로 인한 식욕부진, 속쓰림, 호흡불편감은 환자 진술 상 경감되었으며, 항암화학요법을 적용하지 않았던 2017년 9월 이후에는 해당 증상은 모두 관해 되었다. 같이 호소하였던 소화 불량 및 변비 증상도 7차례 입원 및 외래 치료를 진행하면서 점차 호전되었다.
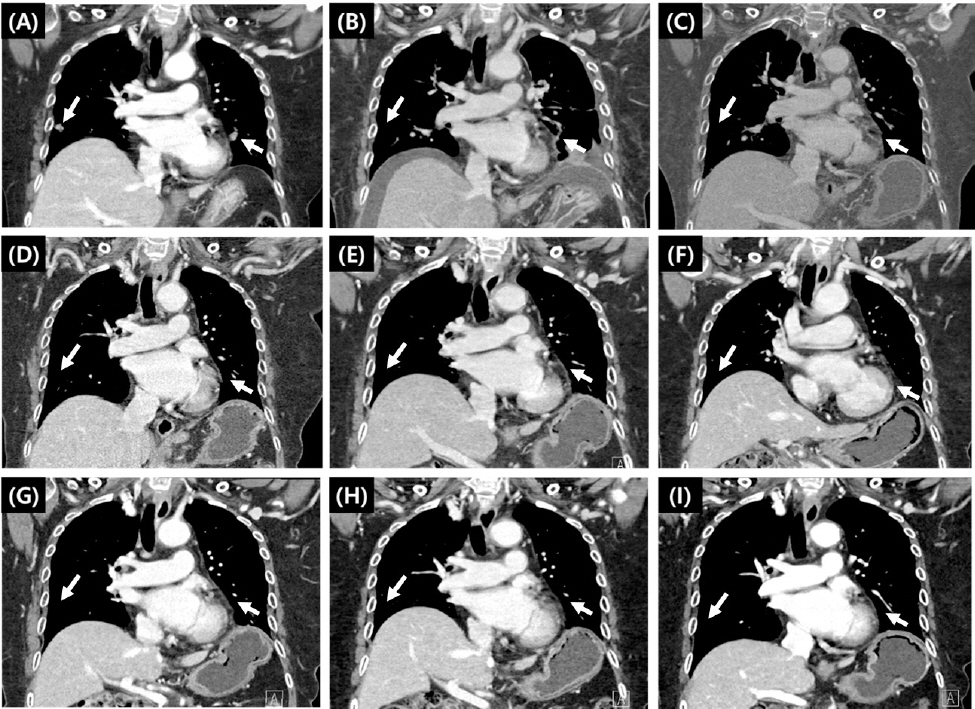
Evaluation of treatment by CT scan.
New metastatic masses were found on April 21, 2017 (A). Decreased extent of suspicious metastatic nodules in both lungs was found (white arrows), alongside the presence of cardiomegaly with pleural effusion on November 13, 2017 (B). Stable state of lung metastasis on April 12, 2018 (C). No interval changes of both lung metastasis on July 18, 2019 (D), May 23, 2020 (E), December 8, 2020 (F), June, 8, 2021 (G), July 4, 2022 (H) and October 10, 2022 (I).
III. 고 찰
췌장암은 초기 단계에서 진단하기 어려우며, 수술적 절제만이 완치할 수 있는 중재로 알려져 있다. 하지만 통계적으로 췌장암 환자 중 10-20%만이 절제 가능한 상태이고, 50-60%는 원격 전이가 동반되고 있으며, 20-30%는 국소적으로 진행된 절제 불가능한 상태로 진단된다11. 또한 2017년 기준 췌장암의 5년 상대생존율은 12.2%로 이 수치는 20년간 거의 변동이 없었다4.
본 환자는 2015년 진단 당시 영상검사 상 pancreatic tail mass가 발견되었고 수술적 절제가 가능하여 췌장의 부분 절제와 전이가 확인된 좌측 부신 및 비장 절제술을 받았다. 수술 후 Gemcitabine과 방사선요법을 병행하였고, 이후 평가에서 폐 전이가 확인되어 2016년 12월 폐엽절제술을 받았다. 추가적인 고식적 항암화학요법을 진행했지만 pneumonia 및 혈구 감소로 인한 기력 저하를 호소하였고, 또다른 미세 lung nodule이 확인되면서 결국 환자는 고식적 항암화학요법 중지하였다. 원격 전이가 나타난 췌장암 환자의 예후는 매우 불량하지만, 본 환자는 항암화학요법을 중단한 뒤 본 병원에서 입원치료와 외래치료를 통해 통합암치료를 지속하였다. 진단 후 8년이 지난 현재에도 생존해 있으며, 주기적인 영상검사로 확인한 결과 미세 lung nodule의 진행성 양상 및 과대사성 병변이 확인되지 않았다. 오히려 항암화학요법을 중단한 이후 항암 부작용이었던 폐렴 및 위염 증상과 골수 억제에 따른 기력저하감은 경감되어 삶의 질도 크게 개선되었다.
본 증례에서 통합암치료에 사용한 침치료와 구법은 항암화학요법의 부작용 완화뿐만 아니라 그 자체로 종양인자 감소, 생존 기간 연장, 종양 크기 감소와 같이 직접적인 항암 효과가 있음이 최신 연구를 통해 밝혀졌다12. 본 환자에게 입원 기간 동안 투약된 진세노필과 RGS의 대표성분인 ginsenoside Rg3는 췌장암세포의 혈관형성 저하와 mRNA의 발현을 하향 조절시켜 결과적으로 항종양 효과를 보임이 in vivo와 in vitro 모델에서 보고된 바 있다13. 항암플러스는 신생혈관 형성 억제 및 VEGF와 bFGF를 억제한다는 효과가 보고된 바 있으며14, 췌장암 수술 후 투여 시 재발 방지에 효과를 보였다는 증례보고도 있었다15.
환자에게 투여한 고용량의 비타민C는 최근 암세포 독성 효과와 후생유전학적 항암작용, 면역조절 방면에서 효과가 있음이 밝혀져 임상적으로 많이 사용하고 있으며, 항암화학요법들과의 동반 효과 및 부작용을 완화시킨다고 밝혀져 있다16. 또한 환자에게 적용한 mistletoe는 세포사멸사를 유도하고 항종양, 항증식에 관여하여 면역조절 효과를 보인다고 알려져 있고, 췌장암 환자의 건강 관련 삶의 질을 개선시키고 생존 기간을 연장하는 데 효과가 있음이 보고되고 있다17. Thymosin α-1은 흉선 조직에서 분리된 펩타이드로 선천 면역반응과 적응 면역 반응을 모두 자극하여 항종양효과가 있음이 확인되었다18.
본 증례는 단일 증례라는 한계와 더불어 한양방의 복합적인 중재가 장기간 적용되었기 때문에 특정 중재의 효과를 논의하기에는 어렵지만, 장기간 통합암치료를 시행했을 때 생존 기간 연장 및 암세포의 진행성 양상 억제가 객관적 지표로 확인되었다는 데 의미가 있다. 또한 항암 중단 후에는 폐렴과 위염이 호전되어 재발되지 않았고, 정량적 지표로 측정되지 않았지만 환자의 진술 및 의무기록 상 기력 저하 및 식욕부진 증상도 완화되어 환자의 삶의 질을 보장하는 치료적 수단으로의 가능성을 확인하였다. 단 진단 당시 췌장 및 부신 절제가 가능하여 원발 병소를 제거한 점이 호전 결과에 영향을 줄 가능성도 배제할 수는 없다고 판단된다.
통합암치료가 항암화학요법이 불가능한 전이성 췌장암환자에게 적용할 수 있는 치료법으로써 효과와 안전성을 검증하기 위해 다수의 환자들 대상으로 한 임상연구들이 추가적으로 필요할 것으로 사료된다.
IV. 결 론
전이성 췌장암 진단 후 통합암치료를 통해 암세포의 추가적인 진행 억제시켜 5년 이상 생존이 확인된 증례가 있어 항암화학요법 및 수술적 중재가 불가능한 환자에게 가능한 치료적 대안으로 제시하는 바이다.