표준 치료를 받고 있는 제2형 당뇨병 환자에 대한 구미강활탕, 평위산, 반하사심탕 복용이 혈당에 미치는 영향 및 안전성 연구
A Retrospective Study of the Effectiveness and Safety of Banhasasim-tang, Gumiganghwal-tang, or Pyeongwee-san in Patients with Type 2 Diabetes Mellitus
Article information
Abstract
Objective:
This study was conducted to evaluate the hypoglycemic effect and safety of herbal extracts in patients with type 2 diabetes mellitus.
Methods:
We investigated 19 hospitalized patients with type 2 diabetes mellitus who were administered Banhasasim-tang (BST), Gumiganghwal-tang (GGT), or Pyeongwee-san (PWS) at Kyung Hee University Korean Medical Hospital for at least three days between January 2012 and December 2021. Their clinical characteristics and laboratory tests were reviewed retrospectively. The glucose-lowering effect of the herbal extracts was assessed by comparing blood glucose levels, including fasting blood sugar (FBS), two-hour postprandial glucose (PP2) levels, and glycated hemoglobin levels. To evaluate the safety of the herbal extract, liver function test and kidney function test results were compared, including aspartate aminotransferase (AST), alanine aminotransferase (ALT), blood urea nitrogen (BUN), and creatinine (Cr).
Results:
After taking herbal extracts, PP2 and HbA1c levels significantly decreased from 205.82 mg/dL to 171.41 mg/dL and 7.58% to 6.62%, respectively. The safety profile reported no significant difference after taking herbal extracts.
Conclusions:
BST, GGT, and PWS may have hypoglycemic effects in patients with type 2 diabetes mellitus taking hypoglycemic medication.
Ⅰ. 서 론
제2형 당뇨병은 인슐린 저항성과 점진적인 인슐린 분비 결함으로 발생하는 질환으로, 전 세계적으로 당뇨병 환자는 지속적으로 증가하고 있으며 진단 연령 또한 낮아지는 추세이다1. 2022년 질병관리청에서 공개한 우리나라 당뇨병 유병률은 2020년을 기준으로 30세 이상 성인의 10.7%를 차지하여 10명 중 1명에 해당하며2, 65세 이상 성인에서는 약 10명 중 3명(27.6%)이다3. 당뇨병은 고혈당과 같은 급성 합병증과 미세혈관 및 대혈관질환 등의 만성 합병증을 야기하여 환자 개인의 삶의 질을 저하시킬 뿐 아니라 사회 및 국가에도 환자 진료에 필요한 재원을 소비하게 하기 때문에 예방하기 위해 적극적인 혈당 조절이 필요하다.
최근의 당뇨병 치료 원칙은 단순한 혈당의 조절보다는 심뇌혈관질환을 포함한 합병증의 치료에 초점을 두고 있으며 합병증 위험도에 대한 평가와 여러 가지 약제들의 조기 복합 처방을 권장하고 있다4. 인슐린, GLP-1 유사체, DPP-4 억제제 등 다양한 약제를 이용한 약물요법뿐만 아니라 운동요법, 식이요법, 자기혈당측정, 자기관리교육 등을 통해 질환에 대해 이해하고 다각도적인 측면에서 혈당개선을 도모하고 있다.
그럼에도 불구하고 당뇨병 환자에 대한 치료 결과가 만족스러운 수준은 아니다. 제2형 당뇨병 성인에게서 일반적인 혈당조절 목표는 당화혈색소 6.5% 미만이지만5, 2020년 자료에 의하면 당뇨병을 가진 성인 10명 중 6~7명만이 당뇨병을 가진 것을 알고 있고, 치료를 받고 있는 경우는 10명 중 6명이었으며, 당화혈색소 6.5% 미만으로 조절되는 경우는 28.3%, 당화혈색소 7.0% 미만으로 조절되는 경우는 56.9%에 불과한 것으로 드러나2 병행할 수 있는 다른 치료법의 필요성이 제기되고 있다.
구미강활탕, 평위산, 반하사심탕은 모두 건강보험심사평가원에서 의료보험용 혼합엑기스제제로 지정한 56종의 한약제제에 해당하며, 56가지 혼합엑기스산제 중 2017년부터 2020년까지 꾸준히 청구건수 1-10위 내에 해당하는 다빈도 처방 약물이다6. 특히 이미 선례연구가 있는 오적산7과 경희의료원에서 복용사례 정보를 수집할 수 없는 처방인 궁하탕을 제외하면 평위산과 구미강활탕은 의료보험용 혼합엑기스제제 중 최빈도 처방에 해당하여 혈당에 미치는 영향을 검증하고자 하였으며, 반하사심탕8,9은 혈당 강하효과가 보고된 바 있으나 사람을 대상으로 한 연구는 아니였기 때문에 본 연구를 통해 혈당 변화를 관찰해보고자 하였다. 또한 세 가지 한약 모두 항염증효과가 있어7,10,11 인슐린저항성 개선효과를 기대해볼 수 있지만 대부분의 연구가 동물을 대상으로 한 실험연구로, 추가적인 연구가 필요한 상황이다.
이에 2012년 1월 1일부터 2021년 12월 31일까지 경희대학교 부속 한방병원에서 입원 치료를 받은 제2형 당뇨병 환자에게 반하사심탕, 평위산, 구미강활탕을 투여하였을 때의 혈당 변화를 후향적으로 관찰하여 보고하는 바이다.
Ⅱ. 연구대상 및 방법
1. 연구대상
본 연구는 2012년 1월 1일부터 2021년 12월 31일까지 경희대학교 부속한방병원에서 3일 이상 입원하여 치료받은 만 19세 이상의 제2형 당뇨병 환자 중에서 입원 기간 동안 반하사심탕, 평위산, 구미강활탕 중 1가지 종류의 혼합엑기스제제를 3일 이상 복용한 환자를 대상으로 하였다. 한방병원 전문의의 처방에 따라 하루 1포씩 2회 또는 3회 복용하였으며, 진단명은 제7차 한국표준질병사인분류 상 제2형 당뇨병에 해당하는 E11을 포함하는 모든 질병코드를 대상으로 하였다. 4가지 혼합엑기스제제는 경희대학교 부속 한방병원에서 사용하는 한국신약의 한방의료보험용 혼합엑기스제제로 제한하였다(Table 1).
연구대상자는 혼합엑기스제제를 복용하는 동안 경구혈당강하제 또는 인슐린의 투약 용량에 변화가 없고, 혼합엑기스제제 복용 기간 및 복용 기간 전후 3일 동안 공복혈당과 식후 2시간 혈당을 포함하여 하루 2회 이상 혈당을 측정한 기록이 있는 경우만 포함하였다. 또한 혼합엑기스제제를 복용하는 기간 중 혈당에 즉각적인 영향을 끼칠 수 있는 전신성 스테로이드 약물을 사용한 경우는 배제하였다.
2. 연구방법
선정기준에 부합하는 연구대상을 선별하기 위해 의무기록팀에 정보를 요청하였으며, 처방전달시스템(Order Communication System, OCS)과 전자의무기록(Electronic Medical Records, EMR)상의 의무기록을 후향적으로 조사하여 인구 통계학적 정보(나이, 성별, 키, 체중)와 주진단명, 당뇨병 진단 시점, 과거력, 식단, 한약 복용력, 투약 중인 당뇨 약물, 처방내역, 각종 검사 결과에 대한 정보를 수집하였다.
혼합엑기스제제를 복용했을 때 혈당에 미치는 효과를 알아보기 위해 약물 복용 시작 3일 전과 후의 공복혈당 수치와 식후 2시간 혈당 수치의 평균값 변화를 각각 비교하였다. 혈당은 자가혈당측정기를 이용해 손가락 끝의 모세혈관 혈액을 채취하여 측정하였다. 혈당 수치의 변화는 혼합엑기스제제의 종류를 기준으로 분류하여 하위집단 분석을 시행하였다. 또한 장기적인 혈당 수치 변화를 살펴보기 위해 약물 복용 시작 및 종료일 기준으로 전후 7일 이내에 시행한 당화혈색소 수치를 수집하였다.
혼합엑기스제제의 안전성을 평가하기 위해 약물 복용 시작일로부터 7일 이전 사이, 약물 복용 종료일로부터 7일 사이에 시행한 간 기능검사와 신 기능검사의 결과를 비교하였으며, Aspartic aminotransferase(AST), Alanine aminotransferase(ALT), γ-glutamyltransferase (GGT), Blood Urea Nitrogen(BUN), Serum Creatinine (SCr) 수치를 이용하였다. 단, 상기 지표에 대해 부분적인 기록만 있는 경우 그 지표에 한해 제한적 분석을 시행하였다.
3. 통계 처리
GraphPad Prism ver. 5(Graphpad software. Inc., San Diego, USA)를 사용하였으며, 정규분포 여부에 따라 Paired t-test 또는 Wilcoxon signed rank test를 통해 통계적 분석을 실시하였다. 연구 대상자의 임상적 특성 및 검사 결과는 평균±표준편차(Mean±S.D.)로 표시하였고, 소수점 셋째 자리에서 반올림하여 소수점 둘째 자리까지 표기하였다. 양방 검정유의도(Two-tailed p-value)는 신뢰도 95%에서 P-value가 <0.05일 때를 기준으로 하였다.
4. 연구 윤리
본 연구는 경희대학교 한방병원의 기관생명윤리위원회(Institutional Review Board, IRB)의 승인을 받았다(KHMC 2022-04-001).
Ⅲ. 결 과
1. 연구대상의 일반적 특성
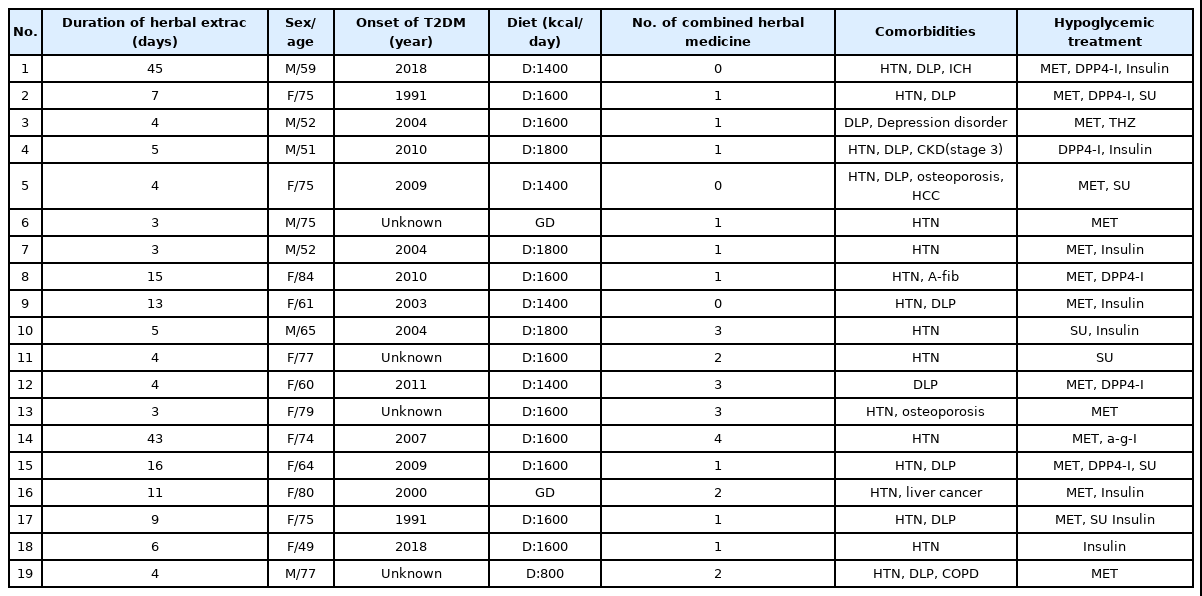
2012년 1월 1일부터 2021년 12월 31일까지 경희대학교 부속 한방병원에서 입원 치료를 받은 2형 당뇨병 환자 중 입원 기간 내에 3일 이상 해당 혼합엑기스제제를 복용한 환자는 26명이었으며, 그 중 혈당검사 결과를 수집할 수 있는 환자는 총 19명이었다(Fig. 1). 연구 대상자들의 평균 연령은 67.11± 12.17세였으며, 그 중 남자가 7명(37%), 여자가 12(63%)로, 여성의 비율이 더 높았다. 평균 신장은 159.33±7.78 cm, 평균 체중은 65.86±11.89 kg로, 체질량지수의 평균값은 25.86±3.85 kg/m2이었다. 대상자들은 입원 기간 중 다른 한약 치료, 침구 치료 등 한의학 치료를 병행하였다. 당화혈색소 수치는 11명의 대상자로부터 얻을 수 있었으며, 평균은 7.38±1.28%이었다(Table 2). 19명의 연구 대상자 중 2명을 제외한 17명은 모두 하루 섭취 칼로리를 제한하는 당뇨 치료 식이를 섭취했다(Table 3).
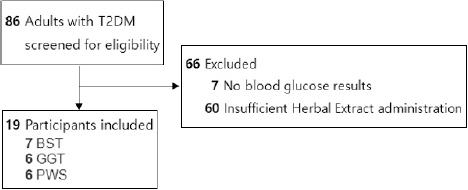
Participant disposition.
T2DM : type 2 diabetes mellitus, BST : Banhasasim -tang, GGT : Gumiganghwal-tang, PWS : Pyeongwi -san
환자들의 주진단명은 뇌경색이 5명(26.3%)으로 가장 많았으며, 그 외에도 중대뇌동맥 협착증, 폐암, 천식과 같은 호흡기계질환, 슬관절염, 척추 협착증과 같은 근골격계 질환, 위마비 등의 소화기계질환이 있었다(Table 3). 대상자들은 고혈압(17명, 89%), 이상지질혈증(10명, 53%), 심방세동(1명, 5%), 만성 신부전(1명, 5%) 등의 기저질환을 가지고 있었다(Table 2).
2. 혼합엑기스산제 복용현황 및 병용약물 분석
연구 대상자 19명 중 반하사심탕을 복용한 환자는 7명(36%), 구미강활탕과 평위산을 복용한 환자는 각각 6명(32%)이었다. 한약 평균 복용기간은 10.35±12.21일이었으며, 15일 이상 복용한 4명이었으며, 대부분의 환자들은 10일 미만으로 복용하였다(13명)(Table 3). 반하사심탕의 평균 복용기간은 10.14±15.43일, 구미강활탕은 14.83±14.41일, 평위산은 6.71±5.05일이었다(Table 5). 2명을 제외한 19명의 환자는 다른 한약을 함께 복용하고 있었다(Table 3).

Change in Efficacy Outcomes Before and After Administration of Herbal Extract with Hypoglycemic Agents
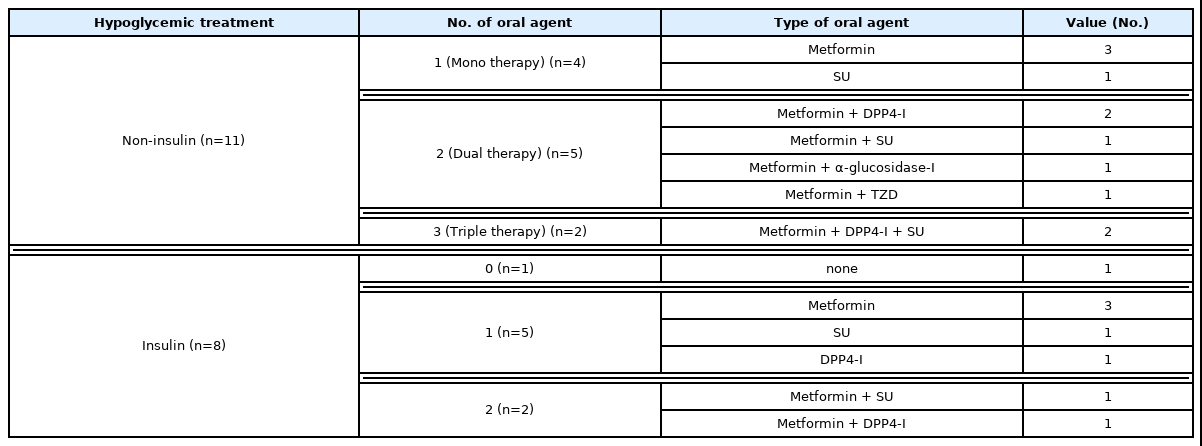
모든 대상자는 혼합엑기스산제를 복용하기 전부터 혈당 조절을 위한 치료를 받고 있었다. 1명을 제외한 18명의 대상자는 1가지 이상의 경구혈당강하제를 복용하고 있었으며, 경구혈당강하제만 복용하는 환자는 11명, 인슐린만 단독 투여하는 환자는 1명, 경구약과 인슐린을 병용 투약하는 환자는 7명이었다. 경구혈당강하제 종류 중 metformin을 가장 많이 복용하고 있었으며(15명, 79%), DPP-4 억제제가 6명(32%), 설폰요소제가 6명(32%), 티아졸리딘디온이 1명(5%), α-글루코시데이스 억제제가 1명(5%)이었다. 한 가지 계열의 경구혈당강하제를 복용하는 경우는 4명(21%)이었으며, 두 가지 이상의 계열의 경구혈당강하제를 동시 복용하는 경우는 9명(47%)으로, 메트포르민과 DDP-4 억제제를 병용하는 경우가 3명(16%)으로 가장 많았다(Table 4).
3. 혼합엑기스제제 복용 전후 혈당 수치 변화
연구 대상자의 공복혈당은 혼합엑기스제제 복용 전 평균 130.35±32.16 mg/dL에서 복용 후 평균 132.82 ±25.02 mg/dL으로 소폭 증가하였다. 하위집단을 살펴보면, 반하사심탕 그룹에서 공복혈당은 복용 전 평균 144.6±26.58 mg/dL에서 복용 후 113.0±13.39으로 감소하였지만 통계적으로 유의미한 차이는 없었다(p>0.05). 구미강활탕 그룹에서 공복혈당은 복용 전 평균 116.67±16.45 mg/dL에서 복용 후 평균 118.5± 11.64 mg/dL로 증가하였고(p>0.05), 평위산 그룹에서 공복혈당은 복용 전 평균 132.17±45.20 mg/dL에서 복용 후 평균 168.4±31.31 mg/dL으로 증가하였다(p>0.05)(Table 5, Fig. 2).

Change in blood glucose before and after co-administration of herbal extracts and hypoglycemic agents.
FBS : fasting blood sugar, PP2 : 2 hours post- prandial plasma glucose, HbA1c : glycated hemoglobin
반면, 혼합엑기스제제를 복용한 대상자의 식후 2시간 혈당 수치는 복용 전 205.82±49.20 mg/dL에서 복용 후 171.41±32.2 mg/dL로 통계적으로 유의미한 수준으로 감소하였다(95% credential interval, [CI], 11.46-57.36; p=0.0058). 하위그룹을 보면, 반하사심탕 그룹에서 식후 2시간 혈당 수치는 복용 전 195±57.89 mg/dL에서 171.8±25.57 mg/dL로 감소하였지만 통계적으로 유의미한 수준은 아니었다(p>0.05). 구미강활탕 그룹에서 식후 2시간 혈당 수치는 복용 전 204.17±42.64 mg/dL에서 복용 후 156.5±31.83로 감소하였으며, 통계적으로 유의미한 수준이었다(95% CI, 14.31-81.03; p=0.0144). 평위산 그룹에서 식후 2시간 혈당 수치는 복용 전 216.5±54.67 mg/dL에서 복용 후 186±35.69 mg/dL으로 감소하였지만 통계적으로 유의한 차이는 없었다(p>0.05)(Table 5, Fig. 2, Fig. 3).

Change in 2-hour postprandial glucose levels before and after administration of each herbal extract and hypoglycemic agents.
19명의 연구 대상자 중 11명에게서 당화혈색소 수치를 얻었으나, 6명에게서 혼합엑기스제제 복용 전후 당화혈색소 수치 변화를 알아낼 수 있었으며, 복용 전 당화혈색소는 평균 7.58±1.32%에서 복용 후 6.62±0.78%로 통계적으로 유의한 감소를 보였다(95% CI, 0.2652 to 1.668; p=0.0165)(Table 6, Fig. 2C). 개별 혼합엑기스제제에 대한 당화혈색소 수치 변화는 사례가 적어 통계를 구할 수 없었다.
4. 혼합엑기스제제 복용 후 간 기능 변화
연구 대상자 중 간질환을 가진 사람은 없었으며, 혼합엑기스제제 복용 전후 AST, ALT 수치는 14명의 대상자에서 얻을 수 있었다. 모든 대상자의 AST, ALT 수치는 복용 전후 모두 정상 범위에 해당하였다. AST 수치는 혼합엑기스제제 복용 전 24.50± 8.53 U/L에서 복용 후 22.58±6.32 U/L로, ALT 수치는 복용 전 17.86±6.36 U/L에서 복용 후 17.08±6.64 U/L로 감소하였지만, 통계적으로 유의한 차이는 없었다(p>0.05)(Table 7).
반하사심탕 그룹의 AST 값과 ALT 값은 복용 전 각각 24.4±5.46 U/L, 18.60±8.26 U/L에서 복용 후 각각 19.00±4.69 U/L, 17.20±8.01 U/L으로 감소하였으며(p>0.05), 구미강활탕 그룹의 AST 값과 ALT 값은 복용 전 각각 22.75±3.30 U/L, 16.5±5.74 U/L에서 복용 후 각각 22.67±2.08 U/L, 13.33±2.31 U/L으로 감소하였다. 평위산 그룹의 AST 값과 ALT 값은 복용 전 각각 26±13.87 U/L, 18.2±5.97 U/L에서 27±8.16 U/L, 19.75±6.99 U/L으로 증가하였지만 통계적으로 유의하지는 않았다(p>0.05).
5. 혼합엑기스제제 복용 전후 신 기능 변화
혼합엑기스제제 복용 전후 BUN과 Creatinine 수치는 14명에게서 구할 수 있었으며, 그 중 1명은 만성 신질환을 가지고 있었다. 만성 신질환이 있는 환자를 포함한 총 3명의 대상자는 혼합엑기스제제를 복용하기 전 BUN, Creatinine 수치가 정상보다 높았다. 그중 2명의 BUN 수치는 혼합엑기스제제를 복용 후 각각 28 mg/dL에서 21 mg/dL, 39 mg/dL에서 20 mg/dL으로 감소하였으나, 만성 신질환이 있던 환자는 BUN 수치가 혼합엑기스제제 복용 전 25 mg/dL에서 복용 후 33 mg/dL로 상승하였다. 3명의 Creatinine 수치는 혼합엑기스제제 복용 전후 각각 1.45 mg/dL에서 1.46 mg/dL, 2.04 mg/dL에서 0.6 mg/dL으로 변화했으며 만성 신질환이 있던 환자는 1.92 mg/dL에서 2.1 mg/dL로 상승하였다. 통계학적으로 유의하지는 않았다(p>0.05). 나머지 연구 대상자 11명의 혼합엑기스제제 복용 전후 BUN, Creatinine 수치는 모두 정상범위 내에 있었다. BUN과 Creatinine 수치 평균값은 혼합엑기스제제 복용 전 각각 18.57±7.65 mg/dL, 0.90±0.55 mg/dL에서 복용 후 16.21±6.65 mg/dL, 0.85±0.46 mg/dL로 감소하였지만 통계적으로 유의한 수준은 아니다(p>0.05).
Ⅳ. 고 찰
당뇨병은 고혈당 자체로서의 문제만이 아니라 심혈관 및 뇌혈관 질환 등을 비롯한 각종 만성 합병증의 직⋅간접적 원인으로 잘 알려져 있어 세심한 관리가 요구되는 중요한 질환이다. 현재 당뇨병 표준 치료는 대한당뇨병학회에서 권고하는 바에 따라 생활습관 교정을 먼저 시도하고 그 후에도 목표 혈당에 도달하지 못하면 경구혈당강하제 단독요법을 시작하며, 단독요법만으로 목표 당화혈색소에 도달하지 못한 경우 기존 약물을 증량하거나 다른 계열 약물과의 병용요법을 조속히 시작한다4.
당뇨병에 대한 수많은 정보와 혁신적인 치료제들이 개발되었지만, 여전히 치료 목표인 당화혈색소 6.5% 미만으로 조절되는 경우는 세 명 중 1명 미만 꼴이며, 당화혈색소 7% 미만으로 조절되는 경우도 절반 정도에 불과한 실정이다. 뿐만 아니라 당뇨병이 진행될수록 인슐린 및 경구혈당강하제 병용 요법의 비율은 증가하는데 비해 혈당 조절이 지속적으로 악화되어 HbA1c는 유병기간 5년 미만 7.1%에서 20년 이상 시 7.7%로 지속적으로 증가하는 경향을 보이며 미세혈관합병증인 신부전의 위험성이 상승한다는 보고12가 있어 보다 효과적인 치료방법의 필요성이 부각되고 있다. 또한 저혈당, 체중증가, 위장장애, 간독성 등의 부작용을 호소하거나13 인슐린 주사 치료에 대한 부담감 및 거부감으로 인해 대다수의 환자가 경구용 혈당강하제 및 생활습관 교정으로만 혈당 조절을 시행하고 있기 때문에 성공적으로 치료 목표에 도달하지 못하고 있다14. 이처럼 기존 치료제의 한계점으로 인해 당뇨병 환자를 위한 보완대체요법 또는 보다 유효한 치료법이 요구되어 왔으며15 그 중 하나의 대안으로 한약을 통한 인슐린 저항성 개선 및 혈당 강하 효과에 대한 연구가 꾸준히 진행되고 있고 있다16.
초반에는 당뇨와 유사한 증상(渴而多飮, 消穀善飢, 渴而尿數有膏油)을 공유하고 있는 개념인 消渴을 중심으로 문헌적 고찰 연구가 진행되었고17, 점차 본초 중심 연구로 발전하여 단미제로는 밀몽화18, 길경19, 목단피20, 금전초21, 포공영22, 맥문동23의 항당뇨효과가 보고되었으며, 상백피와 오미자는 인슐린 분비를 촉진하고, 목향, 상엽, 창출은 인슐린 저항성 감소 효과가 있다고 알려졌다24. 복합제제 관련해서는 대보음환25, 양격산화탕26, 황금탕27의 항당뇨효능이 보고된 바 있다. 그 외 혈당강하효과를 보고한 증례보고논문도 있으나 대체로 실험연구(60.3%)에 치우치고 있는 실정으로13, 한약치료가 실질적인 치료법으로써 자리매김하기 위해서는 추가적인 연구를 통해 효과 및 안전성에 대한 검증이 필요하다.
이에 저자는 56종의 혼합엑기스산제 중 다빈도 처방 상위 10종 약물에 해당하는 반하사심탕, 구미강활탕, 평위산을 복용한 제2형 당뇨병 환자의 혈당 변화를 후향적으로 관찰하였다.
반하사심탕은 기능성소화불량, 소화성궤양, 항암치료 등 소화기 질환에 응용되어온 대표적인 한약물로28, 약물로 당뇨를 유발한 쥐에게 4주간 투여했을 때 공복혈당 수치와 염증인자인 TNF-α가 유의미하게 감소하였다는 보고8가 있으며, 지방 분화 억제 효능뿐 아니라 지방 분화전사인자인 C/EBPα 및 PPAR-γ 또한 농도 의존적으로 유의하게 감소시킨다고 밝혀져 체중 감소 효과를 기대할 수 있고, 더불어 항염증 효과가 있어 이를 통한 인슐린 저항성 개선에도 도움이 될 것으로 추정된다29. 구미강활탕은 혈당강하 효과가 있다고 알려져 있으며8, NO나 PGE2 생성을 억제하는 동시에 염증성 사이토카인인 IL-6 생성 억제하는 항염증 효과가 알려져 있다9. 평위산은 농도와 상관없이 TNF-α, IL-6, PGE2를 유의성 있게 감소시키며 염증 완화 효과가 있다고 알려져 있으나10, 항당뇨효과와 관련한 연구는 없었다. 상기 연구들은 모두 동물실험이었으며, 사람을 대상으로 혈당 강하 효과를 평가한 임상연구는 부재하였다는 한계가 있다.
이에 한방병원에 입원하여 경구혈당강하제를 복용하거나, 인슐린을 투여하거나, 혹은 병용요법을 시행하고 있는 제2형 당뇨병 환자를 대상으로 반하사심탕, 구미강활탕 또는 평위산을 3일 이상 복용한 사례를 수집하였다. 2명을 제외한 17명의 환자는 식이요법을 병행하고 있었다.
혼합엑기스제제 복용 전후의 혈당 수치 변화를 비교하였을 때, 공복혈당 수치는 평균 2.47 mg/dL 증가하였으나 통계적으로 유의미하지는 않았고, 식후 2시간 혈당 수치는 평균 34.41 mg/dL 감소하여 통계적으로 유의하였다. 반하사심탕을 복용한 그룹은 공복혈당과 식후 2시간 수치가 각각 평균 31.60 mg/dL, 23.2 mg/dL 감소하였으나 통계적으로 유의한 수준은 아니었다. 구미강활탕을 복용한 그룹은 공복혈당 수치가 평균 1.83 mg/dL 증가하였으나 통계적으로 유의하지는 않았으며, 식후 2시간 혈당 수치는 평균 47.67 mg/dL 감소하여 통계적으로 유의했다. 평위산 그룹은 식후 2시간 혈당 수치가 평균 30.5 mg/dL 감소하였으나 통계적으로 유의하지는 않았다. 구미강활탕과 평위산을 복용한 그룹에서 공복혈당 수치가 증가한 원인은 명확히 제시할 수 없으나 늦은 시각 음식 섭취, 수면불량, 한약제제의 짧은 반감기를 고려해볼 수 있다. 혼합엑기스제제 복용 후 당화혈색소 수치는 평균 0.96% 감소하여 통계적으로 유의했다.
혼합엑기스제제 복용 후 당뇨병 진료지침에서 제시한 치료 목표에 도달하였는지 확인하였다. 혼합엑기스 제제 복용 후 당화혈색소 수치는 평균 6.62%로, 치료목표인 6.5%에 근접하였다. 반하사심탕과 구미강활탕을 복용한 경우 모두 공복혈당 치료 목표인 130 mg/dL 미만과 식후 2시간 혈당 목표인 180 mg/dL 미만에 도달하였다. 평위산을 복용한 경우 식후 2시간 혈당 평균은 186 mg/dL로 치료 목표 내로 도달하지는 못했지만 평위산 복용 전인 216.5 mg/dL보다 치료목표에 근접했음을 알 수 있다.
본 연구의 결과는 식이요법과 함께 표준치료를 받고 있음에도 치료 목표에 도달하지 못한 제2형 당뇨병 환자들에게 당화혈색소 수치 및 식후 2시간 혈당이 감소되었다는 점에서 혈당 수치 개선의 의미가 있었다. 특히 본 연구에서 혈당 강하효과가 비교적 두드러지게 나타난 반하사심탕과 구미강활탕의 경우 추가적인 연구를 통해 혈당 강하 효과에 대한 평가가 필요할 것으로 사료되는데, 기존에 알려진 항염증 효능을 통해 인슐린 저항성 개선효과30를 기대해볼 수 있기 때문이다.
본 연구의 한계점으로는 병원에서 제공한 식사를 제외한 음식 섭취량 및 활동량의 변화, 한약을제외한 한방치료 정보를 파악할 수 없고, 혼합엑기스제제 복용기간이 짧았으며, 약물별로 충분한 피험자 수를 확보하지 못했다는 점이다. 또한 환자마다 기존에 복용하고 있던 한약은 청혈단, 청장캡슐 등으로 종류가 상이하였는데, 혼합엑기스제제 복용 중 용량이나 용법이 변경된 사례는 없었음에도 혈당에 미치는 영향이 알려진 바 없어 추가적인 연구가 필요할 것으로 사료된다.
Ⅴ. 결 론
본 연구는 제2형 당뇨병을 진단받은 한방병원 입원환자를 대상으로 한방의료보험용 혼합엑기스제제인 반하사심탕, 구미강활탕, 평위산 투약을 표준치료와 병행하였을 때, 식후 2시간 혈당을 통계적으로 유의미하게 감소시킴을 알 수 있었다. 반하사심탕은 공복혈당과 식후 2시간 혈당을 모두 감소시켰지만 통계적으로 유의한 수준은 아니었다. 구미강활탕은 식후 2시간 혈당 수치를 통계적으로 유의하게 감소시켰다. 평위산은 식후 2시간 혈당 수치를 감소시켰지만 통계적으로 유의한 수준은 아니었다. 혼합엑기스제제를 복용 후 6명의 당화혈색소 수치가 통계적으로 유의한 수준으로 감소하였다. 또한 간 기능과 신 기능 측면에서 안전하다는 점을 확인하였다.
감사의 글
본 연구는 보건복지부의 재원으로 한국보건산업진흥원의 보건의료기술 연구개발사업 지원에 의하여 이루어진 것임(HF20C0022).