조위승기탕으로 호전된 암 환자의 마약성 진통제로 인한 변비 치험 1례
A Case Report on Opioid-Induced Constipation in a Patient with Cancer Treated by Jowiseunggi-tang
Article information
Abstract
Objective:
Jowiseunggi-tang (JWSGT) is a traditional herbal medicine commonly used for purgative activity in constipation. This study evaluates JWSGT for the treatment of opioid-induced constipation (OIC), the most common and debilitating gastrointestinal effect of opioid use.
Methods:
A 64-year-old man with floor of mouth cancer was hospitalized for OIC, and JWSGT was administered orally twice a day for 10 days, along with acupuncture, moxibustion, and cupping. The primary outcome measures were defecation type according to the Bristol Stool Form Scale (BSFS) and the frequency of bowel movements. The Brief Fatigue Inventory (BFI) and the Functional Assessment of Cancer Therapy-General (FACT-G) were used as secondary measures.
Results:
After three days of JWSGT administration, spontaneous bowel movements were observed two to three times per week with improved BSFS from type 2 to 4. A reduction in BFI score (8.7 to 2.0) and an increase in FACT-G score (44.3 to 59.0) suggested an improvement in fatigue level and quality of life.
Conclusion:
This is the first report to assess the efficacy of JWSGT for the management of OIC in patients with cancer, and JWSGT may be an effective option to improve symptoms and quality of life in this group.
Ⅰ. 서 론
암 환자에서 통증은 근치적 치료 이후 39%, 항암치료 중 55%, 진행성, 전이성 및 말기에서 66%의 높은 유병률을 보이며, 전체 암 환자의 38%가 중등도 이상의 통증을 호소하는 것으로 보고되어 있다1. 이러한 중등도 이상의 암성 통증을 조절하기 위하여 아편유사제의 마약성 진통제는 주요한 치료제이나 복용 시 부작용이 동반되어 나타날 수 있다2. 위장관에 분포되어 있는 아편유사제 수용체가 마약성 진통제로 인해 활성화될 경우 위장관의 운동 및 분비에 지장을 주어 정상 위장관 기능을 억제하게 되면 변비 외에도 구역, 구토, 구강건조, 식도역류, 복부 불편감과 같은 다양한 부작용이 동반될 수 있다. 이 중 구역 및 구토는 마약성 진통제를 반복 투여할 시 내성이 생기면서 호전되나, 변비는 내성이 생기지 않는 부작용으로 투약 기간 동안 지속되는 것으로 알려져 있다3.
마약성 진통제로 인한 변비(opioid-induced constipation, OIC)는 마약성 진통제가 중추신경계와 더불어 소화기계에 작용하면서 이차적으로 발생하는 질환의 범주이다. 로마 기준 IV에서는 기능성 위장관 질환이 아닌 마약성 진통제로 인한 부작용으로 분류하였으며, 마약성 진통제를 복용하면서부터 배변 습관 및 형태의 변화, 배변 횟수의 감소, 과도한 힘 주기, 불완전 배변감 또는 배변습관과 연관되어 환자가 고통을 느끼는 경우로 정의된다4. OIC는 마약성 진통제의 가장 흔한 부작용으로 암성 통증으로 인해 마약성 진통제를 사용하는 환자의 52-87%에서 나타나는 것으로 보고되어 있다5. OIC는 암 환자의 삶의 질에 부정적인 영향을 줄 뿐만 아니라 지속적인 변비는 장 폐색과 분변 매복과 같은 심각한 후유증으로 이어질 수 있으며, 진통제에 대한 환자의 순응도에 영향을 주어 추후 통증관리에 어려움을 초래할 수 있기에 적절한 중재가 필요하다6.
기존의 임상진료지침에서는 암 환자의 OIC에 대하여 완하제를 일차 치료제로 권고하고 있는데 일반적으로 삼투성 완하제 또는 자극성 완하제가 선호된다7. 그러나, 완하제의 경우 OIC의 발생 기전에 대한 직접적인 접근이 아닌 관계로 OIC 환자의 약 50%만이 완하제 치료에 호전을 보이는 것으로 보고되어 있다8. 서방형 옥시코돈/날록손 혼합제제(Prolonged-release oxycodone/naloxone)가 OIC의 위험도를 감소시키며, 호전이 없는 OIC 환자에게는 말초 뮤-아편유사제 수용체 길항제(peripherally acting mu opioid receptor antagonists, PAMORAs)와 같은 새로운 표적 치료제를 사용할 수 있다고 권고하고 있으나 PAMORAs의 근거가 되는 대다수의 임상연구가 비암성 통증 환자를 대상으로 한다는 제한점이 존재한다7,9.
암 환자의 OIC에 대하여 한약치료10, 전침치료11, 혈위자극치료12 등의 임상연구가 보고된 바가 있으나, 한의학적 치료가 OIC에 효과적이라는 근거는 아직 제한적이다. 이에 저자는 마약성 진통제로 인한 변비가 있는 암 환자에게 조위승기탕(調胃承氣湯)을 중심으로 한 한의치료를 시행하여 유의한 효과를 얻었기에 치료경과를 다음과 같이 보고하는 바이다.
Ⅱ. 증 례
1. 환 자 : 임 ⃝(64/M)
2. 진 단 : 구강저암(malignant neoplasm of floor of mouth)
3. 최초 진단일 : 2020년 7월 6일
4. 주소증 : 구강통증, 식욕부진, 변비
5. 과거력 : 고혈압, 고지혈증, 알코올성 간경변, 급성 신손상
6. 수술력 : 담낭절제술(2009), 입바닥암절제술, 혀 밑 림프절 절제술, 양측 선택적경부절제술, 기관절개술(2020년 07월 15일)
7. 사회력 : 과거흡연(1~1.5갑/일, 40년), 과거음주(소주 1병/일, 40년)
8. 가족력 : 당뇨(母), 뇌혈관질환(母), 대장암(弟)
9. 현병력
상기 64/M 2020년 7월 6일 구강저암으로 진단받고 7월 15일 입바닥암절제술, 혀 밑 림프절 절제술, 양측 선택적경부절제술, 기관절개술 시행 받았다. 병리학적 소견상 병기는 3기였으며 2020년 8월부터 9월까지 수술 후 항암방사선 동시요법(concurrent chemoradiation therapy)를 시행 받았다. 항암화학요법은 총 6주기로 cisplatin 40 mg/m2을 1주 간격으로 시행하였고, 방사선요법은 1주기 항암화학요법 시행일에 동시에 시작하여 총 6300 cGy를 33회로 나누어 시행하였으며 매주 5회씩 7.5주 동안 시행하였다. 2020년 9월 중순경부터 좌측 구강 통증 심화되어 이로 인한 경구식이 어려워져 2021년 10월 5일 본원 혈액종양내과로 입원하였으며 마약성 진통제인 펜타닐 경피 패치(fentanyl transdermal patch), 속효성 경구용 옥시코돈(oxycodone)의 투여 및 경정맥영양 시행하며 통증 및 식사량이 소폭 호전되었으나 충분한 식이 어려우며, 펜타닐 경피 패치 부착 후 시작된 변비에 대하여 적극적 한방치료 원하여 2020년 10월 13일부터 2020년 10월 29일까지 본과로 전원하여 입원치료를 시행하였다.
10. 초진 시 계통문진
1) 수 면 : 양호, 통증 또는 야뇨로 인한 각성 1-2회, 재입면난 별무
2) 식사/소화 : 식욕 별무, 미음 1공기*3끼/양호
3) 대 변 : 1회/1주, 경변
4) 소 변 : 주간뇨 6회, 야간뇨 1회
5) 한출/한열 : 통증 있을 시 두면부 열감 및 전신 특히 두면부로 자한증상 동반
6) 설진/맥진: 홍설(紅舌), 황태(黃苔)/맥부삭(脈浮數)
7) 복 진 : 소복만(少腹滿)
8) 체 격 : 164.8 cm, 57.5 kg
9) 기 타 : ECOG(Eastern Cooperative Oncology Group) 수행상태 1점
11. 초진 시 이상 검사 소견 : 중등도 이상의 혈액검사 이상 소견은 보이지 않았다.
12. 한의치료
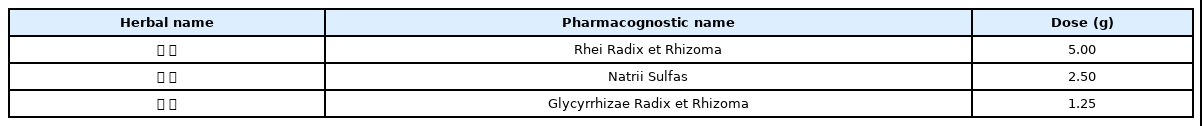
입원 기간 중 2020년 10월 20일부터 29일까지 위장조열(胃腸燥熱)로 인한 변비 완화를 목적으로 조위승기탕 과립제(한국신약, Table 1)를 하루 한 포씩 2회 식후 30분에 투약하였다. 침구치료는 입원 기간 동안 매일 1일 1회 stainless steel 재질의 1회용 멸균 호침(0.20×30 mm, 동방침구제작소)을 사용하여 풍지(GB20), 곡지(LI11), 합곡(LI4), 족삼리(ST36), 태충(LR3) 등의 혈위와 필요에 따라 아시혈을 추가하여 20개 내외의 자침을 시행하고 20분간 유침하였고, 중완(CV12), 관원(CV4)에 1일 1회 40분 간접구를 시행하였으며, 상완(CV13), 중완(CV12), 하완(CV10), 양측 양문(ST21), 족삼리(ST36)에 각 3장씩 직접구를 실시하였다. 부항치료는 요배부 불편감을 호소할 시 간헐적으로 배수혈에 건식부항을 실시하였다.
13. 복용 약물
입원 당시 마약성 진통제로 fentanyl transdermal patch 62 mcg/hr를 부착 중이었고 환자의 통증 호소에 따라 10월 14일 75 mcg/hr, 10월 16일 87 mcg/hr, 10월 20일 100 mcg/hr로 증량하여 유지하였으며 돌발성 통증에는 oxycodone 10 mg 1T를 투여하였다. 동맥경화용제로 ezetimibe/ rosuvastatin 10/10 mg 1T qd, fenofibrate 160 mg 1T qd, clopidogrel 75 mg 0.5T qd를 복용중이었고, 혈압강하제로는 telmisartan/amlodipine 40/5 mg 1T qd를 복용하였으며 간장질환용제로 biphenyl dimethyl dicarboxylate/ursodeoxycholic acid 12.5/50 mg 2C qd를 복용하였고, 혈관강화제 및 순환개선제로 naftazone 10 mg 1T tid, pentoxifylline 400 mg 1T tid를 복용하며 상기 약물 투여는 동일하게 유지하였다.
14. 평가 방법
치료 기간 중 대변의 횟수, 양을 기록하고 대변양상은 Bristol Stool Form Scale(BSFS)을 사용하여 평가하였다, 이는 임상 및 연구에서 배변 상태를 평가하기 위한 가장 흔히 쓰이는 도구로 형태에 따라 7가지로 분류하여, type 1와 2는 경변으로 변비를 의미하고 type 3부터 5는 보통변으로 type 4가 가장 정상변이며 type 6와 7은 연변으로 설사라고 판단한다(Table 2)13. 더불어 암 관련 증상의 변화에 따른 피로도와 삶의 질의 연관성을 관찰하기 위하여 2종의 설문지를 입원 시, 입원 7일차, 퇴원 시 총 3회 시행하였다. Brief Fatigue Inventory(BFI)는 피로도 및 이로 인해 일상생활에 지장을 주는 정도를 측정하기 위한 9개의 항목으로 이루어져 각 문항을 0점부터 10점으로 측정하여 평균값이 1~3점까지는 경증, 4~6점까지는 중등도, 7~10점까지는 중증을 의미한다14. Functional Assessment of Cancer Therapy-General(FACT-G)는 삶의 질을 신체(7문항), 사회/가족(7문항), 정서(6문항), 기능(7문항)의 4가지 영역으로 구분하여 평가하며 각 항목별로 0~4점으로 측정하여 최고점은 108점으로 점수가 높을수록 삶의 질이 높음을 의미한다15.
15. 연구윤리
본 연구는 치험 1례 보고로 임상연구심의위원회(Institutional Review Board, IRB)의 심의에서 심의면제를 받았다(IRB File No. KHNMCOH 2022-04-004).
16. 치료 경과
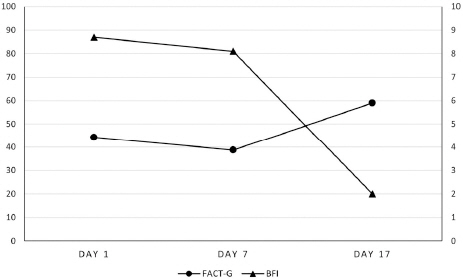
평소 주 3회 빈도로 배변하였으나 2021년 10월 5일 마약성 진통제 투여 후 7일간 무대변양상으로 입원 전날 글리세린 관장 시행 후 경변 양상의 BSFS type 2로 약 150 g 배변하였다. 본과 입원 이후 관장에 대한 거부감 있어 시행하지 않던 중 변의는 있으나 지속적인 무대변양상 호소하여 입원 8일차부터 조위승기탕을 투여하였다. 입원 10일차(복용 3일째)부터 주 2-3회 자발적 배변 유지되며 경변 양상의 BSFS type 2로 약 50 g씩 2회 배변하였고 배변시 용력과 잔변감을 호소하였다. 입원 13일차에 보통변 양상의 BSFS type 3으로 약 100 g 배변하였고 입원 14일차에 보통변 양상의 BSFS type 3으로 약 70 g 배변하였으며 잔변감은 이전 대비 감소하였으나 배변 시 용력은 상동하였다. 입원 17일차에 보통변 양상의 BSFS type 4로 약 70 g 배변하였으며 배변 시 용력 및 잔변감 모두 소실되었다(Fig. 1). BFI는 입원 시 8.7점에서 입원 7일차에 8.1점으로 중증 피로도를 유지하였으나 퇴원 시 2.0점 정도의 경증 피로도로 호전되었으며, FACT-G는 입원 시 44.3점에서 입원 7일차에 38.7점으로 낮아지는 경향을 보였으나 퇴원 시 59.0점으로 상승되어 삶의 질이 개선되었음을 보여주었다(Fig. 2). 퇴원 이후로도 조위승기탕을 하루 2회 복용하며 주 2-3회 배변 유지되었고, fentanyl transdermal patch를 100 mcg/hr에서 50 mcg/hr로 감량한 이후에는 간헐적으로 조위승기탕을 복용하며 배변상태가 유지되었다.
III. 고찰 및 결론
상기 구강저암 환자는 수술 후 항암방사선 동시요법을 시행 받는 도중 심화된 구강통증에 대하여 fentanyl transdermal patch 62 mcg/hr, 속효성 경구용 oxycodone 10 mg 1T(전원 당시 기준)을 사용하고 있던 자로, 이후 통증 호소에 따라 fentanyl transdermal patch 100 mcg/hr로 증량하여 유지하는 동안 자발적 배변이 없었다. 본과 입원 이후 무대변양상 지속되어 입원 8일차부터 위장조열(胃腸燥熱)로 인한 변비의 완화를 목적으로 조위승기탕(調胃承氣湯) 과립제를 한 포씩 하루 2회 복용하도록 하였다. 복용 3일차부터 주 2-3회 자발적 배변이 가능하였고 Bristol Stool Form Scale(BSFS) type 2에서 type 4로 변화되어 배변 상태의 개선을 확인하였으며, Brief Fatigue Inventory(BFI)로 평가한 결과 8.7점에서 2.0점으로 감소하였고 삶의 질을 Functional Assessment of Cancer Therapy-General (FACT-G)로 평가한 결과 44.3점에서 59.0점으로 상승하였다.
마약성 진통제로 인한 변비(opioid-induced constipation, OIC)는 마약성 진통제 치료를 받는 암환자를 포함한 모든 인구집단에서 가장 흔하게 호소하는 부작용으로, 진행성 암 환자의 52% 및 말기 암 환자의 87%에서 나타나는 것으로 보고되어 있다5,7. 로마기준 IV에 따르면 마약성 진통제를 시작하거나 변경하거나 용량을 증가시키면서 변비의 증상이 시작되거나 악화되며, 대표적인 증상은 전체 배변 중 25% 이상에서 과도한 힘 주기, 단단하거나 덩어리진 대변, 잔변감, 직장항문 폐색감, 원활한 배변을 위한 수조작이 필요한 경우 또는 주 3회 미만의 배변 등으로 이 6가지 특성 중 2가지 이상을 만족하여야 한다. 또한, 완하제를 사용하지 않는 경우 묽은 변은 거의 없어야 한다4. 본 증례의 환자는 평소 주 3회 빈도로 배변하던 중 마약성 진통제 투여 이후 자발적 배변 불가능하여 주 1회 관장을 통해 배변하였고, 본원 검사상 대장의 악성종양, 협착 등 변비의 뚜렷한 원인이 될 기질적인 질환을 찾을 수 없었으며, 대변양상은 BSFS type 2로 배변 시 과도한 힘 주기 및 불완전한 배변감을 호소하였다. 따라서 로마 기준 IV에 의거하여 OIC로 진단할 수 있는 경우이다.
장관의 정상적인 수축과정을 조정하는 베타-엔도르핀(beta-endorphin)과 같은 내인성 아편유사제 펩티드는 장관신경계(enteric nervous system)의 신경세포에서 합성되는데, 마약성 진통제와 같은 외인성 아편유사제가 투여되어 장관신경계에 있는 뮤(mu)-아편유사제 수용체에 결합하면 신경전달물질의 분비가 과도하게 억제되어 연동운동이 저해되고 점액 분비가 감소되어 변비가 발생하게 된다3. 유럽종양학회(European Society of Medical Oncology, ESMO) 임상지침에 따르면, 마약성 진통제를 투여할 경우 예방적으로 완하제를 병용하고 일차 치료제로 완하제를 사용할 것을 권고하며 일반적으로 삼투성 완하제 또는 안트라퀴논(anthraquinone)제제와 같은 자극성 완하제가 선호된다8. 상기환자는 구강통증으로 인한 경구복용에 대한 불편감으로 더 이상의 경구약물의 추가를 원하지 않아 완하제는 복용하지 않는 상태였으며 관장치료에 대한 거부감 있어 본과 입원 이후 시행하지 않던 중, 구강통증의 완화 및 변비증상의 지속 있어 한약 과립제를 투약하였다. 본 증례에서 사용된 조위승기탕은 약리학적으로 자극성 완하제와 삼투성 완하제의 복합제제로써 투여되었다고 볼 수 있는데, 대황의 사하활성 물질인 안트라퀴논류는 수분과 전해질의 재흡수를 억제하는 효능을 가지며 장관신경계를 자극하여 연동운동을 촉진하며16, 망초(Na2SO4⋅10H2O)는 장에서 거의 흡수되지 않고 삼투작용에 의해 완하작용을 보인다17.
암 환자의 경우 이미 질병 그 자체로 삶의 질이 저하되어 있기 때문에 암 환자에 있어서 변비가 삶의 질에 미치는 영향은 매우 중요한 문제이다18. DYONISOS 연구에서는 암성 통증 환자에서 고용량 마약성 진통제로 인한 변비 및 위장관 기능이상의 유병률 및 삶의 질에 대한 영향을 평가하였고, 그 연구결과 Patient Assessment of Constipation Quality of Life(PAC-QoL)와 12-item short form health survey(SF-12) 모두 변비가 없는 환자대비 OIC 환자군에서 통계적으로 유의한 감소가 있었다19. 또한, OIC는 암성 통증 치료에 대하여 환자의 만족도를 저하시켜 환자가 변비증상을 완화하기 위해 마약성 진통제를 감량하거나 중단하게 되는 경우가 발생하는데, 이로 인해 통증 호소가 증가하고 삶의 질 또한 저하되게 된다18. PROBE 1 연구에서는 만성 통증 환자의 33%가 위장관 관련 부작용으로 인해 마약성 진통제를 감량 또는 중단하였고, 이들 중 통증 증가를 경험한 환자의 86%에서 삶의 질과 일상생활 활동이 중증도에서 심각한 수준으로 감소하였다20. 본 증례의 경우 피로에 의한 일상생활의 지장 및 암 환자의 포괄적인 삶의 질을 평가하기 위하여 BFI와 FACT-G를 사용하였다. 조위승기탕을 포함한 한의복합치료 이후 이러한 피로도 및 삶의 질이 개선되었는데, 이는 변비 증상의 완화뿐 아니라 전원 전 복용하던 약물투여를 유지하며 구강통증의 경우 입원시 평균 NRS(Numeric Rating Scale) 7에서 퇴원시 평균 NRS 3으로 통증강도가 감소하였고, 식이는 LD(Liquid diet)에서 SD(Soft diet)로 개선되는 등 전반적인 암 관련 증상의 완화와 관련된 것으로 사료된다.
한의학적으로 변비는 대장의 전도기능(傳導機能)이 상실된 것으로, 원인에 따라 열비(熱秘)는 청열윤장(淸熱潤腸)하고 기비(氣秘)는 순기도체(順氣導滯)하며 허비(虛秘)는 익기양혈(益氣養血)하고 냉비(冷秘)는 온장통변(溫腸通便)한다21. 상기 환자의 경우 통증과 함께 동반되는 두면부 열감, 소화양호 및 경변 증상과 홍설(紅舌), 황태(黃苔), 맥부삭(脈浮數)의 설진 및 맥진을 바탕으로 조열(燥熱)이 진액(津液)을 손상하여 장관의 운동성이 저하된 위장조열(胃腸燥熱)로 변증하여 조위승기탕을 처방하였다. 조위승기탕은 상한론(傷寒論)에 처음 등장하였으며 양명병부실증(陽明腑實證)에 사하(瀉下)를 목적으로 대황(大黃), 감초(甘草), 망초(芒硝)로 구성된 방제이다22. 암환자 OIC의 치료에 대한 한의학적 연구로는 문헌고찰 1편이 보고되어 있으며23, 중국에서 시행된 임상연구 3편10-12이 확인되었다. 한약중재연구에서는 소승기탕 합 증액탕 복용군을 자극성 완하제군과 비교하여 변비증상 및 삶의 질이 통계적으로 유의하게 개선되었고10, 침중재연구에서는 족삼리(ST36) 및 천추(ST25) 전침치료군과 위장관 운동촉진제군을 비교하였으나 증상 호전에 있어 두 군간의 차이가 유의하지 않았다11. 또한, 혈위에 간섭파치료를 시행하여 삼투성 완하제와 비교한 혈위자극치료 연구에서는 증상 및 삶의 질의 개선이 보고되었으나 증상 호전에 있어서 대조군과의 통계적 유의성을 얻지는 못하였다12. 소승기탕 합 증액탕을 복용한 기존 연구10와 조위승기탕을 사용한 본 증례에서 대황을 중심으로 한 승기탕류가 사용되어 변비 증상이 완화되었던 바, 암 환자의 OIC에 대하여 일반적으로 활용될 수 있을지에 대해 추가적인 연구의 필요성이 있다.
본 증례보고는 국내에서 암 환자의 OIC에 대하여 조위승기탕을 사용한 최초 보고이며, 변비약으로 사용되는 대부분의 제제약(대황, 대승기탕, 소풍순기원, 자윤탕 등)이 비보험제제인 반면, 조위승기탕은 보험제제로 의료비 부담을 최소화할 수 있는 점에서 의의가 있다. 그러나, 단일 증례로 대상자의 수가 제한되어 있고 변비에 특이성을 가지는 삶의 질 평가도구인 PAC-QoL가 아닌 FACT-G가 사용되었으며, 투약 중단이후 추적관찰이 이루어지지 않아 장기간의 효과를 파악하기 어렵다는 한계가 존재한다. 향후 보다 객관적인 증례보고 및 임상연구의 축적을 통해 진전된 논의가 필요할 것으로 사료된다.
감사의 글
본 연구는 보건복지부의 재원으로 한국보건산업진흥원의 보건의료기술연구개발사업 지원에 의하여 이루어진 것임(HF20C0038).