합성의약품으로 호전되지 않은 소화기 증상 환자(KCD K-코드)에 대한 반하사심탕 제제 병용의 효과 : 후향적 차트 분석
Effectiveness of Additional Administration of a Banha-sasim-tang Formulation to Patients with Gastrointestinal Symptoms (KCD K-code) Not Improved by Western Medicines: A Retrospective Chart Review
Article information
Abstract
Objectives
The aim of this study was to evaluate the effectiveness of additional administration of Banha-sasim-tang formulation to patients with gastrointestinal symptoms that did not improve with Western medicines.
Methods
The patients who met the inclusion and exclusion criteria were analyzed retrospectively. A paired t-test was performed on the Nepean Dyspepsia Index-Korean version (NDI-K) scores before and after administering the Banha-sasim-tang formulation.
Results
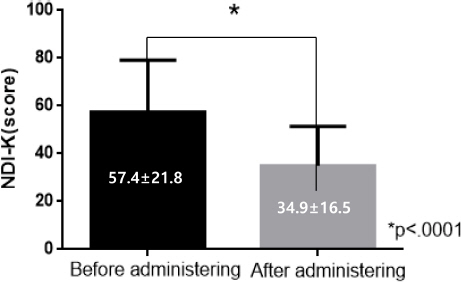
A total of 27 subjects were included. The mean duration of taking the Banha-sasim-tang formulation was 15.6±3.1 days. The most commonly used Western medicine before taking the Banha-sasim-tang formulation was rebamipide. The means of the NDI-K score were 57.4±21.8 before administering Banha-sasim-tang formulation and 34.9±16.5 after administration, and the difference was statistically significant (p<0.0001). No serious side effects were encountered while taking the Banha-sasim-tang formulation.
Conclusions
For patients whose gastrointestinal symptoms do not improve with Western medicines, additional administration of Banha-sasim-tang formulation may be an option. However, as this study is a retrospective chart review, prospective, large-scale, double-blind studies are needed in the future.
Ⅰ. 서 론
반하사심탕은 상한론과 금궤요략에 수록된 처방으로 다양한 유형의 소화기 증상의 개선을 목표로 처방되는 방제이다1. 반하사심탕의 효과와 안전성은 다양한 연구들에 의해 보고되고 있다. 박 등2은 기능성 소화불량 증상에 대한 반하사심탕의 효과와 안전성을 보고하였고, Xu 등3은 만성 역류성 식도염에 대한 반하사심탕의 식도 점막 보호 효과를 보고하였으며, 신 등4은 반하사심탕이 역류성 식도염 동물 모델에서 위의 운동성과 하부 식도 괄약근을 조절한다고 보고한 바 있다. 뿐만 아니라 반하사심탕은 한의사들에 의해 빈번하게 사용되는 처방인만큼 합성의약품과의 관련 연구도 적지 않다. Wang 등5은 역류성 식도염으로 인한 기침 증상에 대해 반하사심탕과 proton pump inhibitor(PPI)의 병용치료와 PPI의 단독치료를 비교하여 병용치료가 더 유의한 효과를 가짐을 보고하였다. 이렇게 반하사심탕의 효과 및 기전에 관한 연구가 많음에도 불구하고 합성의약품에 비해 반하사심탕은 대중들의 접근성이 높지 않은 실정이다. 김 등6의 연구에 따르면 의약품 지출 비용이 있는 자들 중 72.4~81.8%가 합성의약품에 지출 경험이 있었고, 그에 대한 비용은 2만원 이하가 가장 많았으나, 한약 및 첩약은 9.4%만이 지출 경험이 있었으며, 그에 대한 비용은 10만원 초과가 가장 많았다. 반하사심탕을 포함한 한약에 대한 대중들의 접근성이 낮은 이유가 여러 가지가 있을 수 있지만 기존의 연구6를 고려할 때 비용적인 문제를 무시할 수 없을 것이다. 특히 소화기 증상을 경험하고 있는 환자의 10명 중 9명은 의료기관을 방문하지 않고 시중에서 판매하는 소화제나 소화 보조제를 복용한다는 것7,8까지 고려한다면 한약의 경제성의 확보 역시 매우 중요하다고 할 수 있다. 한약의 임상적 효과 뿐만 아니라 경제성까지 고려했을 때 첩약의 대안으로 제시되는 것이 한약제제로, 한약제제는 첩약에 비해 가격이 저렴하며, 소청룡탕에 한정된 연구이긴 하지만 백 등9의 연구에 따르면 High-performance liquid chromatography(HPLC)를 이용하여 소청룡탕 첩약과 제제의 동등성을 평가했을 때 매우 유사한 것이 확인된 바 있다.
본 연구에서는 의사에게 처방받은 합성의약품으로 소화기 증상의 호전이 없었던 환자들이 첩약이 아닌 반하사심탕 과립제를 복용하고 유의미한 개선을 보인 것이 후향적 차트 분석에 의해 확인되었기에 보고하는 바이다.
II. 방 법
1. 연구대상
본 연구진은 2021년 04월 01일부터 2021년 09월 30일까지 원광대학교 광주한방병원을 방문하여 속쓰림, 소화불량 등 소화기 증상을 주소로 과립형태의 반하사심탕 과립제를 복용했던 자들을 대상으로 후향적 차트 분석을 실시하였다. 본 연구는 원광대학교 광주한방병원의 IRB 심의에 통과되었다(WKIRB 2021-13).
1) 포함 기준
(1) 한국표준질병사인분류(Korean Standard Classification of Diseases, KCD)상 소화기 질환과 관련된 진단을 받고 반하사심탕 과립제를 복용한 자
(2) 반하사심탕 과립제 복용 전후로 NDI-K가 측정되었고, 측정 간격이 최소 일주일 이상인 자
(3) 소화기 증상을 치료하기 위해 의사의 처방하에 합성의약품을 복용하였으나 호전을 보지 못해 기존의 합성의약품에 병행하여 반하사심탕 과립제를 복용하게 된 자
2) 제외 기준
(1) 복용 중인 합성의약품 혹은 건강기능식품이 정확하게 조사되지 않은 자
(2) 반하사심탕 과립제를 복용하면서 첩약을 포함한 다른 한약제제를 복용한 자
2. 반하사심탕 제제
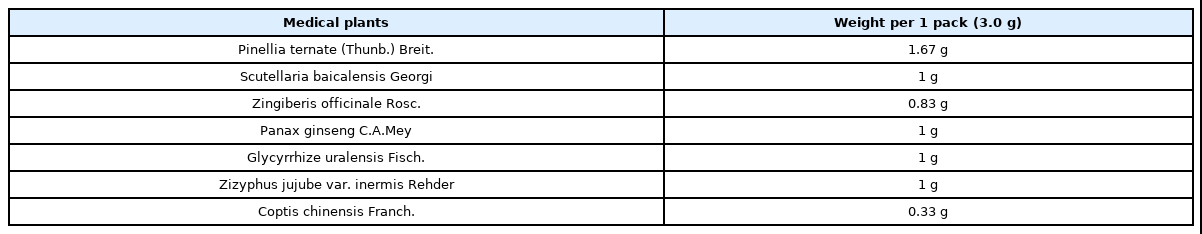
본 연구 대상자들이 복용한 반하사심탕은 황갈색의 과립제(제일반하사심탕엑스과립. 제조의뢰자: 제일헬스사이언스, 제조원: 한솔신약)로 1포에 3.0 g이며, 함유된 약재의 종류 및 용량은 Table 1에 표기하였다. 일반적으로 1포를 1회로 하여 하루에 2회 내지 3회를 식전, 식간 또는 식후에 복용한다. 반하사심탕 과립제 복용 이외에 결과에 영향을 미칠 수 있는 추가적인 생활교육 등은 실시하지 않았다.
3. Nepean Dyspepsia Index-Korean version(NDI-K)10
NDI-K는 증상 점수 표, 삶의 질에 대한 문항, 가중치에 대한 문항으로 구성되어 있는데11, 본 대상자들은 모두 증상 점수 표만으로 평가되었다. 증상 점수 표는 15개의 소화기 증상(상복부의 통증, 상복부의 불쾌함, 상복부의 쓰림, 가슴쓰림, 상복부의 경련, 가슴의 통증, 조기만복감, 위산역류, 식후 포만감, 상복부의 압박감, 상복부 팽만감, 구역, 트림, 구토, 쉼쉬기가 좋지 않음)의 빈도, 강도, 괴로운 정도에 대하여 평가하는 설문지로 지난 2주간을 기준으로 한다11. 총점은 195점으로 점수가 높을수록 소화기 증상이 심함을 의미한다. NDI-K는 반하사심탕 과립제 복용 전에 측정되었고, 반하사심탕 과립제를 최소 1주일 이상 복용한 이후의 시점에 재측정되었다.
4. 통계적 분석
반하사심탕 과립제 복용 전후의 NDI-K 점수의 변화를 확인하기 위해 대응표본 t 검정(paired t-test)을 시행하였으며, 유의수준(p)이 0.05 미만인 경우를 유의한 것으로 인정하였다.
III. 결 과
1. 연구 대상자의 일반적 특성
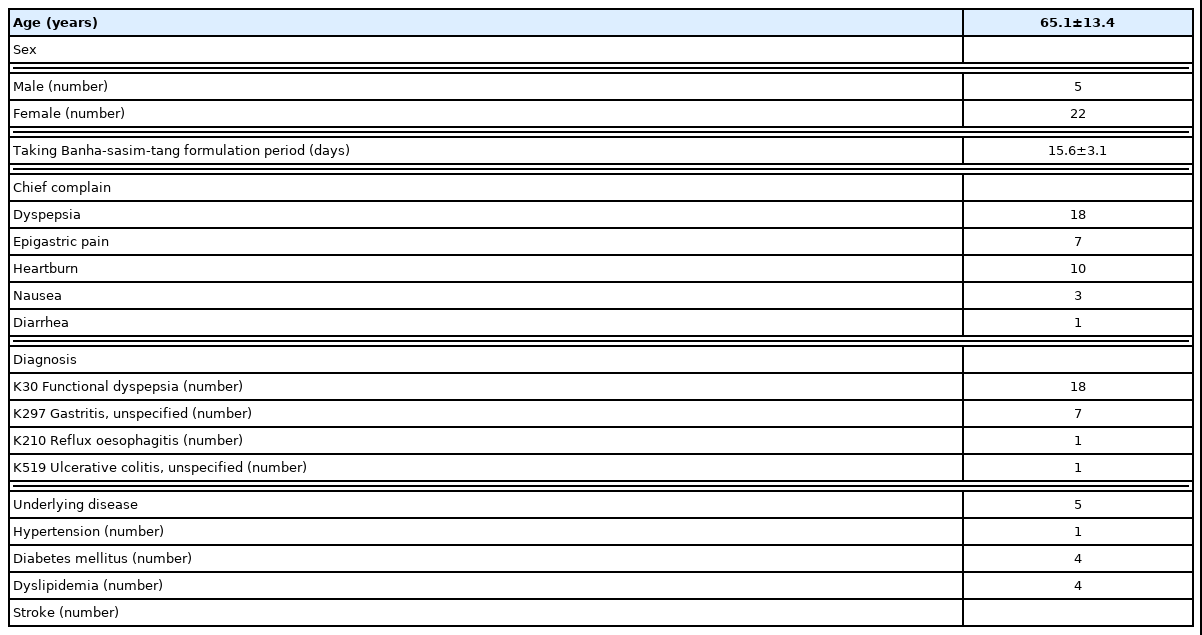
2021년 04월 01일부터 2021년 09월 30일까지 과립형태의 반하사심탕 과립제를 복용한 환자는 총 54명이었으며, 이 중 19명은 합성의약품 복용 없이 단독으로 반하사심탕 과립제를 복용하였고, 7명은 NDI-K가 평가되지 않았으며, 1명은 반하사심탕 과립제가 맛이 쓰다는 이유로 3일만 복용하고 중단하였기 때문에 포함기준에 해당되지 않아 평가에서 제외되었다. 따라서 총 27명의 대상자가 후향적으로 분석되었다(Fig. 1). 연구 대상자들의 일반적 특성은 Table 2에 나타냈으며, 복용 중인 합성의약품에 대한 정보는 Table 312,13에 나타냈다. 대상자들은 다양한 기전의 합성의약품을 복용하고 있었으며, 많게는 3종류의 합성의약품을 복용하고 있었다. 3종류의 합성의약품을 복용하는 환자가 3명, 2종류를 복용하는 환자가 7명, 1종류를 복용하는 환자가 17명이었다.
2. 부작용
반하사심탕 과립제를 복용 중에 부작용을 호소한 대상자는 없었다.
IV. 고 찰
본 연구는 소화기 증상 개선을 위해 의사에게 처방받은 합성의약품을 복용하였으나 호전이 없어 과립형태의 반하사심탕 과립제를 병행 복용한 환자들을 대상으로 후향척 차트 분석을 실시하였으며, 그 결과 환자들의 NDI-K 점수의 유의미한 변화를 확인하였다.
NDI-K는 Talley 등14이 소화기 증상 정도를 평가하기 위하여 개발한 NDI를 한국형으로 이 등10이 표준화한 설문지이다. Arinton 등15은 omeprazole과 ranitidine의 효과를 NDI를 이용해 평가하였으며, Hashash 등16도 flupenthixol과 melitracen의 효과를 NDI를 이용해 평가하였다. 이들 연구를 참고로 본 연구에서도 반하사심탕 과립제를 복용하기 전후의 NDI-K 점수를 후향적으로 평가하였으며, 반하사심탕 과립제 복용 이후 NDI-K 점수가 유의미하게 낮아진 것을 확인할 수 있었다. 본 연구의 대상자들의 반하사심탕 과립제 복용 전의 평균 NDI-K점수는 57.4점, 복용 후의 평균 NDI-K 점수는 34.9점이었는데, Talley 등17의 보고에 따르면 소화불량 환자군의 NDI는 평균 44.7점, 소화불량 환자가 아닌 군에서의 NDI 점수는 10.5점이었다. 이를 고려할 때, 본 연구의 대상자들은 반하사심탕 과립제를 복용한 뒤에도 소화기 증상이 여전히 남아있는 것으로 볼 수 있다. 하지만 의사의 처방하에 복용한 합성의약품으로도 효과를 보지 못한 증상들이 반하사심탕 과립제를 복용하면서부터 NDI-K상 유의미한 호전을 보였기 때문에 본 연구는 의미가 있을 것으로 사료된다. 특히 본 연구에 포함된 환자들 중 2명은 levosulpiride 성분의 합성의약품을 복용하고 있었는데, levosulpiride는 약인성 파킨슨증(drug-induced parkinsonism)을 빈번하게 유발할 수 있어18 주의해야 하는 약물이다. 국내 보고19에 따르면 약인성 파킨슨증 환자들 중 원인 약물이 levosulpiride인 경우가 가장 많다. 따라서 반하사심탕 과립제는 소화불량, 속쓰림, 상복부 통증 등의 소화기 증상을 합성의약품만으로는 개선이 되지 않을 때 병행해볼 수 있을 뿐만 아니라, 빈번한 부작용을 가진 합성의약품의 대안이 될 가능성도 가지고 있는 것으로 사료된다.
본 연구의 한계점은 다음과 같다. 첫째, 본 연구에서 유의미한 증상 개선을 가져온 반하사심탕 과립제의 기전을 명확히 알 수 없다는 점이다. 기존의 연구3,4들에서 반하사심탕의 효과를 식도 점막 보호 효과, 혹은 위의 운동성과 하부 식도 괄약근의 조절 등으로 설명한 것들을 고려할 때, 본 연구에서 사용된 반하사심탕 과립제 역시 그와 유사한 기전을 통해 작용한 것이라 추정된다. 둘째, 대조군이 없고, 후향적 분석 대상자가 27명으로 전체 소화기 환자군을 대표하기 위한 인원으로는 충분하다고 할 수 없으며, 대상자가 의도적으로 선정되었다는 점이다. 그러나 소수의 대상자들에서도 유의한 결과가 도출되었고, 기존의 반하사심탕 연구 결과1,2에도 부합하므로 본 연구 결과의 신뢰성은 낮지 않을 것으로 사료된다. 셋째, 반하사심탕을 복용하면서도 기존에 복용하던 합성의약품은 그대로 복용하도록 했기 때문에 뒤늦게 합성의약품의 효과가 발현된 것임을 완전히 배제할 수는 없다. 하지만 본 연구에서 합성의약품 복용기간과 복용 전후의 증상의 변화를 구체적으로 조사하지 못한 것은 환자들이 언제부터 합성의약품을 복용했는지 기억을 못할 정도로 복용 기간이 오래되었기 때문이었으므로 뒤늦게 합성의약품의 효과가 나타난 것이라고 보기는 매우 어려울 것으로 사료된다. 넷째, 효과를 평가하기 위한 변수로 NDI-K만을 사용했다는 점이다. 하지만 NDI-K는 소화기 증상을 가진 환자를 대상으로 시행하는 신뢰도와 타당도가 검정된 질병-특이적 삶의 질 평가 도구일 뿐만 아니라 조 등20이 기능성 소화불량증에 합성의약품인 mosapride가 효과가 있는지를 판단하기 위해 NDI-K만을 사용하였고, 이 등21도 rabeprazole과 mosapride 병용제제의 유효성을 평가하기 위해 NDI-K 만을 사용한 것을 고려할 때 본 연구 결과의 신뢰성은 낮지 않을 것으로 사료된다.
V. 결 론
본 연구는 이러한 한계에도 불구하고 합성의약품 복용으로 소화기 증상 호전이 없어 과립형태의 반하사심탕 과립제를 복용한 27명의 환자를 후향적으로 차트 분석을 하였고, NDI-K상 유의미한 변화를 확인하였다. 향후 구체적인 증상을 타겟으로 하면서 위약 대조, 무작위배정, 이중맹검 설계가 된 대규모의 전향적 연구가 이루어진다면 과립형태의 반하사심탕 과립제의 임상적 효과를 보다 구체적으로 보여줄 수 있을 것으로 사료된다.
감사의 글
이 논문은 (주)제일한방의 지원에 의하여 수행되었음.