C형간염에 대한 한약의 치료효과 : 체계적 문헌고찰과 메타분석
Effect of Herbal Medicine on Hepatitis C: a Systematic Review and Meta-analysis
Article information
Abstract
Objectives:
The present study aimed to provide clinical evidence on the effect of herbal medicine on the treatment of hepatitis C using a systematic review and meta-analysis of randomized controlled trials (RCTs).
Methods:
This study included RCTs that verified the effects of herbal medicine for the treatment of hepatitis C. A literature search of English, Chinese, and Korean databases was performed, and the selected literature was assessed to investigate the risk of bias.
Results:
The analysis included 14 RCTs. The total effective rate was the most commonly used outcome measure. The meta-analysis revealed that the total effective rate and total bilirubin difference were higher and that the recurrent rate was lower in the herbal medicine group than in the western medicine group (RR: 1.20, 95% CI: 1.06-1.35, p=0.003, I2=52; MD: 0.52, 95% CI: -0.62 to 1.66, p=0.37, I2=0; RR: 0.35, 95% CI: 0.11-1.09, p=0.07, I2=0). The included RCTs had relatively poor quality and a small sample size.
Conclusion:
Treatment with herbal medicine was found to be partially effective in treating hepatitis C. The included RCTs had relatively poor quality and a small sample size. This study can serve as a foundation for further clinical studies on the development of treatment methods for hepatitis C based on herbal medicine.
I. 서 론
급성 바이러스 간염은 주로 간을 침범하는 바이러스에 의해 발생하는 전신감염증이다. 대부분의 급성 바이러스 간염은 다섯 가지 종류의 바이러스 병원체(hepatitis A virus, hepatitis B virus, hepatitis C virus, the HBV-asociated delta agent or hepatitis D virus, hepatitis E virus)가 관여하고 있으며, 이 중 C형 간염 바이러스(hepatitis C virus, HCV)는 flavivirus와 비슷한 한 가닥의 RNA 바이러스로 전파경로는 혈액과 타액을 통한 감염, 성적 전파, 수직 감염 등이 있다1,2. HCV는 만성간염, 간경변증 및 간세포암종에 의한 사망 및 간이식의 주요 원인이다3. 2012~2014년의 국민건강영양조사에서 성인 HCV 항체 유병률은 0.7%로 보고되고 있다4.
HCV는 대부분의 경우 뚜렷한 임상 증상 없이 만성간염으로 이행되며, 이후 20% 정도의 비율로 간섬유화로 진행되게 된다1,2. 이로 인해 C형 간염에 대한 일반국민과 의료진의 인지도가 낮고 진단이 늦어져 질병에 의한 경제적 부담이 증가되고 있다4,5.
최근 발생한 서울 양천구 ◯◯의원(2015년 10월), 원주 ◯◯정형외과, 제천 ◯의원(2016년 1월) 등 오염된 주사기나 주사침의 재사용 등으로 발생한 C형간염 집단감염 사태로 인해 언론매체들에서 많은 기사들이 나오고 사회적 관심이 높아져서 정부와 관련 학회들이 해결을 모색하고 있다5.
HCV의 의학적 치료는 1990년대 인터페론 단독요법을 시작으로 발전을 거듭하여 5~6년 전까지만 해도 페그인터페론-리바비린의 병합요법이 표준 치료법으로 널리 사용되어 왔다. 그러나 투약의 불편성, 약물 부작용, 유전자형에 다른 치료반응의 차이 등의 문제점도 있었다. 2011년경 바이러스에 직접 작용하는 약제인 1세대 direct antiviral agent (DAA)가 상용화된 이후 2013~2014년에 2세대 및 3세대 DAA가 출시된 이후에는 90%에 달하는 치료성공률(sustained virologic response, SVR)을 보인다6,7.
HCV의 한의학적 치료는, 바이러스 간염의 타입과 무관하게 濕熱燻蒸, 熱毒內熾, 氣滯虛寒, 氣滯濕阻으로 辨證하여 茵蔯四苓散이나 茵蔯淸肝湯을 기본으로 가감하여 치료한다1.
HCV의 한의학적 치료에 관한 국내 연구를 살펴보면, 최 등의 뇌경색을 동반한 C형 간염환자의 치험례8 및 김 등의 만성 C형 간염환자의 interferon과 ribavirin 병용요법의 부작용에 대한 침구치료9 등의 증례논문과 김 등의 인진청간탕의 실험연구10등이 보고되고 있으나, 증례 보고나 실험연구에 한정되어있고, 임상연구나 문헌고찰은 없는 상태이다.
이에 저자는 C형 간염의 한약치료의 효과를 객관적으로 평가하기 위해, C형 간염 환자를 한약으로 치료한 무작위 임상연구를 대상으로 체계적 문헌고찰 및 메타 분석을 시행하여 그 결과를 보고하자고 한다.
II. 연구대상 및 방법
1. 연구대상
C형 간염 환자를 대상으로 한약의 효과를 연구한 국내외 한의학 논문을 대상으로 하였다. PICO-SD (Participants, Intervention, Comparison, Outcome, Study Design) 형식에 따라 진행하였다.
1) 연구대상(Participants) : C형간염 환자
2) 중재(Intervention) : 한약의 단독치료 혹은 양약과의 병합치료
3) 비교중재(Comparison) : 양약 혹은 무 처치 대조군
4) 결과(Outcome) : 제한 없음.
5) 연구유형(Study Design) : 무작위배정 비교 임상시험(randomized controlled trial, RCT)
2. 연구방법
1) 데이터베이스 및 문헌검색 전략
논문 검색은 국내 데이터베이스인 국가과학기술정보센터(National Discovery for Science Leaders, NDSL), 한국교육학술정보원(Research Information Sharing Service, RISS), DBpia(http://www.dbpia.co.kr), 전통의학정보포털(Oriental Medicine Advanced Searching Integrated System, OASIS), 한국학술정보(Korean studies Information Service System, KISS)와 영문 데이터베이스 검색 사이트인 Pubmed, Embase, Cochrane Library, 그리고 중국 검색 데이터베이스인 중국학술정보원 CNKI(Chinese National Knowledge Infrastructure Database) 총 9개 검색원에서 시행하였다.
국내의 검색 엔진 키워드는 ‘C형간염’, ‘한약’, ‘한의학’을 사용하였다. 영문 검색 엔진 키워드는 ‘Hepatitis C’, ‘RCT’, ‘randomized controlled trials’, ‘herbal medicine’, ‘chinese medicine’이었다. 중국 검색 엔진은 검색 범위를 Medicine & Public Health 내 Traditional Chinese Medicine, Traditional Chinese Medicinal Herbs와 Combination of Traditional Chinese Medicine with Western Medicine 항목으로 한정하였고, Full text를 검색범위로 하여 ‘丙型肝炎’, ‘Hepatitis C’를 키워드로 사용하였다. 상기한 검색 키워드들은 검색엔진의 특성에 맞추어 조합하여 2019년 2월 1일부터 2019년 2월 3일까지 검색을 시행하였다. 검색기간은 검색엔진들이 지원하는 개시 시점부터 2019년 1월 31일까지이며, 언어는 제한을 두지 않았다.
2) 문헌선택
문헌 선별에는 두 명의 연구자(KEJ, KKL)가 참여하였으며, 독립적으로 시행하였다. 검색된 문헌을 취합하여 중복 문헌을 우선 제외하였고, 1차 선별은 제목과 초록을 바탕으로, 2차 선별은 전문을 검토하여 선정하였다. 연구자 간 의견불일치 발생 시 제 3의 연구자(KKM)의 의견을 구하였다.
선정기준은 C형간염 환자에게 한약 단독치료 혹은 한약과 양약 병합치료를 시행한 무작위배정 비교임상시험 연구를 대상을 하였다. 대조군 시술은 양약 혹은 무 처치 대조군으로 하였다. C형간염을 대상으로 하지 않은 연구, 비무작위 대조시험, 단일 한약재 추출물 치료, 원저가 아닌 연구, 학위논문 등을 배제하였다.
3) 자료추출 및 내용 분석
선별된 문헌의 전문을 확인하여 각 문헌의 출판연도, 진단기준, 연구대상의 수와 특성, 중재군 및 대조군의 중재시술(투여약물 및 투여방법), 치료기간, 추적기간, 치료결과, 이상반응 등의 자료를 추출하였다.
4) 문헌의 질 평가
본 연구에서는 연구의 질 평가를 위해 코크란 비뚤림 위험(Cochrane’s Risk of Bias, RoB) 도구를 사용하여 7가지 영역에 대하여 ‘high’, ‘low’, ‘unclear’로 평가하였다. 두 명의 연구자(KEJ, KKL) 간 합의 및 제 3의 연구자(KKM)의 의견을 구하였다.
5) 요약 측정치 및 자료합성
결과 합성은 Review Manager(RevMan) 5.3을 이용하였다. 치료전후 AST, ALT, Total Bilirubin 같은 연속형 자료의 경우 평균차(mean difference, MD) 또는 표준화 평균차(standardized mean difference, SMD)를 95% 신뢰구간과 함께 표시하였고, 총유효율, HCV-RNA 음성률, 재발률 등 이분형 자료의 경우 상대위험도(Risk ratio, RR)와 양측 95% 신뢰구간(CI)을 이용하여 표시하였다. 문헌간의 이질성(heterogeneity)검사는 Higgin’s I2 test를 이용하였으며, Higgin’s I2 값이 0%-40%인 경우 이질성이 적다고 판단하였다11. 이질성이 높은 경우 치료기간에 따라 나누어 subgroup analysis를 시행하였다.
III. 결 과
1. 자료선별
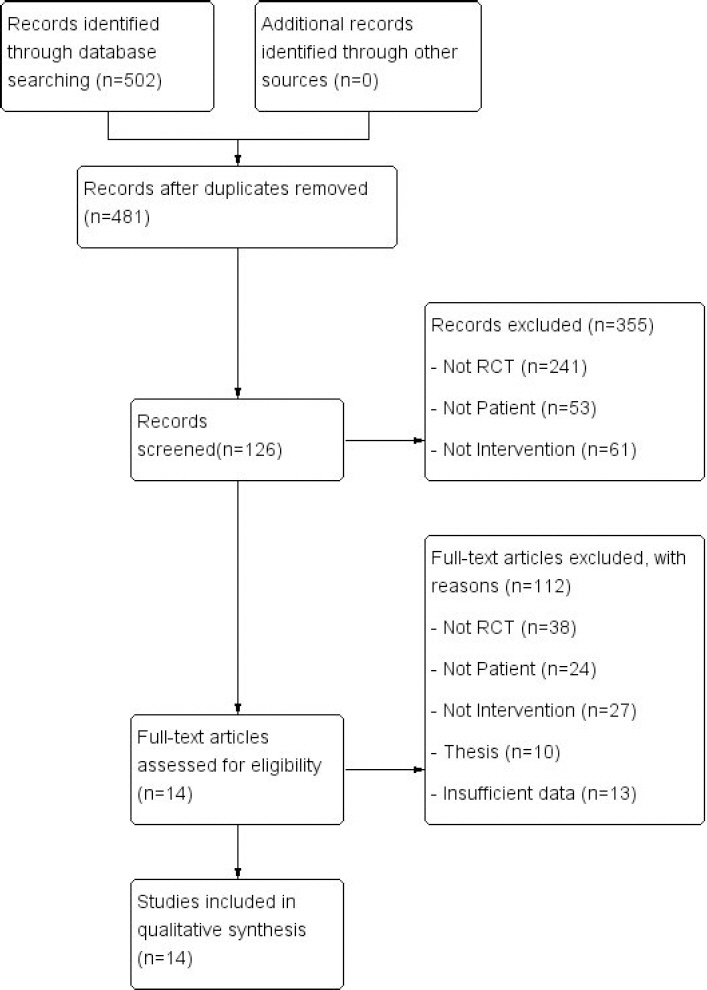
2019년 2월 1일부터 2019년 2월 3일 총 9개의 데이터베이스에서 검색한 결과 502편의 문헌 중 중복된 문헌 21편을 제외하고 481편이었다. 제목과 초록을 통해 C형간염과 관련 없는 논문, 한약치료가 아닌 논문, RCT가 아닌 논문 355편을 제외하였다. 1차 선별된 126편의 논문의 원문을 검토한 후 RCT가 아닌 논문, 치료대상이 C형간염이 아닌 논문, 치료군과 대조군이 선정기준에 부합하지 않은 논문, 학위논문, 치료방법에 대한 불충분한 자료를 제시하는 논문 112편을 제외하였고, 선정기준에 부합하는 14편을 2차적으로 선정하였다(Fig. 1).
2. 선정 문헌의 특성
1) 연구 설계
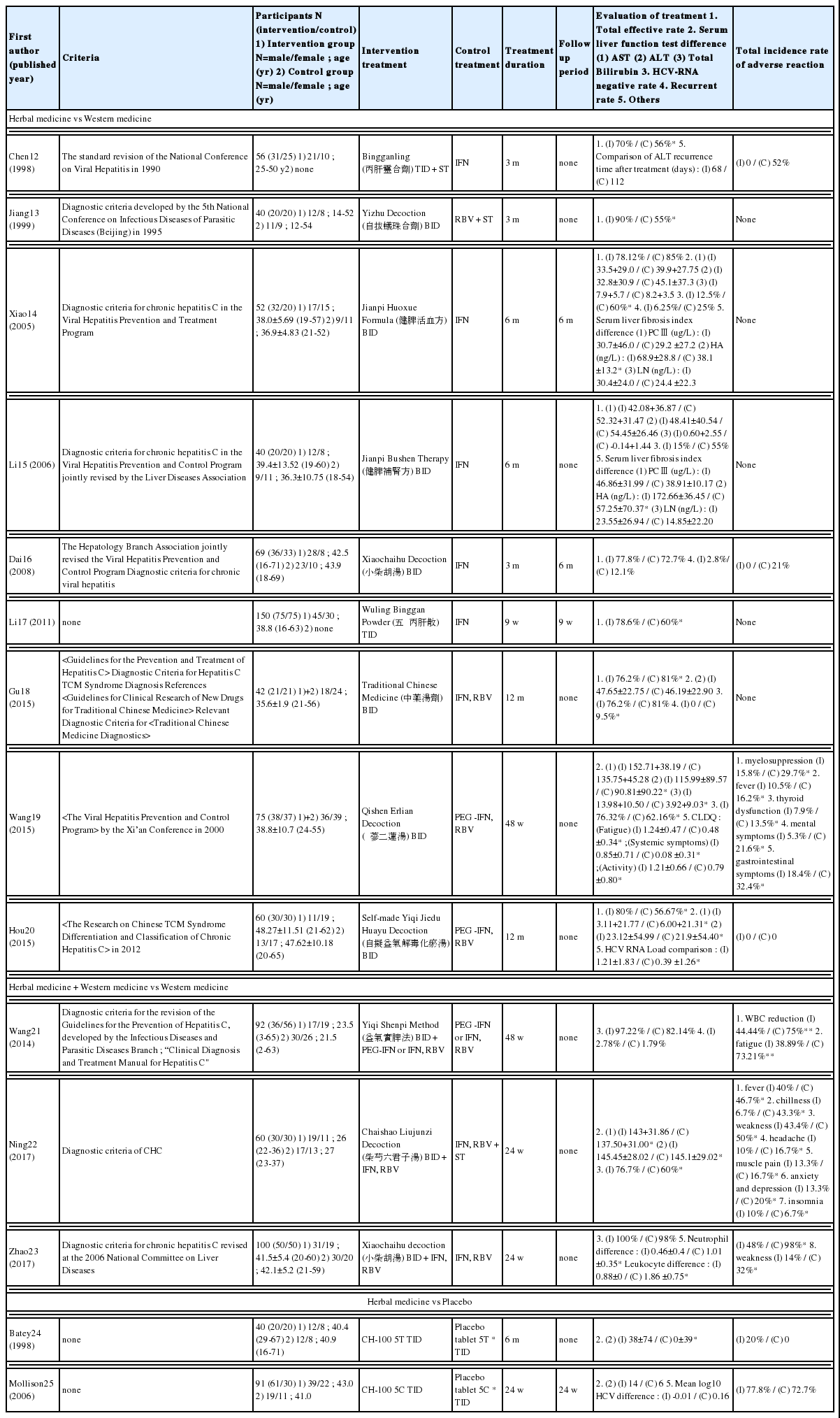
최종 선정된 14편의 연구는 1998년부터 2017년까지 중국과 호주에서 시행된 RCT 연구이다. C형간염에 대한 한약 단독 또는 한약과 양약의 비교 9편12-20, 한약과 양약 병합치료와 양약의 비교 3편21-23, 한약과 위약의 비교 2편24,25이었다(Table 1).
2) 연구 대상
연구 대상의 수는 치료군 중심으로 20명부터 75명으로, 남녀성비는 남자가 여자보다 많은 경우 10편, 적은 경우 4편이었다. 연구대상의 나이는 3세부터 71세로 다양하였고, 평균 나이를 나타낸 논문은 12편으로, 평균 나이는 30대와 40대가 5편씩으로 가장 많았다.
3) 치료 방법
선별된 논문은 모두 한약치료를 대상으로 하였으며, 한약은 주증상이나 변증에 따라 기본처방에 약재를 가감하기도 한 논문이 있었으나, 본 연구에서는 각 논문에서 사용된 기본처방과 그에 대한 약재만을 분석하였다.
처방의 경우 小柴胡湯과 CH-100이 각 2회로 가장 많았고, 丙肝靈合劑, 自拔蟻珠合劑, 健脾活血方, 健脾補腎方, 柴芍六君子湯, 五苓丙肝散, 益氣實脾法, 自擬益氣解毒化瘀湯, 中藥湯劑, 芪蔘二蓮湯가 각 논문에서 사용되었다.
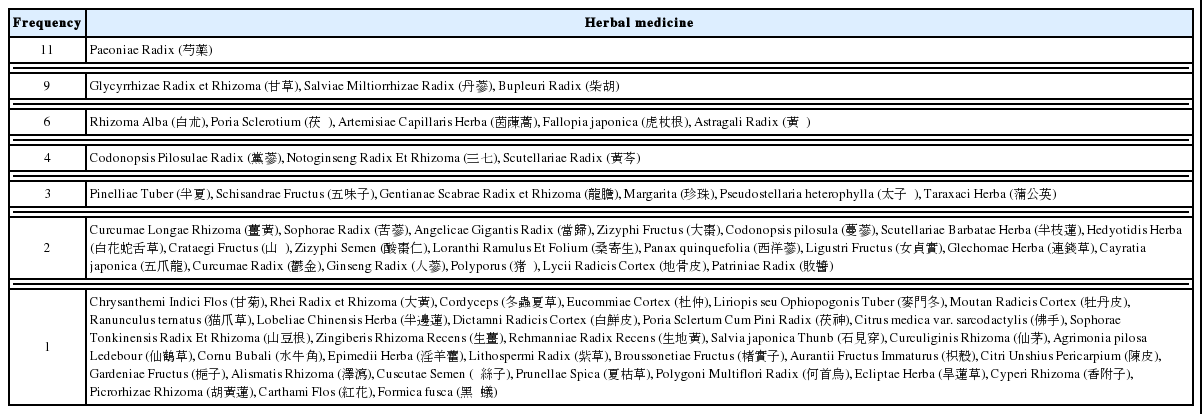
변증을 처방의 선별에 사용한 문헌은 4건으로, 肝鬱脾虛가 3회로 가장 많이 언급되었다. 주된 처방에 증상이나 변증별 가감을 사용한 문헌은 6건이었다(Table 2). 한약재의 경우 芍藥이 11회, 甘草, 丹蔘, 柴胡가 각 9회, 白朮, 茯苓, 茵蔯蒿, 虎杖根, 黃芪가 각 6회였다(Table 3). 모든 논문에 한약 복용 횟수가 언급되었으며, 하루 세 번 복용이 4편, 두 번 복용이 10편이었다.

Composition of the Herbal Preparations and Traditional Chinese Medicine (TCM) Pattern Used in Treatment
4) 대조군
대조군은 양약 치료군이 12편12-23, placebo군이 2편24,25이었다. 양약치료는 interferon 단독치료(n=5), peginterferon과 ribavirin 병합치료(n=3), interferon과 ribavirin 병합치료(n=3), ribavirin 단독치료(n=1) 순으로 사용되었다.
5) 치료기간 및 추적기간
약물투여기간은 9주부터 48주로, 평균 190.5일이었다. 9주가 1편, 12주가 3편, 24주가 6편, 48주가 4편이었다. 추적기간을 언급한 논문은 총 4편으로, 9주가 1편, 24주가 3편이었다.
6) 평가지표
선정된 문헌에서 평가지표로 총유효율(Total effective rate), 간수치 변화(Serum liver function test difference; AST, ALT, total bilirubin), HCV-RNA 음성률(HCV-RNA negative rate), 재발률(Recurrent rate), 간섬유화수치(Serum liver fibrosis index difference; PCIII, HA, LN), HCV-RNA 정량비교(HCV RNA Load comparison), HCV-RNA의 로그값 차이(Mean log10 HCV difference), ALT 회복시간(ALT recurrence time), CLDQ(Chronic Liver Disease Questionnaire) 점수 차이, 호중구(Neutrophil)와 백혈구(Leukocyte) 수치 비교 등을 사용하였다. 이 중 총유효율은 8편, 간수치 변화와 HCV-RNA 음성률은 각 7편, 재발률은 4편의 연구에서 평가지표로 사용하였다.
7) 이상반응 보고
이상반응은 14편의 논문 중 9편의 논문에서 언급하였다. 한약 치료군과 양약 치료군을 비교한 연구에서 이상반응은 총 4편에서 보고되었으며, 이 중 3편에서 양약 치료군의 이상반응이 한약 치료군보다 많이 나타났음을, 1편에서는 두 치료군 모두 이상반응이 나타나지 않았음을 보고하였다. 한약과 양약의 병합치료군과 양약치료군을 비교한 연구 3편 모두 양약 치료군의 이상반응이 한약과 양약 병합치료군보다 많이 나타났다고 보고하였다. 한약과 placebo군의 비교 연구 2편은 모두 한약 치료군에서 이상반응이 더 많이 발생하였다고 보고하였다.
8) 출판편향
출판 편향(Publication bias)을 평가하기 위해 깔때기 분포(Funnel plot)를 사용하려고 하였으나 메타 분석에 포함된 연구가 10개 미만이라서 출판 편향이 평가되지 못했다.
3. 코크란 비뚤림 위험(Cochrane’s Risk of Bias, RoB)을 이용한 평가
본 연구에서 선정된 14편의 모든 연구에 대해 RoB를 이용하여 평가하였다(Fig. 2). 무작위 배정순서 생성 항목은 난수표를 이용한 4편18,20,22,23의 논문과 block randomization을 이용한 1편25의 논문은 low risk로 평가하였고, 나머지 언급이 없는 논문은 unclear risk로 평가하였다. 배정순서은폐 및 눈가림 항목에 대해서는 독립적인 random code를 사용한 1편24의 논문과, 연구 참여자에게 눈가림을 시행했다고 언급한 1편25의 논문은 low risk로 평가하였으나, 대부분 문헌에 배정순서은폐 및 눈가림 항목에 대한 언급이 없어 unclear risk로 평가하였다. 불완전한 결과자료 항목은 대조군 3례의 치료중단에 대하여 언급이 없고 결과에 영향을 미친 1편16의 논문을 제외하고 결측치가 없거나 결측치가 있더라도 사유가 명시되고 결과치에 영향을 미치기 않았기에 low risk로 평가하였다. 선택적보고 항목은 모두 등록된 프로토콜을 찾을 수 없어 unclear risk로 평가하였다. 그 외 비뚤림 항목에서는 평가할 정보가 충분하지 않고, 근거가 없는 경우가 대부분이기에 unclear risk로 평가하였다.
4. 메타분석 결과
총유효율, 치료 전 후 AST, ALT, total bilirubin 수치변화, HCV-RNA 음성률, 재발률이 선정된 문헌의 공통된 결과변수이므로, 한약치료와 양약치료의 효과를 비교한 연구를 대상으로 메타분석을 실시하였다.
1) 총유효율(Total effective rate)
총유효율은 치료 후 호전정도를 치유, 유효, 무효로 나누어 효과를 평가하는 방법을 사용하였다. 한약치료와 양약치료의 총유효율을 비교한 6편의 연구들의 측정치를 합성한 결과 risk ratio값은 1.20배(95% CI: 1.06 to 1.35, p=0.003)로 한약치료는 양약치료보다 C형간염에 유의한 효과가 있는 것으로 나타났다(Fig. 3). I2값은 52%으로 추가적으로 치료기간에 대한 subgroup analysis를 시행하였으나 I2값이 감소하지 않아 제시하지 않았다.
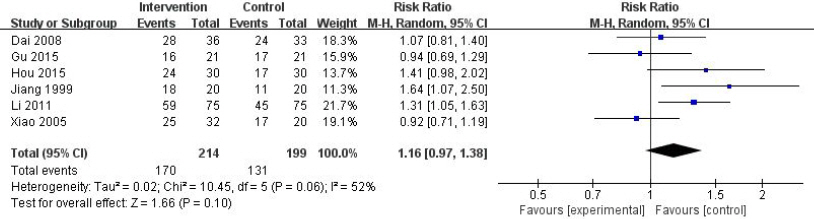
Forest plot comparison: herbal medicine (HM) vs Western medicine (WM), outcome: total effective rate.
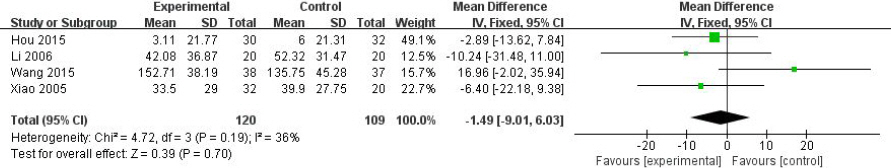
(2) AST 수치변화(AST Difference)
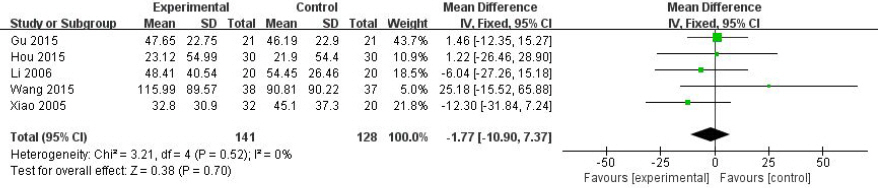
4편의 연구들의 측정치를 합성한 결과 결합된 MD 추정값이 -1.49IU(95% CI: -9.01 to 6.03, p=0.70)로 통계적으로 유의하지는 않지만 양약치료가 한약치료보다 치료전후 AST 감소량이 더 큰 경향을 보였다. I2값은 36%로 나타났다(Fig. 4).
(3) ALT 수치변화(ALT Difference)
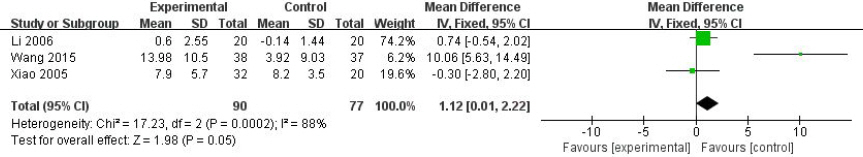
5편의 연구들의 측정치를 합성한 결과 결합된 MD 추정값은 -1.77IU(95% CI: -10.90 to 7.37, p=0.70)로 통계적으로 유의하지는 않지만 양약치료가 한약치료보다 치료전후 ALT 감소량이 더 큰 경향을 보였다. I2값은 0%로 연구간 이질성은 매우 낮게 나타났다(Fig. 5).
(4) Total Bilirubin 수치변화(Total Bilirubin Difference)
3편의 연구들의 측정치를 합성한 결과 결합된 MD 추정값은 1.12IU(95% CI: 0.01 to 2.22, p=0.05)로 한약치료가 양약치료보다 치료전후 total bilirubin 감소량이 높은 것으로 나타났으나(Fig. 6), I2값이 88%로 이질성이 높게 나타나 subgroup analysis를 시행하였다. 치료기간이 6개월인 두 연구14,15의 메타분석 결과 결합된 MD 추정값은 0.52IU(95% CI: -0.62 to 1.66, p=0.37)로 통계적으로 유의하지는 않지만 한약치료가 양약치료보다 치료전후 total bilirubin 감소량이 상대적으로 큰 것으로 나타났다. I2값은 0%로 연구간 이질성은 매우 낮게 나타났다(Fig. 7).
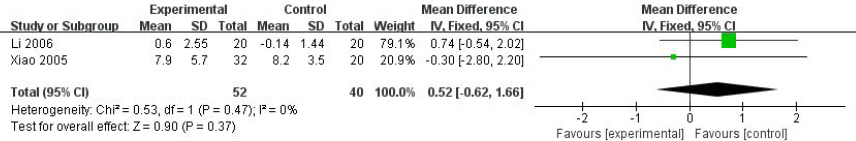
Forest plot comparison: HM vs WM, outcome: total bilirubin difference; subgroup (treatment period : 6 months).
(5) HCV-RNA 음성률(HCV-RNA Negative Rate)
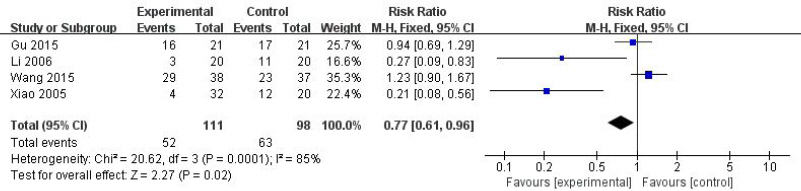
4편의 연구들의 측정치를 합성한 결과 Risk Ratio 값은 0.77배(95% CI: 0.61 to 0.96, p=0.02)로 양약치료가 한약치료보다 효과가 높게 나타났으나(Fig. 8), I2값이 85%로 이질성이 매우 높게 나타나 subgroup analaysis를 시행하였다. 치료기간이 6개월인 두 연구14,15의 메타분석 결과 Risk Ratio 값은 0.24배(95% CI: 0.11 to 0.49, p=0.0001)로 양약치료가 한약치료보다 유의한 치료효과가 있는 것으로 나타났다. I2값은 0%로 연구간 이질성은 매우 낮게 나타났다(Fig. 9).

Forest plot comparison: HM vs WM, outcome: HCV-RNA negative rate; subgroup (treatment period : 6 months).
(6) 재발률(Recurrent rate)
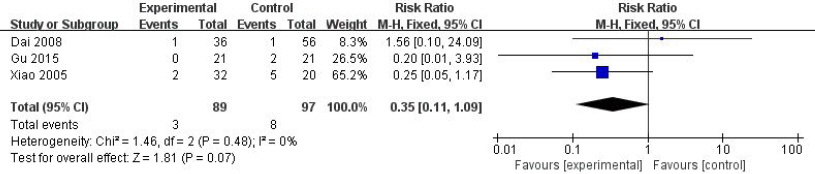
3편의 연구들의 측정치를 합성한 결과 Risk Ratio 값은 0.35배(95% CI: 0.11 to 1.09, p=0.07)로 통계적으로 유의하지는 않지만 한약치료는 양약치료보다 재발률이 낮게 나타났다. I2값은 0%로 이질성은 매우 낮게 나타났다(Fig. 10).
IV. 고 찰
본 연구에서는 현재까지 이루어진 C형간염에 대한 한약치료의 무작위대조임상연구를 체계적으로 고찰하여 그 효과를 알아보고 임상적 근거 자료를 마련하고자 체계적 문헌 고찰 및 메타 분석을 시행하였다. 문헌의 선별은 C형간염 환자에게 한약 단독 혹은 보조치료나 양약과의 병용치료를 시행한 RCT 연구를 포함하였다.
본 연구에서 선정된 14편의 연구는 1998년부터 2017년까지 중국과 호주에서 시행되었다. 치료방법은 한약 치료군과 양약 치료군의 비교 연구가 9편, 한약과 양약 병합 치료군과 양약 치료군의 비교 연구가 3편, 한약 치료군과 위약군의 비교 연구가 2편이었다.
한약의 치료로는 小柴胡湯, CH-100이 각 2회 사용되었고, 한약재는 芍藥이 11편에 사용되었다. 小柴胡湯은 항염증, 항산화, 간 보호와 재생, 면역조절, 항암 등의 효능을 통해 만성간염과 간경변증의 치료에 다용되는 처방이다. 小柴胡湯의 간 보호 효능에 대한 실험연구는 CCL4에 의한 간세포 독성 억제와 보호효과, H2O2에 대한 보호효과 등이 보고되고 있다26.
CH-100은 猪苓, 丹蔘, 茵蔯蒿, 茯苓, 蒲公英, 芍藥, 黃芪, 桑寄生 등 총 19가지 한약재로 구성된 탕약이다. CH100에 대한 기존 연구로는 간 손상의 동물 모델에서 보호 효과27 등이 보고되었고, 현재 국내에 이루어진 연구는 없는 상태이다.
다빈도 한약재인 芍藥의 경우, H2O2에 의한 신경 세포사멸의 억제, 항산화계 활성화, 간독성 완화효과, 뇌내출혈로 유발된 신경세포의 사멸 억제, 혈소판응집 억제 등이 보고되고 있으며, 이 중 간독성 완화효과와 Nrf2 活性化를 통한 芍藥의 肝保護效果가 C형 간염에 芍藥을 응용할 근거가 될 것으로 사료된다28.
국내에서는 C형간염에 대해 濕熱燻蒸, 熱毒內熾, 氣滯虛寒, 氣滯濕阻의 4가지 변증유형으로 나누고 있으나, 본 연구의 사용된 변증은 肝鬱脾虛, 脾腎陽虛, 肝腎陰虛, 氣虛邪戀, 濕熱中阻로 국내의 변증 유형과 달리 濕熱中阻 외에는 肝虛, 脾虛, 腎陰虛, 氣虛 등 주로 虛한 것으로 변증하여 치료하는 것을 알 수 있다.
대조군의 양약치료 중 interferon 단독치료(n=5), peginterferon과 ribavirin 병합치료(n=3), interferon과 ribavirin 병합치료(n=3), ribavirin 단독치료(n=1) 순으로 사용되었다. interferon 단독요법은 1990년경에 최초 사용되었으나, 치료율이 10%에 불과하여, 이후 peginterferon 알파와 ribavirin의 병합요법이 표준 치료법으로 사용되었다, 하지만 치료율은 50% 정도였고, 투약의 불편성, 약물 부작용, 유전자형에 다른 치료반응의 차이 등의 문제점을 보였다. 최근 주로 사용되는 HCV의 치료약은 direct antiviral agent (DAA)로 12~24주 투약으로 90%에 달하는 치료성공률(sustained virologic response, SVR)을 보인다6. 우리나라에서도 2015년에 interferon 없는 경구 DAA병합치료가 처음 승인된 이후 사용되고 있는 상황이다3. 이에 본 연구의 양약치료군 치료약물(interferon, peginterferon, ribavirin)과 한약치료의 치료효과의 비교가 한계점이 있으며, 향후에는 최근 다용되고 있는 치료약물인 DAA 등과의 치료효과를 비교한 연구가 추가적으로 이루어져야할 것으로 사료된다.
중재 결과를 평가하기 위한 도구들을 살펴보면 총유효율 8편, 간수치 변화와 HCV-RNA 음성률 각 7편, 재발률 4편이었으며, 그 외에도 간섬유화수치, HCV-RNA 정량비교, HCV-RNA의 로그값 차이, ALT 회복시간, CLDQ, 호중구와 백혈구 수치 비교 등이 사용되었다. 총유효율이 가장 많이 사용되었으나, 각 연구별로 유효율 평가에 대한 기준이 제시되어있고 통일된 기준은 제시되지 않았다.
이상반응은 14편의 논문 중 9편의 논문에서 언급하였다. 한약 치료군과 양약 치료군을 비교한 연구에서 이상반응은 총 4편에서 보고되었으며, 이 중 3편12,16,19에서 양약 치료군의 이상반응이 한약 치료군보다 많이 나타났음을, 1편20에서는 두 치료군 모두 이상반응이 나타나지 않았음을 보고하였다. Wang19의 연구에서는 myelosuppression, fever, thyroid dysfunction, mental symptoms, gastrointestinal symptoms 등의 부작용 발생에서 한약치료군보다 양약치료군에서 유의하게 발생률이 높았음을 보고하였다. 한약과 양약의 병합치료군과 양약치료군을 비교한 연구 3편21-23 모두 양약 단독치료군의 이상반응이 한약과 양약 병합치료군보다 많이 나타났다고 보고하였고, Wang21은 WBC reduction과 fatigue 발생률이, Ning22은 fever, chillness, weakness, headache, muscle pain, anxiety and depression과 insomnia 발생률이, Zhao23의 연구는 weakness 발생률이 양약 단독치료군에서 유의하게 높음을 보고하였다. 한약과 placebo군의 비교 연구 2편은 모두 한약 치료군에서 이상반응이 더 많이 발생하였다고 보고하였다. 한약 치료가 양약치료보다 안전하고 부작용이 적다고 판단할 수 있으며, 한약과 양약의 병합치료 시 양약 단독치료보다 부작용 발생률이 더 낮다고 볼 수 있다.
비뚤림 위험에 대한 평가에서 무작위 배성순서에 대하여 5편의 연구18,20,22,23,25, 배정순서은폐 및 눈가림에 대하여 2편의 연구24,25에서 비뚤림을 최소화하기 위한 방법이 기술되었고, 그 외 대다수의 연구에서 배정밥법과 배정순서 은폐, 평가자의 눈가림, 선택적 결과보고에서 비뚤림을 최소화하기 위한 방법이 기술되어있지 않아 비뚤림을 판단하기 어려웠다. 향후 연구에서 비뚤림을 줄이기 위한 방법이 기술되어야한다고 사료된다.
14편의 연구에서 총유효율, AST, ALT, total bilirubin 수치변화, HCV-RNA 음성률, 재발률을 평가도구로 하여 메타분석을 시행하였다. 한약치료군과 양약치료군을 비교한 결과 한약치료군에서 총유효율이 1.20배로 유의한 효과가 있는 것으로 나타났으나 I2값은 52%로 나타났다. Total bilirubin 수치변화의 경우 이질성이 88%로 높아 치료기간으로 subgroup analysis를 시행한 결과 한약치료가 양약치료보다 효과적이었으나 통계적으로 유의하지는 않았다. 재발률은 한약치료군에서 양약치료군에 비해 0.35배로 치료효과가 높게 나타났으나 통계적으로 유의하지는 않았다. AST와 ALT 수치변화는 양약치료군에서 한약치료군보다 감소량이 더 크게 나타나 치료효과가 높게 나타났으나 통계적으로 유의하지는 않았다. HCV-RNA 음성률은 이질성이 높아 subgroup analysis를 시행한 결과 양약치료가 한약치료보다 유의한 효과가 있는 것으로 나타났다. 이질성은 각 연구의 연구 대상수가 20명부터 75명으로 적으며, 치료에 사용된 처방 및 치료기간이 다르고 각 결과 값의 변동 폭이 매우 높아서 발생된 것으로 판단된다.
본 연구의 분석의 대상이 된 논문이 14편으로 수가 매우 적었고, 국외 자료 중 일본 및 기타 비영어권 데이터베이스를 포함하지 못하였다. 대상 연구들의 연구대상 수가 적고, 각 연구들의 설계를 비교하였을 때 처방 및 복용량, 치료기간, 환자들의 병정기간 등이 상이하였으며, 논문들의 질이 전반적으로 낮아 메타분석의 비교 결과 신뢰도는 불명확하였다.
이러한 한계에도 불구하고, 체계적인 고찰과 메타 분석 결과 총유효율, total bilirubin 수치변화, 재발률에 한약치료가 효과적인 것으로 확인되었다. 그리고 한약 단독치료나 한약과 양약 병용치료군에서 양약치료군보다 안전하다고 나타났다. 본 연구가 향후 체계적인 임상 연구 설계에 기초 자료를 제공할 것이며, 추후 C형간염의 한약치료에 대하여 잘 설계된 대규모 RCT 연구가 필요할 것으로 사료된다.
V. 결 론
본 연구에서는 C형간염에 대한 한약치료의 효과에 대하여 파악하기 위해 2019년 1월 31일까지 발표된 논문을 분석한 결과 다음과 같은 결론을 얻었다.
1. 총 14편의 무작위대조임상연구가 선정되었으며, 한약 치료군과 양약 치료군의 비교 연구가 9편, 한약과 양약 병합 치료군과 양약 치료군의 비교 연구가 3편, 한약 치료군과 위약군의 비교 연구가 2편이었다.
2. 중재 효과에 대한 평가 도구로는 총유효율이 8편으로 가장 많이 보고되었으며, 이상반응은 총 9편의 논문에서 언급되었다.
3. 14편의 논문 중 12편의 논문에서 양약 투여를 중재방법으로 사용하였으며, 사용된 양약은 interferon 단독치료(n=5), peginterferon과 ribavirin 병합치료(n=3), interferon과 ribavirin 병합치료(n=3), ribavirin 단독치료(n=1) 순이었으며 모두 C형간염 치료제이다.
4. 메타 분석한 결과 한약치료는 양약 치료보다 총유효율, total bilirubin 수치 변화와 재발률에서 치료효과가 더 높은 것으로 나타났다.
5. 분석한 논문들의 연구 질이 비교적 낮았으며, 평가 항목에 대한 비뚤림의 위험이 대부분 불확실하다고 판단되었다.