韓茵蔯, 鬱金, 山査, 丹蔘 발효복합추출물이 RAW264.7 및 HUVEC 세포에서 나타나는 이상지질혈증 관련 염증인자 발현 및 항산화에 미치는 영향
The Effects of an Extract of Fermented Artemisiae Iwayomogii Herba, Curcumae Longae, Crataegi Fructus and Salviae Miltiorrhizae Radix on Anti-inflammation Associated with Dyslipidemia and Anti-oxidation in RAW264.7 and HUVEC Cells
Article information
Abstract
Objectives
To investigate the effect of fermented extract of Artemisiae Iwayomogii Herba, Curcumae Longae, Crataegi Fructus and Salviae Miltiorrhizae Radix (FMH) on anti-inflammation associated with dyslipidemia and anti-oxidation in RAW264.7 and HUVEC cells.
Methods
The total polyphenols, total flavonoids, DPPH radical scavenging activity, ABTS radical scavenging activity, and cytotoxicity of FMH were measured. RAW264.7 cells treated with FMH were tested for production of NO, and for cytokine and LTB4 levels and HUVEC cells treated with FMH were examined for production of cDNA of genes related to inflammation.
Results
FMH contained polyphenols and flavonoids. The DPPH and ABTS radical scavenging activity of FMH increased in a concentration-dependent manner.
FMH treatment inhibited the production of nitric oxide (NO), cytokines, and LTB4 in RAW264.7 cell when compared to the untreated control group.
FMH decreased the transcription of pro-inflammatory genes, whereas it increased transcription of anti-inflammatory genes, in HUVEC cells.
Conclusion
FMH is effective as an antioxidant and for treatment and prevention of dyslipidemia, atherosclerosis, ischemic heart disease, stroke, and other cardiocerebrovascular diseases.
I. 서 론
2016년 사망원인통계에 따르면 암에 이어 2, 3위를 차지하는 주요 사망원인이 심장질환과 뇌혈관질환으로, 특히 심장질환으로 인한 사망은 꾸준히 증가하는 추세이다1. 심뇌혈관질환 위험인자에는 고혈압, 당뇨, 이상지질혈증, 흡연, 비만 등이 있으며 이중 고혈압의 유병률은 크게 변화가 없는 반면 당뇨병, 이상지질혈증, 비만은 증가하고 있다2. 우리나라의 심뇌혈관질환으로 인한 사망 중 동맥경화성 질환이 가장 많으며, 그 중 죽상동맥경화증이 임상적으로 큰 의의를 갖는다. 죽상동맥경화가 발생하면 혈관 내막에 콜레스테롤 침착과 세포증식이 일어나 혈관내경이 좁아지게 되며 이는 말초로의 혈액순환장애를 초래하여 허혈성 심장질환이나 뇌경색 등을 유발하는데, 이상지질혈증은 이러한 동맥경화의 위험성을 뚜렷이 증가시키는 것으로 증명되었다3. 이상지질혈증은 혈청콜레스테롤이나 트리글리세리드가 비정상적인 높은 수치를 나타내거나 high density lipoprotein(HDL)-cholesterol이 비정상적인 낮은 수치를 나타내는 질환으로, 자각증상이 없지만 방치하면 동맥경화성 질환을 유발하고 특히 관상동맥질환의 가장 중요한 독립적 위험인자로서 위험하여 이를 조기에 발견하고 치료하는 것이 중요하고 이를 위해 생활습관을 교정하고 약물을 적절히 사용할 필요가 있다4,5.
약물로는 주로 스타틴 계열이 사용되는데, 최근 스타틴이 당뇨병 신규 발생을 증가시킨다는 연구 결과가 있으며, 인지기능 저하가 관찰되었다는 보고가 있다2. 이러한 부작용 때문에 이상지질혈증에 대한 한약물 치료 연구도 꾸준히 이루어지고 왔으며, 처방으로 加味地黃湯6, 凉膈散火湯7 등이 있고 단일약재로도 다양한 연구가 진행되어 그 유효성을 밝힌 바 있다8. 그 중 한인진과 울금은 복합추출물로도 연구된 바 있으며9 이를 기초로 단일약재들을 가미한 연구가 지속적으로 나오고 있다10-13.
이상지질혈증은 한의학적으로 痰濁, 血瘀의 범주에 속하며14, 이상지질혈증이 유발하는 동맥경화증 또한 痰飮, 瘀血, 寒凝, 氣滯, 虛勞 등의 범주에 속한다3. 痰飮의 개념 중 체내에 들어온 水液이 정상적으로 운화되지 못해 전신에 고루 분포하지 못하는 것, 瘀血의 개념 중 혈액자체의 성분이 바뀌어서 유속과 생리기능에 이상이 생긴 혈액, 혈관의 병변으로 혈전들이 생겨 혈류가 불창한 것 등15이 이상지질혈증의 개념과 유사하다고 볼 수 있다.
발효는 오래전부터 인류가 자연에서 발견한 유용한 기술로서, 미생물작용을 이용하여 식품에 좋은 향, 맛, 조직감 등을 부여하고 유효성분 증진작용 및 유효성분을 더 작은 단위로 분해하여 쉽게 장관에 흡수될 수 있게 하는 작용을 하며, 비위기능이 떨어지는 사람들에게도 적합하다16.
이상지질혈증에 대한 단일 발효 한약재 연구는 발효백하수오17, 솔잎발효액18 등 다수가 있으나 발효 한약재들의 복합추출물에 대한 연구는 부족한 실정이다.
본원 한방병원에서 이상지질혈증치료를 위해 사용하고 있는 청혈플러스는 韓茵蔯, 鬱金, 山査, 丹蔘으로 이루어져 있으며, 유의한 효능이 있는 것으로 기존에 연구된 바 있다19.
본 저자는 이에 착안하여 상기 청혈플러스 구성 발효 약재의 복합추출물이 이상지질혈증에 효과가 있는지를 규명하려는 의도로 실험적 연구를 진행하게 되었으며, 유의성 있는 결과를 얻었기에 보고한다.
II. 재료 및 방법
1. 재 료
1) 약 재
본 실험에 사용한 한인진, 울금, 산사, 단삼은 ㈜옴니허브에서 구입하여 대전대학교 TBRC-RIC에서 정선 후 사용하였다.
2) 시 약
사용된 시약은 monosodium glutamate(MSG : Sigma, U.S.A.), glucose(Sigma, U.S.A.), dulbecco’s Modified Eagle’s Medium(DMEM : Gibco BRL, U.S.A.), EGM™-2 Medium(Lonza, Switzerland), EGM™-2 SingleQuots™ Kit(Lonza, Switzerland), fetal bovine serum(FBS : Gibco BRL, U.S.A.), penicillin-streptomycin(Sigma, U.S.A.), antibiotic-antimycotic (Sigma, U.S.A.), trypan blue(Sigma, U.S.A.), EZ-Cytox (Daeilab, Korea), lipopolysaccharide(LPS : Sigma, U.S.A.), hydrogen peroxide(H2O2 : Sigma, U.S.A.), nitric oxide detection kit(Intron Biotechnology, Korea), mouse cytokine milliplex map immunoassay kit(Millipore, U.S.A.), LTB4 Parameter Assay Kit (R&D systems Co., U.S.A.), dulbecco’s phosphate buffered saline(D-PBS : Welgene, Korea), 1,1- diphenyl-2-picryl-hydrazyl(DPPH : Sigma, U.S.A.), 2,2’-azinobis-(3-ethylbenzothiazoline-6-sulfonic acid)(ABTS : Sigma, U.S.A.), folin-Ciocalteu’s phenol reagent(Merck., Germany), gallic acid(Sigma, U.S.A.), quercertin(Sigma, U.S.A.), sodium carbonate (Sigma, U.S.A.), aluminum nitrate nonahydrate (Sigma, U.S.A.), potassium acetate solution(Sigma, U.S.A.), (2,7)-dichlorodihydrofluorescin diacettate (DCFH-DA : Sigma, U.S.A.), Total RNA prep kit(Intronbio, Korea), AccuPower CycleScript RT PreMix(Bioneer, Korea), SYBR Green(Qiagen, Germany), DEPC-DW(Bioneer Co., Korea)등이다.
3) 기 기
사용된 기기는 rotary vacuum evaporator(Büchi B-480, Switzerland), freeze dryer(EYELA FDU-540, Japan), CO2 incubator(Forma scientific Co., U.S.A.), clean bench(Vision scientific, Korea), autoclave(Sanyo, Japan), vortex mixer(Vision scientific, Korea), centrifuge (Hanil, Korea), deep-freezer(Sanyo, Japan), ice-maker (Vision scientific, Korea), plate shaker(Lab-Line, U.S.A.), luminex(Millipore, U.S.A.), micro plate reader (Molecular Devices, U.S.A.), flow cytometer(Becton Dickinson, U.S.A.), Nanodrop(Thermofisher, U.S.A.), Alpha Cycler 1 PCRmax(PCRmax, U.K.) real time PCR(Qiagen, Germany)등이다.
2. 방 법
1) 시료 추출 및 발효
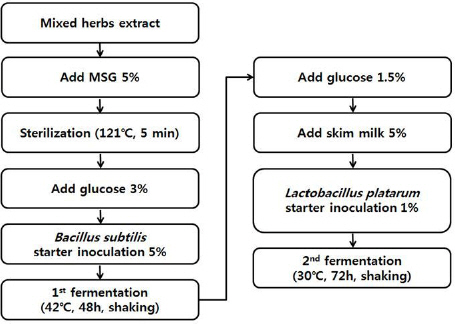
한인진, 울금, 산사, 단삼 각각 30 g에 증류수 2000 ml를 넣어 3시간 동안 환류추출을 한 후 여과액에 고초균(Bacillus subtilis)과, 젖산균(Lactobacillus platarum)을 이용한 혼합발효를 진행하였다(Fig. 1). 이후 발효된 물질을 rotary vacuum evaporator로 감압 농축하였으며, 농축된 용액을 freeze dryer로 동결 건조하여 얻어낸 발효복합추출물(fermentation mixed herbs extract 이하, FMH) 분말 24.31 g(수율 20.26%)을 초저온 냉동고(-80 °C)에서 보관하며 실험에 필요한 농도로 증류수에 희석해 사용하였다.
2) 항산화 효능평가
(1) 총 polyphenol 함량 측정
FMH 1 ml에 50% Foiln-Ciocalteu’s phenol reagent 0.5 ml를 가하여 실온에서 3분간 반응시켰다. 반응용액에 Na2CO3 포화용액 1 ml와 7.5 ml 증류수를 차례로 혼합하여 30분간 정치시킨 뒤, 14,000 g에서 10분간 원심분리한 후 상등액을 취해 760 nm 파장에서 흡광도를 측정하였다. 총 phenol 함량은 gallic acid를 표준물질로 이용하여 작성한 검량선에 따라 함량을 구하였다.
(2) 총 flavonoid 함량 측정
FMH 0.1 ml과 80% 에탄올 0.9 ml을 혼합한 혼합물 0.5 ml에 10% aluminium nitrate와 1M potassium acetate 0.1 ml 그리고 80% 에탄올 4.3 ml을 가하여 실온에 40분 방치한 뒤 415 nm 파장에서 흡광도를 측정하였으며, quercetin을 이용하여 작성한 표준곡선으로부터 함량을 구하였다.
(3) DPPH radical 소거능 측정
FMH의 최종 농도가 1, 10, 100, 1,000(μg/ml)의 농도로 될 수 있게 희석시켰으며, 에탄올에 용해시킨 0.2 mM의 DPPH 용액 150 μl와 FMH를 각각 100 μl씩 혼합하여 37 °C에서 30분간 반응 시켰다. 반응 후 517 nm 파장에서 흡광도를 측정하였다. 시료액의 대조군은 증류수를 넣었으며, DPPH 용액의 대조군으로서는 에탄올을 넣어 보정값을 얻었다. 그 후 DPPH radical 소거율((대조군의 흡광도-시료 첨가군의 흡광도)×100/대조군의 흡광도)을 계산하였다.
(4) ABTS radical 소거능 측정
FMH의 최종 농도가 1, 10, 100, 1,000(μg/ml)의 농도로 될 수 있게 희석시켰으며, ABTS 용액은 7.4 mM ABTS(2,2-azino-bis-(3-ethylbenzothiazoline -6-sulfonic acid))와 2.6 mM potassium persulphate를 제조한 후, 암소에 하루 동안 방치하여 양이온 (ABTS⋅+)을 형성시킨 다음 732 nm에서 흡광도를 측정하여 흡광도 값이 1.5 이하가 나오도록 희석하고, 희석된 ABTS⋅+ 용액 150 μl와 FMH를 각각 5 μl 혼합하고, 실온에서 10분간 반응시킨 후, 732 nm 파장에서 흡광도를 측정하였다. 항산화능은 증류수를 대조군으로 하여 대조군에 대한 ABTS radical 소거율(시료 첨가군의 흡광도×100/(1-대조군의 흡광도))을 백분율로 나타내었다.
3) 세포 배양
RAW264.7 세포는 10% fetal bovine serum(FBS)와 1% penicillin-streptomycin으로 조성된 DMEM 배지를 사용하였으며, human umbilical vein endothelial cell(HUVEC) 세포는 EGM™-2 Medium과 EGM™-2 SingleQuots™ Kit으로 혼합된 배지를 사용하여 37 °C, 5% CO2 조건이 유지되는 세포배양기에서 배양하였으며, 2-3일 주기로 계대 배양하여 실험을 진행하였다.
4) 세포 생존율 측정
96 well plate에 RAW264.7 세포와 HUVEC 세포를 1.5×105 cells/well로 분주하여 24시간 동안 배양 하였다. 실험을 하기 전에 새로운 배양액으로 교체하였고, FMH를 각각 1, 10, 100(μg/ml)의 농도로 처리하여 다시 24시간 동안 배양하였다. 배양 후 10 μl의 EZ-Cytox 용액을 첨가하여 세포배양기에서 30분간 반응시켰다. 반응 후 450 nm에서 흡광도의 변화를 측정하여 대조군에 대한 세포 생존율을 백분율로 표시 하였다.
5) 항염증 효능평가
(1) 세포 내 nitric oxide(NO) 생성량 측정
96 well plate에 RAW264.7 세포를 1.5×105 cells/well로 분주하여 24시간 동안 배양 하였다. 배양 후 새로운 배양액으로 교체하였으며, FMH 1, 10, 100 (μg/ml)의 농도와 1 μg/ml LPS를 함께 처리하여 다시 24시간 동안 배양하였다. 이 후, N1 buffer를 50 μl씩 각 well에 처리하여 10분간 상온에서 반응 한 후, N2 buffer를 50 μl씩 각 well에 처리하고 10분간 반응시켰다. 반응 후 540 nm 파장에서 흡광도를 측정한 뒤 대조군에 대한 백분율로 나타내었다.
(2) 세포 내 cytokine 생성량 측정
12 well plate에 RAW264.7 세포를 2×105 cells/well로 분주하여 24시간 동안 배양 하였다. 배양 후 새로운 배양액으로 교체하였으며, FMH 1, 10, 100 (μg/ml)의 농도와 1 μg/ml LPS를 함께 처리하여 다시 24시간 동안 배양하였다. 이후, 배양액을 1,200 rpm에서 5분간 원심분리하여 얻은 상등액과 standard를 96 well plate에 25 μl씩 분주하고 assay buffer 및 matrix buffer, antibody-immobilized beads를 각 25 μl씩 가하여 혼합한 후 2시간 동안 실온에서 반응시키고, washing 완충 용액을 이용하여 2회 세척하였다. 세척 후 25 μl의 detection antibody을 가하여 1시간 동안 실온에서 반응시키고 추가로 25 μl의 Streptavidin-Phycoerythrin을 가하여 30분 동안 실온에서 반응시킨 뒤 washing 완충 용액을 이용하여 2회 세척하였다. 세척 후 PBS를 150 μl 넣고 5분 간 shaking한 후 Luminex를 이용하여 측정한 결과를 절대 값으로 표시하였다.
(3) 세포 내 leukotriene B4(LTB4)생성량 측정
12 well plate에 RAW264.7 세포를 2×105 cells/well로 분주하여 24시간 동안 배양 하였다. 배양 후 새로운 배양액으로 교체하였으며, FMH 1, 10, 100 (μg/ml)의 농도와 1 μg/ml LPS를 함께 처리하여 다시 24시간 동안 배양하였다. 이후, 배양액을 1,200 rpm에서 5분간 원심분리하여 얻은 상등액과 standard를 96 well plate에 100 μl씩 넣고 37 °C에서 90분간 반응시켰다. 반응 후 washing buffer를 이용하여 3회 세척 작업을 진행한 후 100 μl의 detection antibody를 넣어 다시 37 °C에서 60분간 반응시키고 세척하였다. 세척 후 HRP conjugate를 100 μl씩 넣어 37 °C에서 30분간 반응시키고 세척한 뒤 substrate reagent를 90 μl씩 넣어 37 °C에서 15분간 반응시키고 50 μl의 stop solution을 추가하여 ELISA reader기를 통해 450 nm에서 흡광도를 측정하였으며, standard curve를 기준으로 절대 값으로 표시하였다.
6) 세포 내 유전자 발현량 측정
(1) RNA 추출
6 well plate에 HUVEC 세포를 106 cells/well로 분주하여 24시간 동안 배양하였다. 배양 후 새로운 배양액으로 교체하였으며, FMH 1, 10, 100(μg/ml)의 농도와 1 μg/ml TNF-α를 함께 처리하여 다시 24시간 동안 배양하였다. HUVEC 세포를 PBS로 2회 씻어준 뒤 easy blue 1 ml와 chloroform 200 μl를 넣고 vortexing 해준 후 13,000 rpm, 4 °C에서 10분 동안 원심분리 하였다. 그 후 상층액 400 μl와 binding buffer 400 μl를 실온에서 1분 동안 반응시킨 뒤 반응액 700 μl를 column에 주입하여 13,000 rpm에서 30초 동안 원심분리 하였다. Column에 washing buffer A를 700 μl 넣고 13,000 rpm에서 30초 동안 원심분리 후 washing buffer B를 700 μl 넣고 동일하게 원심분리 하였다. Column 하단을 Ep tube로 교체한 후 column에 elution buffer를 50 μl 넣고 1분 동안 반응시킨 뒤 13,000 rpm에서 1분 동안 원심분리하여 추출된 total RNA를 모았다.
(2) cDNA 합성
역전사(reverse transcription) 반응은 RT premix kit의 mixture(reaction buffer, dNTPs mixture, RNase inhibitor, stabilizer, oligo dT15 primer)를 사용하여 total RNA 1 μg이 되도록 diethyl pyrocarbonate (DEPC) 처리된 증류수에 최종 부피가 20 μl가 되도록 하여 첨가하였다. 이 20 μl의 반응 혼합액을 잘 섞은 뒤 45 °C에서 60분 반응시켜 first-strand cDNA를 합성한 후 95 °C에서 5분 동안 방치하여 M-MLV RT를 불활성화 시킨 다음 합성이 완료된 cDNA를 polymerase chain reaction (PCR)에 사용하였다.
(3) 유전자 발현량 측정
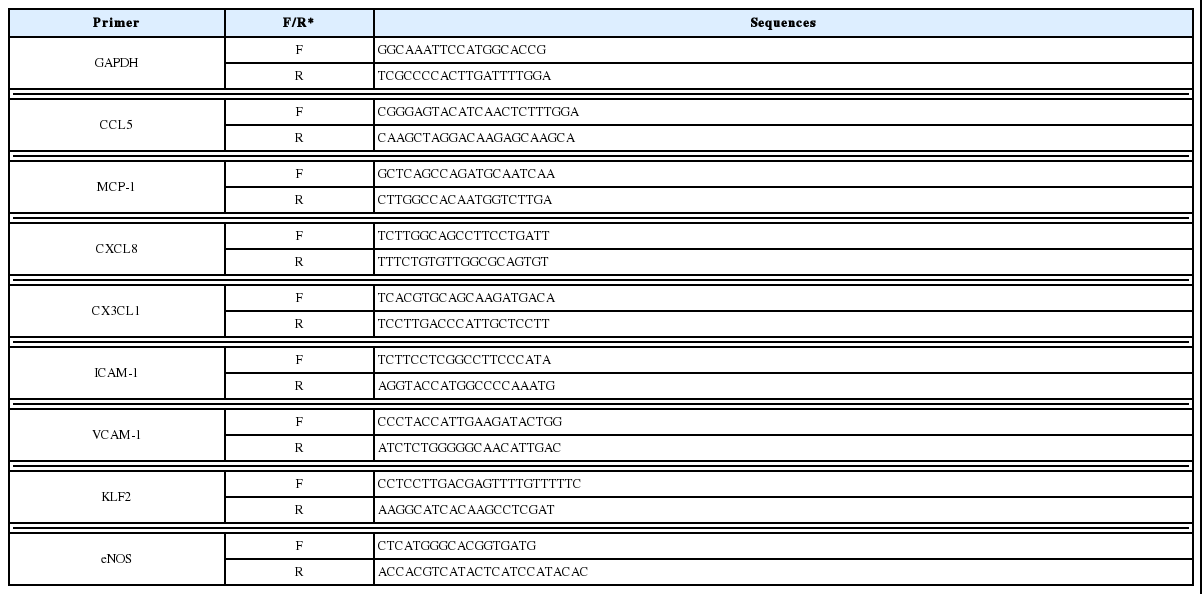
합성이 완료된 cDNA를 증폭시키기 위하여 real-time PCR을 진행하였으며, real-time 전용 tube에 cDNA 1 μl, 각 primer 2 μl, SYBR Green 10 μl, DEPC-DW 5 μl씩 넣어 다음과 같이 진행하였다. 94 °C에서 5분 동안 반응한 다음 94 °C에서 15초, 60 °C에서 30초, 72 °C에서 30초를 40회 반복하여 진행하였고 이 후 유전자 발현량은 대조군에 비하여 계산하였으며, 사용된 primer의 sequence는 Table 1과 같다.
3. 통계처리
실험 결과는 SPSS 24.0의 unpaired student’s T-test와 ANOVA를 사용하여 통계처리 하였고 p<0.05, p<0.01 및 p<0.001 수준에서 그 유의성을 검정하였다.
III. 실험 결과
1. 항산화 효능평가
1) 총 polyphenol 함량 측정
Gallic acid를 표준물질로 하여 FMH에 존재하는 총 polyphenol 함량을 측정한 결과, 8.74±0.30 GAE/g으로 나타났다(Table 2).
2) 총 flavonoid 함량 측정
Quercetin을 표준물질로 하여 FMH에 존재하는 총 flavonoid 함량을 측정한 결과, 1.83±0.19 mg/g으로 나타났다(Table 3).
3) DPPH radical 소거능 측정
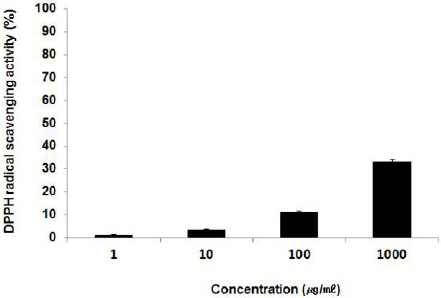
FMH의 DPPH radical 소거능을 측정한 결과, 1, 10, 100, 1,000(μg/ml) 농도에서 각각 1.03±0.30%, 3.68±0.11%, 11.15±0.73%, 33.34±1.00%로 나타나, DPPH radical 소거능의 농도 의존적인 증가가 나타났다(Fig. 2).
4) ABTS radical 소거능 측정
FMH의 ABTS radical 소거능을 측정한 결과, 1, 10, 100, 1,000(μg/ml) 농도에서 각각 2.42±0.23%, 4.64±0.26%, 11.08±0.61%, 43.66±0.14%로 나타나, ABTS radical 소거능의 농도 의존적인 증가가 나타났다(Fig. 3).
2. 세포생존율 측정
RAW264.7 세포에서 세포생존율을 측정한 결과, 대조군이 100.00±2.96%로 나타났을 때, FMH 1, 10, 100, 200 μg/ml에서 각각 106.85±3.33%, 109.36±2.43%, 103.77±6.48%, 57.10±1.72%로 나타났다(Fig. 4A).
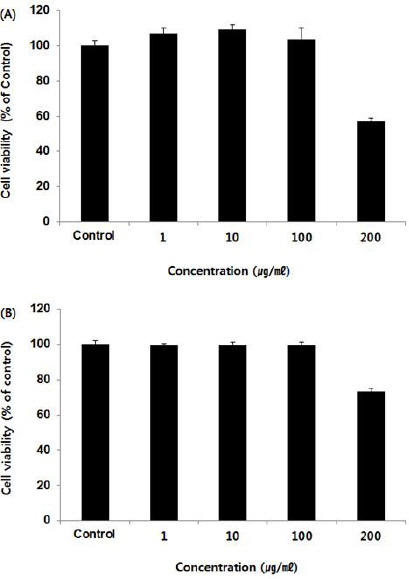
Cell viability of RAW264.7 cells and HUVEC cells were treated FMH.
RAW264.7 cells and HUVEC cells were treated by 1, 10, 100, and 200 μg/ml of FMH for 24 h. Treated cells were exposed by EZ-Cytox for 30 min and then absorbance were measured at 450 nm using microplate reader. Cell viability were calculated as percentage versus control. The result were presented by the mean±S.D from three independent experiments. (A) RAW264.7 cell, (B) HUVEC cell
HUVEC 세포에서 세포생존율을 측정한 결과, 대조군이 100.00±2.19%로 나타났을 때, FMH 1, 10, 100, 200 μg/ml에서 각각 99.77±0.82%, 99.75±1.37%, 99.96±1.16%, 73.16±1.91%로 나타났다(Fig. 4B).
3. 항염증 효능평가
1) 세포 내 NO 생성량 측정
RAW264.7 세포 내 NO 생성량을 측정한 결과, 정상군은 21.92±2.80%, 대조군은 100.00±2.12%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 88.45± 0.71%, 86.47±2.07%, 79.49±2.20%로 나타나, 모든 농도에서 대조군에 비해 유의성 있는(* : p<0.05, ** : p<0.01) 감소가 나타났다(Fig. 5).
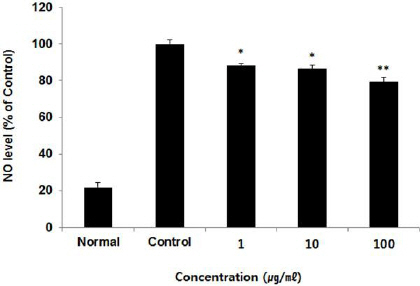
Effect of FMH on NO level in RAW264.7 cells.
RAW264.7 cells were treated by 1, 10, and 100 μg/ml of FMH with 1 μg/ml LPS for 24 h. Treated cells were exposed by nitric oxide detection kit and then absorbance were measured at 540 nm using microplate reader. Level of NO were calculated as percentage versus control. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01 compared to control).
2) 세포 내 cytokine 생성량 측정
(1) Interleukin 1β(IL-1β)
RAW264.7 세포 내 IL-1β 생성량을 측정한 결과, 정상군은 46.05±0.82 pg/ml, 대조군은 123.34±3.27 pg/ml로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 120.85±1.52 pg/ml, 105.73±9.18 pg/ml, 97.01±0.51 pg/ml로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(* : p<0.05, *** : p<0.001) 감소가 나타났다(Fig. 6).

Effect of FMH on IL-1β level in RAW264.7 cells.
RAW264.7 cells were treated by 1, 10, and 100 μg/ml of FMH with 1 μg/ml LPS for 24 h. Treated cells were measured by mouse cytokine milliplex map immunoassay kit. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, *** : p<0.001 compared to control).
(2) Interleukin 6(IL-6)
RAW264.7 세포 내 IL-6 생성량을 측정한 결과, 정상군은 116.80±27.32 pg/ml, 대조군은 151839.83±2593.07 pg/ml로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 106293.60±18652.25 pg/ml, 91706.27±9382.48 pg/ml, 81373.25±12175.46 pg/ml로 나타나, 모든 농도에서 대조군에 비해 유의성 있는(* : p<0.05, ** : p<0.01, *** : p<0.001) 감소가 나타났다(Fig. 7).

Effect of FMH on IL-6 level in RAW264.7 cells.
RAW264.7 cells were treated by 1, 10, and 100 μg/ml of FMH with 1 μg/ml LPS for 24 h. Treated cells were measured by mouse cytokine milliplex map immunoassay kit. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01, *** : p<0.001 compared to control).
(3) Tumor necrosis factor α(TNF-α)
RAW264.7 세포 내 TNF-α 생성량을 측정한 결과, 정상군은 8088.67±174.67 pg/ml, 대조군은 15005.33 ±346.69 pg/ml로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 14033.67±792.87 pg/ml, 12661.25±316.43 pg/ml, 11670.67±346.43 pg/ml로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(* : p<0.05, ** : p<0.01) 감소가 나타났다(Fig. 8).
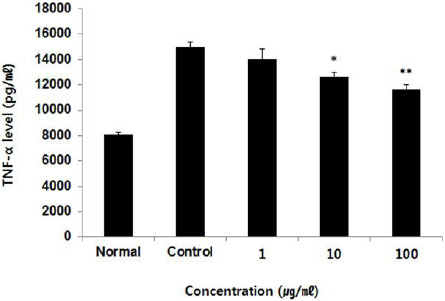
Effect of FMH on TNF-α level in RAW264.7 cells.
RAW264.7 cells were treated by 1, 10, and 100 μg/ml of FMH with 1 μg/ml LPS for 24 h. Treated cells were measured by mouse cytokine milliplex map immunoassay kit. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01 compared to control).
3) 세포 내 LTB4 생성량 측정
RAW264.7 세포 내 LTB4 생성량을 측정한 결과, 정상군은 15.06±1.19 pg/ml, 대조군은 102.15±2.36 pg/ml로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 102.20±1.68 pg/ml, 76.19±2.15 pg/ml, 62.78±3.44 pg/ml로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(** : p<0.01, *** : p<0.001) 감소가 나타났다(Fig. 9).

Effect of FMH on LTB4 level in RAW264.7 cells.
RAW264.7 cells were treated by 1, 10, and 100 μg/ml of FMH with 1 μg/ml LPS for 24 h. Treated cells were measured by LTB4 Parameter Assay Kit. The result were presented by the mean±S.D from three independent experiments (Significance of results, ** : p<0.01, *** : p<0.001 compared to control).
4. 세포 내 유전자 발현량 측정
1) CCL5
HUVEC 세포 내 CCL5 유전자 발현량을 측정한 결과, 정상군은 0.13±0.05%, 대조군은 1.00±0.01%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 1.04±0.08%, 0.93±0.08%, 0.23±0.02%로 나타나, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(*** : p<0.001) 감소가 나타났다(Fig. 10).

Effect of FMH on CCL5 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. CCL5 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, *** : p<0.001 compared to control).
2) Monocyte chemoattractant protein 1(MCP-1)
HUVEC 세포 내 MCP-1 유전자 발현량을 측정한 결과, 정상군은 0.10±0.01%, 대조군은 1.00±0.15%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 0.99±0.09%, 0.79±0.05%, 0.50±0.04%로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 (* : p<0.05, ** : p<0.01) 감소가 나타났다(Fig. 11).

Effect of FMH on MCP-1 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. MCP-1 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01 compared to control).
3) CXCL8
HUVEC 세포 내 CXCL8 유전자 발현량을 측정한 결과, 정상군은 0.10±0.01%, 대조군은 1.00±0.01%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 1.02±0.04%, 0.98±0.05%, 0.50±0.03%로 나타나, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(*** : p<0.001) 감소가 나타났다(Fig. 12).
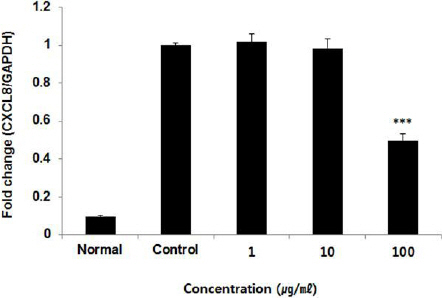
Effect of FMH on CXCL8 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. CXCL8 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, *** : p<0.001 compared to control).
4) CX3CL1
HUVEC 세포 내 CX3CL1 유전자 발현량을 측정한 결과, 정상군은 0.40±0.06%, 대조군은 1.00±0.02%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 1.02±0.03%, 0.88±0.07%, 0.60±0.06%로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 (* : p<0.05, *** : p<0.001) 감소가 나타났다(Fig. 13).
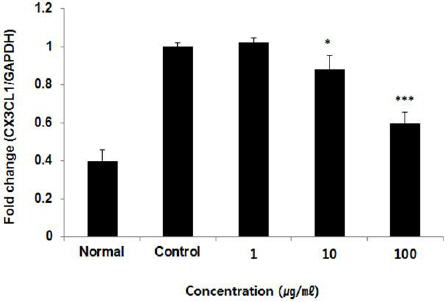
Effect of FMH on CX3CL1 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. CX3CL1 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, *** : p<0.001 compared to control).
5) Intercellular adhesion molecule 1(ICAM-1)
HUVEC 세포 내 ICAM-1 유전자 발현량을 측정한 결과, 정상군은 0.24±0.12%, 대조군은 1.00±0.12%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 1.13±0.07%, 0.55±0.01%, 0.41±0.02%로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 (** : p<0.01, *** : p<0.001) 감소가 나타났다(Fig. 14).
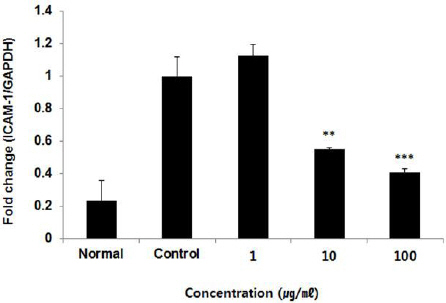
Effect of FMH on ICAM-1 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. ICAM-1 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, ** : p<0.01, *** : p<0.001 compared to control).
6) Vascular cell adhesion molecule 1(VCAM-1)
HUVEC 세포 내 VCAM-1 유전자 발현량을 측정한 결과, 정상군은 0.17±0.11%, 대조군은 1.00±0.07%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 0.67±0.10%, 0.73±0.06%, 0.42±0.14%로 나타나, 100 μg/ml 농도에서 대조군에 비해 유의성 있는(* : p<0.05) 감소가 나타났다(Fig. 15).

Effect of FMH on VCAM-1 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. VCAM-1 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05 compared to control).
7) Krűppel-like Factor 2(KLF2)
HUVEC 세포 내 KLF2 유전자 발현량을 측정한 결과, 정상군은 2.12±0.22%, 대조군은 1.00±0.11%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 0.74±0.03%, 1.74±0.09%, 2.35±0.01%로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 (* : p<0.05, ** : p<0.01) 증가가 나타났다(Fig. 16).
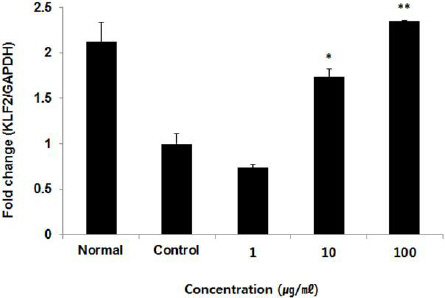
Effect of FMH on KLF2 mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. KLF2 mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01 compared to control).
8) Endothelial nitric oxide synthase(eNOS)
HUVEC 세포 내 eNOS 유전자 발현량을 측정한 결과, 정상군은 3.65±0.23%, 대조군은 1.00±0.11%로 나타났을 때, FMH 1, 10, 100 μg/ml에서 각각 0.60±0.16%, 2.01±0.04%, 2.42±0.01%로 나타나, 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 (* : p<0.05, ** : p<0.01) 증가가 나타났다(Fig. 17).

Effect of FMH on eNOS mRNA expression levels in HUVEC cells.
HUVEC cells were treated by 1, 10, and 100 μg/ml of FMH with TNF-α for 24 h. eNOS mRNA expression levels were measured by polymerase chain reaction. The result were presented by the mean±S.D from three independent experiments (Significance of results, * : p<0.05, ** : p<0.01 compared to control).
IV. 고 찰
전 세계적으로 발생하는 연간 약 5700만 명의 사망자 중 허혈성 심질환 및 뇌졸중으로 인한 사망자가 약 1500만 명 정도 되며, 이는 최근 15년간 가장 주요한 사망원인이었다20. 선진국에서는 지난 수십 년 동안 심혈관계질환에 의한 사망이 감소하고 있는 반면, 국내에서는 오히려 급속히 증가하고 있다. 심혈관계질환의 위험인자로는 남자의 경우에는 고혈압, 흡연, 이상지질혈증으로 확인되었으며 여자는 고혈압, 이상지질혈증, 당뇨병, 흡연의 순서로 영향을 미치는 것으로 밝혀졌는데, 다른 위험인자들은 이전보다 감소하거나 잘 조절되고 있는 반면 식습관이나 운동 같은 생활습관의 악화와 이로 유발되는 혈중 지질 농도의 증가가 심혈관질환의 발병에 중요한 역할을 하고 있다21.
이상지질혈증은 한의학에서 직접적으로 언급되어 있지는 않지만 비슷한 내용을 찾아볼 수 있는데, ≪靈樞⋅衛氣失常論≫에 ‘肥人多, 有膏, 有肉’이라고 한 것과 ≪靈樞⋅五癃津液別篇≫에 ‘五穀之津液, 和合而爲膏, 內滲入于骨空, 補益髓腦而下流于陰股’22라고 기록되어 있어 膏를 이상지질에 대한 언급으로 유추해볼 수 있다. 이상지질혈증은 津液의 일종으로 水穀에서 來源하고 血中에 들어가 영양물질이 되는 血脂가 과다하거나 장부의 기능실조로 대사가 실조되면 발생하며, 痰濁과 血瘀로 보고 祛痰 및 化瘀시키는 治法을 사용한다23.
발효는 고분자 당이 떨어져 나가며 저분자화되어 체내흡수율이 증가되게 하는 기전을 가지며 이로써 생체 이용률을 증가시키는데, 한약의 유효성분은 대개 고분자 당류로 구성되어있기 때문에 최근 발효한약이 관심을 모으고 있으며 발효시 원래의 성질이 변하여 새로운 치료 작용을 기대할 수 있다24. 이에 본 저자는 비교적 안전성이 높은 천연물 중 기존에 많은 선행연구를 통해 이상지질혈증치료에 사용되던 청혈플러스 구성약재의 발효 복합추출물로 연구를 진행하게 되었다.
韓茵蔯은 利水滲濕藥에 해당하며 性은 微寒하고 味는 苦辛하고 淸濕熱한다. 동맥죽상경화모델 집토끼에게 한인진전탕액을 복용시킨 결과 혈중 이상지질상태가 개선되었으며 동맥궁이나 내장병변 보호작용이 나타났다25,26.
鬱金은 活血祛瘀藥에 해당하며 性은 寒하고 味는 辛苦하고 活血消瘀, 解鬱祛痰시킨다. 동맥죽상경화모델 집토끼와 흰쥐에게 울금전탕액을 복용시켰더니 혈중 콜레스테롤이 낮아졌으며, 관상동맥내막의 지질침착을 감소시켰다25,26.
山査는 消食藥에 해당하며 性은 微溫하고 味는 酸甘하며 行氣消食散瘀작용을 한다. 동맥죽상경화모델 집토끼의 정맥에 산사추출물을 주사하였더니 혈중 콜레스테롤 저하작용이 있었으며 기관의 콜레스테롤 침착을 줄여 혈압을 낮추는 역할을 하였다25,26.
丹蔘은 活血祛瘀藥에 해당하며 性은 微寒하고 味는 苦하고 活血祛瘀 작용을 한다. 최근엔 관상동맥경화나 혈전폐색 등에 좋은 치료효과가 있다고 밝혀졌다25,26.
이상지질혈증에 관한 연구에서는 대체로 항산화, 항염증을 같이 진행하게 된다. 이는 이상지질혈증이 동맥경화를 유발하는 과정에서 산화적스트레스가 결정적인 역할을 하며 염증반응이 포함되고, 나아가 노화나 암까지 유발 가능하기 때문이다27.
RAW264.7 세포에서 세포생존율을 측정한 결과 FMH농도가 1, 10, 100 μg/ml에서 각각 106.85±3.33%, 109.36±2.43%, 103.77±6.48%로 나타났다(Fig. 4A). HUVEC 세포에서 세포생존율을 측정한 결과 FMH 1, 10, 100 μg/ml에서 각각 99.77±0.82%, 99.75±1.37%, 99.96±1.16%로 나타났다(Fig. 4B). 이로써 실험이 주로 진행된 농도에서 안전한 것으로 확인되었다. 그리고 두 세포 모두 FMH 200 μg/ml 이상의 농도에서는 80% 이하의 생존율을 보였다.
FMH에 존재하는 총 polyphenol 함량은 8.74±0.30 GAE/g으로 나타났으며(Table 2), 총 flavonoid 함량을 측정한 결과, 1.83±0.19 mg/g으로 나타났다(Table 3). 이로써 FMH에는 항산화물질이 들어있는 것을 알 수 있다.
FMH의 농도를 1, 10, 100, 1,000(μg/ml)로 희석시키고 DPPH assay와 ABTS assay를 시행하였더니 DPPH radical 소거능과 ABTS radical 소거능은 농도 의존적인 증가를 보였다(Fig. 2, 3). 이 결과로 볼 때 FMH가 항산화능을 나타내는 것으로 사료된다.
RAW264.7 세포 내 NO생성량을 측정한 결과, 실험한 모든 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 5). IL-1β 생성량을 측정한 결과 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났고(Fig. 6), IL-6 생성량은 모든 농도에서 대조군에 비해 유의성 있는 감소가 나타났으며(Fig. 7), TNF-α 생성량은 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 8). LTB4는 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 9). 따라서 FMH는 세포 내 항염증 작용을 하는 것으로 사료된다.
GAPDH는 유전자 발현량 측정 실험에서 이 유전자의 발현량을 기준으로 측정하고자 하는 유전자 발현량을 상대정량 하는데 쓰이며28, Chemokine은 백혈구유주 및 염증반응의 주요한 역할을 하며 혈관신생을 매개하여 종양성장이나 전이에 관여하는 작은 단백질로, 본 실험에서 측정한 CCL5, MCP-1, CXCL8, CX3CL1은 chemokine에 속한다29. ICAM-1, VCAM-1은 세포접합분자로, 동맥경화의 초기 과정 중 염증반응을 유발한다30.
HUVEC 세포 내 CCL5 유전자 발현량을 측정한 결과 FMH 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 10). 세포 내 MCP-1 유전자 발현량은 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났으며(Fig. 11). CXCL8 유전자 발현량은 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 12). CX3CL1 유전자 발현량은 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났으며(Fig. 13), ICAM-1 유전자 발현량은 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났고(Fig. 14) VCAM-1 유전자 발현량은 100 μg/ml 농도에서 대조군에 비해 유의성 있는 감소가 나타났다(Fig. 15). KLF2 유전자 발현량은 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 증가가 나타났고(Fig. 16), eNOS는 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있는 증가가 나타났다(Fig. 17). 따라서 FMH는 세포 내 항염증 작용을 하는 것으로 사료된다.
본 연구에서는 한인진, 울금, 산사, 단삼 복합추출물을 발효시켜 실험하였는데, 이전의 비발효 복합추출물 연구 실험과는 세포상태, 사용된 시약, cytokine 측정에 사용되는 antibody 등의 차이가 있어 그 결과를 절대적 수치로 비교하기는 불가능하다. 하지만 발효가 유효성분의 흡수를 용이하게 한다는 사실과, 발효를 이용하여 약재의 더 좋은 효능을 얻었다는 보고가 지속적으로 나오고 있는 것을 고려한다면 본 연구의 좋은 결과에 발효가 긍정적인 역할을 하였을 것으로 생각해 볼 수 있다. 추후 발효군과 비발효군의 효능 비교를 위해 같은 조건 안에서 통제되는 두 군에 대한 연구가 추가적으로 필요할 것으로 보인다.
종합하여 보면, FMH는 산화적 손상 및 이상지질혈증으로 인한 염증반응과 이로써 발생하는 죽상동맥경화증, 허혈성 심질환, 뇌졸중 등 심뇌혈관계질환의 예방과 치료에 유효할 것으로 보인다. 다만, 본 실험에서는 세포 연구만을 다루어 혈중 cholesterol level의 측정이 이루어지지 않아 이상지질혈증 자체의 개선 효능을 명확히 판단하기는 어렵다. 따라서 향후 in vivo실험을 통해 이러한 부분을 명확히 밝힐 필요가 있다고 사료된다.
V. 결 론
한인진, 울금, 산사, 단삼 발효복합추출물(FMH)의 항염증 및 항이상지질 효능을 객관적으로 검증하기 위하여 마우스 대식세포인 RAW264.7 세포와 인간 탯줄 정맥 내피 세포인 HUVEC 세포를 통해 다양한 인자를 확인한 결과 다음과 같은 결론을 얻었다.
1. FMH는 8.74±0.30 GAE/g의 polyphenol 함량과 1.83±0.19 mg/g의 flavonoid 함량을 나타내었으며, DPPH 및 ABTS radical 소거능을 농도의존적으로 증가시켰다.
2. FMH는 NO와 IL-6 생성량을 모든 농도에서 대조군에 비해 유의성 있게 감소시켰으며, IL-1β, TNF-α, LTB4 생성량을 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있게 감소시켰다.
3. FMH는 CCL5, CXCL8, VCAM-1 유전자 발현량을 100 μg/ml 농도에서 대조군에 비해 유의성 있게 감소시켰으며, MCP-1, CX3CL1, ICAM-1 유전자 발현량을 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있게 감소시켰다. 또한 KLF2와 eNOS 유전자 발현량을 10, 100 μg/ml 농도에서 대조군에 비해 유의성 있게 증가시켰다.
이상의 결과를 종합해 볼 때, 발효복합추출물은 항산화효능과 RAW264.7 세포 및 HUVEC 세포에서 항염증 및 항이상지질혈증 효능이 실험적으로 규명되었다. 추후 in vivo 실험을 통한 혈중지질평가 및 관련 연구가 필요하리라 사료된다.