파킨슨병 관련 실험 연구에서 육계의 신경 보호효과에 대한 고찰
Abstract
Objective:
The purpose of this study was to investigate the effect of cinnamon on the treatment of Parkinson’s disease (PD) and to introduce its use in Korea.
Method:
We searched the experimental studies in electronic databases (PubMed, CNKI, Wanfang, CiNii, J-STAGE, Science ON, and OASIS) using the key search terms “cinnamic acid”, “cinnamon”, “cinnamomum”, “Parkinson’s disease”, “Parkinson disease”, “Parkinsonism”, and “dopamine”. This study only involved experimental studies (in vivo and in vitro) that adopted cinnamon as a single administration and measured indicators relating to Parkinson’s disease, including parkin, tyrosine hydroxylase (TH), and dopamine.
Results:
A Total of 11 literature studies were selected, and they all showed that treatment with cinnamon has a neuroprotective effect. Cinnamon activated neuroprotective factors and restored neurotransmitters and it reduced the rate of oxidative stress and inflammation in neurons. As a result, cell viability was upregulated, while cell apoptosis and neurodegeneration were downregulated. Five in vivo studies, through behavioral tests, also confirmed that cinnamon recovers locomotor function in PD models.
Conclusion:
We identified that cinnamon is an effective neural protector and improves motor performance in behavioral testing in the experimental PD studies.
Keywords: cinnamon, Parkinson’s disease, dopamine, review
Ⅰ. 서 론
파킨슨병은 안정시 떨림, 서동증, 경직, 자세 불안정의 4가지 주요 징후를 특징적으로 발생시키는 병으로, 치매, 뇌졸중과 더불어 3대 노인성 질환에 속한다 1. 2019년 기준 국내의 파킨슨병 환자는 110,147명으로 10년 전과 비교해 약 1.8배 증가하였다 2. 인구 고령화의 급속한 진행추세를 고려하면 앞으로 더욱 증가할 것으로 추산된다. 파킨슨병은 중뇌 흑색 치밀부의 도파민 신경세포의 손상 혹은 소실로 인해 선조체에 도파민이 결핍되어 나타난다. 하지만 현재까지는 신경 세포를 재생시키거나 소실을 정지시킬 수 있는 치료방법은 존재하지 않으며 3, 도파민 전구 물질이나 도파민 작용제 등을 투여하는 방법들이 주로 사용되고 있다 3,4. 그러나 치료의 핵심적인 약물로 사용되는 레보도파는 장기간 복용하면 운동기복 증상(motor fluctuation)이나 이상운동증(dyskinesia) 등이 나타나는 한계가 있다. 이를 대체하기 위한 새로운 약물들이 개발되고 있지만, 약물 이상반응이나 효과기간이 점점 짧아지는 등의 문제가 남아 있다 4. 이에 다양한 보완치료에 대한 수요와 기대가 이어지고 있으며, 한의 임상에서도 補腎養肝息風方, 補腎活血顆粒, 抑肝散. 六君子湯 등의 처방을 이용한 연구가 소개되고 있고 5,6 침 치료와 봉독약침 등 다양한 치료 방법이 사용되고 있다. 여러 연구들을 통해 한방치료의 병행 투여에서 양방 치료약 단독투여에 비해 통증 및 운동증상 개선효과가 유의하게 증가됨이 확인되어 7-10 보완 치료로서도 의미가 있음이 보고되고 있다. 한편 최근 들어, 한의학의 주요 약재 중 하나인 육계의 주성분이 파킨슨병 모델의 도파민 신경세포에서 신경보호효과를 나타내며, 운동 증상의 개선에도 유효하다는 실험 연구 결과가 지속적으로 보고되고 있다 11-17. 이에 저자는 육계를 이용한 파킨슨병 관련 실험 연구들을 대상으로 문헌고찰을 통해 다음과 같은 결과를 얻었기에 이를 보고하고자 한다.
Ⅱ. 대상 및 방법
1. 검색 엔진 선택 및 검색 방법
국내 검색 엔진 키워드는 ‘육계’, ‘계지’, ‘계피’, ‘cinnamic acid’, ‘cinnamon’, ‘cinnamomum’, ‘파킨슨병’, ‘Parkinson’s disease’, ‘Parkinson disease’, ‘Parkinsonism’ 및 ‘dopamine’이었고, 영어권 검색 엔진 키워드는 ‘cinnamic acid’, ‘cinnamon’, ‘cinnamomum’, ‘Parkinson’s disease’, ‘Parkinson disease’, ‘Parkinsonism’, ‘dopamine’이었다. 중국 검색 엔진 키워드는 ‘肉桂’, ‘桂枝’, ‘桂皮’, ‘cinnamic acid’, ‘cinnamon’, ‘cinnamomum’, ‘帕金森氏病’, ‘帕金森’, ‘震颤性麻痹’, ‘震颤麻痹’, ‘多巴胺’, ‘Parkinson’s disease’, ‘Parkinson disease’, ‘Parkinsonism’, ‘dopamine’이었다. 일본 검색 엔진 키워드는 ‘肉桂’, ‘桂皮’, ‘桂枝’, ‘パーキンソン病’, ‘ドパミン’을 사용하였다.
검색은 2020년 9월 10일에 시행하였으며, 검색기간은 검색 엔진이 지원하는 개시 시점부터 검색 시점까지를 범위로 하였다. 문헌의 언어 제한은 두지 않았다.
2. 선정기준과 제외기준
1) 선정 기준
(1) 동물이나 세포를 대상으로 한 실험연구
(2) cinnamomum 분말, 추출물, 정유 또는 cinnamomum이 인체 내에서 대사되는 형태의 물질을 단독으로 이용한 경우
(3) 파킨슨병 치료 효능을 나타내는 지표를 측정한 경우
2) 배제 기준
(1) 다른 성분 및 약물과 병용한 경우
(2) 파킨슨병에 특이적인 지표가 포함되지 않은 경우
3. 자료 선정 및 분석
국내외 검색엔진에서 검색된 문헌을 취합한 후 먼저 논문 제목, 출판연도, 저자를 참고하여 중복문헌을 제거하였다. 문헌의 선정기준과 제외기준에 따라 제목(title)과 초록(abstract)을 토대로 1차 선별과정이 이루어졌다. 이후 두 명의 검토자(HH, HJ)가 1차 선정 문헌을 대상으로 문헌의 전문을 검토하는 2차 선별과정을 거쳐, 파킨슨병에의 육계 응용 가능성에 대한 실험 연구 여부를 판단하여 최종 문헌 선정 및 분석을 진행하였다.
4. 데이터 추출
본 연구에서는 연구디자인 분석을 위하여 최종적으로 포함된 문헌들 각각의 전문을 확인하여 연구 기본 정보, 표본 정보(종, 수), 중재기간, 시험군의 중재(투여약물 및 방법), 대조군의 중재(투여약물 및 방법), 평가 도구 및 결과 값 등에 대한 자료를 추출하였다. 추출한 자료를 바탕으로 각 문헌들의 특성에 대하여 고찰을 시행하였다.
Ⅲ. 결 과
1. 문헌 선별
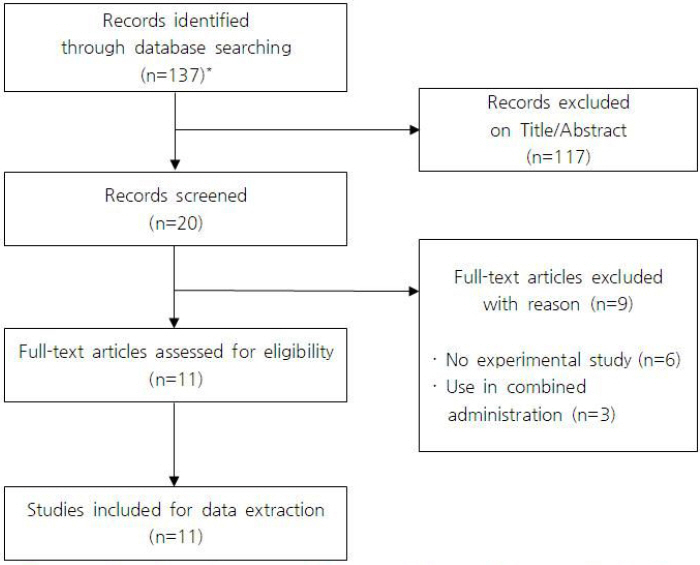
최초 245개 문헌이 검색되었으며, 108개 중복 문헌을 제외하여 1차적으로 137개 문헌이 선정되었다. 선정 및 제외기준에 따라 문헌의 제목과 초록을 검토하여 육계나 파킨슨병에 관련 없는 117개의 문헌을 배제하였다, 2차 스크리닝 단계에서는 전문 읽기를 통해 타 약물과 병용 투여(加味桂枝加葛根湯)된 문헌 1개, cinnamon 화합물을 사용한 문헌 2개, 실험논문이 아닌 문헌 6개를 배제하여 11개 문헌이 최종선택 되었다( Fig. 1).
Fig. 1
PRISMA flow diagram for process of literature search.
The numbers of articles are as follows and the numbers contain duplicate data: PubMed=48, CNKI=105, Wangfang=62, J-STAGE=25, CiNii=2, OASIS=0 and ScienceON=0
2. 문헌 분석
1) 선정 문헌의 특성
11건의 실험 연구 중 in vivo 논문이 5편 11,14,16,18,19 in vitro 논문이 5편이었으며 12,15,17,20,21 in vivo와 in vitro 실험을 동시에 진행한 논문도 1편 13 있었다. 6편은 미국에서 보고되었고, 나머지 5편은 한국, 중국, 이란, 이스라엘, 호주에서 각각 1편씩 보고되어 세계 각국에서 다양하게 이루어지고 있다는 것을 알 수 있었다.
2) 실험 대상에 대한 분석
in vivo 실험 6건에서는 유전자 이식된 A53T mice를 대상으로 한 연구가 1건 11, C57BL/6 mice가 4건 13,14,16,18, 초파리를 이용한 연구가 1건 19 있었다. 6건의 in vitro 실험에서는 PC-12 cell과 SH-SY5Y cell이 각각 2건 12,17, 1건 15씩 이용되었고, 쥐나 태아로부터 분리한 신경세포 및 아교세포를 이용한 실험은 3건 13,20,21이었다.
아울러, 11개의 논문에서 파킨슨병 양상을 야기하기 위한 목적으로 사용한 방법은 다양하였으나 MPTP (MPTP-HCl, MPP+ 포함)주입법이 5편 13,14,16,18,21으로 가장 많이 사용되었고, 6-OHDA 주입이 2편 12,17에서 사용되었다. transgenic 11, H 2O 215, crossing system 19방법이 각각 1번씩 이용되었다. Khasnavis 20의 연구에서는 파킨슨병 양상을 일으키지 않고 treatment 이후 정상세포에서의 파킨슨병 관련 인자들의 변화를 확인하였다.
3) 중재내용 분석
본 연구에서 종합한 문헌들은 정상 모델과 파킨슨병 형태를 인위적으로 일으킨 모델에 육계의 다양한 형태를 투여하거나, 혹은 육계를 투여한 군과 투여하지 않은 대조군에 동일한 파킨슨병 유발과정을 시행하여 그 결과를 비교하는 방식으로 진행되었다.
실험마다 사용된 육계의 형태는 다양했는데, 동물모델을 대상으로 한 연구들에서 가장 높은 빈도로 이용된 형태는 기본상태의 powder 형태로 3건 11,13,18의 실험에서 모두 100 mg/kg만큼 투여되었다. 다음으로 NaB(Sodium Benzoate)가 두 연구에서 각 100 mg/kg 13, 50 mg/kg 18으로 사용되었다. 그 외에 cinnamic acid 100 mg/kg 14, cinnamaldehyde 10 mg/kg 16, CEppt 0.75 mg/mL 19가 사용되었다. 세포단위 연구에서는 NaB가 가장 많이 사용되었는데 각 0.25 13, 0.5 20, 1 21 mM의 양으로 이용되었고, cinnamaldehyde는 2건에서 각 0.1 μM 15, 5, 10 μM 12 사용되었다. Ramazani 12의 연구에서는 cinnamaldehyde 외에도 essential oil과 extracts을 20 μg/mL 사용하였으며, cinnamon flavonoid 40, 60, 80 μg/mL 사용한 문헌도 1편 17 있었다. cinnamon 투여는 복강내주사 1건 16을 제외하고는, 모든 동물 모델에게 oral 혹은 needle을 이용해 gavage 형태로 투여되었다 11,13,14,18,19. cinnamomum의 종을 언급한 5개의 논문 중에서 C. cassia와 C. verum을 모두 사용한 1개의 논문 12 제외하고는, 모두 C. verum을 사용하였다고 보고하였다 11,12,13,18. 또한 기전을 파악하기 위하여, 의심경로의 중간매개체를 결핍시킨 상태와 정상상태를 비교하는 연구 설계도 2편 13,14에서 이루어졌으며, 다른 compounds와 비교하는 형태 15도 있었다.
4) 평가 도구
평가 변수들은 항산화 및 도파민 관련세포의 생존 등 보호효과를 나타내는 지표와 세포 독성 및 산화 등의 손상을 나타내는 지표, 혹은 도파민 호르몬 자체의 수치로 대별될 수 있다.
Intervention의 진행과 함께 상승하는 지표에는 tyrosine hydroxylase(TH) 13,14,16,17, Parkin, DJ-1 11,18,20, cell viability, survivin 12,14, superoxide dismutase(SOD) 17, glial cell line-derived neurotrophic factor(GDNF) 13, (PARK1, 2를 제외한) PARK gene 20, p62 16이 있었다. 이와 함께, 도파민 관련 물질 Dopamine, 3,4- dihydroxyphenlacetic(DOPAC), homovanillic acid (HVA) 14,18이 있다. 반대로, 감소하는 지표로는 α-synuclein (α-syn) 11,19,20, p-syn 11, Inducible nitric oxide synthase (iNOS) 11,18,21, ROS 12, glial fibrillary acidic protein (GFAP) 11,18, BCL-2 associated X protein(BAX) 17, caspase-9 16, cytochorme(cyt-c) 12, poly-ADP ribose- polymerase-1(PARP-1) cleavage 15, IBA 1 11, light chain 3(LC3) 16, apoptosis/DNA damage 17, cluster of diffferentiation molecule 11B/C(CD11b) 21이 사용되었다.
Table 1
Summary of Animal Model in Studies (in vivo)
|
Study ID |
Model |
Intervention. |
Administration (duration) : capacity |
Outcomes measures. |
Behavior test. |
Result |
|
Raha (2020)11
|
Transgenic A53T mice (n=5) |
1) Standard
2) A53T+0.5% MC
3) A53T+cinnamon |
Oral (60 d) : 100 mg/kg |
DJ-1, Parkin, α-syn, p-syn, GFAP, iNOS, IBA1 |
Barnes maze open field, Pole, rotarod |
⋅Neuroprotective proteins were increased. (↑)
⋅Locomotor functions were restored. (↑)
⋅neuroinflammation, α/p-syn were reduced. (↓) |
|
|
Patel (2019)13
|
C57BL/6 mice (n=5) |
1) Standard
2) Standard+NaB
4) Standard+NaFO |
Oral (10 d) : 100 mg/kg |
GDNF |
- |
⋅GDNF level was increased even in normal model. |
|
|
C57BL/6 mice (n=5) |
1) Standard+saline
2) MPTP+0.5% MC
3) MPTP+NaB
4) MPTP+cinnamon |
Oral (7 d) : 100 mg/kg |
GDNF, TH |
Rotarod, open field |
⋅TH, GDNF level were increased. (↑)
⋅Locomotor function was improved. (↑) |
|
|
Prorok (2019)14
|
C57BL/6 mice (n=5) |
1) Standard
2) MPTP
3) MPTP+0.1% MC
4) MPTP+cinnamic acid |
Gavage needle (7 d) : 100 mg/kg |
TH, dopamine, DOPAC, HVA |
Rotarod, open field |
⋅TH, Neurotransmitters were protected. (↑)
⋅Locomotor function was improved. (↑) |
|
|
C57BL/6 mice (n=5) |
1) MPTP
2) MPTP+PPARβ (-) +cinnamic acid
3) MPTP+PPARα (-) +cinnamic acid |
Oral (7 d) : 100 mg/kg |
TH, dopamine, DOPAC, HVA |
Rotarod, open field |
⋅In the study aimed at mechanism investigation, PPARα was identified as the main route. |
|
|
Bae (2018)16
|
C57BL/6 mice (n=5) |
1) Standard
2) MPTP
3) MPTP+
cinnamaldehyde |
I,p, inj. (7 d) : 10 mg/kg |
TH,p62 protein LC3 puncta |
- |
⋅autophagy, Loss of dopamine neuron fiber were reduced. (↓) |
|
|
Khasnavis (2014)18
|
C57BL/6 mice (n=4) |
1) Standard
2) MPTP
3) MPTP+MC
4) MPTP+cinnamon |
Gavage needle (7 d) : 100 mg/kg |
TH, Parkin, DJ-1, dopamine iNOS, GFAP |
Rotorod, open field |
⋅neurotransmitter, neuroprotective proteins, TH were protected. (↑)
⋅Locomotor function was improved. (↑)
⋅Neuroinflammation was reduced. (↓) |
|
5) MPTP+NaFO
6) MPTP+NaB |
: 50 mg/kg |
|
|
Shaltiel-Karyo (2012)19
|
Drosophila (n=50) |
1) Standard
2) Standard+cinnamon
3) α-syn A53T
4) α-syn A53T+ cinnamon |
Medium (19 d) : 0.75 mg/mL |
α-syn |
Climbing |
⋅Locomotor function was improved. (↑)
⋅Accumulation of α-syn was reduced. (↓) |
Table 2
Summary of Cell Model in Studies (in vitro)
|
Study ID |
Model |
Intervention |
Duration : capacity |
Outcomes measures |
Result |
|
Ramazani (2020)12
|
PC12 cell |
1) Standard
2) 6-OHDA (100 μM)
3) 6-OHDA+essential oil of cinnamon
4) 6-OHDA+extracts of cinnamon |
24h : 20 μg/mL |
ROS, cyt-c, Survivin, P-p44/42, p44/42 |
⋅Cyt-c was decreased. (↓) : EO>Extracts>cinnamaldehyde
⋅Survivin was increased. (↑) : EO, Extracts
⋅P-p44/42, p44/42 were decreased. (↓) : EO |
|
|
5) 6-OHDA+ cinnamaldehyde |
5, 10 μM |
|
|
Patel (2019)13
|
Human astrocytes |
1) control siRNA+NaB
2) CREB (-) siRNA+NaB |
4h : 250 μM |
GDNF |
⋅In a study aimed at mechanism investigation CREB was identified as the main route. |
|
|
Maiolo (2018)15
|
SH-SY5Y cells transfected with human TH isoform1 |
1) Standard
2) H2O2 (150 μm)
3) H2O2+cur/caff/pic
4) H2O2+cinnamaldehyde |
1h : 100 nM |
Cell viability, PARP-1 cleavage |
⋅Cell viability was increased. (↑) |
|
|
Zeng (2017)17
|
PC12 cell |
1) Standard
2) 6-OHDA (100 μM)+ vitamin C
3) 6-OHDA+cinnamon flavonoids |
40, 60, 80 μg/mL |
SOD, cl Caspase-9, MDA, DNA damage, Bax/Bcl-2, apoptosis |
⋅Cell viability, SOD were increased. (↑)
⋅Apoptosis, DNA damage, Bax/Bcl-2 rate, cl Caspase-9, MDA were decreased. (↓) |
|
|
Khasnavis (2012)20
|
Primary neurons from fetal brain |
1) Standard
2) Standard+NaFO
3) Standard+NaB |
24h : 0.5 mM |
DJ-1 |
⋅DJ-1 was increased. (↑) |
|
|
|
primary astrocytes of SJL/J mice (F) |
6h : 0.5 mM |
DJ-1, Parkin, PINK1, LRRK2, HtrA2, α-syn |
⋅DJ-1, Parkin, PINK1, LRRK2, HtrA2 were. increased (↑)
⋅α-syn was decreased. (↓) |
|
|
Brahmachari (2009)21
|
Primary microglia of mouse |
1) Standard
2) MPP+ (1 μM)
3) MPP++ NaFO
4) MPP++ NaB |
6h : 1.0 mM |
Surface marker (CD11b/c, CD68), iNOS |
⋅Expression of iNOS and surface molecules were decreased. (↓) |
대다수의 문헌에서 intervention에 의해서 수치가 상승하는 지표와 하강하는 지표를 복합적으로 사용하였고 11,12,15,17,20, 3건에서는 상승하는 지표만을 13,14,18, 그 외 2건에서는 하강하는 지표만을 측정하였다 19,21.
3. 연구결과 및 기전
1) 연구결과
문헌들을 종합해 본 결과, 육계와 그 대사물질들의 투여는 파킨슨병 유발과정과의 전후순서에 상관없이 흑색질 속에서 직접적으로 생물학적인 작용을 나타낸다는 것을 알 수 있었다. 육계의 투여는 총 11개의 모든 문헌에서 다양한 파킨슨병 관련 인자들을 정상화하는 방향으로 조절하였다. 다양한 지표들이 사용되었지만, 뇌 내 세포의 생존률 증가, 사멸과 손상 감소, 운동능력 개선의 작용으로 대별할 수 있다.
신경세포 보호 효과는 DJ-1, Parkin 등과 같은 산화 스트레스로부터 신경세포들을 보호하는 인자들의 활성화 11,12,15,17,18,20 및 도파민 작용성 세포들을 영양⋅보호하는 GDNF의 증가를 통해 확인할 수 있다 13. 이외에도 도파민성 신경세포의 대표적 표지로서 파킨슨병환자에게서 필연적으로 감소되는 TH 역시 정상수치에 근사하게 보호되었고 13,14,16,18, 선조체 내의 dopamine의 복구도 야기되었다 14,18. 반면에 iNOS, Caspase-9 등의 염증반응 및 신경퇴화 유도물질의 발현은 억제되었다 11,12,16-18,20,21. 파킨슨병 환자의 뇌에는 α-syn이 응집된 루이소체가 특징적으로 축적되는데, 여러 실험에서 육계가 α-syn의 축적과 응집 자체를 저해하며 11,19,20 인산화된 구조까지도 억제하는 것을 확인할 수 있었다 11. Barnes maze, open field test, Pole test, rotarod test, climbing test 등의 행동시험이 이루어진 총 5건 in vivo의 실험에서 파킨슨병이 유발된 실험동물의 운동성 장애가 대조군에 비해 명백하게 호전된 것이 확인되었다.
2) 기 전
신경보호 기전을 찾기 위한 실험을 추가적으로 진행한 2편의 문헌에서 각각, 유전자의 전사를 조절하는 세포전사인자인 cAMP response element-binding protein(CREB) 13과 유전자 발현을 조절하는 핵수용체인 Peroxisome proliferator activated receptor α (PPARα) 14의 존재가 육계의 신경세포 보호효과 발현에 필수적인 것으로 나타났다.
Ⅳ. 고찰 및 결론
파킨슨병은 신경전달물질인 도파민을 생성하는 도파민 신경세포 소실로 인해 운동성 및 비운동성 증상이 나타나는 신경퇴행성 질환이다. 알츠하이머 치매 다음으로 흔한 신경퇴행성 질환이며 22 다양한 치료 약물이 개발되어 있으나, 아직까지 약물 이상반응이나 수반되는 다양한 증상을 치료하는데 한계가 있는 실정이다. 최근 육계의 주요 성분이 파킨슨병 실험 연구에서 신경 보호 효과가 있음을 시사하는 연구들이 지속적으로 발표되고 있다. 이에 본 연구는 파킨슨병 치료에 대한 육계의 활용 가능성을 확인하기 위하여 문헌검색을 통해 얻어진 실험 연구들을 분석하였다.
Cinnamon은 녹나무과의 육계나무 Cinnamomum cassia 또는 기타 동속 근연식물을 사용하는 약재이다. 한의학에서는 육계와 계지로 사용되며, 일상생활에서는 계피 혹은 시나몬이라는 이름의 향신료로서 많이 사용된다. 국내에서 사용되는 육계 또는 시나몬은 Cinnamomum의 대표적인 두 종인 실론계피나무 C. verum과 육계나무 C. cassia이며, 세계적으로 유통량을 조사해보면 육계가 훨씬 많이 사용되고 있다.
스리랑카와 인도남부가 원산지인 C. verum(시나몬)는 甘味가 강하고 향미가 부드러우며, 어린 수피를 채취하여 사용하는 경우가 흔한 반면, 중국남부와 베트남이 원산지인 C. cassia(육계)는 辛味가 강하며, 여러 해를 지난 두꺼운 수피를 채취하여 香味가 강한 것을 주로 사용하는 특징이 있다. 그러나 성분에 있어서는 공통적으로 cinnamaldehyde를 주성분으로 가지고 있어 24 전체적인 작용 또한 동일하며, 효능의의 차이는 미미하다는 실험결과도 보고되었다 12. 한편 C. cassia는 1 g 당 약 3~5 mg의 Coumarin 성분을 함유하고 있어, 다량을 장기간 투여할 경우에는 간독성의 우려가 있으므로 주의해야 한다 31. 육계는 전통적으로는 溫裏祛寒의 작용이 뛰어나 腎陽을 補하는 목적으로 주로 사용되어 왔고, 최근에는 항염증 및 항불안 효과 등의 효능도 가진다고 보고되고 있다 23. 육계의 주요 구성성분은 cinnamaldehyde로 산화작용에 의해서 cinnamic acid로 전환된다. cinnamic acid는 간에서 β-oxidize되어 체내에서는 NaB로 존재한다 24. NaB는 BBB를 통과할 수 있기 때문에 표적대상인 흑색질에서도 효과적으로 작용할 수 있다. 이 NaB는 글라이신 대사 장애와 간 대사 장애의 치료약으로서 FDA 승인을 받았다 25,26. 객관적이고 엄격한 기준 하에서 안정성이 입증되었다는 사실을 알 수 있다. 최근에는 공황장애, 우울증, 다발성 경화증 등에서 증상개선 효과가 관찰되어 연구가 지속되고 있으며, 다양한 방면에서 잠재성을 확인할 수 있다. 게다가 체내에 축적되지 않고 24시간 이내 소변을 통해 배설되므로 부작용에 대한 우려가 비교적 적은 물질이다 27. 그렇기에 본 연구에서 수집한 실험들에서는 cinnamon powder 형태와 cinnamaldehyde, cinnamic acid의 성분 형태만이 아니라 체내에서 대사된 형태인 NaB를 이용하여 육계의 효능을 알아보았다. 파킨슨병을 유발시킨 모델을 대상으로 한 in vivo 및 in vitro의 실험 결과, 육계 투여가 중뇌 흑질 신경세포에서의 손상 진행을 감속시키는 효과를 나타내는 것이 확인되어졌다. 아울러 정상모델에 육계를 투여한 후 파킨슨병 관련 지표들의 측정을 추가로 진행한 문헌들도 있었다. DJ-1, GDNF, α-syn 등의 지표가 사용된 2편의 문헌에서는 13,20, 정상 모델에서도 파킨슨병 모델에서와 유사한 변화가 나타났다. 다만 육계를 투여한 정상 동물군에서의 행동 및 운동 능력을 측정한 Shaltiel 19의 연구에 따르면, 그 변화가 뚜렷하지 않았다. 즉, 정상 신경세포의 손상을 방지하는 효과가 있음을 유추할 수 있기에, 예방차원에서의 cinnamon 복용은 신경세포 보호차원에서는 어느 정도 의미가 있을 수 있다. 그러나 정상범위의 운동능력을 향상시키기 위한 목적으로는 의미가 없다고 해석할 수 있다. 앞서 Patel 13에서 육계의 신경세포 보호효과 발현에 필수적인 것으로 나타난 CREB은 파킨슨병과 관련된 TH, parkin, GDNF 등도 조절한다 28. Prorok 14의 PPAR은 염증반응, 동맥경화증 진행과 관련 있다. 최근 이외의 여러 작용이 추가적으로 보고된 바 있으며 29, 저자는 앞서 예상 주요 경로로 언급된 CREB을 증가시키는 작용에 주목하였다 24. 즉, PPAR 본래의 항염증작용에서 그치는 것이 아니라 파킨슨병에 특이적인 효과가 나타나는 것은 CREB 증가 때문이라고 생각한다. 이 두 논문은 독립적인 2가지 경로를 각각 발견해낸 것이 아니라, PPARα라는 큰 경로 안의 핵심 궤도인 CREB을 확인한 것이라 볼 수 있다. 이러한 기전 연구는 육계 투여에 앞서, 효능이 최대로 발현될 수 있는 조건들을 알려 준다. 향후 지속적인 연구로 추가적인 경로들이 명확해진다면, 파킨슨병에 대한 육계의 효용성이 더욱 높아질 것이다. 한편, Ramazani 12의 연구에서는 육계의 essential oil과 powder, cinnamaldehyde를 비교하여, 추출방식에 따른 효과를 분석하였다. 그 결과, essential oil이 세포 사멸 관련인자인 cyt-c를 가장 큰 폭으로 감소시켰으며, 세포 생존율 관련 인자인 survivin은 상승시키고, 세포 사멸과 관련된 P-p44/42, p44/42 levels은 감소시키는 작용도 나타냈다. 이 결과는 essential oil이 다양한 작용을 나타내며 효과적일 수 있음을 보여준다. 다만 육계 내의 essential oil은 그 함유량이 5%로 적은 편이다 30. 그러므로 향후에 추출 및 투여방법에 대한 연구가 필요할 것으로 사료된다. 본 연구는 파킨슨병 관련인자들의 육계 및 주요성분 투여 전후 변화를 측정하는 실험 논문들을 분석하여, 파킨슨병 치료에 대한 적용 가능성을 검토해보았다. 앞선 연구들에서 육계의 항산화, 항염증 및 신경 보호효과가 확인되어, 파킨슨병을 비롯한 신경퇴행성 질환에의 활용해 볼 가치가 있을 것이라고 생각된다. 또한 여러 행동검사를 통해 파킨슨병 동물 모델에서의 운동능력 개선효과도 관찰할 수 있었기에, 파킨슨병 환자들의 ‘신체활동 제한’에도 긍정적인 영향을 미칠 수도 있을 것으로 추정할 수 있다. 육계는 오랜 세월동안 다양한 지역에서 식품과 향신료로 널리 사용되어왔기 때문에, 안전성 면에서도 유리한 측면이 있다. 그러나 현재까지 진행된 대부분의 연구들이 모두 세포 모델 혹은 동물 모델을 대상으로 하는 실험 연구 위주로 진행되어, 추가적인 임상연구가 필요할 것으로 사료된다.
감사의 글
본 연구는 한국보건산업진흥원을 통해 보건복지부 「한의약선도기술개발사업」의 재정 지원을 받아 수행된 연구임 (HB16C0023).
참고문헌
1. The Korean Movement Disorder Society. Report to expand the policy supporting Parkinson's disease in Korea. Seoul 2007:
3. Kim JH. Analysis of prescription of Parkinson's drug using HIRA-NPS data. Master s'thesis, Graduate School of Sungkyunkwan University 2020:
4. Lee JJ. Pharmacological treatment in Parkinson's disease. J Korean Neurol Assoc 2019:37(4):335–44. doi:10.17340/jkna.2019.4.1.  5. Guideline center for Korean Medicine. Korean medicine clinical practice guideline for Parkinson's disease. Seoul 2017Available from: http:// www.nckm.or.kr. accessed Oct 10, 2020. 6. Cho KH. Korean medicine treatment of Parkinson's disease Paju: Mulgogisup: 2018. p. 123–6.
7. Lee SH, Lim S. Clinical effectiveness of acupuncture on Parkinson disease:A PRISMA-compliant systematic review and meta-analysis. Medicine 2017:96(3):e5836doi:10.1097/MD.0000000000005836.  8. Doo KH, Lee JH, Cho SY, Jung WS, Moon SK, Park JM, et al. A prospective open-label study of combined treatment for idiopathic Parkinson's disease using acupuncture and bee venom acupuncture as an adjunctive treatment. J Altern Complement Med 2015:21(10):598–603. doi:10.1089/acm.2015.0078.  9. Hartmann A, Mullner J, Meier N, Hesekamp H, van Meerbeeck P, Habert MO, et al. Bee venom for the treatment of Parkinson disease –A randomized controlled clinical trial. PLoS One 2016:11(7):e0158235doi:10.1371/journal.pone.0158235.  10. Yang SB, KIm YJ, Lee HM, Lee SH, cho SY, Park JM, et al. Effects of korean medicine on postural instability and gait difficulty in patient with Parkinsonism:Retrospective Study. J Korean Med 2017:38(3):96–102. doi:10.13048/jkm.17028.  11. Raha S, Dutta D, Roy A, Pahan K. Reduction of Lewy body pathology by oral cinnamon. J Neuroimmune Pharmacol 2020:doi:10.1007/s11481 -020-09955-2.  12. Ramazani E, YazdFazeli M, Emami SA, Mohtashami L, Javadi B, Asili J, et al. Protective effects of Cinnamomum verum, Cinnamomum cassia and cinnamaldehyde against 6-OHDA-induced apoptosis in PC12 cells. Mol Biol Rep 2020:47(4):2437–45. doi:10.1007/s11033-020-05284-y.  13. Patel D, Jana A, Roy A, Pahan K. Cinnamon and its metabolite protect the nigrostriatum in a mouse model of Parkinson's disease via astrocytic GDNF. J Neuroimmune Pharmacol 2019:14(3):503–18. doi:10.1007/s11481-019-09855-0.  14. Prorok T, Jana M, Patel D, Pahan K. Cinnamic acid protects the nigrostriatum in a mouse model of Parkinson's disease via Peroxisome Proliferator -Activated Receptorα. Neurochem Res 2019:44(4):751–62. doi:10.1007/s11064-018-02705-0.  15. Maiolo SA, Fan P, Bobrovskaya L. Bioactive constituents from cinnamon, hemp seed and polygonum cuspidatum protect against H2O2 but not rotenone toxicity in a cellular model of Parkinson's disease. J Tradit Complement Med 2018:8(3):420–7. doi:10.1016/j.jtcme.2017.11.001.
16. Bae WY, Choi JS, Jeong JW. The neuroprotective effects of cinnamic aldehyde in an MPTP mouse model of Parkinson's disease. Int J Mol Sci 2018:19(2):551doi:10.3390/ijms19020551.  17. Zeng H, He G, Huang H, Li Y. Protective effect of total flavonoids of Cinnamomi cortex on PC12 cell injured by 6-Hydroxydopamine. Zhong Yao Cai 2017:40(12):2936–40. doi:10.13863/ j.issn1001-4454.2017.12.043.
18. Khasnavis S, Pahan K. Cinnamon treatment upregulates neuroprotective proteins Parkin and DJ-1 and protects dopaminergic neurons in a mouse model of Parkinson's disease. J Neuroimmune Pharmacol 2014:9(4):569–81. doi:10.1007/s11481 -014-9552-2.  19. Shaltiel-Karyo R, Davidi D, Frenkel-Pinter M, Ovadia M, Segal D, Gazit E. Differential inhibition of α-synuclein oligomeric and fibrillar assembly in Parkinson's disease model by cinnamon extract. Biochim Biophys Acta 2012:1820(10):1628–35. doi:10.1016/j.bbagen.2012.04.021.  20. Khasnavis S, Pahan K. Sodium benzoate, a metabolite of cinnamon and a food additive, upregulates neuroprotective Parkinson disease protein DJ-1 in astrocytes and neurons. J Neuroimmune Pharmacol 2012:7(2):424–35. doi:10.1007/s11481-011-9286-3.  21. Brahmachari S, Jana A, Pahan K. Sodium benzoate, a metabolite of cinnamon and a food additive, reduces microglial and astroglial inflammatory responses. J Immunol 2009:183(9):5917–27. doi:10.4049/jimmunol.0803336.  22. de Lau LM, Breteler MM. Epidemiology of Parkinson's disease. Lancet Neurol 2006:5(6):525–35. doi:10.1016/S1474-4422(06)70471-9.  23. Korean medicine pharmacology Compilation committee. Korean medicine pharmacology 4th ed. Seoul: Shinilbooks: 2015. p. 150–7.
24. Ranasinghe P, Pigera S, Premakumara GAS, Galappaththy P, Constantine GR, Katulanda P. Medicinal properties of 'true'cinnamon (Cinnamomum zeylanicum):a systematic review. BMC Complement Altern Med 2013:13(1):275doi:10.1186/1472-6882-13-275.
25. Neuberger JM, Schweitzer S, Rolland M, Burghard R. Effect of sodium benzoate in the treatment of atypical nonketotic hyperglycinaemia. J Inherit Metab Dis 2000:23(1):22–6. doi:10.1023/a:1005642728513.  26. Leonard JV, Morris AA. Urea cycle disorders. Semin Neonatol 2002:7(1):27–35. doi:10.1053/ siny.2001.0085.  29. Yoon MJ, Lee HH. The physiological function of PPARα. Biochemistry and Molecular Biology News 2004:24(1):22–31.
31. Choe JG. Research on the coumarin analysis in the cinnamon contained foods for standardization &specification. Korea Food &Drug Administration 2009:
|
|












