Ⅰ. 서 론
최근 우리나라에서는 서구화된 식습관 및 운동량 부족, 비만, 스트레스 등으로 인하여 각종 심혈관계 질환이 증가하고 있으며, 이와 가장 관련 있는 원인으로 알려진 고지혈증이 화두가 되고 있다1. 고지혈증이 지속될 경우 각종 심혈관계 및 뇌혈관질환 등 여러 가지 질환이 발생할 수 있으므로 예방 및 관리가 중요하다.
고지혈증은 최근에는 이상지질혈증(dyslipidemia)이라는 용어로 많이 불리고 있으며 여러 원인으로 발생될 수 있으나 고콜레스테롤혈증, 고중성지방혈증 및 저HDL 콜레스테롤혈증 이라는 공통적인 증상을 보이며 이들을 구성하는 지단백들이 심혈관질환을 유발하는 주요한 요인들로 알려져 있다2.
이상지질혈증에 대한 국내 2015년 이상지질혈증 치료지침에 따르면, 총콜레스테롤, LDL-콜레스테롤, HDL-콜레스테롤 및 중성지방에 대한 수치와 심혈관질환의 유무에 따라 statin계열의 HMG CoA 환원효소 억제제를 일차 권고하고 있고, non-statin 계열의 fibrate, ezetimibe, omega-3 fatty acid의 사용을 환자의 특성에 따라 각 제제들을 일차적으로 또는 statin과 병용투여 하도록 제안하였다3. 하지만, 최근의 관찰연구를 살펴보면, 일차적으로 다용하고 있는 statin의 경우 당뇨병 유병률을 증가시키며, 당뇨병 위험군 환자에 대한 statin 투여는 유의한 위험인자라고 보고된 바가 있어 약물의 사용에 있어서 한계점을 보이고 있다4.
한의학적 관점에서 이상지질혈증 개념은 肝의 疏泄機能 이상과 脾의 運化失調로 濕濁해진 穢濁之氣가 체내에 정체되면서 瘀血, 濕濁이 血脈에 발생하는 것으로5 설명된다. 이상지질혈증의 유발 원인을 濕이나 瘀血, 痰飮 등으로 변증하여 치료 하는 다양한 연구들이 시행되고 있다6-13. 또한 이상지질혈증 관련 한약재의 약리학적 접근이나 單方, 또는 여러 한약재의 복합처방을 연구에 적용하고 있다13-20.
이에 저자는 한의학적 처방의 항이상지질혈증 효과에 관한 국내 연구들21-25 중에서 茵蔯蒿, 鬱金, 山楂, 丹蔘으로 구성된 청혈플러스(Chunghyul Plus, 이하 CHP로 표기) 연구에 주목하였으며, 추가 약재를 가미하여 나오는 결과값을 실험적으로 규명하고자 하였다. 청혈플러스는 마우스 모델 실험 연구에서 항고지혈증 및 항산화 효능이 입증되었으며22, 임상에서도 다양한 환자의 지질 대사 지표 개선 증례들이 보고된 바 있다19. 추가 한약재로는 오가피를 주목하였는데, 오가피 추출물은 체내지질농도와 체내 산화 스트레스 정도를 조절함으로써 심혈관계 질환의 위험을 감소시킨다는 연구 결과가 있다26.
본 실험에서는 청혈플러스가 지질대사에 효능을 나타낸 연구 결과들27,28에 착안하여, 기존 청혈플러스에 오가피를 가미하여서 최근 이상지질혈증의 주된 요인으로 대두되고 있는 염증에 대해 어떠한 효능이 있을지 과학적으로 확인하고자 진행하였다. 또한 체내 산화 스트레스와 관련하여 DPPH radical 소거능, ABTS radical 소거능을 측정함으로써 항산화 효능을 평가하고자 하였다. 즉, 인간 혈관내피세포인 Human Umbilical Vein Endothelial Cells (HUVECs)에서 혈관 염증을 유도하는 세포부착인자, NF-κB 및 MAPKs 신호전달체계와 자유 라디칼에 대한 실험을 통하여, 이상지질혈증과 관련된 항염증 및 항산화 작용을 객관적으로 제시하고자 한다.
Ⅱ. 재료 및 방법
1. 재 료
1) 시료
본 실험에 사용한 오가피청혈플러스(Acanthopanax sessiliflorum Cheonghyeol plus 이하, ASCP로 표기)의 구성 약재들은 대전한약국에서 구입하여 사용하였으며, 한 첩의 내용 및 분량은 다음과 같다(Table 1).
2) 시 약
시약은 ASCP의 안정된 실험농도 및 대조군과 비교되는 효과를 측정하기 위하여 1,1–diphenyl-2- picryl-hydrazyl(DPPH : Sigma-Aldrich, U.S.A.), 2,2’-azinobis-(3-ethylbenzothiazoline-6-sulfonic acid)(ABTS : Sigma-Aldrich, U.S.A.), gallic acid (Sigma-Aldrich, U.S.A.), EGM™-2 endothelial cell growth medium-2 bullekitTM(Lonza, U.S.A.), gelatin solution(Sigma-Aldrich, U.S.A.), tumor necrosis factor-α human(TNF-α : Sigma-Aldrich, U.S.A.), trypan blue(Sigma-Aldrich, U.S.A.), trypsin-EDTA solution(Welgene, Korea), dulbecco’s phosphate buffered saline(D-PBS : Welgene, Korea), EZ-cytox(Daeilab, Korea), human MCP-1 ELISA kit(Komabiotech, Korea), human ICAM-1 ELISA kit(Komabiotech, Korea), human VCAM-1 ELISA kit(Komabiotech, Korea), total RNA prep kit(Intronbio, Korea), accupower cyclescript RT premix(Bioneer, Korea), SYBR Green(Qiagen, Germany), DEPC-DW(Bioneer, Korea), pierce™ BCA protein assay Kit(Thermo Fisher, U.S.A), RIPA lysis and extraction buffer (Thermo Fisher, U.S.A.), protease inhibitor cocktail (Sigma-Aldrich, U.S.A.), phosphatase inhibitor cocktail 2(Sigma-Aldrich, U.S.A.), phosphatase inhibitor cocktail 3(Sigma-Aldrich, U.S.A.), bovine serum albumin(BSA : Gendepot, U.S.A.), miracle-star™ western blot detection system(Intron Biotechnology, Korea), primary antibody(Cell Signaling, U.S.A.), secondary antibody(Jackson immunoresearch, U.S.A.) 등을 사용하였다.
3) 기 기
기기는 ASCP를 시료로 사용할 수 있는 상태가 되도록 알맞게 정제하고 또한 그 효능을 측정하기 위하여 rotary vacuum evaporator(EYELA FDU-540, Japan), freeze dryer(ilShinbiobase, Korea), CO2 incubator(Sanyo, Japan), clean bench(Vision scientific, Korea), vortex mixer(Vision scientific, Korea), autoclave(Sanyo, Japan), centrifuge(Vision scientific, Korea), ice-maker(Vision scientific, Korea), deep-freezer (Sanyo, Japan), plate shaker(Lab-Line, U.S.A.), microplate reader(Molecular Devices, U.S.A.), nanodrop (Thermo Fisher, U.S.A.), luminex(Millipore, U.S.A.), alpha cycler 1 PCRmax(PCRmax, U.K.) real time PCR(Qiagen, Germany), mini trans-Blot(Bio-RAD, U.S.A.), chemidoc fusion FX(Vilber Lourmat, France) 등을 사용하였다.
2. 방 법
1) 시료 추출
ASCP 1첩 분량(50 g)에 500 ml의 증류수를 넣어 100 ℃에서 3시간 동안 추출하였으며, 추출물을 여과지로 여과한 후, rotary vacuum evaporator를 통해 감압농축하고 freeze dryer를 사용하여 동결건조를 진행하여 7.96 g(수득률 : 15.92%)의 분말을 얻었으며, -20 ℃에 보관하면서 사용하였다.
2) 세포 배양
Human umbilical vein endothelial cell (HUVEC)은 0.2% gelatin solution으로 코팅된 plate에 EGM™-2 medium과 EGM™-2 singlequots™ kit로 혼합된 배지를 사용하여 5% CO2, 37 ℃ 조건이 유지되는 세포배양기에서 배양하였으며, 2-3일을 주기로 계대 배양하여 실험을 진행하였다
3) 세포생존율 측정
HUVEC을 48 well plate에 1×106 cells/well로 분주하여 24시간에 걸쳐 배양하였다. 24시간 후, ASCP를 50, 100, 200, 400 μg/ml의 농도로 처리하여 다시 24시간 동안 배양하였다. 배양 후 배양액 100 μl당 10 μl의 EZ-Cytox 용액을 첨가하여 세포배양기에서 30분 동안 반응시켰다. 반응 후 450 nm에서 흡광도의 변화를 측정하였으며 대조군에 대한 세포생존율을 백분율로 표시하였다.
4) DPPH radical 소거능 측정
ASCP의 최종 농도가 1, 10, 100, 1000 μg/ml의 농도로 될 수 있도록 희석시켰고, 에탄올에 용해시킨 0.2 mM DPPH 용액 150 μl 및 시료를 100 μl씩 혼합하여 37 ℃에서 30분 동안 반응시켰다. 반응 후 517 nm 파장에서의 흡광도를 측정하였다. 시료의 대조군은 증류수를 넣었으며, DPPH radical 소거능은 아래의 식을 따라 계산하였다.
소거능(%)=

5) ABTS radical 소거능 측정
ASCP의 최종 농도가 1, 10, 100, 1000 μg/ml의 농도로 될 수 있도록 희석시켰으며, ABTS 용액은 7.4 mM ABTS(2,2-azino-bis- (3-ethylbenzothiazoline -6-sulfonic acid))와 2.6 mM potassium persulphate 를 제조 후, 이를 암소에서 하루 동안 방치해 양이온 (ABTS+)이 형성된 다음 732 nm에서의 흡광도를 측정하여서 흡광도 값이 1.5 이하 값으로 나오도록 희석시켰다. 희석된 ABTS+ 용액 95 μl와 시료를 5 μl씩 혼합하여 실온에서 10분간 반응시킨 후에, 732 nm 파장에서 흡광도를 측정하였다. 시료의 대조군은 증류수를 넣었으며, ABTS radical 소거능은 아래의 식을 따라 계산하였다.
소거능(%)=

6) 단백질 발현량 측정
6 well plate에 HUVEC을 1×106 cells/well로 분주하여 24시간 동안 배양하였다. 배양 후 ASCP를 50, 100, 200 μg/ml의 농도로 처리하고 1시간 뒤, 10 ng/ml의 TNF-α를 추가하여 12시간 동안 배양하였다. 이때 대조군은 TNF-α를 추가하여 염증반응을 일으키기만 한 군으로, ASCP농도 처치를 않았다. 이 후, 1200 rpm에서 5분 동안 원심분리하여 얻은 세포를 D-PBS로 2회 세척하고 세포 pellet에 protease inhibitor cocktail Ⅰ, phosphatase inhibitor Ⅱ, Ⅲ가 포함된 RIPA buffer를 넣어 단백질을 추출하였다. 추출한 단백질은 BCA proein assay kit를 이용하여 정량하였으며, sample loading buffer와 섞어 95 ℃에서 5분간 반응시켜 준비하였다. 준비된 단백질은 10% acrylamide gel을 통해 SDS-PAGE하여 크기별로 분리하였으며, PVDF membrane에 이동시켰다. 단백질이 옮겨진 membrane을 3% BSA에 담가 상온에서 2시간 동안 반응시켰다. TBS-T buffer를 이용하여 세척하고 primary antibody를 넣어 4 ℃에서 16시간 동안 반응시켰다. 다시 3회 세척하고 secondary antibody를 넣어 상온에서 1시간 동안 반응시켰으며, 다시 세척하고 ECL solution을 통해 단백질을 발색시켰다. 이후, chemidoc fusion FX를 통해 단백질 발현량을 분석하였다.
7) 유전자 발현량 측정
(1) RNA 추출
6 well plate에 HUVEC을 1×106 cells/well로 분주하여 24시간 동안 배양하였다. 배양 후 ASCP를 50, 100, 200 μg/ml의 농도로 처리하고 1시간 뒤, 10 ng/ml의 TNF-α를 추가하여 12시간 동안 배양하였다. 이 후, 1200 rpm에서 5분간 원심분리하여 얻은 세포에 chloroform 200 μl와 easy blue 1 ml를 넣고 vortexing 한 후, 13000 rpm, 4 ℃에서 10분간 원심분리 하였다. 상층액 400 μl 및 binding buffer 400 μl를 실온에 1분 동안 반응시킨 후 반응액 700 μl를 column으로 주입하고 13000 rpm에서 30초 동안 원심분리하였다. Column 안에 washing buffer A를 700 μl 넣고 13000 rpm에서 30초 동안 원심분리한 후에, washing buffer B를 700 μl 넣어 동일하게 원심분리 하였다. Column 하단을 1.5 ml tube로 교체 후, column에 elution buffer를 30 μl 넣고 1분간 반응시킨 뒤 13000 rpm에서 1분 동안 원심분리하여 total RNA를 추출하였다.
(2) cDNA 합성
역전사(reverse transcription) 반응은 RT premix kit의 mixture(reaction buffer, RNase inhibitor, dNTPs mixture, stabilizer, oligo dT15 primer) total RNA를 1 μg 넣고 DEPC-DW을 최종 부피가 20 μl가 되도록 첨가하였다. 이 혼합액을 잘 섞은 후에, 45 ℃에서 60분 동안 반응시키고 first-strand cDNA를 합성하여, 95 ℃에서 5분 동안 방치하여 M-MLV RT를 불활성화시켜 합성이 완료된 cDNA를 polymerase chain reaction(PCR)에 사용하였다.
(3) 유전자 증폭
합성이 완료된 cDNA를 증폭시킬 수 있도록 real-time PCR을 시행하였으며, real-time 전용 tube에 cDNA 1 μl, 각 primer 2 μl, DEPC-DW 5 μl, SYBR Green 10 μl씩 넣어 95 ℃에서 2분 동안 반응시키고 다음 95 ℃에서 5초, 62.5 ℃에서 30초를 40회 반복하여 유전자를 증폭시켰다. 유전자 발현량은 대조군에 대한 비로 계산하였으며, 사용된 primer의 sequence는 Table 2와 같다.
Table 2
The Sequences of Primers
| Primer | F/R* | Sequences |
|---|---|---|
| MCP-1 | F | GCTCAGCCAGATGCAATCAA |
| R | CTTGGCCACAATGGTCTTGA | |
| ICAM-1 | F | TCTTCCTCGGCCTTCCCATA |
| R | AGGTACCATGGCCCCAAATG | |
| VCAM-1 | F | CCCTACCATTGAAGATACTGG |
| R | ATCTCTGGGGGCAACATTGAC | |
| β-actin | F | ATCGTGGGGCGCCCCAGGCACCA |
| R | GGGGTACTTCAGGGTGAGGA |
8) 바이오마커 생성량 측정
6 well plate에 HUVEC을 1×106 cells/well로 분주하여 24시간 동안 배양하였다. 배양 후 ASCP를 50, 100, 200 μg/ml의 농도로 처리하고 1시간 뒤, 10 ng/ml의 TNF-α를 추가하여 12시간 동안 배양하였다. 배양액을 1200 rpm에서 5분 동안 원심분리하여 얻은 상층액과 standard를 96 well plate로 100 μl씩 넣고 37 ℃에서 2시간 반응시켰다. 반응 후, washing buffer를 이용하여 4회 세척 작업을 한 뒤에, 100 μl의 detection antibody를 넣고 다시 37 ℃에서 2시간 반응시키고 세척하였다. 세척 후에, HRP conjugate를 100 μl씩 넣고 37 ℃에서 30분간 반응시켜 세척한 뒤 substrate reagent를 100 μl씩 넣어 37 ℃에서 15분간 반응시키고 100 μl의 stop solution을 추가하여 micro reader를 통해 450 nm에서의 흡광도를 측정하였으며, standard curve를 이용하여 절대 값으로 표시하였다.
Ⅲ. 실험 결과
1. 세포생존율
세포생존율을 측정한 결과, 대조군이 100.00±2.61%로 나타났을 때, ASCP 50, 100, 200, 400 μg/ml에서 각각 100.55±2.72%, 99.33±0.76%, 99.53±3.77%, 80.62± 3.05%로 400 μg/ml 이상의 농도에서 90% 이하의 세포생존율이 나타났다(Fig. 1).
Fig. 1
Cell viability of ASCP in HUVEC.
HUVEC were treated by 50, 100, 200, and 400 μg/ml of ASCP for 24 h. Treated cells were reacted by EZ-Cytox for 30 min and then absorbance were measured at 450 nm using micro plate reader. Cell viability were calculated as percentage relative to the control. The result were presented by the mean±S.D from three independent experiments.

2. DPPH radical 소거능
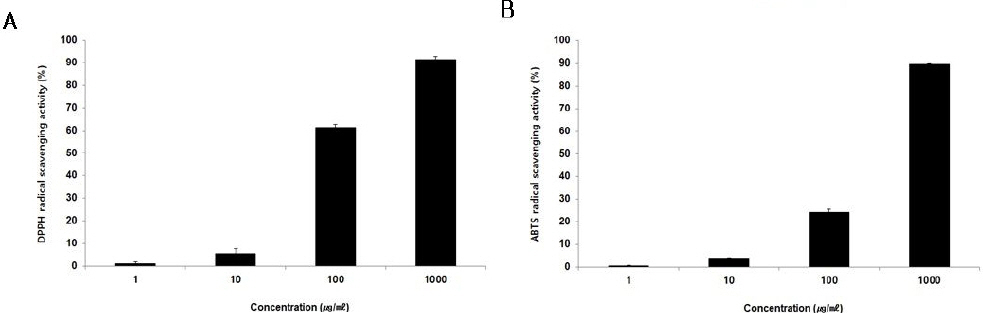
DPPH radical 소거능을 측정한 결과, ASCP 1, 10, 100, 1000 μg/ml 농도에서 각각 0.96±0.85%, 5.55± 2.19%, 61.29±1.50%, 91.35±1.44%로, DPPH radical 소거능의 농도 의존 적인 증가가 나타났다(Fig. 2A).
Fig. 2
DPPH radical scavenging activity (A) and ABTS radical scavenging activity (B) of ASCP.
ASCP was incubated at 1, 10, 100, and 1000 μg/ml with DPPH solution for 30 mins. DPPH radical scavenging activities were determined by measurement of absorbance at 517 nm and ABTS radical scavenging activities were determined by measurement of absorbance at 732 nm. The results were expressed as mean±S.D from three independent experiments.
3. ABTS radical 소거능
ABTS radical 소거능을 측정한 결과, ASCP 1, 10, 100, 1000 μg/ml 농도에서 각각 0.49±0.15%, 3.83± 0.19%, 24.25±1.28%, 89.76±0.19%로, ABTS radical 소거능의 농도 의존 적인 증가가 나타났다(Fig. 2B).
4. 단백질 발현량
1) NF-κB
NF-κB 단백질 발현량을 측정한 결과, 정상군에서 0.44±0.10, 대조군에서 1.00±0.05, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.80±0.02, 0.59±0.04, 0.45±0.05로 나타나 모든 농도에서 대조군에 비해 유의성 있는(** ; p<0.01, *** ; p<0.001) 감소가 나타났다(Fig. 3A).
Fig. 3
Effect of ASCP on NF-κB (A) and IκBα (B) protein expression level in HUVEC.
HUVEC were treated 50, 100, and 200 μg/ml of ASCP with 10 ng/ml TNF-α for 12 h. The total cell extracts were subjected to 10% SDS-PAGE and western blot analysis with the respective primary and secondary antibodies. The result were presented by the mean±S.D from three independent experiments (Significance of results, * ; p<0.05, ** ; p<0.01, *** ; p<0.001 compared to control).

2) IκBα
IκBα 단백질 발현량을 측정한 결과, 정상군에서 0.28±0.06, 대조군에서 1.00±0.08, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.80±0.04, 0.64±0.02, 0.54±0.03로 나타나 모든 농도에서 대조군에 비해 유의성 있는(* ; p<0.05, ** ; p<0.01, *** ; p<0.001) 감소가 나타났다(Fig. 3B).
3) ERK
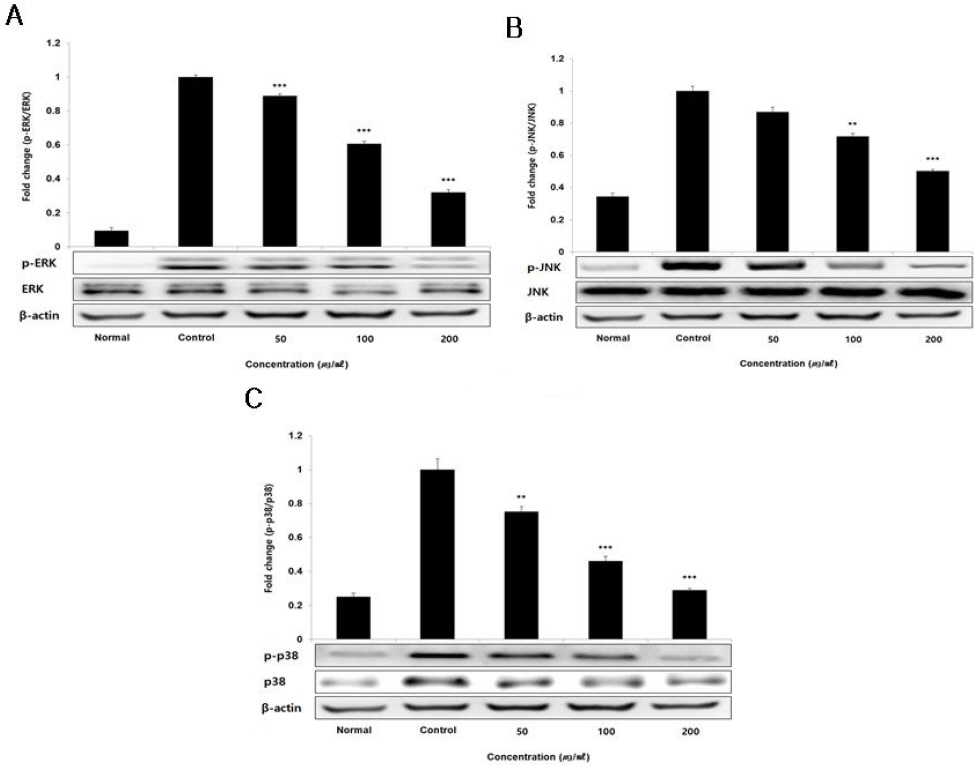
ERK 단백질 발현량을 측정한 결과, 정상군에서 0.09±0.02, 대조군에서 1.00±0.01, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.89±0.01, 0.61±0.01, 0.32±0.02로 나타나 모든 농도에서 대조군에 비해 유의성 있는(*** ; p<0.001) 감소가 나타났다(Fig. 4A).
Fig. 4
Effect of ASCP on ERK (A), JNK (B) and p38 (C) protein expression level in HUVEC.
HUVEC were treated 50, 100, and 200 μg/ml of ASCP with 10 ng/ml TNF-α for 12 h. The total cell extracts were subjected to 10% SDS-PAGE and western blot analysis with the respective primary and secondary antibodies. The results were presented by the mean±S.D from three independent experiments (Significance of results, ** ; p<0.01, *** ; p<0.001 compared to control).
4) JNK
JNK 단백질 발현량을 측정한 결과, 정상군에서 0.34±0.02, 대조군에서 1.00±0.03, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.87±0.03, 0.72±0.02, 0.50±0.01로 나타나 100 μg/ml 이상의 농도에서 대조군에 비해 유의성 있는(** ; p<0.01, *** ; p<0.001) 감소가 나타났다(Fig. 4B).
5) p38
p38 단백질 발현량을 측정한 결과, 정상군에서 0.25±0.02, 대조군에서 1.00±0.06, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.75±0.03, 0.46±0.03, 0.29±0.01로 나타나 모든 농도에서 대조군에 비해 유의성 있는(** ; p<0.01, *** ; p<0.001) 감소가 나타났다(Fig. 4C).
5. 유전자 발현량
1) MCP-1
MCP-1 유전자 발현량을 측정한 결과, 정상군에서 0.12±0.05, 대조군에서 1.00±0.05, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.97±0.03, 0.95±0.03, 0.67± 0.02로 나타나 200 μg/ml 이상의 농도에서 대조군에 비해 유의성 있는(*** ; p<0.001) 감소가 나타났다(Fig. 5A).
Fig. 5
Effect of ASCP on MCP-1 (A), ICAM-1 (B), VCAM-1 (C) mRNA expression level in HUVEC.
HUVEC were treated 50, 100, and 200 μg/ml of ASCP with 10 ng/ml TNF-α for 12 h. The mRNA expression level were measured using a quantitative real-time PCR (qRT-PCR). The results were presented by the mean±S.D from three independent experiments (Significance of results, * ; p<0.05, *** ; p<0.001 compared to control).

2) ICAM-1
ICAM-1 유전자 발현량을 측정한 결과, 정상군에서 0.11±0.03, 대조군에서 1.00±0.05, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.92±0.03, 0.75±0.03, 0.67± 0.02로 나타나 모든 농도에서 대조군에 비해 유의성 있는(* ; p<0.05, *** ; p<0.001) 감소가 나타났다(Fig. 5B).
3) VCAM-1
VCAM-1 유전자 발현량을 측정한 결과, 정상군에서 0.07±0.08, 대조군에서 1.00±0.04, ASCP 50, 100, 200 μg/ml 농도에서 각각 0.67±0.02, 0.20±0.04, 0.19±0.02로 나타나 모든 농도에서 대조군에 비해 유의성 있는(*** ; p<0.001) 감소가 나타났다(Fig. 5C).
6. 바이오마커 생성량
1) MCP-1
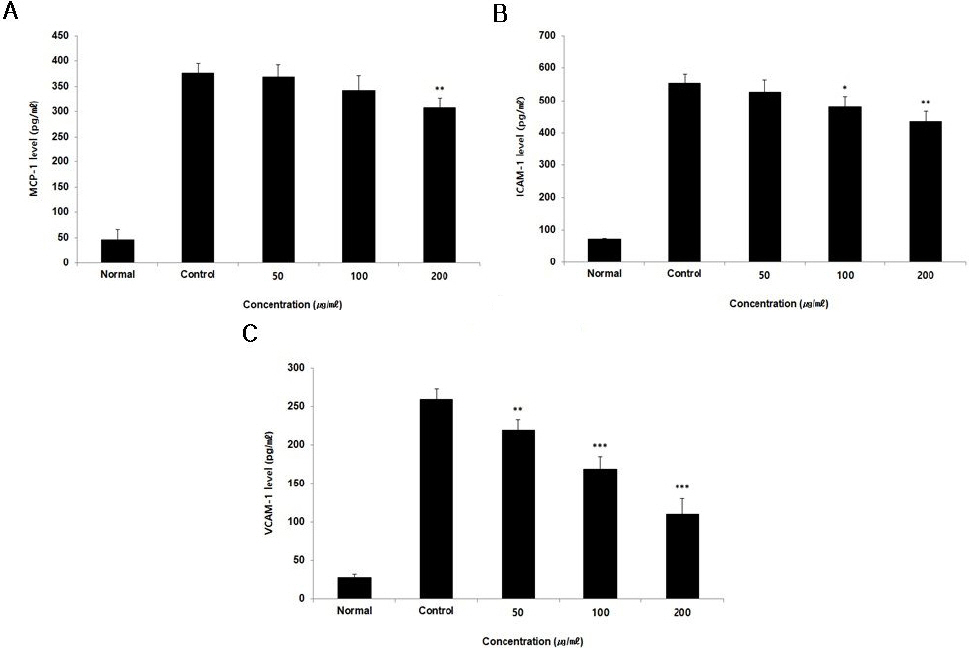
MCP-1 생성량을 측정한 결과, 정상군에서 46.17± 19.95 pg/ml, 대조군에서 376.20±19.26 pg/ml, ASCP 50, 100, 200 μg/ml 농도에서 각각 368.75±24.12 pg/ml, 342.50±28.95 pg/ml, 307.29±20.10 pg/ml로 200 μg/ml 이상의 농도에서 대조군에 비해 유의성 있는(** ; p<0.01) 감소가 나타났다(Fig. 6A).
Fig. 6
Effect of ASCP on MCP-1 (A), ICAM-1 (B), VCAM-1 (C) level in HUVEC.
HUVEC were treated 50, 100, and 200 μg/ml of ASCP with 10 ng/ml TNF-α for 12 h. MCP-1 level was measured using a ELISA kit. The results were presented by the mean±S.D from three independent experiments (Significance of results, * ; p<0.05, ** ; p<0.01, *** ; p<0.001 compared to control).
2) ICAM-1
ICAM-1 생성량을 측정한 결과, 정상군에서 71.95± 2.45 pg/ ml, 대조군에서 553.19±28.04 pg/ml, ASCP 50, 100, 200 μg/ml 농도에서 각각 527.23±37.30 pg/ml, 479.30±33.91 pg/ml, 435.73±30.83 pg/ml로 100 μg/ml 이상의 농도에서 대조군에 비해 유의성 있는(* ; p<0.05, ** ; p<0.01) 감소가 나타났다(Fig. 6B).
3) VCAM-1
VCAM-1 생성량을 측정한 결과, 정상군에서 28.04± 4.29 pg/ ml, 대조군에서 259.22±13.57 pg/ml, ASCP 50, 100, 200 μg/ml 농도에서 각각 219.87±13.51 pg/ml, 168.94±15.38 pg/ml, 110.26±19.83 pg/ml로 모든 농도에서 대조군에 비해 유의성 있는(** ; p<0.01, *** ; p<0.001) 감소가 나타났다(Fig. 6C).
Ⅳ. 고 찰
이상지질혈증이란 혈중에 총콜레스테롤, 중성지방, LDL콜레스테롤이 증가되어 있거나 HDL콜레스테롤이 감소되어 있는 상태를 말한다. 최근 몇 년간 미국을 포함한 여러 나라의 경우에는 이상지질혈증의 발생이 상대적으로 감소하고 있으나29, 우리나라의 경우는 오히려 증가되고 있다3. 2015년 우리나라 국민건강통계 보고서에 따르면, 만 30세 이상 성인에서의 고콜레스테롤혈증 유병률은 17.9%로 확인되는데, 이는 2014년 14.7%에 비해 3.2%가 증가된 것이며 2005년에 비해선 두 배 이상 증가한 수치이다30.
전 세계적으로 심혈관계 질환으로 인한 사망은 가장 많은 사망 원인으로, 우리나라에서는 암에 이어 두 번째로 주요한 사망원인으로 조사되고 있다31. Korean Heart Study(KHS)에 따르면 이상지질혈증은 고혈압, 당뇨병, 흡연과 함께 한국인의 심혈관계 질환에 큰 영향을 미치는 주요 위험인자로 고열량식, 고지방식 등 서구화된 식습관과 정적인 생활방식 등의 원인으로 인해 유병률이 꾸준히 증가하는 추세이다3,31.
통계학적인 증가 및 위험성으로 인해 이상지질혈증 치료에 관련하여 관심이 대두되는 가운데, 국내의 연구에서 이상지질혈증 관련 다양한 한약 추출물 연구가 이어지고 있으나, 본 저자는 실제 임상에서 활용 중이며 기존에 효과가 입증된 정량화 된 복합추출물에 대하여 추가 한약재를 가미한 결과값을 살펴보고 객관화하는 것이 필요하다고 판단하였다.
이상지질혈증은 한의학적 관점에서 보았을 때 肥甘厚味의 外因과 肝脾腎 기능실조의 內因의 의해 痰濕, 瘀血이 생겨 발병하며, 本虛標實한 상태이므로 滋補肝腎, 調理脾胃하여 扶正하고 活血化瘀, 利濕化痰하여 祛邪하는 치료법이 제안된다32.
선행된 문헌 자료와 연구 결과들을 토대로 한의학적으로 또는 약리학적으로도 항이상지질혈증 효능이 증명된 茵蔯, 山査, 鬱金, 丹蔘 네 가지 약재의 복합추출물인 청혈플러스는 여러 병원에서 임상적으로 환자들의 이상지질혈증에 적용하여 치료에 활용하고 있으며, statin계 약물과 병용했을 때 뿐만 아니라 단독요법 사용으로도 유의한 효과를 갖는다19. 또한 청혈플러스는 본 논문에서 사용한 지표인, 염증을 유도하는 세포부착인자 및 항산화 효능지표를 사용한 기존 연구22,27에서 그 효과가 입증되었으므로 이를 토대로 시행한 본 실험에서도 유의미할 것임을 알 수 있다.
본 실험에선 기존 청혈플러스에 오가피를 가미하여 효능을 알아보고자 하였으며, 구성 약재들은 五加皮, 茵蔯蒿, 鬱金, 山楂, 丹蔘으로 각각 동량으로 진행하였다. 각각의 효능을 살펴보면, 먼저 茵蔯蒿는 利水滲濕藥에 속하며 국화과에 속한 다년생 본초인 사철쑥과 비쑥의 전초를 건조한 것으로33, 간에 작용하여 황달을 치료하는 방면으로 많은 연구가 시행된 약제이며 최근 지질대사에 관련된 연구가 다수 진행되고 있다23. 鬱金은 活血祛瘀藥에 속하며 생강과에 속한 다년성 숙근 본초인 鬱金 Curcuma aromatica Salisb의 槐根을 건조한 것으로, 心, 肝, 膽經에 歸經하여 淸心凉血, 活血止痛, 行氣解鬱, 疏肝利膽하는 효능이 있다33. 鬱金은 고콜레스테롤 식이 흰 쥐 모델에서 항산화계를 활성화시켜 조직의 산화적 손상을 감소시켜 항산화 효능이 증명된 바 있다34. 山楂는 消食健胃, 行氣散瘀하는 효능으로 肉食積滯, 心腹刺痛, 疝氣疼痛 등의 증상을 개선시키며 강심, 혈압강하, 관상동맥확장작용이 있어 고지혈증 및 죽상동맥경화증 등에 사용한다33. 성 등의 연구에서는 산사 추출물은 지방세포 분화 억제 및 지방 분해 작용과 간 기능 개선 효과 있는 것으로 추정되며, 간 보호 기능성 물질로서 활용 가능성을 입증하였다35. 丹蔘은 活血祛瘀, 調經止痛, 凉血消癰하는 약물로 月經不調, 産後瘀滯 腹痛, 癥瘕積聚, 跌打損傷, 癰瘡腫毒 등 거의 모든 瘀血의 증상에 사용되며 최근에 와서는 肝脾腫大와 관상동맥경화성 심장병과 고혈압, 혈전폐쇄성 맥관염에 비교적 좋은 치료 효과가 있다고 알려져 있다33. 또한 죽상동맥경화모델 집토끼의 정맥에 단삼추출물을 주사하였을 때 심장 관상동맥이 확장되면서 혈류량이 증가하고 맥박수 또한 감소하여 단삼의 항이상지질혈증 효능을 확인한 바 있다36. 五加皮는 두릅나무과에 속한 낙엽관목인 오갈피나무로, 본초학상 祛風濕强筋骨藥에 속하며 肝, 腎經에 歸經하여 祛風濕, 補肝腎 하는 효능이 있다33. 오가피 추출물은 과산화지질함량, 혈청 지질 성분, 항산화능 및 항산화 효소 활성과의 상호작용에서, 고지방 섭취 시 생성되는 다량 유리기를 제거하기 위해 체내 지질 과산화물의 생성을 감소시켜 glutathione 함량을 증가시키면서 SOD, catalase, GST와 GSH-Px 활성이 증가하여 세포 내 유리활성기의 신속한 제거를 통해 유리기로부터 받는 세포손상을 억제하여 체내 항산화능을 높이는 효과가 있는 것으로 관찰된 바가 있어26 이상지질혈증에 효과가 보일 것으로 판단하고, 기존 청혈플러스에 가미를 진행하였다.
혈중 LDL-cholesterol은 혈관내피세포의 기질과 쉽게 결합하여 혈관 내막에 침윤된다. 침윤된 LDL-cholesterol이나 혈액의 염증 관련 인자들은 내피세포의 기능부전을 유발하고 내피세포를 활성화시켜 염증 유전자나 혈관 부착분자의 발현을 증가시킨다. 산화 LDL은 단핵구, T 세포, 대식세포 등의 활성화를 유발하면서 만성적인 염증 상태를 일으켜 혈관 내막으로 이동한 혈관평활근세포가 산화 변형된 지단백을 흡수하여 섬유판을 형성한다. 따라서 죽상동맥경화에서 가장 중요하다고 볼 수 있는 위험인자는 혈중 cholesterol의 상승이며, 이상지질혈증을 치료하는 것이 관상동맥질환의 발병률을 낮출 수 있음이 밝혀졌다. 체내에는 이러한 산화 작용을 최소화시키기 위한 것으로 항산화 효소계와 selenium, Vit C, Vit E 등의 항산화 영양소들이 있다37.
그러므로 이상지질혈증에 관한 연구에서는 대개 항산화, 항염증을 같이 진행하게 된다. 본 실험은 이상지질혈증에서의 ASCP의 효능을 입증하기 위해 약물이 HUVECs에서 혈관 염증을 유도하는 세포부착인자인 NF-κB 및 MAPKs 신호전달체계에 어떤 영향을 주는지 살펴보았다. HUVECs에서의 항산화 효능을 검증하기 위해선 세포 독성에 관한 세포생존율과 DPPH radical, ABTS radical 소거능을 측정하였다. 항염증 효능을 검증하기 위해 HUVECs에서 염증 단백질 합성에 관여하는 중요한 pathway인 NF-κB, IκBα와 MAPKs의 ERK, JNK, p38의 단백질 발현량을 측정하였으며, 세포부착인자인 MCP-1, ICAM-1, VCAM-1의 유전자발현량 및 바이오마커 생성량을 측정하였다.
본 연구에서 사용한 HUVECs는 각종 장기의 혈관의 안팎을 경계 짓는 구조물로 응고인자를 생성하고 염증 세포를 이동시키며 cytokine을 생성하거나, 혈관의 긴장상태를 결정하는 체내에서 중요한 생리적 기능을 가진 세포들이다38.
먼저 HUVEC 에서의 세포생존율을 살펴보았다. ASCP를 50, 100, 200, 400 μg/ml의 농도로 처리하여 배양 후 배양액 100 μl당 10 μl의 EZ-Cytox 용액을 첨가하여 세포배양기에서 30분 동안 반응시켰다. 측정한 결과 50, 100, 200, 400 μg/ml에서 각각 100.55±2.72%, 99.33±0.76%, 99.53±3.77%, 80.62±3.05%로 나타났다(Fig. 1). ASCP는 400 μg/ml 이상의 농도에서 대조군에 비해 유의미한 생존율 감소, 즉 세포독성을 나타낸 것으로 보아 실험이 주로 진행된 200μg/ml 이하에서는 세포독성에 안전한 것으로 사료된다.
ASCP의 항산화능을 검증하기 위해 DPPH, ABTS를 활용하여 HUVECs에서 ASCP의 radical 소거능을 측정하였다. 그 기전을 살펴보면, 산화스트레스에 의해 생체 내에서 생성된 자유라디칼로 인해 세포손상이 발생하며 그 결과로 노화 및 질병이 발생하게 되는데, DPPH(2,2-diphenyl-1- picrylhydrazyl)는 자유라디칼의 화합물로서 자유라디칼 소거능을 측정할 때 이용될 수 있다. 또한 방향족 화합물 및 아민류인 ascorbic acid 및 tocopherol 등의 환원능을 이용하여 항산화능을 측정할 때 사용되고 있다39. ABTS를 이용한 소거능 방법은 free radical이 실험체의 항산화력 물질에 의해 제거되었을 때 radical 특유의 색인 청록색이 탈색되는 것을 이용한 측정법으로, 장점은 chain breaking antioxidants와 hydrogen- donating antioxidants 모두를 측정할 수 있는 점, aqueous phase와 organic phase 모두 적용할 수 있으며 표준물질을 사용함으로써 추출물간 상대비교가 가능하다는 점이다40. 각 농도에 따른 소거활성능을 조사하기 위해 ASCP의 최종 농도가 1, 10, 100, 1000 μg/ml의 농도로 될 수 있도록 희석시켰으며, DPPH, ABTS radical 소거능 실험에서 모두 농도 의존적으로 증가시키는 결과를 보였다(Fig 2).
ASCP의 항염증을 검증하기 위해 NF-κB 및 MAPKs 신호전달체계에서 TNF-α를 추가하여 염증반응을 일으킨 후의 단백질 발현량을 측정하였다. 핵 전사 인자인 nuclear factor-κB(NF-κB)는 염증을 조절하는 역할을 하는데, 다양한 pro-inflammatory cytokine 및 cyclooxygenase-2(COX-2), inducible nitric oxide synthase(iNOS)의 전사를 유도함으로써 interleukin(IL)-1β, IL-6, tumor necrosis factor (TNF)-α 및 prostaglandin E2(PGE2)와 nitric oxide (NO)의 분비를 증가시킨다40. NF-κB는 유비쿼터스 전사 인자 복합체로, IκB kinase에 의해 촉매되는 IκBα가 인산화 과정을 거친 다음 IκBα가 분리될 때에 활성화된다42. 활성화된 NF-κB는 세포핵으로 이동하고 결국 몇몇의 염증 매개체를 생성한다43. 전형적인 NF-κB의 활성화 경로는 IKKβ-의존성 IκB 분해에 의해 NF-κB를 억제하고 있는 IκB 활성을 조절하는 것이다44. MAPK(mitogen-activated protein kinase)는 ERK(extracellular signal-regulated kinase), p38, JNK(c-Jun N-terminal kinases)의 단백질을 포함하는 개념으로, lipopolysaccharide(LPS) 등 다양한 자극을 통해 활성화되면 핵내 전사인자로서 염증 반응이 일어날 때 중요한 역할을 하게 된다45. ASCP를 50, 100, 200 μg/ml의 농도로 처리하고 10 ng/ml의 TNF-α를 추가하여 배양 후 단백질을 추출한 결과, NF-κB(Fig. 3A), IκBα(Fig. 3B), ERK(Fig. 4A), p38(Fig. 4C) 단백질 발현량에서 ASCP는 모든 농도에서 대조군에 비해 유의성 있는 감소를 보였다. JNK 단백질 발현량에서 ASCP는 100 μg/ml 이상의 농도에서 대조군에 대해 유의한 감소를 보였다(Fig 4B).
Chemokine은 염증반응 및 백혈구 유주의 주요한 역할을 하는 작은 단백질로, 혈관신생을 매개하여 종양성장이나 전이에 관여한다. 이상지질혈증과 관련하여, 동맥경화와 같은 혈관병변이 발생할 때도 chemokine이 매개하는데, MCP-1은 혈압에 의해 손상된 혈관평활근에 찌꺼기가 쌓이도록 매개하며, 이는 콜레스테롤이나 단핵구의 침착을 유발한다46. ICAM-1은 분자량 90-120 kD의 당단백으로 5개의 면역글로불린 도메인을 포함하는 것이며, 혈관 내피세포, 상피세포, 림프구 등 여러 종류의 세포들에 분포한다. 또한 TNF-α, IL-1, γ-interferon 등의 cytokine에 의해 자극을 받을 때 발현이 증가하며, 단핵구, 중성구, 림프구 등에 분포하는 β2 integrin 중 lymphocyte function-associated antigen-1 (LFA-1)의 리간드로 작용한다47,48. VCAM-1은 110 kD인 당단백이며 6개의 면역 글로불린 도메인을 포함하고 있고, 혈관 내피세포에서 처음 클로닝 되었다49. 이것은 cytokine의 자극으로 발현이 증가하며, very late antigen-4(VLA-4)의 리간드로서 α4β1 integrin과의 상호작용을 통하여 단핵백혈구를 염증이 발생된 곳으로 이동되도록 유도하는 역할을 하는 것으로 알려져 있다50. 이들 immunoglobulin superfamily와 integrin이 서로 리간드와 수용체로 작용하면서 혈관 내피세포에 부착된 염증세포를 고정시키는 역할을 하는 것이다. 본 연구에선 이를 바탕으로, Quantitative real-time polychain reaction (qRT-PCR)법을 이용하여 ASCP를 50, 100, 200(μg/ml)으로 처리하여 유전자 발현량을 조사하였다. MCP-1 mRNA 발현량은 ASCP 200μg/ml 이상의 농도에서 대조군에 비하여 유의성 있는 감소가 나타났다 (Fig. 5A). ICAM-1(Fig. 5B), VCAM-1(Fig. 5C) mRNA 발현량은 모든 ASCP 농도에서 대조군에 비해 유의성 있는 감소가 나타났다. ASCP를 50, 100, 200(μg/ml)으로 처리한 바이오마커 생성량에서는 MCP-1(Fig. 6A)은 200μg/ml 이상의 농도에서, ICAM-1(Fig. 6B)은 ASCP 100μg/ml 이상의 농도에서 대조군에 비해 유의한 감소가 나타났고, VCAM-1의 생성량은 ASCP 모든 농도에서 대조군에 비해 유의한 감소를 보였다(Fig. 6C).
이상의 결과들을 종합해 보면, ASCP는 DPPH 및 ABTS radical 소거능을 농도 의존적으로 증가시킴으로써 항산화효능이 규명되었으며, 염증 조절인자인 NF-κB 및 MAPKs 신호전달체계에서 유의성 있는 감소를 보여 항염증효능이 규명되었다. 또한 염증성 chemokine인 MCP-1 및 부착인자(ICAM-1, VCAM-1)의 유전자 발현량과 바이오마커가 유의하게 감소하여 항염증효능이 규명되었다.
그러므로 ASCP는 이상지질혈증으로 인한 염증반응과 이로써 발생하는 죽상동맥경화증과 여러 심뇌혈관계질환의 예방과 치료에 유효할 것으로 생각된다. 다만, 본 실험에서는 세포 실험만을 다루어 혈중의 cholesterol level은 측정되지 않았다는 한계점이 있다. 따라서 향후 in vivo실험 및 동물 실험을 통해 직접적인 평가를 시행한 추가 연구가 필요할 것으로 사료된다.
Ⅴ. 결 론
오가피청혈플러스(ASCP)의 이상지질혈증 관련 항산화 및 항염증 효능을 평가하기 위하여 인간 탯줄 정맥 내피 세포(HUVEC)를 통해 DPPH, ABTS radical 소거능, NF-κB 및 MAPKs 신호전달체계의 단백질 발현량, MCP-1 및 부착인자(ICAM-1, VCAM-1)의 유전자 발현량과 바이오마커를 확인한 결과 다음과 같은 결론을 얻었다.
1. ASCP는 HUVEC에서 DPPH, ABTS radical 소거능을 농도 의존적으로 증가시킨다.
2. ASCP는 HUVEC에서 NF-κB, IκBα, ERK, p38 단백질 발현량에서 모든 농도에서 대조군에 비해 유의하게 감소시켰으며, JNK 단백질 발현량에서는 100 μg/ml 이상 농도에서 대조군에 비해 유의하게 감소시켰다.
3. ASCP는 HUVEC에서 MCP-1 mRNA 발현량을 200 μg/ml 이상의 농도에서 대조군에 비해 유의하게 감소시켰으며, ICAM-1, VCAM-1 mRNA 발현량을 모든 농도에서 대조군에 비해 유의하게 감소시켰다. MCP-1 바이오마커 생성량을 200 μg/ml 이상의 농도에서, ICAM-1 바이오마커 생성량을 100 μg/ml 이상의 농도에서 대조군에 비해 유의하게 감소시켰으며, VCAM-1 바이오마커 생성량을 모든 농도에서 유의하게 감소시켰다.
이상의 결과로 볼 때, ASCP는 항산화 및 항염증효과가 있어 항이상지질혈증 효능이 있음을 규명하였다. 이를 바탕으로 이상지질혈증으로 인한 죽상동맥경화증 및 심⋅뇌혈관질환의 예방 및 치료약으로서 ASCP의 활용을 기대하는 바이다.











