중국 및 한국 Database에서의 위식도 역류질환에 대한 반하사심탕의 효과에 대한 최근 10년간의 연구경향
Abstract
Objectives:
The purpose of this research is to examine the recent clinical research trends on the efficiency of traditional herb medicine (THM) on gastroesophageal reflux disease (GERD), and to provide clinical evidence of herbal medicine Banhasasin-tang or Banxiexin decoction by using a systemic review and meta-analysis of randomized trials (RCTs).
Methods:
In this study, randomized controlled trials (RCTs) were included that verified effects of traditional herbal medicine (THM), including a Banxia-xiexin-tang decoction, as a treatment for GERD. A study of the literature in Chinese and Korean databases was performed for papers published from January 1, 2010, to January 1, 2020. The selected literature was assessed by Cochrane’s risk of bias (RoB).
Results:
A total of 90 RCTs met the inclusion criteria. Except for four RCT studies, all studies identified the effect of a Banxia-xiexin-tang decoction in the treatment of GERD. The effectiveness of treatment was significantly higher in the intervention group than in the control group, as shown through various evaluation indicators, including the reflux disease diagnostic questionnaire (RDQ). Adverse effects were reported in 22 articles (24.44%).
Conclusions:
Treatment with Banhasasin-tang, or a Banxia-xiexin-tang decoction, was found to be effective in treating GERD. However, due to the low quality of available studies, the significance of this conclusion is somewhat limited. This study could serve as a foundation for further clinical studies on the development of diagnosis and treatment methods for GERD based on Korean medicine.
Keywords: gastroesophageal reflux disease, GERD, Banxiexin decoction, Banhasasin-tang, traditional herb medicine, THM
I. 서 론
위식도 역류질환(gastoesophageal reflux disease, GERD)은 위 내용물이 식도로 역류하여 불편한 증상을 유발하거나, 이로 인해 합병증을 유발하는 질환이다. ‘불편한 증상’은 위식도 역류와 관련된 증상들이 삶의 질에 나쁜 영향을 주는 경우를 의미한다. 가슴쓰림(heartburn)이나 위산역류(acid reflux)가 전형적으로 나타나며, 이는 역류가 지나치게 많이 일어나 식도로 넘어온 위산과 위 내용물이 식도점막을 자극하여 아픈 증상을 유발하는 것이며, 역류된 위산이 식도를 지나 인후부까지 넘어와 후두염이나, 천식, 만성 기침 등의 합병증을 유발하기도 한다. GERD의 주요 합병증은 협착증(stricture), Barrett’s oesophagus{장상피화생 및 이형성증(intestinal metaplasia and dysplasia)}, 식도 선암(oesophageal adenocarcinoma) 등이 있으며, 식도에 임상적으로 유의한 출혈 혹은 천공(perforation)이 드물게 발생하기도 한다 1. GERD는 내시경 검사상 미란(erosion)의 유무에 따라 미란성식도염과비미란성 식도질환으로 나눌 수 있으며, 각각의 역류증상의 여부에 따라 전자는 역류성식도염{미란성 역류질환(erosive reflux disease, ERD)}과 역류증상이 없는 미란성식도염, 후자는 비미란성 역류질환{비미란성 역류질환(non-erosive reflux disease, NERD)}과 역류증상이 없는 비미란성 식도질환으로 나눌 수 있다 2,3. 발병 원인으로 하부식도조임근(lower esophageal spincter, LES)의 이완과 낮은 압력 등에 의한다고 알려져 있다 4.일부 환자에서 생활습과 개선만으로 증상이 호전되기도 하지만, GERD호전과 악화가 반복되는 만성적인 질환이므로 대부분 생활요법과 위산 분비 억제 치료의 병행이 필요하며, 약물치료 중단 후에는 재발률이 높아 재발방지를 위해 장기간 치료가 이루어지기도 한다 5. 약물치료 시 산 분비를 억제할 수 있는 히스타민2 수용체차단제(H 2receptor antagonist)가 주로 사용되며, 위장운동촉진제의 약제를 통한 하부식도의 압력과 위배출을 증가시키거나, 프로톤 펌프억제제(proton pump inhibitor, PPI)로 위내 산도를 pH4 이상으로 유지하는 방법을 대표적으로 사용한다 2. 이러한 약물치료요법 이외에 생활습관개선, 외과 요법 등의 치료요법이 있다. 내과적 치료에 실패한 경우나 만성적으로 PPI를 사용해야 하는 젊은 환자의 경우에는 복강경을 이용한 위저추벽성형술(fundoplication)을 시행하기도 한다 3. 위식도 역류질환은 한의학적으로 “呑酸”, “吐酸”, “噎膈”, “胸痺” 등의 범주에 해당되고, 肝胃不和, 痰濕鬱阻, 胃氣虛逆 등으로 辨證하여 각각 舒肝和胃降逆, 淸化濕痰 和胃降逆, 健脾胃降逆氣의 治法을 활용하며 4, 四逆散合小半夏湯加減, 溫膽湯加味, 香砂六君子湯合 旋覆代赭湯 등의 처방을 辨證에 따라 사용한다 6. 半夏瀉心湯은 ≪傷寒論≫의 <太陽病脈證辨治下>편 149번 조문에 최초로 수록되어 結胸, 心下滿, 痞의 증상이 진단의 핵심이며 7, ≪金櫃要略≫에도 ‘嘔而腸鳴 心下痞者 半夏瀉心湯主之’로 기록되어 있으며 8, 이는 半夏瀉心湯의 증상이 心下痞滿不痛, 乾嘔, 嘔吐, 腸鳴下痢를 치료하는 대표적인 處方으로 인식되는 주요 문헌적인 근거가 된다 9, 임상에서는 기능성 소화불량증 뿐 만 아니라 GERD에도 적극적으로 활용되고 있으며, 급만성 위장관 카타르, 발효성 설사, 급성 위장관염 등에 많이 사용되고 있다 10. 국내 GERD의 한의치료 중 한약치료 관련실험연구는半夏瀉心湯 11이외에도 二陳湯加味方 12-16관련연구가 5편으로 가장 많이 있으며, 이외에도 金銀花추출물 17과 吳茱萸 물 추출물 18,19, 黃連 추출물 20,茵蔯蒿 추출물 21, 楡根皮 추출물 22, 海螵蛸瓦楞子牡蠣와 Esomeprazole의 치료효과에 대한 비교 연구 23,半夏生薑小半夏湯 24, 떫은감 陳皮 복합 25, 大黃 甘草 복합 26, 左金丸 27 등의 약재 또는 처방 추출물에 대한 다양한 실험연구들이 있었다. GERD 관련 체계적 문헌고찰 연구로, 역류성식도염에서 二陳湯加味方의 효과에 대한 문헌적 고찰 28과 CAJ검색을 통한 침구치료의 임상연구 동향에 대한 체계적 문헌 고찰이 있었다 2. 임상연구는 대부분 증례보고형 형식에 그치고 있는 실정이다. 半夏瀉心湯에 대한 국내연구는 관련 임상연구 동향분석 또는 체계적 문헌 고찰 연구로 Jeon 등 29의 半夏瀉心湯에 대한 임상연구분석과, 항암화학요법으로 인한 증상에 대한 체계적 문헌 고찰 연구가 있었다 30. 半夏瀉心湯은 기능성 소화불량증 31,32 및 소화성 궤양 33 등의 GERD을 포함한 다양한 소화기계 질환에 증상 개선에 유용한 것으로 여러 관련 임상 연구들을 통해 알려져 있다. 급성십이지장 손상에 대한 半夏瀉心湯의 방어효과 34, 위궤양에 대한 半夏瀉心湯과 Cimetidine의 병용투여 35 등의 GERD외에 소화기계질환 및 증상에 대한 실험연구들이 있었으며, 또한CINV(Chemotherapy-Induced Nausea and Vomiting) 36에 대한 혈맥주입 약침과 같이 항암요법으로 인해 발생하는 오심, 구토, 및 구내염 29,30 등의 증상에 효과가 있을 뿐만 아니라,心, 肝, 脾, 腎臟 등의 주요장기에 대한 항암제의 독성에 대해 방어 효과가 있음을 밝히기도 하였다 37-40. 중국에서는 환자-대조군 연구를 통한 한약 또는 중서 결합치료와 양약 간의 치료율을 연구들 41이나 체계적 문헌 고찰 또한 다수 존재하나, 국내에서는 GERD에 대한 半夏瀉心湯의 빈번한 임상 활용에도 불구하고, 그 효능이 체계적으로 검토된 문헌은 2011년 발표된 Choi 41 등의 논문이외에는 드문 실정이다. 이에 따라 중국 및 한국에서의 GERD에 半夏瀉心湯을 이용한 한약치료에 대한 동향을 살펴보고 향후 한약 치료 연구의 객관적 근거를 마련하는데 바탕이 되기 위하여 중국에서 이루어지고 있는 GERD에 대한 임상연구의 기초자료를 제시하고자 CNKI(Chinese National Knowledge Infrastructure Database) 검색을 통한 최근 10년간 발표된 임상 논문을 분석하여, 체계적 문헌 고찰 및 메타연구를 진행하였다.
II. 연구대상 및 방법
1. 문헌검색 전략 및 선정방법
논문 검색은 대표적 중국논문 검색 데이터베이스인 중국학술정보원 CNKI(Chinese National Knowledge Infrastructure Database, including China Academic Journals Full-text Database(CJFD), China Doctoral Dissertations and Masters’ Theses Full-text Database (CDMD)와 국내 데이터베이스인 국가과학기술정보센터(National Discovery for Science Leaders, NDSL), 한국교육학술정보원(Research Information Sharing Service, RISS), 전통의학 정보 포털(Oriental Medicine Advanced Searching Integrated System, OASIS), 한국학술정보(Korean studies Information Service System, KISS)의 검색원에서 2020년 3월 4일 검색을 시행하였다. 검색어는 “胃食管返流病”, “食管反流病”, “半夏泻心”의 조합을 사용하였으며( Table 1), GERD의 최근 10년간 경향을 알아보기 위해 2010년 1월부터 2020년 1월까지 발간된 논문전체를 대상으로 선별하였다.
Table 1
Search Strategy on CNKI (CJFD, CDMD)
|
검색어: 2010-2020. 중영문혼합검색 |
|
((SU=GERD+“gastroesophageal reflux disease"+胃食管返流病+胃食道逆流症+胃食道逆流性疾病+胃食管反流病+胃食道逆流疾病+“gastric acid reflux"+“Acid Reflux Gastric"+“reflux gastric acid"+“gastric acid reflux disease"+“gastro-esophageal reflux"+“gastro esophageal reflux"+“reflux gastro-esophageal"+“gastroesophageal reflux disease"+“relux gastroesophageal"+“esophageal reflux"+“gastro-oesophageal reflux"+“gastro oesophageal reflux"+“reflux gastro-oesophageal"+胃食管反流+胃酸反流+胃酸倒流+胃酸反流病+胃食道逆流+胃食管反流+胃酸逆流+“esophagitides peptic"+“esophagitis reflux"+“peptic esophagitides"+“peptic esophagitis"+“reflux esophagitides"+“reflux esophagitis"+反流性食道炎+反流性食管炎+返流性食管炎+食管炎+逆流性食道炎+消化性食管炎)OR(TI=GERD+“gastroesophageal reflux disease"+胃食管返流病+胃食道逆流症+胃食道逆流性疾病+胃食管反流病+胃食道逆流疾病+“gastric acid reflux"+“Acid Reflux Gastric"+“reflux gastric acid"+“gastric acid reflux disease"+“gastro-esophageal reflux"+“gastro esophageal reflux"+“reflux gastro-esophageal"+“gastroesophageal reflux disease"+“relux gastroesophageal"+“esophageal reflux"+“gastro-oesophageal reflux"+“gastro oesophageal reflux"+“reflux gastro-oesophageal"+胃食管反流+胃酸反流+胃酸倒流+胃酸反流病+胃食道逆流+胃食管反流+胃酸逆流+“esophagitides peptic"+“esophagitis reflux"+“peptic esophagitides"+“peptic esophagitis"+“reflux esophagitides"+“reflux esophagitis"+反流性食道炎+反流性食管炎+返流性食管炎+食管炎+逆流性食道炎+消化性食管炎)OR(AB=GERD+“gastroesophageal reflux disease"+胃食管返流病+胃食道逆流症+胃食道逆流性疾病+胃食管反流病+胃食道逆流疾病+“gastric acid reflux"+“Acid Reflux Gastric"+“reflux gastric acid"+“gastric acid reflux disease"+“gastro-esophageal reflux"+“gastro esophageal reflux"+“reflux gastro-esophageal"+“gastroesophageal reflux disease"+“relux gastroesophageal"+“esophageal reflux"+“gastro-oesophageal reflux"+“gastro oesophageal reflux"+“reflux gastro-oesophageal"+胃食管反流+胃酸反流+胃酸倒流+胃酸反流病+胃食道逆流+胃食管反流+胃酸逆流+“esophagitides peptic"+“esophagitis reflux"+“peptic esophagitides"+“peptic esophagitis"+“reflux esophagitides"+“reflux esophagitis"+反流性食道炎+反流性食管炎+返流性食管炎+食管炎+逆流性食道炎+消化性食管炎))AND((SU=半夏泻心+“banxia xiexin"+“ban xia xie xin"+banxiaxiexin+pinelliae+“pinelliae tuber"+“pinellia heart draining")OR(TI=半夏泻心+“banxia xiexin"+“ban xia xie xin"+banxiaxiexin+pinelliae+“pinelliae tuber"+“pinellia heart draining")OR(AB=半夏泻心+“banxia xiexin"+“ban xia xie xin"+banxiaxiexin+pinelliae+“pinelliae tuber"+“pinellia heart draining"))AND((SU=对照+随机+randomised+randomized)OR(TI=对照+随机+randomised +randomized)OR(AB=对照+随机+randomised+randomized)) |
2. 선정 및 배제기준
검색된 논문에서 사람을 대상으로 한 무작위 대조군 연구(randomized controlled trial, RCT)를 포함하고, 단일군 전후연구, 종설논문, 단행본, 인터넷자료 혹은 비 출판 자료는 제외하였다. 대상자는 NERD와 ERD의 구분 없이 위식도 역류질환(GERD)을 포함하는 것을 우선시하였으며, 위식도 역류질환으로 인한 기침(gastric cough, gastroesophageal reflux-related chronic cough, gastroesophageal reflux cough, GERC) 또는 연하곤란과 항암요법치료 이후 발생한 GERD 환자 등의 연구는 제외하였다.
半夏瀉心湯을 중심으로 한 한약치료의 GERD에 대한 임상효과를 알아보는 것이 목적이었으므로 한약을 중재로 사용하여 GERD 환자를 치료한 연구를 포함하였다. 즉, 한약 단독군과 양약 단독군을 비교한 연구, 한약과 양약 병용군과 양약 단독군을 비교한 연구를 대상으로 선정하였다. 다만 탕약, 환(丸), 과립(顆粒)형태 만을 연구대상으로 하고, 침, 뜸 또는 기타생활 및 운동 치료가 병용된 연구는 연구대상에서 제외되었다.
한약치료의 중재에서 선정 및 배제기준은 辛開苦降法과 같이 논문에 치료법으로 기재(stated as a treatment in a paper, 이하 ST)되었으나 처방구성은 半夏瀉心湯의 기본방에 약재를 가감한 처방을 중재로 사용한 Sun 42-45 등의 연구는 연구대상에 포함하였다. 半夏厚朴湯加味, 柴胡瀉心湯. 旋覆代赭湯合左金丸 등의 처방을 중재로 사용한 연구와, 和降法代表方, 疏肝和胃降逆湯, 淸胃降逆方 등을 사용한 연구는 半夏, 黃芩, 人蔘, 甘草, 黃連, 大棗, 生薑, 乾薑을 半夏瀉心湯의 기본방으로 全載하였을때, 기본 처방구성이 누락되어 있어 제외하였다. 또한, 半夏瀉心湯에 四逆散, 小柴胡湯 등을 합방한 처방을 중재로 사용한 연구는 半夏瀉心湯의 단독 효과를 확인하기 어려워 제외하였다. 한약과 양약 병용치료군에서 사용한 양약과 양약단독 치료군의 대조군에서 사용한 양약의 종류가 다른 연구 또한 제외하였다.
3. 문헌선택 및 자료분석
두 명의 독립된 연구자(JYJ, KYJ)가 진행하였으며, 검색된 문헌의 서지 정보를 서지관리 프로그램인 Endnote X8을 활용하여 정리 및 관리하여 각자 검색 결과를 상호 비교하여 누락되는 연구가 없게끔 하였다. 중복제거 기능을 이용하여 검색된 논문들 중 중복되는 논문을 제거하였다. 1차로 제목(title)과 초록(abstract)을 통해 연구 대상, 중재 및 무작위 대조군 연구 구조와 관련 없는 논문을 배제하고, 2차로 선정된 논문에 대해 원문을 다운로드 하여 추가 정보 확인 후, 선정기준에 부합하지 않는 논문들은 제외하였다. 또한, 두 명의 연구자는 독립으로 최종 선정된 연구들의 연구 설계, 연구 대상자, 진단도구, 평가지표, 주요결과 등에 대해 각각 분석하였다. 추출된 자료는 서지학 정보, GERD 진단기준, 중재, 결과변수, 비뚤림위험 등의 항목에 따라 정보를 추출하였다. 의견이 불일치할 경우 2명의 연구자 간의 합의 및 제 3의 연구자(HSH)의 자문을 구하여 최종 포함 여부를 결정하였다.
4. 문헌의 질 평가
본 연구에서는 코크란 비뚤림위험도구(Cochrane’s Risk of Bias, 이하 RoB)를 이용한 비뚤림위험 측정을 시행하고, 메타분석에 포함하였다. 독립된 2명의 연구자(JYJ, KYJ)가 세부 항목을 평가하였으며 의견이 불일치할 경우 2명의 연구자 간의 합의 및 제 3의 연구자(HSH)의 자문을 구하여 토의를 거쳐 합의하였다. RoB는 체크리스트 방식과 영역평가 방식의 결합된 형태를 갖추고 있으며, 문항을 단순화한 반면 같은 문항에 대한 주관적이거나 자의적인 답변의 가능성을 최소화하고 평가자의 연구방법론에 대한 이해도와 숙련도에 따른 평가 결과의 변동을 최소화하기 한 노력을 기울여 만들어진 도구이다. 각 문항에 대하여 문헌의 본문에 어떠한 내용이 있는지에 따라 비뚤림 위험이 “높음(high risk of bias)”, “낮음(low risk of bias)” 혹은 “불확실(uncertain)”로 정한다. 무작위 대조 임상연구에서 비뚤림 종류는 선택 비뚤림, 실행 비뚤림, 결과 확인 비뚤림, 탈락 비뚤림, 보고 비뚤림의 다섯 가지로 구성되어 있으며, RoB도구는 무작위 배정순서 생성, 배정순서 은폐, 참여자와 연구자의 가림, 결과 평가자의 가림, 불완전한 결과의 처리, 선택 결과 보고, 잠재적인 다른 비뚤림 위험의 7가지 영역으로 평가한다 46,47.
5. 요약 측정치 및 자료합성
결과 합성은 Review Manager(RevMan) 5.3을 이용하였다. 이분형 자료의 경우 상대위험도(Risk ratio, RR)와 양측 95% 신뢰구간(confidence interval, CIs)을 이용하여 표시하였고, 연속형 자료의 경우 평균차를(mean difference, MD) 95% 신뢰구간(CIs)과 함께 표시하였다.
정량 분석이 이루어지는 메타분석에서는 요약 자료(처리효과에 한 측정값 및 해당 신뢰구간)의 크기 차이에 의해 통계 이질성을 가진다. 특히, 한의학은 같은 질병과 증상에 대해서도 한의학적 변증에 따라 한약을 처방하는 것이 특징이자 장점이며, 본 연구는 GERD에 대한 半夏瀉心湯의 전반의 효과를 검증하기 위하였으나, 합방 또는 가감, 유사처방 등의 다양한 종류의 한약이 포함되었으므로 각 연구간의 높은 이질성은 불가피하다. 이는 엄격한 통제 하에 시행되는 비교연구에 있어서는 결정적인 단점으로 작용한다.
연구간의 통계 이질성의 존재여부 평가는 Chi 2 검정 혹은 Higgin’s I 2 통계를 통해 시행하고, α(유의수준) 0.1 혹은 I 2=50%를 기준 값으로 효과 모형(effect model)을 선택하였다 48. 연구결과의 분석 시, 통계적으로 유의한 이질성이 존재하지 않을 때에는 고정효과모형(fixed effect model)에 의한 분석결과를 제시하지만, 본 연구의 메타 분석에서는 발생한 이질성에 해서는 무시하고 연구간의 정성 혹은 정량 이질성이 크다는 전제하에 좀 더 보수인 결과인 변량효과모형(random effect model)을 활용하였다. 이질성이 크고 포함된 연구의 수가 많은 경우는 확고한 결과 평가를 위하여 중재의 유형에 따른 하위그룹 분석을 시행하였다.
II. 본 론
1. 문헌선별
CNKI 데이터베이스로부터 225개의 문헌이 검색되었다. 1차적으로 문헌의 제목과 초록을 검토하여 2010년 이전 발행된 문헌(n=33), RCT가 아닌 연구(n=26), GERD 환자에 대한 경우가 아닌 연구(n=10), 한약을 중재로 사용하지 않은 연구(n=1), 한약 대 한약을 비교한 연구(n=5) 등의 총 75편의 문헌이 본 연구와 일치하지 않는 것으로 배제하여 2차 적으로 150편의 논문이 선정되었다. 이후 전문 검토를 통해 추가적인 정보를 얻어 포함 기준에 맞지 않는 문헌을 제외하였다. 항암요법 후의 GERD, 또는 GERD로 인한 咳嗽 환자를 대상으로 한 연구(n=11), 한약을 중재로 사용하지 않은 연구(n=24), 중복문헌(n=2), 문헌 자체에 접근 불가한 연구(n=5)까지 총 42편의 문헌을 제외하였으며, 반하사심탕 외의 처방이 합방된 경우 또는 반하사심탕의 중재에 부합하지 않은 문헌(n=17), 한약과 양약 병용 치료군에서 사용한 양약과 양약치료군의 대조군에서 사용한 양약의 종류가 다른 문헌(n=1) 18편을 제외하여, 최종적으로 90편의 연구가 체계적 고찰에 포함되었다( Fig. 1).
Fig. 1
Flow chart of the selection process. 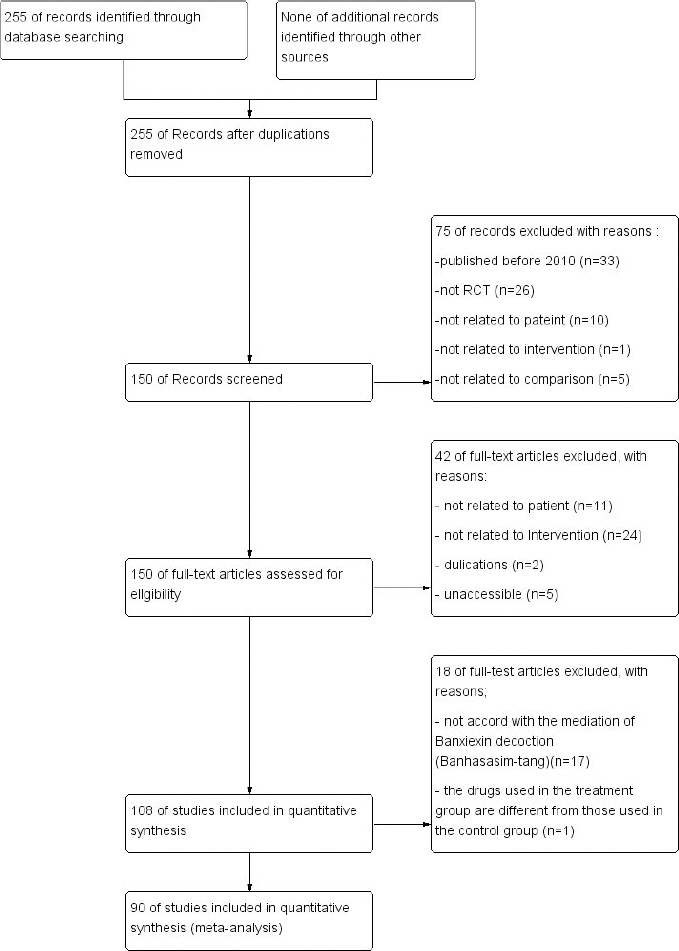
Table 2
Summary of 87 RCTs Included in This Review (THM vs WM, THM+WM vs WM)
|
Study ID (year) |
Sample size [before- drop out] |
Information |
THM (medication capacity, dosage method) |
WM/dosage method |
Evaluation |
Results (P-value) |
Period of treatment |
|
|
Total I) sample size (M/F) C) sample size (M/F) |
Intervention 1. Age (average) (yrs) 2. Course of disease (average) |
Comparison 1. Age (average) (yrs) 2. Course of disease (average) |
|
I. THM vs WM |
|
|
BX vs WM |
|
|
Sun P (2019) |
84 I) 42 (27/15) C) 42 (30/12) |
1. (53.8±2.6)
2. 1.9±0.5 ds |
1. (52.4±2.3)
2. 1.5±0.5 ds |
BX (500 ml, Bid) |
Rabeprazole Sodium Enteric-coated 20 mg/ Qd (MA) + Mosapride 10 mg/ TAD |
1. TER
2. Esophageal dynamics
3. Pressure difference of LES & UES
4. Pressure average of UES((χs) mmHg)
5. RR (2 wks/4 wks) |
1. P>0.05
2. P<0.05
3. P<0.05
4. P<0.05
5. P<0.05
6. (P=0.042/ P=0.046) |
42 ds |
|
|
Huang DH (2018) |
82 I) 41 C) 41 |
|
|
BX (Bid) |
Esomeprazole 20 mg/ BAD + Domperidone 10 mg/ TAD + Hydrotalcite 1 g/ Tid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
3. TSI
4. TEE |
1. P<0.05
2. P<0.05
4. P>0.05 |
8 wks |
|
|
Tang RZ (2018) |
96 I) 48 (14/23) C) 48 (24/24) |
1. 20~65 (37.36±5.50)
2. 2~6 yrs (2.63±1.23 yrs) |
1. 21~65 (37.65±5.35)
2. 2~5 yrs (2.52±1.31 yrs) |
BX (Bid) |
Rabeprazole 20 mg/ Qd (MA) + Domperidone 10 mg/ TAD |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain)
3. Pathological effect |
1. P>0.05
2. P<0.05/ P<0.05/ P<0.05 |
8 wks (1 course =2 wks * 4 courses |
|
|
Chen JM (2018) |
100 I) 50 (29/21) C) 50 (28/22) |
1. 18~71 (49.3±6.2)
2. 3~11 wks (5.0±1.4 wks) |
1. 18~70 (48.5±6.4)
2. 3~12 wks (4.9±1.5 wks) |
BX (Bid) |
Omeprazole Enteric-coated 20 mg/ Qd (MA) + Mosapride Citrate 5 mg/ Tid |
1. TER
2. Cost-effectiveness
3. Sensitivity
4. AE |
1. P<0.05
2. P<0.05
3. P<0.05 (P=0.004)
4. P<0.05 |
8 wks |
|
|
Yang H (2018) |
60 I) 30 (17/13) C) 30 (18/12) |
1. 23~55 (29.45±3.15)
2. 6 mths~6 yrs (1.5±3.6 yrs) |
1. 24~57 (29.89±3.47)
2. 7 mths~6 yrs (2.1±3.6 yrs) |
BX (D) |
Omeprazole 20~60 mg/ Qd~Bid |
1. TER
2. AE |
1. P<0.05 (P=0.002)
2. P<0.05 (P=0.001) |
8 wks |
|
|
Li Y (2018) |
80 I) 40 (27/13) C) 40 (28/12 |
1. 21~64 (39.2±4.2) |
1. 22~65 (40.1±3.2) |
BX (500 ml, D) |
Motilium (Domperidone) 10 mg / Tid + Ranitidine 150 mg/ Bid |
1. TER |
P<0.05 |
4 wks |
|
|
Liu Q (2018) |
78 I) 39 (25/14) C) 39 (25/14) |
1. 23~52 (37.5±14.5) |
1. 23~52 (37.5±12.5) |
BX (D) |
Omeprazole 20~60 mg / Qd~Bid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain)
3. RR
4. AE |
1. P<0.05 (P=0.002)
2. P=0.000/ P=0.000/ P=0.000
3. P<0.05
4. P=0.000 |
NR |
|
|
Li D (2017) |
106 I) 53 (23/30) C) 53 (27/26) |
1. (45.7±2.3)
2. (3.7±1.1 yrs) |
1. (46.3±2.6)
2. (4.1±1.4 yrs) |
BX (150 ml, Bid) |
Omeprazole Enteric-coated 20 mg/ BAD |
1. TER
2. TSI
3. AE |
1. P<0.05
2. P<0.01 |
NR |
|
|
Gu HT (2017) |
162 I) 81 (40/41) C) 81 (42/39) |
1. 25~75 (46.57±7.65)
2. 0.8~14 yrs (5.86±3.42 yrs) |
1. 24~74 (46.37±7.64)
2. 1~13 yrs (5.15±3.25 yrs) |
BX (350 ml, Bid) |
Omeprazole 20 mg/ Bid + Cisapride 10 mg/ TAD |
1. TER
2. TSI |
1. P<0.05
2. P<0.05 |
4 wks |
|
|
Huang FZ (2016) |
128 I) 64 (34/30) C) 64 (33/31) |
1. 25~58 (41)
2. 3 mths~10 yrs (6.5±2.58 yrs) |
1. 27~57 (40)
2. 4 mths~11 yrs (5.5±2.64 yrs) |
BX (300 ml, Bid) |
Cisapride 5 mg/ Tid |
1. TER |
1. P<0.05 |
30 ds |
|
|
He H (2016) |
84 [90] I) 43 [45] (26/19) C) 41 [45] (29/16) |
2. 23~68 (48.5±6.1)
3. 3~90 ds (28.8±9.6 ds) |
1. 21~65 (47.9±7.3)
2. 2~102 ds (30.2±10.5 ds) |
BX (200 ml, D, BAD) |
Pantoprazole 40 mg / Qd (MA) |
1. TER
2. RDQ integral
3. SAS integral
4. SDS integral
5. SF-36 integrals (PR/ RP/ BP/ VT/ RE/ MH/ SF/ GH) |
1. P<0.05
2. P<0.05
3. P<0.05
4. P<0.05
5. P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05 |
|
|
|
Chen J (2016) |
98 I) 49 (25/25) C) 49 (24/25) |
1. 19~74 (52.19±3.25)
2. 10 mths~5 yrs (3.25±0.57 yrs) |
1. 19~74
2. (52.19±3.25)
3. 10 mths~5 yrs (3.25±0.57 yrs) |
BX (150 ml, Bid) |
1. Domperidone 10 mg/ Tid + Rabeprazole Enteric-coated 20 mg/ Qd
2. (heartburn & acid regurgitation increase) Ranitidine Hydrochloride 0.15 g/ Hs |
1. TER
2. AE
3. RR |
1. P<0.05 (P=0.008)
2. P<0.05 (P=0.011)
3. P<0.05 (P=0.014) |
1 mth |
|
|
Feng YC (2016) |
60 I) 32 (18/14) C) 28 (13/15) |
1. 24~56 |
1. 23~58 |
BX (300 ml, Tid) |
Omeprazole 20 mg/ Qd + Motilium (Domperidone) 10 mg/ TAD |
TER |
P<0.05 |
8 wks |
|
|
Sun Q (2016) |
38 I) 19 (12/7) C) 19 (11/8) |
1. 23~67 (42.49±3.08)
2. (2.25±1.19 yrs) |
1. 21~66 (41.97±3.21)
2. (2.38±1.26 yrs) |
BX (300 ml, Bid) |
Itopride Hydrochloride 50 mg/ TAD + Omeprazole 20 mg/ Qd (MA) |
1. TER
2. AE |
1. P<0.05
2. P<0.05 |
2 mths |
|
|
Li L (2016) |
64 I) 32 (20/12) C) 32 (18/14) |
1. 20~60 (40) |
1. 20~65 (42) |
BX |
Rabeprazole 10 mg/ Tid |
1. TER
2. TEE |
1. P<0.05
2. P<0.05 |
8 wks |
|
|
Wang GQ (2016) |
120 I) 60 (38/22) C) 60 (40/20) |
1. 19~68 (46.8±3.5)
2. 2~11 wks (5.03±0.24 wks) |
1. 17~66 (46.3±4.6)
2. 1~11 wks (4.97±0.31 wks) |
BX (D, Bid) |
Omeprazole Enteric-coated 20 mg/ Qd + Mosapride 5 mg/ Qd |
1. TER
2. TEE
3. RR (1 yr) |
1. P<0.01
2. P<0.01
3. P<0.01 |
6 wks |
|
|
Wang HT (2016) |
80 I) 40 C) 40 |
|
|
BX (D, Bid) |
Cisapride 10 mg/ Tid |
1. TER
2. Treatment satisfaction rate
3. CSI (acid reflux/ heartburn/ retrosternal pain) |
1. P<0.05
2. P<0.05
3. P<0.05/ P<0.05/ P<0.05 |
4 wks |
|
|
Wang JP (2016) |
100 I) 50 (28/22) C) 50 (27/23) |
1. 20~70 (45.29±15.86)
2. 5 mths~6 yrs (3.07±1.14 yrs) |
1. 21~69 (2.93±1.09)
2. 6 mths~5 yrs (2.93±1.09 yrs) |
BX (300 ml, D, Bid) |
Rabeprazole 20 mg/ Bid + Mosapride Citrate 5 mg/ Tid |
1. TER
2. RDQ integral (acid reflux/ heartburn/ retrosternal pain/ regurgitation) |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05 |
14 ds |
|
|
Lin MH (2016) |
78 I) 39 (24/15) C) 39 (22/17) |
1. 24~6 (48.2±5.7)
2. 1~10 yrs (4.8±1.5 yrs) |
1. 23~65 (48.5±6.4)
2. 0.5~9 yrs (4.6±1.2 yrs) |
BX (BAD) |
Rabeprazole Enteric-coated 20 mg/ BAD |
1. TER
2. AE |
1. P<0.05
2. P<0.05 |
8 wks (1 course =4 wks *2 courses) |
|
|
Tang L (2016) |
120 I) 60 (32/28) C) 60 (34/26) |
1. 29~45 (39.8±1.2)
2. 1~4 yrs (2.8±0.9 yrs) |
1. 27~43 (39.1±0.9)
2. 1~4 yrs (2.6± 0.5 yrs) |
BX (400 ml, D, Bid) |
Rabeprazole 20 mg/ BAD |
1. TER
2. TSI
3. AE
4. RR (6 mths) |
1. P<0.05 (P=0.040)
2. P<0.05 (P=0.000)
3. P<0.05 (P=0.032)
4. P<0.05 (P=0.005) |
4 wks |
|
|
Xia BL (2015) |
132 I) 66 (32/34) C) 66 (35/31) |
1. 26~65
2. (40±6.3)
3. 3 mths~5 yrs
4. (16±4.3 mths) |
1. 25~67
2. (41±7.2)
3. 4 mths~5 yrs
4. (18±5.3 mths) |
BX (300 ml, D, TAD) |
Omeprazole 20 mg/ BAD + Domperidone 10 mg/ TAD |
1. TER
2. Endoscopic classification |
1. P<0.05 |
NR |
|
|
Dai BH (2015) |
54 I) 27 C) 37 |
|
|
BX (D, Bid) |
Omeprazole 20 mg/ BAD |
1. TER |
1. P<0.05 |
8 wks |
|
|
Wang T (2015) |
96 I) 48 (28/20) C) 48 (25/23) |
1. (43.2±12.5) |
1. (44.9±11.5) |
BX (100 ml, Bid (8AM, 4PM)) |
Cisapride 5 mg/ TAD + Pantoprazole Sodium Enteric-coated 20 mg/ Qd |
1. TER
2. Total integral of TCM syndromes |
1. P<0.05
2. P<0.05 |
8 wks |
|
|
Shou HC (2015) |
86 I) 43 (24/19) C) 43 (23/20) |
1. (51.7±13.5)
2. 2~10 yrs |
1. (52.6±12.9)
2. 1~9 yrs |
BX (300 ml, D, Tid) |
Cisapride 10 mg/ TAD |
1. TER
2. TSI |
1. P<0.03
2. P<0.05 (P=0.002) |
60 ds |
|
|
Li HP (2015) |
80 I) 40 C) 40 |
|
|
BX (150 ml, D, BAD) |
Omeprazole Enteric-coated 20 mg/ BAD + Motilium (Domperidone) 10 mg/ TAD |
1. TER
2. AE |
1. P<0.05
2. P>0.05 |
2 mths (1 course =4 wks *2 courses) |
|
|
Guo FX (2014) |
80 I) 40 (21/19) C) 40 (23/17) |
1. 23~65 (42.5±8.2) 2. 3 mths~7 yrs (2.3±0.7 yrs) |
1. 25~69 (43.1±7.4)
2. 5 mths~6 yrs (2.2±1.0 yrs) |
BX (D, Bid) |
Rabeprazole Enteric-coated 10 mg/ Qd + Mosapride 5 mg/ Tid |
1. TER
2. TEE |
1. P<0.05 (P=0.017)
2. P<0.05 (P=0.021) |
8 wks |
|
|
Jiang LQ (2014) |
60 I) 30 (19/11) C) 30 (20/10) |
1. 38~67 (50.3)
2. 3~48 mths (25.3 mths) |
1. 40~69 (51.9)
2. 4~50 mths (26.7 mths) |
BX (300~400 ml, D, Bid) |
Cisapride 5 mg/ Bid + Omeprazole 20 mg/ Bid Or Lansoprazole 30 mg/ Bid |
1. TER
2. TSI
3. AE |
1. P<0.05
2. P<0.05
3. P<0.05 |
2 mths |
|
|
Kang XQ (2014) |
62 I) 31 C) 31 |
|
|
BX (500 ml, Bid) |
Ranitidine 150 mg/ Bid + Domperidone 10 mg/ Tid |
1. TER
2. TEE
3. AE |
|
4 wks (1 course =1/2 mths +3 hds *2 courses) |
|
|
Chen YX (2014) |
116 I) 58 C) 58 |
|
|
BX |
Rabeprazole 10 mg/ Qd |
1. TSC |
1. P<0.05 |
8 wks |
|
|
WANG JY (2014) |
137 I) 68 (39/29) C) 69 (41/28) |
1. 21~64 (45.2±4.4) |
1. 22~63 (46.2±5.3) |
BX (Bid) |
Pantoprazole 40 mg/ Qd (MA) |
1. RDQ frequency integrals 1) Symptom frequency efficacy of RDQ (acid reflux/ heartburn/ retrosternal pain/ regurgitation) 2) Total frequency efficacy of RDQ
2. RDQ degree integrals 1) Symptom integrals of RDQ (acid reflux/ heartburn/ retrosternal pain/ regurgitation) 2) Total integral of RDQ
3. SAS integral
4. SDS integral
5. SF-36 integral (PR/ RP/ BP/ VT/ RE/ MH/ SF/ GH) |
1. 1) P>0.05/ P>0.05/ P>0.05/ P>0.05 2) P>0.05
2. 1) P>0.05/ P>0.05/ P>0.05/ P>0.05 2) P>0.05
3. P<0.05
4. P<0.05
5. P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05 |
8 wks |
|
|
Li JL (2014) |
113 I) 57 C) 56 |
|
|
BX (300 ml, D, Tid) |
Rabeprazole Sodium Enteric-coated 20 mg/ Bid |
1. TER |
1. P<0.05 |
NR |
|
|
Zhou JF (2013) |
60 I) 30 C) 30 |
|
|
BX (150 ml, D, Bid) |
Esomeprazole 20 mg/ Bid + Domperidone 10 mg/ TAD |
1. TER
2. TEE |
1. P<0.05
2. P<0.05 |
8 wks |
|
|
Liu ZY (2013) |
68 I) 34 (34/15) C) 34 (13/21) |
1. 20~65 (46.25)
2. 4 mths~8 yrs |
1. 21~67 (43.23)
2. 5 mths~6 yrs |
BX (300 ml, D, BAD) |
Omeprazole 20 mg/ Qd (MA) + Itopride Hydrochloride 50 mg/ TAD |
1. TER |
1. P<0.05 |
8 wks |
|
|
Zhang JW (2013) |
92 I) 46 (21/25) C) 46 (20/26) |
1. 19~68 (51.23±14.21)
2. 6 mths~15 yrs (5.67±2.37 yrs) |
1. 20~69 s (52.39±14.65)
2. 8 mths~17 yrs (5.73±2.41 yrs) |
BX (Bid) |
Omeprazole Enteric-coated 20 mg/ BAD |
1. TER
2. Total integral of TCM syndromes
3. TCM syndrome integrals (acid reflux/ heartburn/ abdominal pain/ abdominal distention/ miscellaneous/ belching/ insomnia)
4. TEE
5. AE |
1. P>0.05 (P=0.7256)
2. P<0.05 (P=0.081)
3. P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05/ P>0.05
4. P>0.05 (p=0.4316)
5. P<0.05 (P=0.053) |
2 mths |
|
|
Ye MB (2013) |
86 I) 43 (20/23) C) 43 (21/22) |
1. 20~58 (35.62±7.51)
2. (1.81±1.05 yrs) |
1. 21~56 (36.27±6.99)
2. (1.95±0.97 yrs) |
BX (150 ml, Bid) |
Omeprazole Enteric-coated 20 mg/ BAD |
1. TER (4 wks/ 6 mths)
2. TSI (4 wks/ 6 mths) |
1. P<0.05/ P<0.05
2. P>0.05/ P<0.05 |
4 wks |
|
|
Chen X (2013) |
116 I) 58 C) 58 |
|
|
BX (D, Bid) |
Rabeprazole 20 mg/ Bid + Mosapride tartrate 5 mg/ Tid |
1. TER
2. Total integral of TCM syndromes |
1. P<0.05
2. P<0.05 |
4 wks |
|
|
Cao WY (2013) |
64 I) 32 (26/6) C) 32 (22/10) |
|
|
BX (D) |
Domperidone 10 mg/ Tid + Ranitidine 150 mg/ Bid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain)
3. TEE |
1. P<0.05
2. P<0.05/ P>0.05/ P<0.05
3. P<0.05 |
8 wks (1 course =4 wks * 2 courses) |
|
|
Wang YP (2013) |
100 I) 50 C) 50 |
|
|
BX (140 ml, Bid) |
Ranitidine 150 mg/ Bid + Motilium (Domperidone) 10 mg/ TId |
1. TER
2. CSI
3. (epigastric pain/ acid reflux & heartburn/ nausea & vomiting) |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05 |
2 wks |
|
|
Yang Q (2013) |
127 I) 64 (21/43) C) 63 (17/46) |
1. (50.42±10.01)
2. (29.62±43.40 mths) |
1. (46.27±12.19)
2. (24.43±38.72 mths) |
BX (200 ml, Bid) |
Pantoprazole 40 mg/ Qd (MA) |
1. TER
2. Total RDQ integral
3. RDQ frequency integrals 1) Symptom frequency efficacy of RDQ (acid reflux/ heartburn/ retrosternal pain/ regurgitation) 2) Total frequency efficacy of RDQ
4. RDQ degree integrals 1) Symptom integrals of RDQ (acid reflux/ heartburn/ retrosternal pain/ regurgitation) 2) Total integral of RDQ
5. PSQI integral
6. HAD integral |
1. P>0.05
2. P>0.05 (P=0.135)
3. 1) P>0.05 (P=0.136/ P=0.263/ P=0.706/ P=0.378) 2) P>0.05 (P=0.104)
4. 1) P>0.05/ P>0.05/ P>0.05/ P>0.05 2) P>0.05
5. P<0.05
6. P<0.05 |
8 wks |
|
|
Hou JX (2012) |
68 I) 48 (25/23) C) 20 (7/13) |
1. 28~69 (43)
2. 2 mths~4 yrs (1.6 yrs) |
1. 31~70 (41)
2. 1 mth~3.5 yrs (3.5 yrs) |
BX (150 ml, D, BAD) |
Omeprazole 20 mg/ Qd + Mosapride 5 mg/ Qd |
1. TER
2. RR (1 yr) |
1. P<0.05
2. P<0.05 |
30 ds |
|
|
Shen YL (2012) |
83 I) 43 (27/16) C) 40 (26/14) |
1. 26~70 (51.2± 11.5) |
1. 27~70 (50.9±11.4) |
BX (500 ml, Bid) |
Omeprazole 20 mg/ BAD + Domperidone 10 mg/ TAD |
1. TER
2. Endoscopic classification (Grade A/B/C/D) |
1. P<0.01 (P=0.001)
2. P<0.05/ P<0.05/ P<0.05/ P<0.05 |
56 ds (1 course =14 ds * 4 courses) |
|
|
Chen XJ (2012) |
80 I) 40 (21/19) C) 40 (20/20) |
1. 24~67 (45.12±1.4)
2. 4 mths~4 yrs (13.1±1.65 mths) |
1. 26~65 (45.87±1.6)
2. 3 mths~5 yrs (13.3±1.75 mths) |
BX (400 ml, BAD) |
Rabeprazole 10 mg/ Qd (MA) + Motilium (Domperidone) 10 mg/ TAD + Sucralfate 0.75 g/ TAD |
1. TER
2. TSI 3. RR |
1. P<0.05
2. P<0.05 |
8 wks (1 course =14 ds * 2 courses) |
|
|
Yang Q (2012) |
127 I) 64 (21/43) C) 63 (17/6) |
1. (50.42±10.01)
2. (29.62±43.40 mths) |
1. (46.27±12.19)
2. (24.43±38.72 mths) |
BX (200 ml, Bid) |
Pantoprazole 40 mg/ Qd (MA) |
1. TER
2. TSI
3. TCM syndrome integrals (acid reflux/ heartburn/ belching/ epigastralgia & predilection for warmth and pressure by hand/ chest pain/ dry mouth & bitter taste/ appetite reduction)
4. Efficiency of syndromes (acid reflux/ heartburn/ belching/ epigastralgia & predilection for warmth and pressure by hand/ chest pain/ dry mouth & bitter taste/ appetite reduction) |
1. P>0.05
2. P>0.05
3. P>0.05/ P>0.05/ P<0.01/ P>0.05/ P>0.05/ P<0.05/ P<0.01
4. P>0.05/ P>0.05/ P<0.05/ P>0.05/ P>0.05/ P<0.05/ P<0.05 |
8 wks |
|
|
Shi YP (2012) |
104 I) 52 (28/24) C) 52 (32/20) |
|
|
BX |
Omeprazole 20 mg/ Qd |
1. TER
2. Total efficiency of Symptom relief
3. TEE
4. AE |
1. P>0.05
2. P<0.05
3. P<0.05 |
4 wks |
|
|
Jin HB (2012) |
68 I) 36 (21/15) C) 32 (18/14) |
1. 21~58 (35)
2. 3 mths~5 yrs |
1. 22~60 (36.5)
2. 3 mths~4 yrs |
BX (300 ml, D, Tid~Qid) |
Omeprazole 20 mg/ BAD + Motilium (Domperidone) 10 mg/ TAD |
1. TER
2. RR (6 mths) |
1. P<0.05
2. P<0.05 |
8 wks |
|
|
Ye F (2011) |
96 I) 56 (31/25) C) 30 (16/14) |
1. 23~6 (45±0.5)
2. 3 mths~5 yrs (12±0.45 mths) |
1. 25~63 (46±0.5)
2. 2 mths~6 yrs (13±0.22 mths) |
BX (400 ml, D, BAD) |
Rabeprazole 10 mg/ Qd (MA) + Sucralfate 0.75 g/ TAD + Motilium (Domperidone) 10 mg/ TAD |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain) |
1. P<0.01
2. P<0.05/ P<0.05/ P<0.05 |
8 wks (1 course =4 wks * 2 courses) |
|
|
Li YF (2011) |
68 I) 44 (21/23) C) 24 (12/12) |
1. 18~67 (36.4)
2. 14 ds~6 yrs (2 yrs) |
1. 17~62 (38.2)
2. 2 mths~5 yrs (1.5 yrs) |
BX (D, Bid) |
Cisapride 10 mg/ Tid |
1. TER |
1. P<0.01 |
8 wks |
|
|
Tang YQ (2011) |
65 I) 35 C) 30 |
|
|
BX (400 ml, D, BAD) |
Omeprazole 20 mg/ Qd + Mosapride 5 mg/ Tid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain)
3. TEE |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05
3. P<0.05 |
8 wks (1 course =4 wks * 2 courses) |
|
|
Duan XF (2011) |
72 I) 36 C) 36 |
|
|
BX (150 ml, BAD) |
Omeprazole 20 mg/ BAD + Cisapride 10 mg/ TAD |
1. TER |
1. P<0.05 |
4 wks |
|
|
Xu YJ (2010) |
50 I) 35 (21/14) C) 15 (9/6) |
1. 21~42
2. 2 mths~7 yrs |
1. 25~48
2. 2 mths~5 yrs |
BX (300 ml, D, BAD) |
Omeprazole 10 mg/ Qd |
1. TER
2. TEE |
1. P<0.05
2. P>0.05 |
8 wks |
|
|
Mo X (2010) |
76 I) 40 (22/18) C) 36 (20/16) |
1. 21~57
2. 3 mths~7 yrs |
1. 19~63
2. 2 mths~5 yrs |
BX (Bid) |
Omeprazole 20 mg/ Bid + Motilium (Domperidone) 10 mg/ Tid |
1. TER |
1. P<0.01 |
12 wks (1 course =4 wks *3 courses) |
|
|
Liu HY (2010) |
60 I) 30 (12/18) C) 30 (14/16) |
1. (42±11)
2. (30±9 mths) |
1. (41±10)
2. (31±10 mths) |
BX (400 ml, Bid) |
Domperidone 10 mg/ TAD + Ranitidine 150 mg/ Bid |
1. TER
2. TEE |
1. P<0.05
2. P>0.05 |
1 mth |
|
|
Liu LQ (2010) |
100 I) 60 (37/23) C) 40 (26/14) |
1. 25~40 (47.4)
2. 0.5 mths~9 yrs (4.5 yrs) |
1. 21~68 (45.7)
2. 2 mths~10 yrs (4.5 yrs) |
BX (100 ml, Bid) |
Rabeprazole 20 mg / Bid (MA, Hs) |
1. TER
2. RR (1 yr) |
1. P<0.05
2. P<0.05 |
4 wks |
|
|
Lu W (2010) |
78 I) 39 (20/19) C) 39 (19/20) |
1. 20~64 (7.35± 4.20)
2. 1~5 yrs (2.63±1.22 yrs) |
1. 22~65 (38.65±5.45)
2. 1~6 yrs (3.12 ±1.31 yrs) |
BX (D, Bid) |
Omeprazole 20 mg/ Qd + Mosapride 5 mg/ Tid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain) |
1. P>0.05
2. P<0.05/ P<0.05/ P>0.05 |
4 wks |
|
|
Gao WW (2010) |
97 I) 60 (35/32) C) 30 (16/14) |
1. 23~75 (48.32)
2. 1 mths~12 yrs (12.56 mths) |
1. 20~78 (50.12)
2. 3 mths~11 yrs (13.24 mths) |
BX (300 ml, D, Tid) |
Rabeprazole 10 mg/ Qd + Motilium (Domperidone) 10 mg/ Tid |
1. TER
2. TSI |
1. P<0.05
2. P<0.01 |
8 wks |
|
|
BX (ST) vs WM |
|
|
Sun XL (2019) |
80 I) 40 C) 40 |
|
|
BX (D, Bid) |
Lansoprazole 30 mg/ Qd (MA) |
1. TER
2. CSI (acid reflux & heartburn/ Burning pain in the stomach/ Chest pain involving two flanks/ dry mouth & bitter taste)
3. TSI |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05
3. P<0.05 |
4 wks (1 course =7 ds *4 courses) |
|
|
Tong SM (2017) |
68 I) 34 (21/13) C) 34 (20/14) |
1. 25~63 (41.42±13.09)
2. 4 mths~3 yrs (8.23±5.13 mths) |
1. 24~65 (43.28±14.21)
2. 5 mths~2.5 yrs (7.88±5.47 mths) |
BX (300ml, D, Tid) |
Pantoprazole Sodium Enteric-coated 40 mg/ Qd + Domperidone 10 mg/ Tid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain/ dysphagia)
3. TSI |
1. P<0.05
2. P<0.05/ P<0.05/ P>0.05/ P<0.05
3. P<0.05 |
4 wks |
|
|
Wang SQ (2015) |
100 I) 50 (23/27) C) 50 (26/24) |
|
|
BX (D, Bid) |
Rabeprazole 10 mg/ Bid |
1. TER
2. TSI
3. CSI (burning discomfort of the stomach/ acid regurgitation or water vomiting/ gastric pain/ fatigued spirit & lack of strength/ lack of warmth in the extremities/ anorexia/ thin sloppy stool
4. TEE
5. RR |
1. P<0.05
2. P>0.05 (P=0.529)
3. P=0.000/ P=0.000/ P=0.000/ P=0.000/ P=0.014/ P=0.009/ P=0.000/ P=0.000/ P=0.000
4. P<0.01 (P=0.000)
5. P<0.05 (P=0.043) |
8 wks |
|
|
Sun XH (2013) |
60 I) 30 (17/13) C) 30 (14/16) |
1. 21~61 (3.54±1.25)
2. 1~6 yrs (3.54±1.25 yrs) |
1. 21~59 (39.23±2.01)
2. 1~6 yrs (3.21±1.24 yrs) |
BX (Bid) |
Omeprazole 20 mg/ Qd (MA) + Motilium (Domperidone) 10 mg/ TAD |
1. TER
2. CSI (acid reflux & heartburn/ Burning pain in the stomach & gastric discomfort/ Chest pain involving two flanks/ Loose stool/ dry mouth & bitter taste)
3. TEE
4. Pathological effect |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05/ P<0.05
3. P<0.05
4. P<0.05 |
30 ds |
|
|
Ⅱ. THM+WM vs WM |
|
|
BX+WM vs WM |
|
|
Chang YJ (2019) |
92 I) 46 (24/22) C) 46 (25/21) |
1. 19~67 (43.57±7.60)
2. 8 mths~6 yrs (3.31±1.42 yrs) |
1. 19~68 (43.61±7.84)
2. 10 mths~6 yrs (3.37±1.46 yrs) |
BX (300 ml, D, Bid) |
Rabeprazole 10 mg/ Bid |
1. TER
2. TSI
3. RR (2 mths) |
1. P<0.05
2. P<0.05 |
2 mths |
|
|
Wang H (2019) |
74 I) 32 (23/19) C) 32 (17/15) |
1. 33-68 (50.8±15.1)
2. 1~9 mths (5.1±2.8 mths) |
1. 34-67 (50.3±15.4)
2. 1~8 mths (4.3±2.5 mths) |
BX (200 ml, Bid) |
Omeprazole 20 mg/ Qd (Hs) + Domperidone 10 mg/ TAD |
1. TER
2. TSI |
1. P<0.05
2. P<0.05 |
4 wks |
|
|
Lu J (2019) |
100 I) 50 (25/25) C) 50 (27/23) |
1. 24~67 (43.27±5.16)
2. 0.5~7 yrs (3.72±1.43 yrs) |
1. 25~68 (42.93±5.87)
2. 0.5~8 yrs (3.93±1.51 yrs) |
BX (D, Bid) |
Rabeprazole 20 mg/ Qd (MA) |
1. TER
2. Efficiency of symptoms (acid reflux/ retrosternal burning sensation/ belching) |
1. P<0.05 (P=0.021)
2. P<0.05 (P=0.017/ P=0.007/ P=0.021) |
8 wks |
|
|
Zhao XY (2018) |
54 I) 27 (14/13) C) 27 (13/14) |
1. 24~66 (45.7±1.7) |
1. 25~65 (45.5±1.6) |
BX (D, Bid) |
Omeprazole 40 mg/ Bid |
1. TER
2. AE |
1. P<0.05 (P=0.001)
2. P<0.05 (P=0.001) |
2 mths |
|
|
Zhang XC (2018) |
80 I) 40 (19/21) C) 40 (21/19) |
1. 25~66 (45.50±0.17) |
1. 26~66 (45.56±0.19) |
BX (D, Bid) |
Omeprazole 20 mg/ BAD |
1. TER
2. CSI (retrosternal discomfort/ regurgitation/ heartburn/ acid reflux) |
1. P<0.05 (P=0.012)
2. P<0.05 (P=0.0002/ P=0.0014/ P=0.0021/ P=0.001) |
NR |
|
|
Wang ZB (2018) |
80 I) 40 (25/15) C) 40 (20/20) |
1. 25~78 (51.5±3.6) |
1. 27~65 (46.1±6.2) |
BX (Tid) |
Cisapride 10 mg/ TAD~Qid |
1. TER
2. AE |
1. P<0.05 (P=0.001)
2. P<0.05 (P=0.001) |
NR |
|
|
Wu YB (2018) |
80 I) 40 (22/18) C) 40 (23/17) |
1. 19~65 (36.3±2.5)
2. 2~10 yrs (4.1±1.9 yrs) |
1. 20~64 (37.1±2.7)
2. 2~9 yrs (3.9±1.8 yrs) |
BX (D) |
Losec 20 mg/ Qd + Mosapride Citrate 5 mg/ Tid |
1. TER |
1. P<0.05 |
4 wks |
|
|
Sun YF (2018) |
134 I) 68 (22/36) C) 66 (22/35) |
1. 27~66 (49.51±9.20)
2. 2~54 mths (26.79±6.37 mths) |
1. 26~64 (48.87±9.08)
2. 1~56 mths (25.58±6.29 mths) |
BX (200 ml, D, Bid) |
Pantoprazole Sodium Enteric-coated 40 mg/ Qd (MA) + Domperidone 10 mg/ TAD |
1. TER
2. RDQ integrals 1) RDQ frequency integrals 2) RDQ degree integrals 3) Total integral of RDQ
3. Ghrelin & VIP levels (Ghrelin/ VIP)
4. AE
5. RR (3 mths) |
1. P<0.05
2. 1) P<0.05 2) P<0.05 3) P<0.05
3. P<0.05/ P<0.05
4. P>0.05
5. P<0.05 |
4 wks |
|
|
Su YF (2018) |
86 I) 43 C) 43 |
|
|
BX (D, Bid) |
Rabeprazole 20 mg/ Bid + Mosapride Citrate 5 mg/ Tid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
3. TSI |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05
3. P>0.05 |
8 wks |
|
|
Liu HD (2018) |
86 I) 43 (22/21) C) 43 (20/23) |
1. 32~65 (48.52±6.37)
2. 1~4 yrs (2.26±0.43 yrs) |
1. 32~65 (48.47±6.44)
2. 1~4 yrs (2.36±0. 27 yrs) |
BX (D, Bid) |
Rabeprazole Sodium Enteric-coated 20 mg/ BAD + Mosapride Citrate 5 mg/ TAD |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain/ regurgitation) |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05 |
8 wks |
|
|
Meng FZ (2018) |
64 I) 32 (18/14) C) 32 (21/11) |
1. 25~65 (43.8±4.2)
2. 6 mths~8 yrs (3.6±1.4 yrs) |
1. 27~64 (42.6±3.8)
2. 3 mths~9 yrs (3.5±1.2 yrs) |
BX |
Rabeprazole 20 mg/ Qd (MA) |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain) |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05 |
8 wks |
|
|
Zhou SN (2017) |
51 I) 27 (9/18) C) 24 (14/10) |
1. 33~69 (53.67±10.00)
2. 0.5~20 yrs (10.00±6.27 yrs) |
1. 33~69 (55.97±8.85)
2. 0.5~20 yrs (8.80±6.14 yrs) |
BX (100 ml, Tid) |
Omeprazole Enteric-coated 40 mg/ Qd + Rebamipide 0.1 g/ Tid |
1. TER
2. TSI (2 wks/ 4 wks)
3. CSI A. 2 wks (epigastric pain/ acid reflux/ belching/ poor appetite/ heartburn/ nausea/ retrosternal pain/ defecation) B. 4 wks (epigastric pain/ acid reflux/ belching/ poor appetite/ heartburn/ nausea/ retrosternal pain/ defecation)
4. Efficiency of symptoms (epigastric pain/ acid reflux/ belching/ poor appetite/ heartburn/ nausea/ retrosternal pain/ defecation) |
1. P<0.05
2. P<0.05/ P<0.05
3. A. P>0.05/ P<0.05/ P>0.05/ P>0.05/ P>0.05/ P>0.05/ P>0.05/ P>0.05/ P<0.05 B. P<0.05/ P<0.05/ P>0.05/ P<0.05/ P>0.05/ P>0.05/ P>0.05/ P>0.05/ P<0.05 |
4 wks |
|
|
Guo KS (2017) |
80 I) 40 (24/16) C) 40 (22/18) |
1. 18~66 (48.43±5.66) |
1. 18~70 (49.02±6.06) |
BX (50 ml, D, Bid) |
Esomeprazole Magnesium Enteric-coated 20 mg/ Qd (MA) |
1. TER |
1. P<0.05 |
6~8 wks |
|
|
Chen YF (2016) |
60 I) 32 (18/14) C) 28 (13/15) |
1. 24~56
2. 6 mths~6 yrs |
1. 23~58
2. 5 mths~9 yrs |
BX (300 ml, D, Tid) |
Omeprazole 20 mg/ Qd (MA) + Motilium (Domperidone) 10 mg/ TAD |
1. TER |
1. P<0.05 |
8 wks |
|
|
Cao Y (2016) |
86 I) 43 C) 43 |
|
|
BX (Bid) |
Mosapride 5 mg/ TAD |
1. TER
2. Disappearance time of symptoms & signs (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
3. TEE |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05 3. P<0.05 |
3 mths (1 course =1 mth * 3 courses) |
|
|
Zhang LJ (2016) |
124 I) 62 C) 62 |
|
|
BX (400 ml, D) |
Mosapride 5 mg/ TAD |
1. TER
2. TEE 3. Disappearance time of symptoms & signs (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
4. TEE
5. RR (4 wks)
6. AE |
1. P<0.05 (P=0.0124)
2. P<0.05
3. P<0.05/ P<0.05/ P<0.05/ P<0.05
4. P<0.05 (P=0.0181)
5. P<0.05 |
3 mths (1 course =1 mth * 3 courses) |
|
|
Ruan SR (2015) |
150 I) 75 C) 75 |
|
|
BX (Tid) |
Cisapride 20 mg/ Qd (MA) |
1. TER
2. TEE
3. AE |
1. P<0.05
2. P<0.05
3. P<0.05 |
4 wks |
|
|
Lin QY (2015) |
90 I) 45 (23/22) C) 45 (23/22) |
1. (49.2±1.8) |
1. (49.5±0.9) |
BX (400 ml, D, Bid) |
Rabeprazole Sodium Enteric-coated 20 mg/ Qd (MA) + Mosapride Citrate 5 mg/ TAD |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
3. TEE |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05/ P<0.05
3. P<0.05 |
8 wks |
|
|
Liu SX (2014) |
49 I) 25 (14/11) C) 24 (12/12) |
|
|
BX (D, Bid) |
Mosapride 5 mg/ TAD |
1. TER
2. Disappearance time of symptoms and signs (acid reflux/ heartburn/ retrosternal pain/ regurgitation)
3. TEE |
1. P<0.05
2. P<0.01
3. P<0.01/ P<0.01/ P<0.01/ P<0.05
4. P<0.01 |
3 mths |
|
|
Liu MG (2014) |
100 I) 50 (28/22) C) 50 (30/20) |
1. 25~68 (48.45±5.88)
2. 3~90 ds (28.55±7.48 ds) |
1. 28~67 (47.55±5.50)
2. 3~85 ds (25.87±6.85 ds) |
BX (D) |
Omeprazole Enteric-coated 20 mg/ Bid + Flupentixol and Melitracen 10 mg/ Qd |
1. TER
2. CSI (acid reflux/ belching/ Distention and pain in the stomach/ hiccup) |
1. P<0.05
2. P<0.05 P<0.05/ P<0.05/ P<0.05 |
1 mth |
|
|
Tan LH (2014) |
116 I) 58 (32/26) C) 58 (34/24) |
1. 31~67 (45.64±3.83)
2. 4 mths~5 yrs (1.25±0.67 ds) |
1. 34~65 (45.83±3.79)
2. 3 mths~4 yrs (1.31±0.68 ds) |
BX (400 ml, D, Bid) |
Motilium (Domperidone) 10 mg/ TAD + Rabeprazole 10 mg/ Qd (MA) |
1. TER
2. CSI (acid reflux/ heartburn/ chest pain) |
1. P<0.05 (P=0.0181)
2. P<0.05/ P<0.05/ P<0.05 |
4 wks |
|
|
Wang Y (2013) |
90 I) 45 (26/19) C) 45 (23/22) |
1. 23~65 2. 3 mths~10 yrs |
1. 30~63
2. 6 mths~12 yrs |
BX (30 ml, D, Bid) |
Rabeprazole Sodium Enteric-coated/ Bid + Mosapride Citrate 5 mg/ TAD |
1. TER
2. TSI
3. TEE
4. RR (4 wks) |
1. P<0.05
2. P<0.05
3. P<0.05
4. P<0.05 |
8 wks |
|
|
Huai XX (2013) |
60 I) 30 (16/14) C) 30 (17/13) |
1. 18~84 (42.54±9.14)
2. 6~36 mths (18 mths) |
1. 17~86 (43.96±10.25)
2. 8~42 mths (16 mths) |
BX (400 ml, Bid) |
Rabeprazole 20 mg/ Bid |
1. TER
2. TEE |
1. P<0.05 (P=0.045)
2. P<0.05 (P=0.030) |
60 ds |
|
|
Tan ZX (2013) |
90 I) 43 (27/16) C) 47 (29/18) |
1. (43.4±6.7)
2. (7.2±1.7 mths) |
1. (45.5±8.3)
2. (8.9±2.1 mths) |
BX (D) |
Omeprazole Enteric-coated 20 mg/ Bid Motilium (Domperidone) 10 mg/ Tid |
1. TER
2. TEE
3. AE |
1. P>0.05
2. P>0.05
3. P>0.05 (P=0.320) |
2 mths (1 courses =4 wks * 2 courses) |
|
|
Bai SC (2012) |
120 I) 60 C) 60 |
1. 19~71 (37)
2. 3 mths~17 yrs |
1. 20~70 (38)
2. 3 mths~15 yrs |
BX (500 ml, D, Bid) |
Omeprazole 20 mg/ Bid + Cisapride 20 mg/ TAD |
1. TER
2. RR (6 monts) |
1. P<0.01 |
1 mth |
|
|
Han XL (2011) |
96 I) 48 (28/20) C) 48 (29/19) |
1. 20~65 |
1. 20~65 |
BX (D) |
Omeprazole Enteric-coated 20 mg/ Bid + Domperidone 10 mg/ Tid |
1. TER |
1. P<0.05 |
1 mth |
|
|
Cheng ZH (2011) |
96 I) 48 C) 48 |
|
|
BX (300 ml, D, Tid) |
Mosapride 10 mg/ TAD + Lansoprazole 15 mg/ Bid |
1. TER
2. CSI (acid reflux/ heartburn/ retrosternal pain) |
1. P<0.05
2. P<0.05/ P<0.05/ P<0.05 |
6 wks |
|
|
Gong SQ (2010) |
110 I) 60 (40/20) C) 50 (35/15) |
1. 20~69 (32.5)
2. 1 wk~20 yrs (11 mths) |
1. 21~68 (33.5)
2. 1 wk~20 yrs (11 mths) |
BX (D, Bid) |
Motilium (Domperidone) 10 mg/ TAD + Omeprazole 20 mg/ Bid |
1. TER |
2. P<0.05 |
4 wks |
Table 3
Summary of 3 RCTs Included in This Review (THM+WM vs THM vs WM)
|
Study ID (year) |
Sample size [before- drop out] |
Information |
THM (medication capacity, dosage method) |
WM /Dosage method |
Evaluation |
Results (P-value) |
Period of treatment (wks) |
|
|
|
Total I) sample size (M/F) C) sample size (M/F) |
Intervention 1 (THM+WM) 1. Age (average) (yrs)
2. Course of disease (average) |
Intervention 2 (THM)
1. Age (average) (yrs)
2. Course of disease (average) |
Comparison (WM)
1. Age (average) (yrs)
2. Course of disease (average) |
THM +WM vs WM |
THM vs WM |
TH +WM vs THM |
|
III. THM+WM vs THM vs WM |
|
|
BX+WM vs BX vs WM |
|
|
Cao CN (2018) |
72 I1) 24 (18/6) I2) 24 (18/6) C) 24 (18/6) |
1. (48.96 ±14.04) |
1. (51.62 ±10.07) |
1. (49.92± 13.29) |
BX (200 ml, D, Bid) |
Rabeprazole Sodium Enteric-coated 10 mg/ Bid |
1. TER
2. TEE
3. TSI
4. SAS integral
5. PSQI integral |
1. P<0.05
2. P<0.05
3. P<0.05
4. P<0.05 |
2. P<0.05
3. P<0.05
4. P<0.05
5. P<0.05 |
4. P<0.05
5. P<0.05 |
8 |
|
|
Cao CN (2016) |
72 I1) 24 (18/6) I2) 24 (18/6) C) 24 (17/19) |
1. (48.96 ±14.04) |
1. (51.62 ±10.07) |
1. (49.92 ±13.29) |
BX (D, Bid) |
Rabeprazole Sodium Enteric-coated 10 mg/ Bid |
1. MSI (4 wks/ 8 wks)
2. SSI (4 wks/ 8 wks)
3. TSI (4 wks/ 8 wks)
4. TEE
5. SAS integrals (4 wks/ 8 wks)
6. SDS integrals (4 wks/ 8 wks)
7. PSQI integrals (4 wks/ 8 wks) |
1. P<α’=0.05/3 (P=0.008)/ P<α’=0.05/3 (P=0.002)
2. P<α’=0.05/3 (P=0.000)/ P<α’=0.05/3 (P=0.000)
3. P<0.05 (P=0.047)/ P<0.05 (P=0.025)
4. P<0.05 (P=0.025)
5. P>0.05/ P<α’=0.05/3 (P=0.000)
6. P>0.05/ P>α’=0.05/3 (P=0.053)
7. P>0.05/ P<α’=0.05/3 (P=0.000) |
1. P<α’=0.05/3 (P=0.000)/ P<α’=0.05/3 (P=0.012)
2. P<α’=0.05/3 (P=0.000)/ P<α’=0.05/3 (P=0.000)
3. P<0.05 (P=0.047)/ P>0.05 (P=0.350)
4. P<0.05 (P=0.011)
5. P>0.05/ P>α’=0.05/3 (P=0.130)
6. P>0.05/ P>α’=0.05/3 (P=0.818)
7. P>0.05/ P>α’=0.05/3 (P=0.125) |
1. P<α’=0.05/3 (P=0.015)/ P>α’=0.05/3 (P=0.568)
2. P>α’=0.05/3 (P=0.03)/ P<α’=0.05/3 (P=0.000)
3. P>0.05 (P=0.617)/ P>0.05 (P=0.117)
4. P>0.05 (P=0.05)
5. P>0.05/ P<α’=0.05/3 (P=0.004)
6. P>0.05/ P>α’=0.05/3 (P=0.061)
7. P>0.05/ P<α’=0.05/3 (P=0.000) |
8 |
|
|
Pan S (2011) |
201 [216] I1) 65 (39/26) I2) 65 (42/26) C) 65 (35/33) |
1. (42.6 ±11.2)
2. (18.6 ±17.7 wks) |
1. (43.2 ±11.5)
2. (18.6 ±17.7 wks) |
1. (45.0 ±11.8) |
BX (D, Bid) |
Esomeprazole 40 mg/ Qd (MA) |
1. Total integral of RDQ
2. TEE
3. AE |
1. P<0.01
2. P<0.05 (P=0.039) |
1. P<0.05 (P=0.023)
2. P<0.05 (P=0.007) |
1. P<0.05 (P=0.048)
2. P<0.05 (P=0.039) |
4 |
1) 연구 설계
최종 선정된 90편의 연구는 모두 중국에서 수행되었다. 4편은 학위논문, 나머지는 모두 중국저널에 실린 논문이었다. 87편이 2-arm study로, 한약 치료군과 양약치료군의 비교연구가 가장 높은 빈도를 차지하였으며(n=59), 다음으로 한약과 양약 병행치료군과 양약단독 치료군을 비교한 연구였다(n=28). 3-arm study는 3편으로, 모두 한약과 양약 병행치료군, 한약 단독 치료군, 양약 단독 치료군을 비교한 연구였다.
2) 연구 대상
(1) 진단 및 변증도구
대상 선정 시 西醫學 진단 기준으로 ≪反流性食管(炎)診斷及治療指南≫(n=16)이 가장 많이 사용되었으며, ≪胃食管反流病(中醫診療/中西醫結合)共識意見≫(n=12), ≪胃鏡檢査(确診)≫(n=12), ≪中國胃食管反流病(專家)共識意見(解讀)≫(n=9), ≪亞太地區GERD診治共識的標準≫(n=5), ≪美國洛杉磯世界胃腸病大會制訂的RE洛杉磯分類標準≫(n=3), ≪內科學≫(n=3)의 순서로 많이 사용되었으며, 이외에도 ≪簡明中西醫結合內科學≫(n=2), ≪食管疾病治療研討會製定的標準≫(n=1), ≪實用中西醫結合診斷治療學≫(n=1), ≪中國胃食管反流病共識意見專家組提出的診斷標準≫(n=1), ≪中藥新藥臨床研究指導原則≫(n=1), ≪中醫診斷與鑒別診斷學≫(n=1), ≪北京國際胃腸病學術會議提出的診斷標準≫(n=1) 등의 다양한 선정기준이 사용되었으며, 이외에도 임상증상에 의한 선정기준이 보고되었다.
中醫學(traditional Chinese medicine, TCM) 辨證 기준으로 ≪中醫病證診斷(療效)標准≫(n=11)가 가장 많이 사용되었으며, ≪胃食管反流病中醫診療專家共識意見≫(n=2)을 포함한 ≪胃食管反流病中西醫結合診療共識意見≫(n=7), ≪中藥新藥臨床硏究指導原則(標准)≫(n=6), ≪中醫內科學≫(n=5), ≪中醫內科疾病診療常規≫(n=2)의 순서로 많이 사용되었다. ≪胃院痛肝胃鬱熱性相關診斷標≫(n=2), ≪中國胃食管反流病共識意見≫(n=1), ≪中醫消化病診療指南≫(n=1), ≪簡明中西醫結合內科學≫(n=1), ≪中醫常見病症診療常規≫(n=1)와 같이 다양한 선정기준이 사용되었다.
(2) 배제기준
신체 혹은 정신적 질환과 동반된 GERD를 배제하기 위해 심혈관, 폐, 간, 신장 등의 주요 장기 및 혈관계 질환이 있는 경우, 소화기계의 암, 궤양 등의 질환과 분문(賁門)마비, 유문(幽門)경색, 십이지장궤양 등의 계통질환이 있는 경우, 소화기계 수술 과거력으로 위경검사를 진행할 수 없는 경우에 대상에서 배제하는 경우도 있었으며. 정신질환자, 임산부 및 수유 여성을 등을 배제 기준으로 제시하였다.
3) 치료개입 및 대조군
(1) 대상자 및 치료 기간
연구대상자 수는 38명에서 201명으로 다양하였다. 치료기간은 1 week에서 12 weeks까지 다양하였으며, 8 weeks(n=45)가 가장 많았으며, 4 weeks (n=27), 12weeks(n=3)와, 2 weeks(n=3), 1 week (n=2), 6 weeks(n=2) 순서로 많았다.
(2) 대조군
대조군은 모두 양약 치료군이었으며, 사용된 양약 종류에 따라 양약(西醫藥; Western Medicine, 이하 WM) 단일 제제(n=39), WM 2제제 복합 사용(n=47), WM 3제제 복합사용(n=4), 등으로 나눌 수 있으며, 단일제제 사용시 Rabeprazole(n=13), Ormeprazole(n=10), Cisapride(n=6)순서로 빈용 되었으며, 이외에도 Mosapride(Domperidone), esomeprazole, Pantoprazole, Lansoprazole, Ranitidine, Itopride hydrochloride, Hydrotalcite, Rebamipide, Flupentixol & Melitracen, Losec, Sucralfate 등이 사용되었다.
4) 결과변수
선정된 90편의 논문에서 측정된 결과변수는 유효율(effective rate)이 가장 많이 사용되었으며(n=106), 이 외에는 反流性疾病診斷問卷(reflux disease diagnostic questionnaire, RDQ)이용한 지표가 많이 사용되었다. 본 연구에서는 가장 많이 사용된 유효율을 중점으로 하여 논문을 분석하였으며, RDQ 등의 임상관련 지표에서는 反酸(acid reflux), 燒心(heartburn), 胸骨後疼痛(retrosternal pain), 反食(regurgitation)등의 빈용된 평가도구를 활용하여 메타분석을 시행하였다. 이 외에 臨床症狀評分標準(clinical symptom integrals) 症狀與體征消失時間比較(disappearance time of symptoms & signs) 등의 임상증상 관련 지표들이 사용되었으며, 胃鏡療效比較(total efficiency of endoscopy), 內鏡檢査總積分(curative effects of endoscopy), LES壓力比較差異均(pressure difference of LES) 등의 내시경관련 결과변수와 匹茲堡睡眠品質指數(Pittsburgh sleep quality Index, PSQI), 焦慮自評量表(self-rating anxiety scale SAS), 抑郁自評量表(self-rating depression scale, SDS), SF-36健康狀況調査表測定患者的生活質量(medical outcome survey 36-item short form, SF-36) {; 包括8個維度: 生理功能(physiological function, PF), 生理職能(role limitations caused by physical problems, RP), 軀體疼痛(bodily pain, BP), 活力(vitality, energy and fatigue, VT), 情感職能(role limitations caused by emotional problems, RE), 情感健康(mental health, MH), 社會功能(social function, SF), 總體健康(general health perceptions, GH), 醫院焦慮抑鬱量表(hospital anxiety and depression scale, HAD) 등이 있었다.
5) 이상반응 및 탈락 보고
대부분의 논문에서는 이상반응에 대한 언급이 없었으나, 선정된 90편의 논문 중 22편의 논문에서 이상반응에 대한 언급이 있었다. 한약 단독 또는 한약과 양약 병용치료군에서 이상반응은 腹瀉(diarrhea)가 가장 많았으며(n=12), 噁心 및 乾嘔를 포함한 嘔吐(nausea &vomiting)(n=5), 頭暈or頭昏(dizziness)(n=4), 乏力or疲勞(fatigue)(n=3), 頭痛(n=2), 腹脹(abdominal distension)(n=2), 大便粘液膿血(mucopurulent hematochezia), 胸悶(chest discomfort)(n=2), 口乾(dry mouth)(n=1), 皮疹(rash)(n=1)의 순서로 많았다. 양약단독 치료군에서도 腹瀉(diarrhea)가 가장 많았으며, 頭暈 또는 頭昏(dizziness)(n=9)이 다음 순서였으며, 噁心 및 乾嘔를 포함한 嘔吐(nausea &vomiting)(n=5), 乏力or疲勞(fatigue)(n=5), 頭昏(dizziness)(n=3), 腹脹(abdominal distension)(n=3), 腹痛(abdominal pain) (n=3), 皮疹(rash)(n=3), 胸悶(chest discomfort)(n=2)의 순서로 보고되었으며, 한약 치료군에 비해 肝酶升高(elevated liver enzyme) 및 轉氨酶升高(elevated transaminase)등의 lab검사상 이상반응(n=3) 및 納差(poor appetite) 및 納呆(anorexia)(n=2), 腰酸(soreness of waist)가 추가로 보고되었다. 양약단독 치료의 대조군과 비교하였을 때, 한약 단독치료군에서는 1편의 연구 73가, 한약과 양약의 병용 치료군에서는 2편의 연구 111, 127가 통계학적 차이가 없음(P>0.05)이 확인되었다. 7편의 연구 56,76,92, 119, 120, 130, 134는 언급이 없었으며, 이들을 제외한 나머지 12편의 연구에서는 통계학적으로 유의한 차이가 있는 것(P<0.05)으로 확인되었다. 추적조사(follow up, F/U)을 시행 및 재발률을 보고한 연구는 19편이었으며, 추적기간은 최단 1 month에서 최장 2 years로 다양하였다. 탈락에 대한 보고는 총 4편의 연구에서 보고하였으며, 그 중 2편은 탈락기준에 해당되는 환자가 존재하지 않아 탈락 환자수가 0명이었다. 재발률, 이상반응 및 탈락보고에 대한 자세한 내용은 Table 2- 5에서 확인할 수 있다.
Table 4
|
Study ID (year) |
Adverse event |
Intervention (number) |
Comparison (number) |
|
Chen JM (2018) |
噁心嘔吐 (nausea and vomiting) |
2 |
6 |
|
腹瀉腹痛 (diarrhea and abdominal pain) |
0 |
2 |
|
頭暈 (dizziness) |
1 |
4 |
|
|
Total |
3 |
12 |
|
|
Yang H (2018) |
頭痛 (headache) |
1 |
3 |
|
腹瀉 (diarrhea) |
1 |
5 |
|
皮疹 (rash) |
0 |
2 |
|
|
Total |
2 |
10 |
|
|
Liu Q (2018) |
頭痛 (headache) |
1 |
3 |
|
腹瀉 (diarrhea) |
2 |
5 |
|
皮疹 (rash) |
0 |
10 |
|
|
Total |
3 |
13 |
|
|
Li D (2017) |
排便增加, 輕微腹瀉 (increased defecation, mild diarrhea) |
1 |
|
|
頭昏腦脹 (dizziness and brain distention |
|
8 |
|
轉氨酶升高 (elevated transaminase) |
|
4 |
|
|
Total |
1 |
12 |
|
|
Chen J (2016) |
乏力 (fatigue) |
|
2 |
|
頭暈 (dizziness) |
|
1 |
|
皮疹 (rash) |
|
1 |
|
|
Total |
0 |
6 |
|
|
Sun Q (2016) |
腰酸 (soreness of waist) |
0 |
1 |
|
頭痛 (headache) |
0 |
1 |
|
噁心 (nausea) |
1 |
3 |
|
|
Total |
1 |
5 |
|
|
Lin MH (2016) |
腹瀉 (diarrhea) |
2 |
|
|
噁心 (nausea) |
|
3 |
|
頭暈 (dizziness) |
|
5 |
|
肝酶升高 (elevated liver enzyme) |
|
2 |
|
|
Total |
2 |
10 |
|
|
Tang L (2016) |
腹痛 (abdominal pain) |
|
4 |
|
腹瀉 (diarrhea) |
2 |
3 |
|
口乾 (dry mouth) |
1 |
1 |
|
胸悶 (chest tightness) |
1 |
2 |
|
皮疹 (rash) |
|
2 |
|
|
Total |
5 |
12 |
|
|
Li HP (2015) |
腹瀉 (diarrhea) |
8 |
6 |
|
Jiang LQ (2014) |
頭暈 (dizziness) |
|
|
|
乏力 (fatigue) |
|
|
|
腹瀉 (diarrhea) |
|
|
|
腹痛 (abdominal pain) |
|
|
|
|
Total |
0 |
6 |
|
|
Kang XQ (2014) |
腹脹 (abdominal distention) |
|
2 |
|
頭暈 (dizziness) |
|
1 |
|
輕微的噁心 (mild nausea) |
1 |
|
|
|
Total |
1 |
3 |
|
|
Zhang JW (2013) |
腹瀉 (diarrhea) |
1 |
|
|
粘液及脓血样便 (mucopurulent hematochezia) |
|
|
|
頭昏 (dizziness) |
|
7 |
|
轉氨酶升高 (elevated transaminase) |
|
4 |
|
|
Total |
1 |
11 |
|
|
Shi YP (2012) |
腹瀉 (diarrhea) |
1 |
2 |
|
乏力 (fatigue) |
2 |
|
|
納差 (poor appetite) |
|
3 |
|
|
Total |
3 |
5 |
|
|
Zhao XY (2018) |
噁心 (nausea) |
1 |
2 |
|
腹瀉 (diarrhea) |
0 |
3 |
|
嘔吐 (vomiting) |
0 |
3 |
|
|
Total |
1 |
8 |
|
|
Wang DS (2018) |
Total |
1 |
7 |
|
|
Wang ZB (2018) |
腹瀉 (diarrhea) |
1 |
5 |
|
頭暈 (dizziness) |
1 |
3 |
|
疲勞 (fatigue) |
1 |
10 |
|
|
Total |
3 |
12 |
|
|
Sun YF (2018) |
腹痛 (abdominal pain) |
1 |
2 |
|
腹瀉 (diarrhea) |
2 |
1 |
|
皮疹 (rash) |
2 |
1 |
|
胸悶 (chest tightness) |
1 |
1 |
|
口乾 (dry moth) |
1 |
|
|
|
Total |
7 |
5 |
|
|
Zhang LJ (2016) |
輕微的 噁心, 腹脹 (mild nausea, abdominal distention) |
3 |
2 |
|
Ruan SR (2015) |
腹瀉 (diarrhea) |
3 |
10 |
|
頭暈 (dizziness) |
1 |
3 |
|
疲勞 (fatigue) |
2 |
5 |
|
|
Total |
6 |
18 |
|
|
Tan ZX (2013) |
腹脹, 腹瀉 (abdominal distension, diarrhea) |
11 |
8 |
|
Cheng ZH (2011) |
噁心 (nausea) |
1 |
|
|
腹脹 (abdominal pain), 納呆 (anorexia) |
|
1 |
|
頭暈 (dizziness) |
|
1 |
|
|
Total |
1 |
2 |
|
|
Pan S (2011) |
大便粘液膿血 (mucopurulent hematochezia) |
3 |
|
|
噁心 (nausea) |
|
2 |
|
|
Total |
3 |
2 |
Table 5
|
Study ID (year) |
Drop out (I/C) |
Information |
|
|
Intervention |
Comparison |
|
He H (2016) |
n=6 (2/4) |
1. Poor compliance, treatment not in accordance with the doctor’s instructions
2. Withdrawal or loss of visit
3. Incomplete data affect the efficacy or index judgment |
|
|
Wang Y (2013) |
n=2 (1/1) |
Comparison of esophageal mucosal inflammation under endoscopy |
|
|
Cao C (2017) |
n=0 |
1. Patient withdraws or loses visit
2. Non-compliant patient
3. The doctor ordered the inclusion to withdraw |
|
|
Pan S (297) |
n=15 (12/3) |
<Drop out> 1. Lose visit (n=8)
2. Go out to work or move, unable to accept recheck (n=4) |
<Reject>
1. Diagnosis of colon cancer (n=1)
1. Diagnosed with diabetes (n=2) |
3. 치료결과의 정성적 분석
선정된 90편의 RCTs 연구들은 각 연구 특징에 따라 분석되었다. 중재와 대조군에 따라 3개의 상위 그룹을 나누고, 한약(traditional herb medicine, 이하 THM) 치료의 중재에 따라 하위그룹을 나누었다. 한약치료의 중재에서 辛開苦降法과 같이 논문에 치료법으로 기재되었으나 처방구성은 半夏瀉心湯의 기본방에 약재를 가감한 처방을 중재로 사용한 Sun 42-45 등의 연구는 BX (ST)의 하위그룹에 세분화하여 분류하였다. 1) THM vs WM
2) THM+WM vs WM
3) THM+WM vs THM vs WM
하위그룹을 나눈 후 연구대상, 중재, 치료방법 및 기간, 치료결과의 효과 크기 등의 상세내용을 Table 2, 3에 정리하였다. 대부분의 연구는 Effective rate를 사용하여 THM 단독 또는 THM+WM의 치료군과 WM 단독 치료의 대조군의 치료효과를 평가하였는데, 대부분의 연구는 통계학적으로 치료군이 대조군에 비해 통계학적으로 유의미한 치료효과를 보였으나, THM vs WM그룹에서는 7편의 연구 49-51,82,91,92, 102에서 통계적으로 차이가 없었으며, THM+WM vs WM의 그룹에서는 1편의 연구 127가, THM+WM vs THM vs WM의 그룹에서는 치료 8주후의 총유효율이 통계적으로 차이가 없음(P>0.05)을 Cao 150의 연구에서 확인되었다. 치료대상의 TCM 辨證 결과를 명시한 연구들에 대하여 다빈도를 중심으로 정리하였으며, 半夏, 黃芩, 人蔘, 甘草, 黃連, 大棗, 生薑, 乾薑을 半夏瀉心湯의 기본방으로 全載하여 한약치료의 중재 처방에 대하여 기본처방 구성 외의 가감 약재에 대해 사용 빈도별로 정리를 하였다( Table 6). 대부분의 연구들이 人蔘을 黨蔘(=蔓參)(n=37) 또는 太子參(n=13)으로 대체하였는데, 이는 가감 약재에서 제외하였다. 辨證은 寒熱錯雜型이 가장 많이 수록되었으며, 肝胃鬱熱, 胃熱熾盛, 寒邪犯胃 순서로 많았다. 가감 약재의 사용빈도는 蒲公英가 가장 높았으며, 白芨, 代赭石, 旋覆花, 吳茱萸의 순서로 많았다. 半夏瀉心湯의 기본 가감된 약재를 위주로 다빈도를 살펴보았을 때, 淸熱解毒 消腫散結 利尿通淋의 효능이 있으며, 肝胃에 歸經하는 蒲公英, 補肺 收斂止血 消腫生肌 斂瘡祛腐의 효능이 있으며, 肝胃肺에 歸經하는 白芨, 降逆止血 平肝潛陽하며 肝大腸心胃에 歸經하는 代赭石, 下氣 補中 降氣止嘔 開胃 軟堅消痞하며 大腸脾胃肺에 歸經하는 旋覆花, 溫中散寒 降逆 理氣燥濕祛痰止嘔의 효능이 있으며 肝脾腎胃로 귀경하는 吳茱萸의 순서로 빈용 되었는데, 이는 辨證의 인용도가 寒熱錯雜, 肝胃鬱熱, 胃熱熾盛, 寒邪犯胃의 순서로 나타난 것과 연관성이 있는 것으로 고려할 수 있다.
Table 6
Frequency of Traditional Chinese Medicine (TCM) Syndrome Differentiation & Added Medicinal Herbs
|
Counting |
TCM syndrome differentiation |
|
19 |
寒熱錯雜 |
|
|
6 |
肝胃鬱熱 |
|
|
4 |
胃熱熾盛, 寒邪犯胃 |
|
|
3 |
肝胃氣滯, 食滯胃腸, 胃失和降, 胃陰虧虛(不足), |
|
|
2 |
肝胃不和, 脾胃虛寒, 脾虛氣滯, 胃燥熱, 胃虛寒, 中虛氣滯 |
|
|
1 |
痰濕內阻, 脾胃氣滯, 脾虛肝鬱, 脾虛胃熱, 胃氣上逆 |
|
|
Counting |
Medicinal herbs |
|
|
15 |
蒲公英 (Taraxcum platycarpum) |
|
|
13 |
白芨 (Mletilla striata) |
|
|
11 |
代赭石 (Haematites), 旋覆花 (Inula japonica), 吳茱萸 (Evodia officinalis) |
|
|
10 |
枳實 (Poncirus trifoliata), 烏賊魚骨 & 海螵蛸 (Sepiella japonica Sasak & Sepia esculenta Hoyle (=Platysepia esculenta)) |
|
|
8 |
白芍藥 (Paeonia albiflora), 柴胡 (Bupleurum falcatum), 枳殼 (Citrus aurantium) |
|
|
6 |
三七根 (Panax notoginseng), (浙)貝母 (Fritillaria thunbergii) |
|
|
5 |
玄胡索(延胡索, 元胡) (Corydalis ternata), 瓜蔞 & 天花粉 (Trichosanthes kirilowii) |
|
|
4 |
瓦楞子 (Arca granosa Linne), 厚朴 (Magnolia obovata) |
|
|
3 |
降(眞)香 (Dalbergia odorifera T. Chen), 白朮 (Atractylodes ovata), 蘇葉 (Perilla frutescens var. acuta), 蘇梗 (Perilla frutescens var. crispa), 鬱金 (Curcuma longa), 竹茹 (Phyllostachys nigra), 黃芪 (Astragalus membranaceus) |
|
|
2 |
鷄內金 (Gallus gallus var. domesticus Brisson), 木香 (Saussurea lappa), 茯苓 (Poria cocos), 砂仁 (Amomum xanthioides), |
|
|
1 |
桔梗 (Platycodon grandiflorum), 蘿蔔子 (Raphanus sativus), 丹蔘 (Salvia miltiorrhiza), 沙參 (Adenophora triphylla var. japonica), 生地黃 (Rehmannia glutinosa (Gaertner) Libosch.), 連翹 (Forsythia suspensa), 薅田藨(茅莓根) (Rubus parvifolius L.), 珍珠 (Pinctada fucada), 陳皮 (Citrus reticulata Blanco), 山査(三仙) (Crataegus pinnatifida), 敗醬草 (Patrinia villosa (Thunb.) Juss), 荷葉 (Nelumbo nucifera), 香附子 (Cyperus rotundus) |
4. 메타분석
선정된 90개의 연구를 중재에 따라 하위그룹으로 분류하였으며, 메타분석 항목에 따라 하위그룹을 세분화 또는 통합하였다. 유효율, 위내시경검사상 총유효율, reflux disease diagnostic questionnaire (RDQ) 등의 평가도구에 따라 분류하여 시행하였다.
1) 총유효율
유효성을 평가하기 위한 양적 합성에 포함된 연구는 총 87이 포함되었으며, 중재의 유형에 따라 BX, BX(ST), BX+WM 등으로 정성적 분석에서 사용한 방법과 유사한 방법으로 하위그룹을 분류하였다. Cao 132, 134 등의 연구는 3-arm study로, THM vs WM와 THM+WM vs WM의 해당 하위그룹의 항목에 따라 결과값을 나누어 분석하였다.
Fig. 2-1
Forest plot of comparison: 1. total effective rate, outcome: 1.1 THM vs WM. 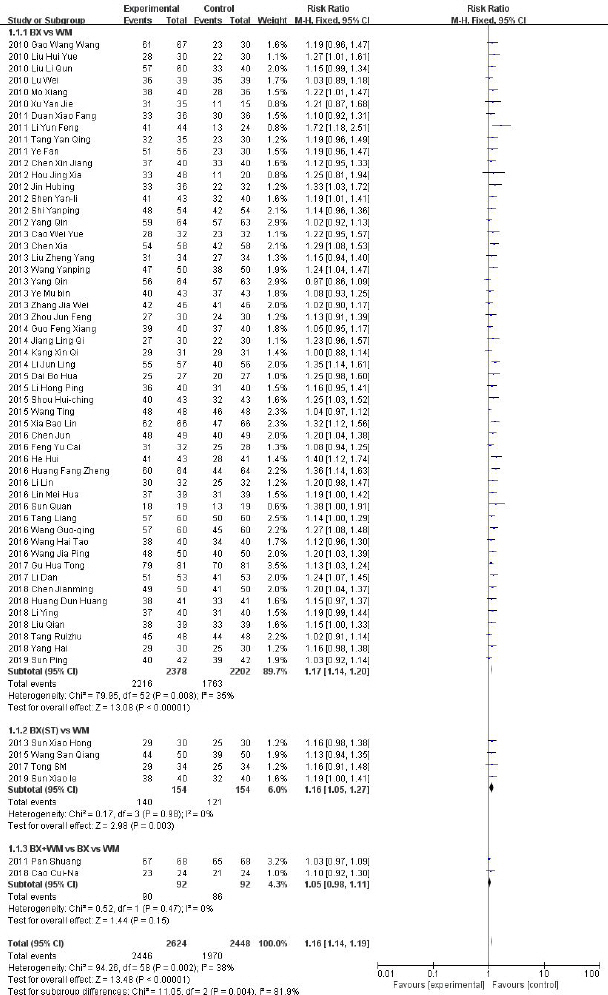
총 59편의 RCT 연구가 포함되었으며, 한약치료군은 양약치료의 대조군에 비해GERD의 유효율에 유의미한 효과를 보였다(N=4888, RR: 1.16, 95%, CI: 1.14 to 1.19, Ρ<0.00001, heterogeneity: χ2=94.26, Ρ=0.002, Ι2=38%).
치료군의 중재에 따라 하위그룹을 나누어 효과 크기를 산출하였을 때, BX(ST)vs WM, BX+WM vs BX vs WM하위그룹은 Ι2=0로 이질성이 상당히 감소하였고, BX vs WM의 하위그룹 또한 Ι2=35%로 이질성이 낮게 유지되었다.
Fig. 2-2
Forest plot of comparison: 1. total effective rate, outcome: 1.2 THM+WM vs WM. 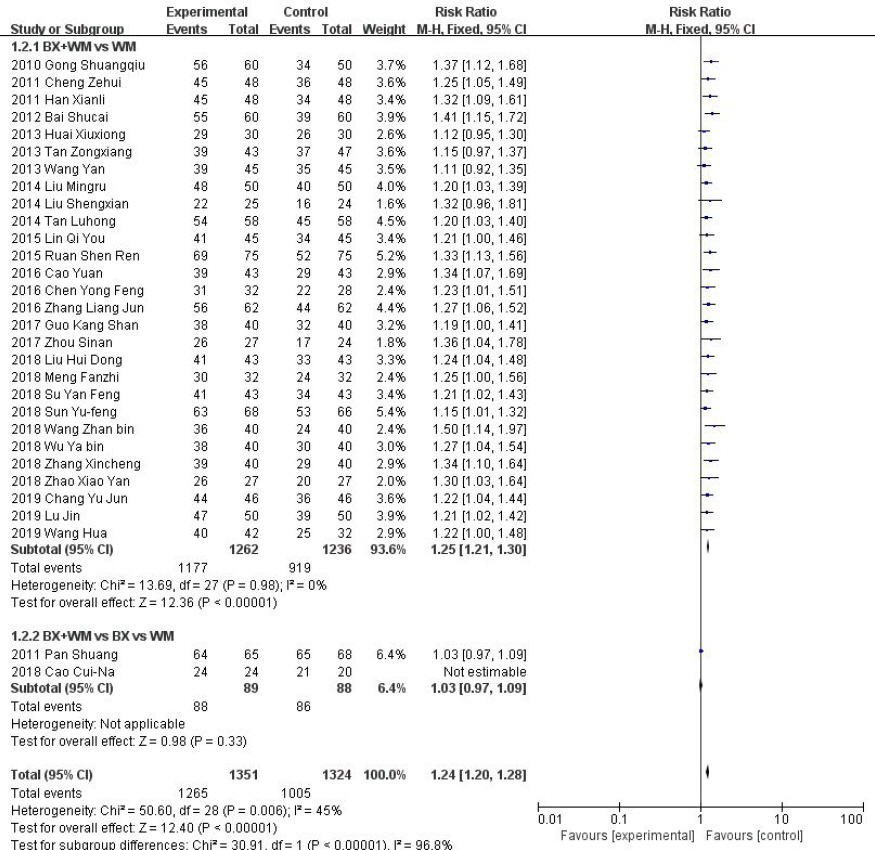
총 30편의 RCT 연구가 포함되었으며, 한약치료와 양약치료를 결합한 치료군은 양약 단독치료의 대조군에 비해 GERD의 유효율에 유의미한 결과를 보였다(N=2675, RR: 1.24, 95%, CI: 1.20 to 1.28, Ρ<0.00001, heterogeneity: χ2=50.60, Ρ=0.006, Ι2=45%). 치료군의 중재별로 하위그룹을 나누어 효과크기를 산출하였을 때, BX+WM vs WM의 하위그룹은 Ι2=0%로 연구간 이질성이 상당히 감소하는 결과를 얻을 수 있었다.
2) 치료기간(n=76)
4 weeks, 8 weeks, 12 weeks의 치료기간을 시행한 문헌을 해당 그룹을 나누어 분석하였다. 총 76편의 RCT 연구가 포함되었으며, 6~8주와 같이 치료기간이 명확하지 않은 Chen 117 등의 논문은 제외하였다. 치료기간에서 1주일은 7일, 1개월은 4주를 기준으로 하여, 30일은 4주, 60일은 8주 등으로 변환하여 치료기간에 따라 나누어 평가하였다. Cao 132, 134 등의 3-arm study 연구는 BX vs WM와 BX+WM vs WM로 해당 하위그룹의 항목에 따라 결과값을 나누어 분석하였다. 4, 8, 12 weeks의 치료기간 모두 한약과 양약 병용 치료 또는 한약 단독치료가 양약 단독 치료의 대조군보다 총유효율에 있어서 통계적으로 유의한 차이가 나타나(P<0.00001) 한약치료 시 치료기간 설정에 참고가 될 수 있을 것으로 사료된다.
Fig. 3-1
Forest plot of comparison: 2. total effective rate, outcome: treatment period (4 weeks). 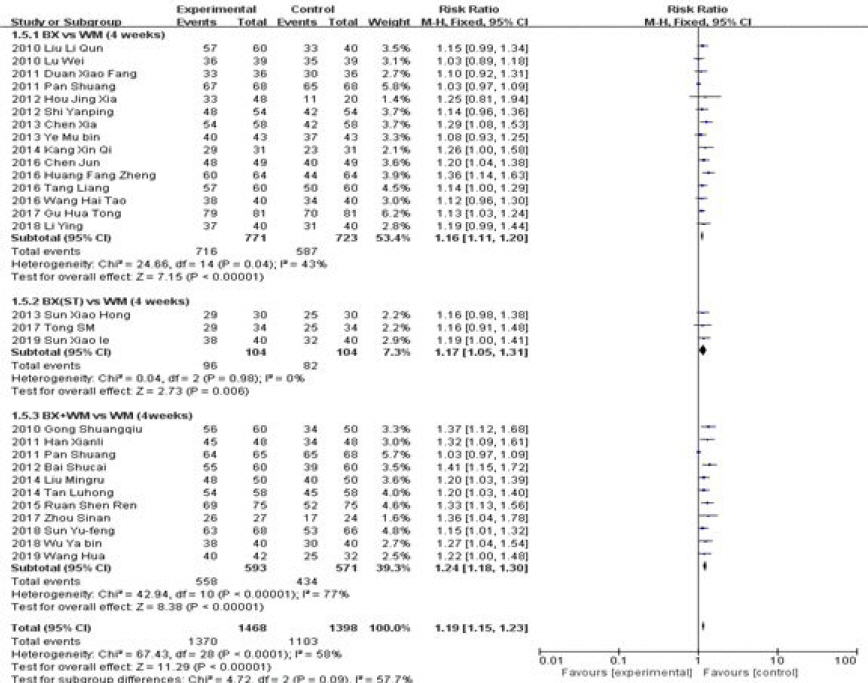
총 29편의 연구가 포함되었으며, 포함된 연구간의 이질성은 Ι2=58%로 약간 있는 것으로 평가되었다. BX vs WM과 BX+WM vs WM의 하의그룹으로 나누어 평가하였을 때, BX vs WM 그룹은 Ι2=43%로 이질성이 소폭 하락하였으며, BX+WM vs WM의 그룹은 Ι2=77%으로 연구간의 이질성이 높아지는 결과를 얻을 수 있었다.
Fig. 3-2
Forest plot of comparison: 2. total effective rate, outcome: treatment period (8 weeks). 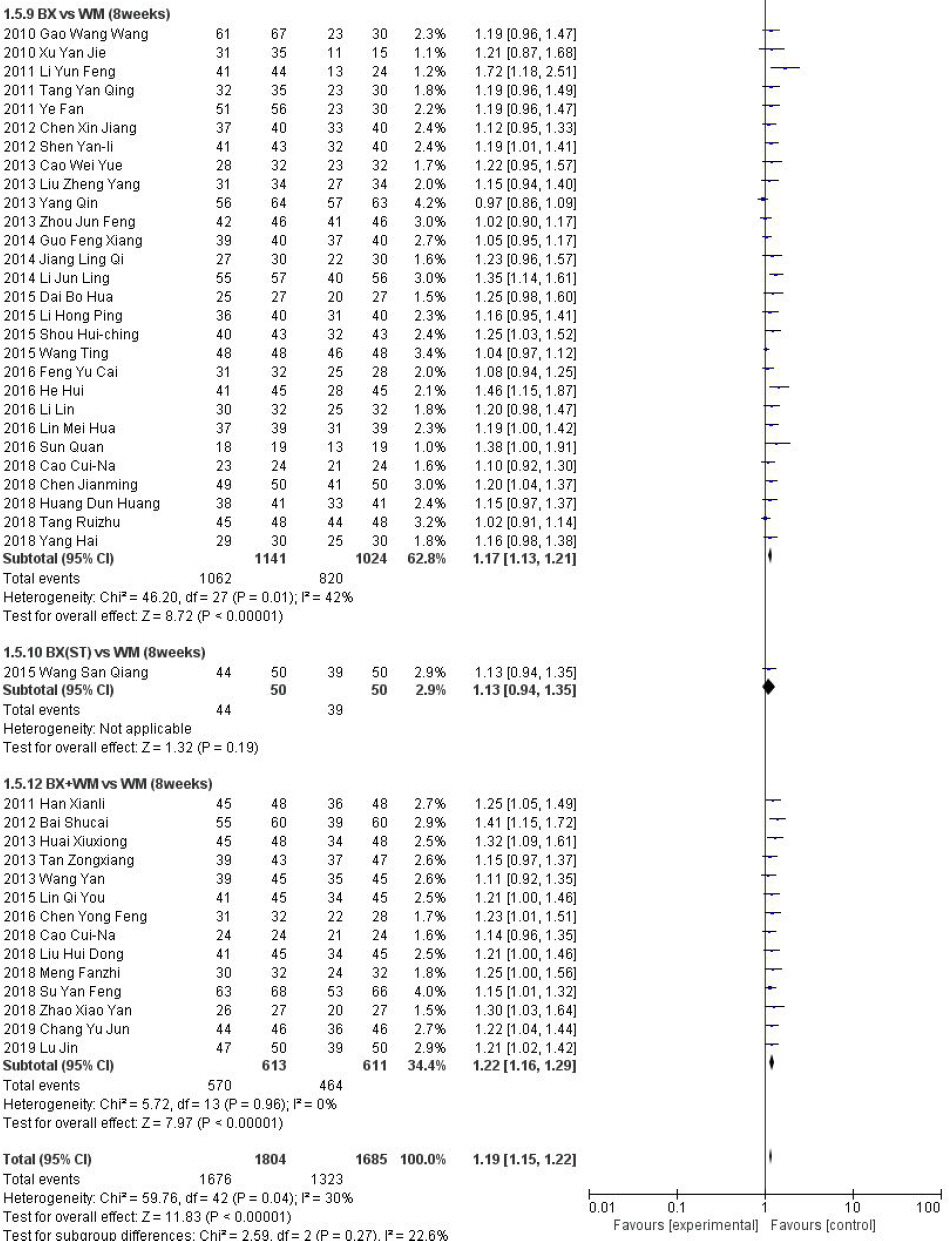
총 43편의 연구가 포함되었으며, 포함된 연구간의 이질성은 Ι2=39%로 낮았다. BX vs WM과 BX+WM vs WM으로 하위그룹을 나누어 평가하였을 때, BX vs WM 그룹은 Ι2=30%로 이질성이 낮게 유지되었으며, BX+WM vs WM의 그룹은 Ι2=0으로 이질성이 상당히 감소하는 결과를 얻을 수 있었다.
Fig. 3-3
Forest plot of comparison: 2. total effective rate, outcome: treatment period (12 weeks). 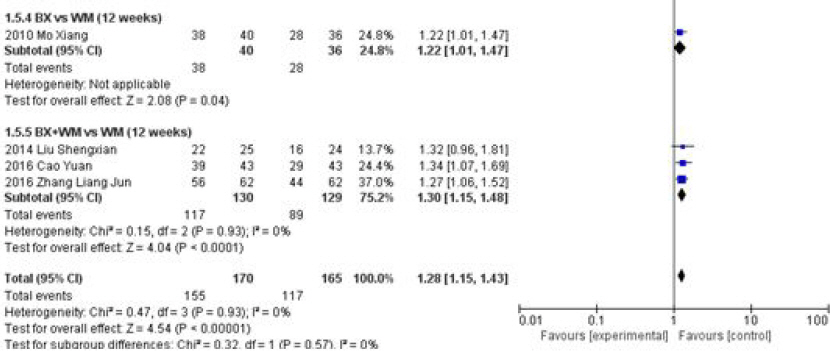
총 4편의 연구가 포함되었으며, 포함된 연구간의 이질성은 Ι2=0%으로 상당히 낮게 평가되었다. BX+WM vs WM의 하위그룹에 포함된 3편의 연구간 이질성 또한 Ι2=0%으로 낮게 유지되었다.
3) 대조군(n=86)
대조군에서 사용된 양약의 종류에 따라 단일 종류를 투약한 연구는 WM 1제제, 2가지 종류의 양약을 병용한 연구는 WM 2제제, 3가지의 양약을 병용한 연구는 WM 3제제로 분류하였으며, 양약의 용량 및 투여횟수와 상관없이 투여된 양약의 종류에 따라 하위그룹을 나누어 메타분석을 하였다. 대조군에서 Cisapride에 Omeprazole 또는 Lansonprazole을 선택하여 병용한 Jiang 75의 논문은 Cisapride+ Omeprazole 또는 Cisapride+Lansonprazole을 각각 몇 명의 환자에게 투약하였는지에 대한 명확한 정보가 없어 메타분석시 배제하였다. 3-arm study의 Cao 132, 134 등의 연구는 양약단독 치료를 시행한 대조군에서 모두 1가지의 양약을 사용하였으며, THM의 치료군과 THM+WM의 치료군을 치료군으로 통합하여 포괄, 산출하여 분석하였다.
Fig. 4-1
Forest plot of comparison: 3. total effective rate, outcome: Western medicine (1 medication). 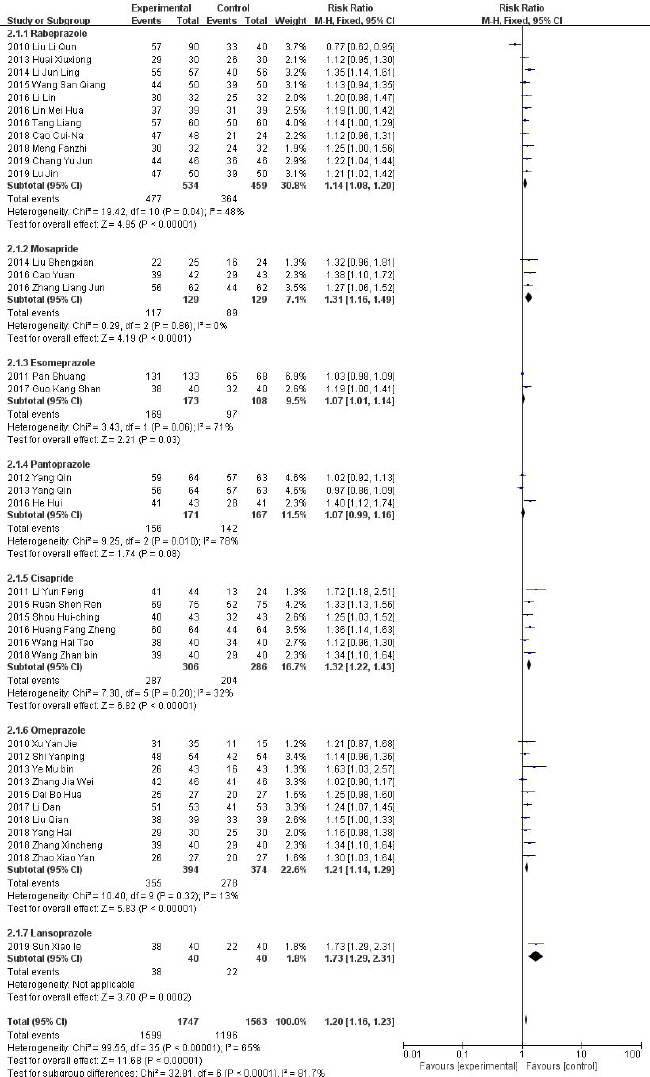
총 36편의 RCT 연구가 포함되었으며 한약 단독 또는 한약과 양약을 병행한 치료군은 양약단독 치료의 대조군에 비해 GERD의 유효율에 유의미한 효과를 보였다(N=3310, RR: 1.20, 95%, CI: 1.16 to 1.23, Ρ<0.00001, heterogeneity: χ2=99.55, Ρ<0.00001, Ι2=65%).
양약의 종류에 따라 7가지로 하위그룹을 나눌 수 있는데, Rabeprazole, Mosapride, Cisapride, Ormeprazole을 양약단독 치료로 사용한 하위그룹은 Ι2=48%, Ι2=0%, Ι2=32%, Ι2=13%로 연구간의 이질성이 감소하는 결과를 얻을 수 있었다.
Fig. 4-2
Forest plot of comparison: 3. total effective rate, outcome: Western medicine (2 medication). 
총 46편의 RCT 연구가 포함되었으며, 한약 단독 또는 한약과 양약을 병행한 치료군은 2가지 종류의 양약을 함께 사용한 양약치료 대조군에 비해 GERD의 유효율에 유의미한 효과를 보였다(N=3953, RR: 1.19, 95%, CI: 1.16 to 1.22, Ρ<0.00001, heterogeneity: χ2=57.23, Ρ=0.10, Ι2=21%). 14가지로 하위그룹을 나눌 수 있으며, 하위그룹에 1편의 연구가 포함된 6개의 하위그룹(Mosapride+Losec, Mosapride+Lansoprazole, Omeprazole+Rebamipide, Omeprazole+Flupentixol and Melitracen, Esomeprazole+Omeprazole, Cisapride+ Pantoprazole)을 제외한 8개의 하위그룹은 모두 연구간의 유의성이 낮게 평가되었으며, 그중 Motilium (Domperidone)+Omeprazole, Motilium (Domperidone)+ Ranitidine, Motilium (Domperidone)+Pantoprazole, Omeprazole+Itopride Hydrochloride, Omeprazole+ Cisapride의 5개의 하위그룹은 Ι2=0%로 연구간의 이질성이 상당히 감소하는 결과를 얻을 수 있었다.
Fig. 4-3
Forest plot of comparison: 3. total effective rate, outcome: Western medicine (3 medication). 
총 4개의 RCT 연구가 포함되었으며, 한약 단독 또는 한약과 양약을 병행한 치료군은 3가지 종류의 양약을 함께 사용한 양약치료 대조군에 비해 GERD의 유효율에 유의미한 효과를 보였다(N=346, RR: 1.17, 95%, CI: 1.07 to 1.27, Ρ=0.0004, heterogeneity: χ 2=0.42, Ρ=0.94, Ι 2=0%). Chen 90, Ye 94의 연구는 Rabeprazole, Motilium (Domperidone), Sucralfate의 3가지 종류의 양약을 병행 투여하였으며, 두 연구간의 이질성은 Ι 2=0%으로 낮게 유지되는 결과를 얻을 수 있었다.
4) Adverse event(Fig. 5)
Fig. 5
Forest plot of comparison: 4. adverse event. 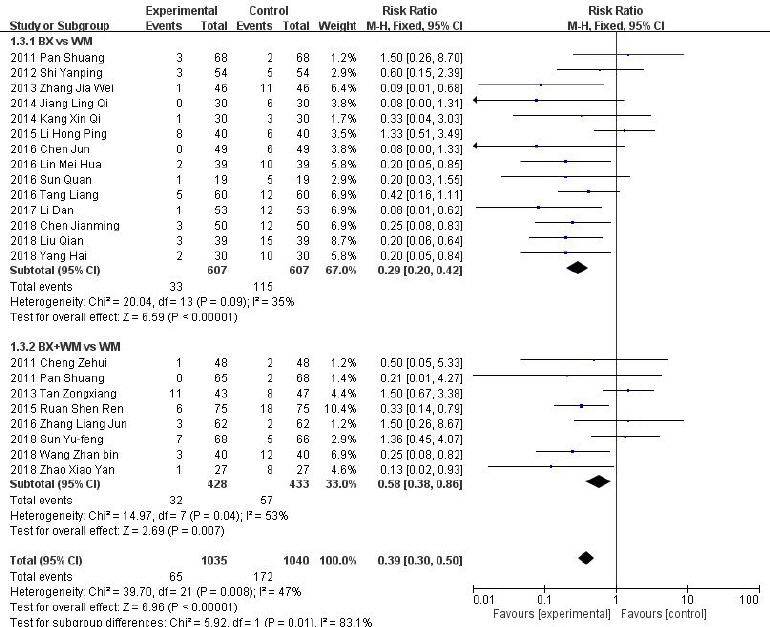
논문에서 부작용 사례를 기재한 연구는 총 22편의 RCT가 포함되었으며, Pan 134의 3-arm study는 BX vs WM, BX+WM vs WM의 하위그룹에 항목에 따라 결과값을 나누어 분석하였다. (1) BX vs WM
총 14편의 RCT 연구가 포함되었으며, 한약 단독 치료군은 양약단독 치료의 대조군에 비해 GERD의 부작용 발생률이 통계적으로 유의하게 적음을 알 수 있었다. 연구간의 이질성은 Ι2=35%로 낮게 평가되었다(N=1214, RR: 0.29 95%, CI: 0.20 to 0.42, Ρ<0.00001, heterogeneity: χ2=20.04, Ρ=0.09, Ι2=35%).
(2) BX+WM vs WM
총 8편의 RCT 연구가 포함되었으며, 한약과 양약을 병용한 치료군은 양약단독 치료의 대조군에 비해 GERD의 부작용 발생률이 통계적으로 유의하게 적음을 확인하였으며, 연구간의 이질성은 Ι2=53%로 약간 있는 것으로 평가되었다(N=851, RR: 0.58, 95%, CI: 0.38 to 0.86, Ρ=0.007, heterogeneity: χ2=14.97, Ρ=0.04, Ι2=53%).
5) Recurrence rate
총 19편의 RCT 연구에서 치료종료 후 추적 관찰하여 재발률을 확인하였다. 치료중재별 하위그룹과 추적기간별 하위그룹을 나누어 메타분석을 시행하였다.
Fig. 6-1
Forest plot of comparison: 5. recurrence rate: BX vs WM. 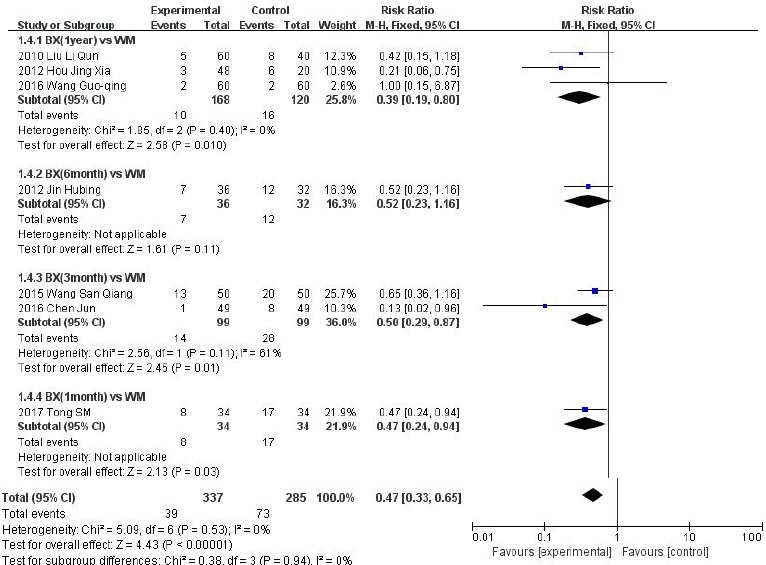
Fig. 6-2
Forest plot of comparison: 5. recurrence rate: BX+WM vs WM. 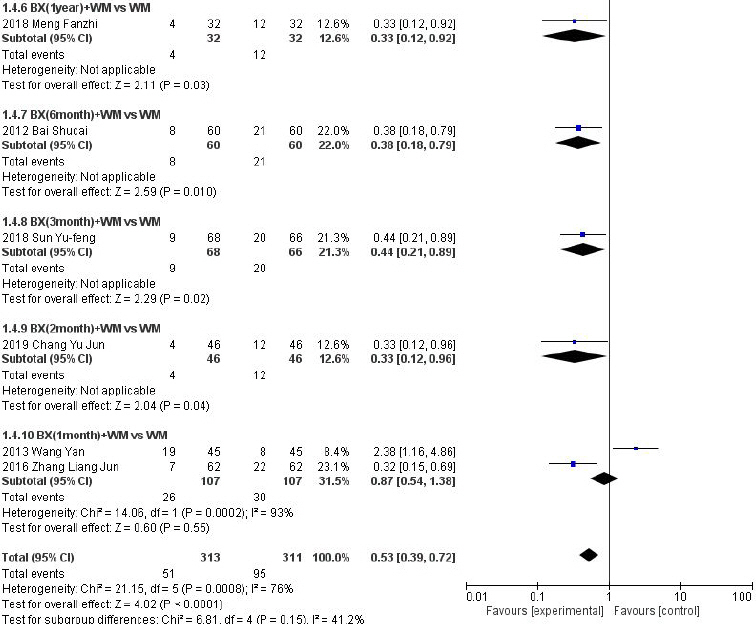
한약단독 또는 한약과 양약을 병행한 치료군은 양약 단독치료의 대조군에 비해 재발률이 통계적으로 유의하게 낮음을 확인하였으며, 연구간의 이질성이 Ι2=54%로 약간 있음을 확인할 수 있었다(N=1246, RR: 0.50, 95%, CI: 0.40 to 0.63, Ρ<0.00001, heterogeneity: χ2=26.35, Ρ=0.010, Ι2=54%). BX vs WM와 BX+WM vs WM의 두 그룹으로 나누어 평가하였을 때 한약 단독 치료군이 한약과 양약을 병행한 치료군보다 통계적으로 더욱 유의한 차이가 나타났다. BX vs WM의 그룹은 연구간의 이질성이 Ι2=0%로 상당히 감소되었으나(N=623, RR: 0.47, 95%, CI: 0.33 to 0.65, Ρ<0.00001, heterogeneity: χ2=5.09, Ρ=0.53, Ι2=0%), BX+WM vs WM의 그룹은 Ι2=76%로 연구간의 이질성이 높아지는 결과를 확인할 수 있었다(N=624, RR: 0.53, 95%, CI: 0.39 to 0.72, Ρ<0.0001, heterogeneity: χ2=21.15, Ρ=0.0008, Ι2=76%).
Fig. 6-3
Forest plot of comparison: 5. recurrence rate. 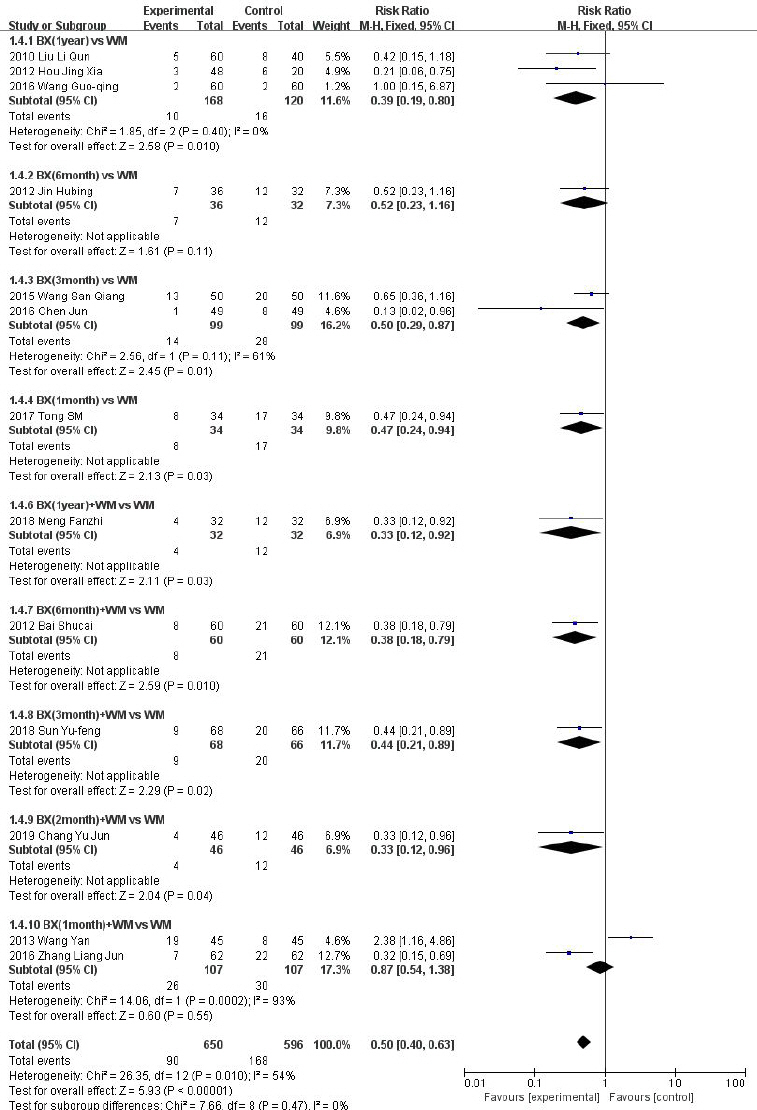
치료 후 추적기간에 따라 1 year, 6 months, 3 months, 2 months, 1 month의 하위그룹으로 나누어 메타분석을 시행하였다. 1 year, 6 months의 하위그룹은 Ι2=0% 연구간의 이질성이 상당히 낮게 평가되었으며, 3 months의 하위그룹 또한 Ι2=30%로 연구간의 이질성이 낮게 평가되었으나, 1 month 하위그룹의 연구간 이질성은 Ι2=88%로 높게 평가되며, 치료군에 비해 통계적으로 차이가 없는(P=0.10) 결과를 확인할 수 있었다.
6) Symptom scores of GERD
GERD에 대한 한약 및 양약의 치료효과 평가지표로 역류성질환 진단 설문지(reflux disease diagnostic questionnaire, RDQ) 또는 中醫症狀積分{traditional Chinese medicine (TCM) symptom scores}가 주로 사용되었으며, RDQ평가도구에는 증상의 총 점수 이외에 反酸(acid reflux), 燒心(heartburn), 胸骨後疼痛(retrosternal pain), 反食(regurgitation)의 4가지 주요증상에 대한 평가 항목도 포함되어 있다. 총 점수와 각 증상별로 그룹을 나누었으며, 중재에 따라 하위그룹으로 분류하였으며, 항목에 따라 하위그룹을 세분화 또는 통합, 재분류하여 메타분석 하였다.
Cao 132, 133 등의 3-arm study의 연구는 BX+WM vs BX vs WM의 하위그룹으로 나누었으며, Revman의 계산기 도구를 사용하여 한약단독 치료군과 한약과 양약 병용 치료군을 통합하여 산출하였다. Liu 등의 3편 118, 119, 122의 연구는 증상의 소멸시간(症狀與體征消失時間比較, comparison of the disappearance time of symptoms and signs)을 평가하여 별도로 분류하여 메타분석 하였다. 총 20편의 RCT 연구에서 치료 전후의 RDQ 총 점수 또는 TCM 증상, 임상증상 총 점수를 평가지표로 사용하였으며, 치료 전후의 反酸과 燒心의 증상점수를 평가한 연구는 22편, 胸骨後疼痛은 12편, 反食은 8편의 연구가 각각의 그룹에 속하였다. 각 증상별로 THM vs WM의 그룹과 THM+WM vs WM의 하위그룹으로 나누어 메타분석을 시행하였다.
Fig. 7-1
Forest plot of comparison: 6. treatment evaluation, outcome: the symptoms total scores comparison. 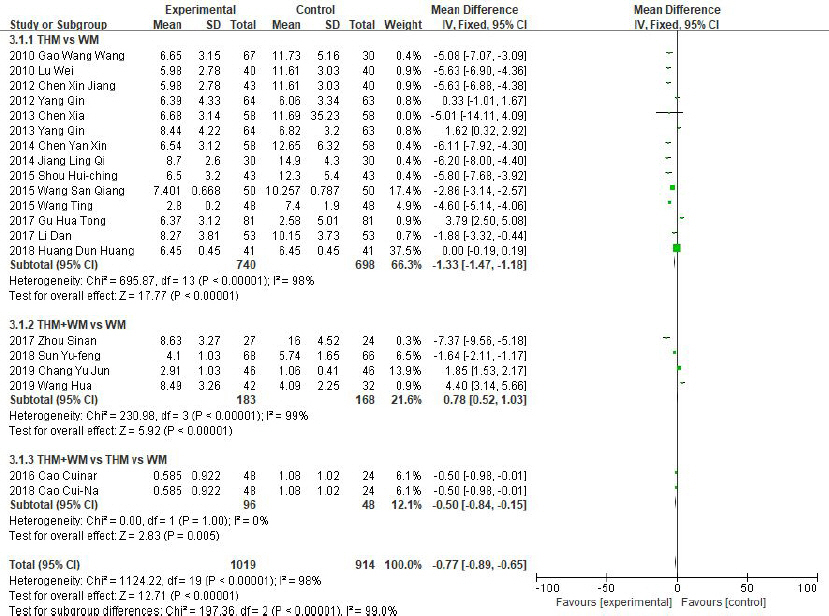
총 20편이 연구가 포함되었으며, 한약 단독 치료 및 한약과 양약을 병행한 치료군 모두 양약 단독 치료의 대조군보다 GERD 질환의 치료 후 증상 총점수에서 통계적으로 유의한 차이가 나타났다(N=1933, MD: -0.77, 95%, CI: -0.89 to -0.65, Ρ<0.00001, heterogeneity: χ2=1124.22, Ρ<0.00001, Ι2=98%). THM vs WM, THM+WM vs WM, THM+WM vs THM vs WM의 세 그룹으로 나누어 이질성을 평가하였을 때, THM vs WM, THM+WM vs WM의 두 그룹은 Ι2=98%, Ι2=99%로 연구간의 이질성이 높게 평가되었으며, THM+WM vs THM vs WM의 그룹은 Ι2=0%로 이질성이 낮게 평가되었다.
Fig. 7-2
Forest plot of comparison: 7. symptoms, outcome: 7.1 acid reflux. 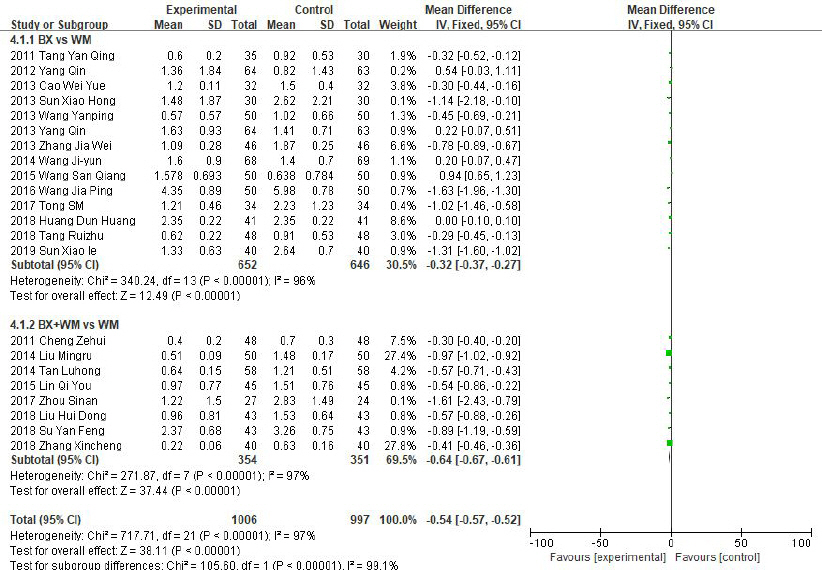
총 22편의 RCT 연구간의 이질성은 Ι2=97%로 높게 평가되었으나, 한약 단독 치료 또는 한약과 양약을 병용하여 치료한 치료군 모두 양약단독 치료의 대조군에 비해 反酸증상에서 통계적으로 유의한 차이가 나타났다(N=2003, MD: -0.54, 95%, CI: -0.57 to -0.52, Ρ<0.00001, heterogeneity: χ2=717.71, Ρ<0.00001, Ι2=97%). THM vs WM의 하위그룹에는 14편의 연구가, THM+WM vs WM의 하위그룹에는 8편의 연구가 포함되었으며, 각 그룹에 속하는 연구간의 이질성은 Ι2=96%, Ι2=97%로 높게 평가되었다.
Fig. 7-3
Forest plot of comparison: 7. symptoms, outcome: 7.2 hearburn. 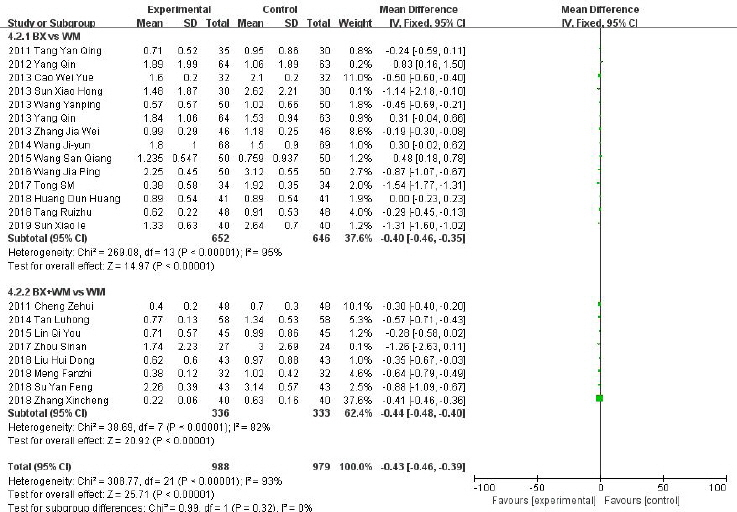
反酸와 유사하게 총 22편의 RCT 연구간의 이질성은 Ι2=93%로 높게 평가되었으나, 한약 단독 치료 또는 한약과 양약을 병용하여 치료한 치료군 모두 양약 단독 치료의 대조군에 비해 燒心 증상에서 통계적으로 유의한 차이가 나타났다(N=1958, MD: -0.43, 95%, CI: -0.46 to -0.39, Ρ<0.00001, heterogeneity: χ2=308.77, Ρ<0.00001, Ι2=93%). THM vs WM의 하위그룹에는 총 16편의 연구가 포함되었으며, 연구간의 이질성은 Ι2=95%로 높게 평가되었다. THM+WM vs WM의 하위그룹에는 총 12편의 연구가 포함되었으며, 연구간의 이질성은 Ι2=82%로 反酸에 속하는 전체 연구간의 이질성보다 수치는 하락하였으나, 여전히 높게 평가되었다.
Fig. 7-4
Forest plot of comparison: 7. symptoms, outcome: 7.3 retrosternal pain. 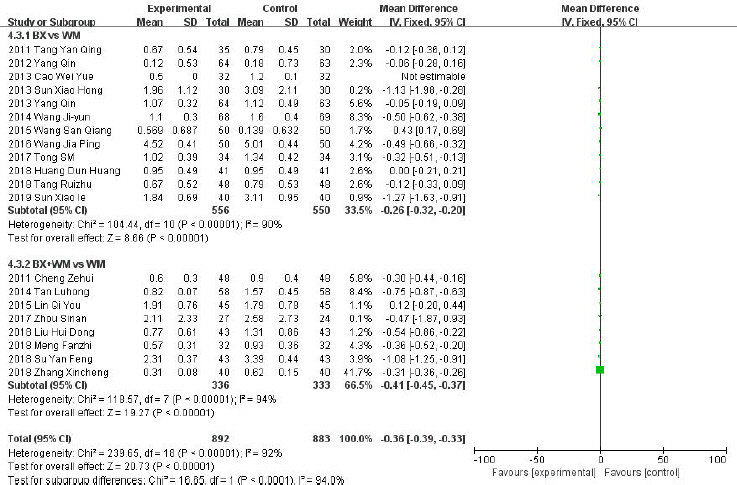
총 18편의 RCT 연구간의 이질성은 Ι2=92%로 높게 평가되었으나, 한약 단독 치료 또는 한약과 양약을 병용하여 치료한 치료군 모두 양약단독 치료의 대조군에 비해 燒心 증상에서 통계적으로 유의한 차이가 나타났다(N=1875, MD: -0.36, 95%, CI: -0.39 to -0.33, Ρ<0.00001, heterogeneity: χ2=239.65, Ρ<0.00001, Ι2=93%). 12편의 연구가 속한 THM vs WM과 6편의 연구가 속한 THM+WM vs WM의 그룹으로 분류하여 메타분석을 시행하였음에도 두 그룹 모두 연구간의 이질성이 Ι2=90%, Ι2=94%로 여전히 높게 평가되었다.
Fig. 7-5
Forest plot of comparison: 7. symptoms, outcome: 7.4 regurgitation. 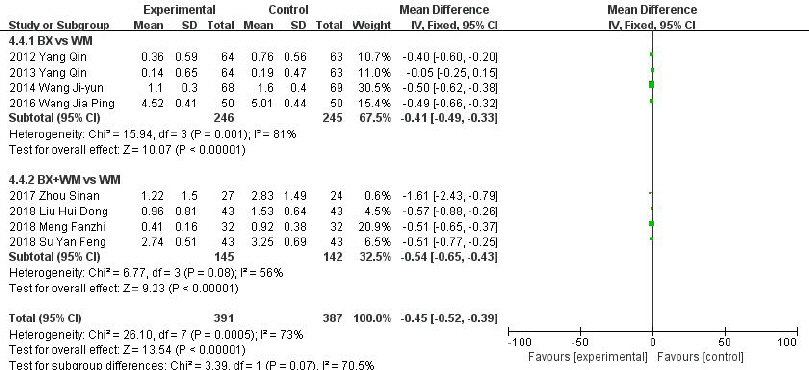
총 8편의 RCT 연구간의 이질성은 Ι2=73%로 높게 평가되었으나, 한약 단독 치료 또는 한약과 양약을 병용하여 치료한 치료군 모두 양약단독 치료의 대조군에 비해 反食 증상에서 통계적으로 유의한 차이가 나타났다(N=778, MD: -0.45, 95%, CI: -0.52 to -0.39, Ρ<0.00001, heterogeneity: χ2=26.10, Ρ=0.0005, Ι2=73%). THM vs WM, THM+WM vs WM의 하위그룹으로 분류하여 메타분석을 시행한 결과, 각각 4편의 연구가 그룹에 속하였으며, THM vs WM의 그룹에 속한 연구간의 이질성은 Ι2=81%로 수치가 더욱 상승하였으나, THM+WM vs WM의 그룹에 속한 연구간의 이질성은 Ι2=56% 감소하여 약간의 이질성이 있는 것으로 평가되었다.
(6) The disappearance time of symptoms and signs(n=3)( Fig. 7-6)
Fig. 7-6
Forest plot of comparison: 7. symptoms, outcome: 7.5 the disappearance time of symptoms and signs. 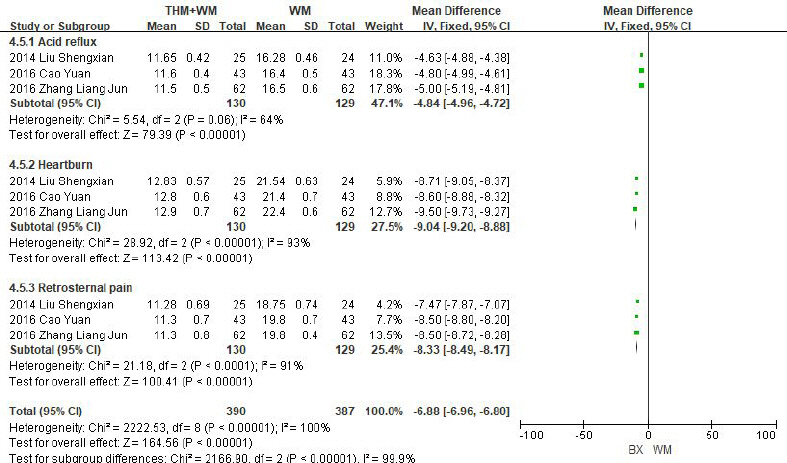
총 3편의 연구가 포함되었으며, 反酸, 燒心, 胸骨後疼痛의 3가지 증상의 증상 소실시간을 평가하였다. 3가지 증상 모두 증상에서 한약과 양약을 병용한 치료군은 양약 단독치료의 대조군보다 증상 소실시간이 통계적으로 유의한 차이가 나타났다(P<0.00001). 연구간의 이질성은 反酸은 Ι2=64%으로 약간의 이질성이 있는 것으로 평가되었고, 燒心 Ι2=93%, 胸骨後疼痛 Ι2=91%로 연구간의 이질성이 모두 높게 평가되었다.
7) Evaluation of GERD using endoscopy
GERD의 증상 평가 도구로 위내시경을 이용한 연구들도 다수 확인할 수 있었다. 먼저 위내시경상 0~2등급으로 증상 단계를 분류하고, 치료 전후의 변화정도(內鏡下反流性食管炎程度變化) 확인을 통해 증상 개선을 확인한 위내시경 총유효율(Total efficiency of endoscopy)로 증상을 평가한 THM vs WM에서는 14편 44,50,56,57,71,72,75,77,84,87,90,91, 102, 103, THM+WM vs WM에서는 4편 104, 105, 111, 115, THM+WM vs THM vs WM에서는 2편 132, 133으로 총 19편의 연구가 확인되었다. 또한, 위내시경상 점막 파손 정도에 따라 A-D의 등급을 분류한 후 치료 전후 비교를 통해 위내시경상 증상 총 점수(內鏡檢査總積分)로 증상을 평가한 Wang 등의 연구 44가 있었으며, Sun 45의 연구는 치료 후 LES의 압력변화(LES壓力比較差異均, pressure difference of LES)로 평가하였다(LES 정상 수치: 길이 2.7~4.8 cm,평균압력<15 mmHg (1 mmHg=0.133 kPa)). 하지만 위내시경 총유효율로 증상 개선도를 평가하는 기준에 대해 자세히 기록되어 있는 문헌 수가 적고, 문헌마다 위내시경상으로 분류한 등급 및 기준이 상이하며, 진단 시 기준으로 사용한 평가도구 지표들이 다양하여 메타분석을 시행하기에는 한계가 있었다.
5. 비뚤림 위험
1) 개별연구의 비뚤림 위험
코크란 비뚤림 위험(Cochrane’s Risk of Bias, RoB)을 이용하여 본 연구에서 선정된 90편의 모든 문헌에 대하여 RoB를 수행하였다( Fig. 8, 9).
Fig. 8
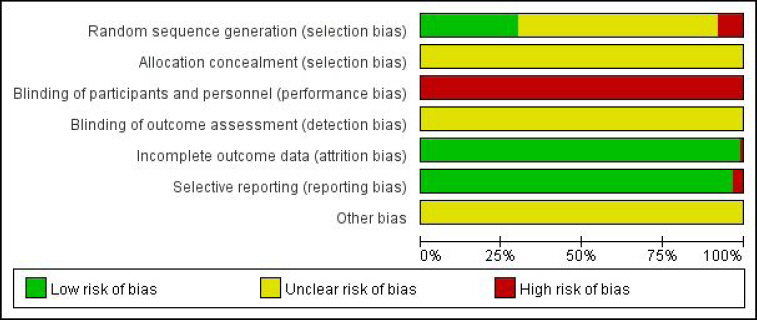
Fig. 9

(1) 선택 비뚤림
선택 비뚤림에서 난수표를 이용한 17편의 논문 49,51,56,59,66,68,90,91, 104, 106, 107, 115, 121, 124및 완전 무작위 추첨법을 사용한 4편의 논문 56,57,61, 127, 컴퓨터코딩의 방법을 이용한 1편의 논문 107과, 단순 무작위 배정(simple randomization)방법을 사용하였음을 기재한 2편의 논문 94, 127 등은 “Low risk”로 평가하였다. 진료 순서를 이용한 6편의 논문 78,81,82, 119, 132, 133은 “High risk”로 평가하였으며, 언급이 없거나 임의 배정을 시행한 논문은 “Unclear risk”로 평가하였다. 대부분의 연구는 눈가림(盲檢, blinding) 항목에 대한 언급이 없어 “Unclear risk”로 평가하였다. (2) 실행 비뚤림 및 결과확인 비뚤림
모든 연구에서 사용된 한약과 양약치료가 확연히 구별되는 중재의 특성상 연구대상자의 눈가림이 불가능하여 “High risk”로 평가였으며, 평가자의 배정 눈가림에 대한 기술이 없어 Unclear risk로 평가하였다.
(3) 탈락 비뚤림
불완전한 결과자료 항목에서는 대부분의 연구가 결측치가 없거나, 결측치 또는 탈락이 있을 경우 탈락에 대한 이유를 기재하고 통계적방법으로 보완하여 “Low risk”로 평가하였으나, Shi 92의 연구는 초록에 기재된 참여자수와 결과에 기재된 참여자수가 상이하나, 결측치 또는 탈락의 이유에 대한 언급이 없어 “High risk”로 평가하였다. (4) 결과보고 비뚤림
선택적 결과보고에 대한 비뚤림 항목에서는 유효율 또는 재발률 평가 및 보고 시 프로토콜 없이 선택적 보고를 한 논문 44, 132, 133은 “High risk”로 평가하였으나, 이 외의 대부분의 논문은 프로토콜을 사용하거나, 프로토콜은 없지만 사전에 계획된 것을 포함하여 예상되는 모든 결과를 보고하고 있어 “Low risk”로 평가하였다. (5) 그 외 비뚤림
기준선의 불균형, 데이터의 이질성 및 오염여부, 이해의 상충 등을 고려하였으며, 모든 연구에서 평가할 만한 충분한 정보나 근거가 대부분 존재하지 않아 “Unclear risk”로 평가하였다.
2) 출판 비뚤림
3-arm study는 THM vs WM과 THM+WM vs WM의 그룹에 나누어 분석하였다. 두 그룹 모두 Funnel plot( Fig 10-1, 10-2)에서 중대한 출판 비뚤림은 나타나지 않았다.
Fig. 10-1
Funnel plot for the outcome of effective rate (THM vs WM). 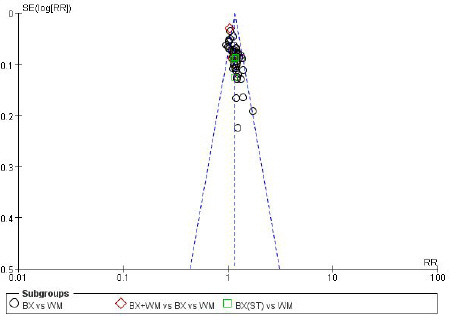
Fig. 10-2
Funnel plot for the outcome of effective rate (THM vs WM). 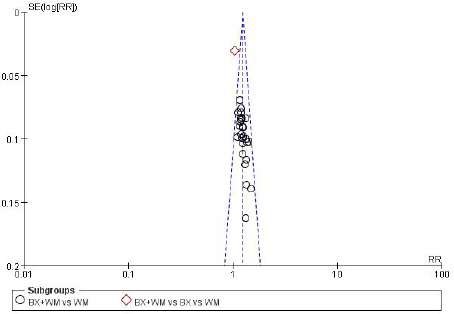
III. 고 찰
위식도 역류질환의 정의는 2006년 몬트리올 합의에서 내용물의 역류로 인하여 불편한 증상이나 합병증이 유발되는 경우’로 정의한 이후 135, 여러 지침에서 유사하게 정의하고 있다. 2012년 국내 임상진료지침에서도 GERD를 ‘위내용물이 식도로 역류하여 불편한 증상을 유발하거나 이로 인하여 합병증을 유발하는 질환’으로 정의하고 있다 136. GERD의 양약치료에 PPI 및 H 2receptor antagonist가 비용대비 효과면에서 우수하여 흔히 사용되나, 심한 식도염의 경우에는 치료효과가 만족스럽지 못하거나 재발의 빈도가 높다 137. PPI는 H 2receptor antagonist보다 위산의 분비를 억제하는 효과가 우수하여 GERD의 일차 치료제로 사용되고 있지만, 장시간 복용 유지 시 골절, 폐렴, 장관 내 감염의 위험도 증가의 부작용이 발생할 수 있으며, Clopidogrel(Plavix ®)와 같은 약제들의 상호작용에 대한 우려가 있음을 Yun 등의 연구에서 보고하였다 137. H 2receptor antagonist에 대한 2012년 국내 임상지침 136 및 WGO 임상진료지침 138에서는 H 2receptor antagonist는 간헐적인 위산 분비를 효과적으로 억제하여 위식도 역류 증상의 조절에 유용함을 권고하고 있다. 따라서 장기간 지속적으로 투약 시 효과가 떨어지며, 장기간 치료를 요하는 GERD의 치료시에는 PPI에 비해 상대적으로 필요성이 낮은 것을 확인할 수 있다. 2019년 발표된 최신 진료지침 고찰 139에 따르면 단기간 혹은 간헐적인 H 2receptor antagonist의 사용은 위산분비를 효과적으로 억제할 수 있기 때문에 PPI의 투약에도 불구하고 야간 산 분비 증가(nocturnal acid breakthrough) 및 야간 증상이 발생하는 환자에게 필요에 따라 자기 전에 H 2receptor antagonist를 추가 투여하는 것이 효과적인 전략이 될 수 있음을 제시하기도 하였으며, 두가지 대표적 약물 이외에도 제산제, 칼슘 경쟁적 산 분비 억제제(potassium- competitive acid blocker, P-CAB) 등의 약물을 GERD 약물치료 시 사용한다 139. 半夏瀉心湯은 ≪傷寒論≫의 <太陽病脈證辨治下>편 149번 조문에 최초로 수록되었으며, 和解劑 중 調和脾胃劑에 속하며, “脾胃不和 心下가 痞滿不痛 하고, 乾嘔 또는 嘔吐하며, 腸鳴下利, 舌苔가 薄黃膩 하고, 脈弦數한 등 증상을 치료하며, 임상에서는 急性胃腸炎, 慢性胃炎, 消化不良, 胃潰瘍 등의 질환에 사용한다.”고 ≪方劑學≫ 9에 기록되어 있다. 일본의 大塚敬節 ≪韓方治療實際≫에서 半夏瀉心湯을 食慾不振⋅嘔吐⋅惡心⋅下利 등의 소화기 질환과 더불어 부인과 질환(月經異常), 정형외과 질환(肩臂痛)에 사용된 증례를 제시하였다 140. 半夏瀉心湯의 처방구성을 살펴보면, 半夏는 辛溫有毒한 약으로 燥濕化痰 降逆止嘔 消痞散結의 효능을 가지고, 黃芩은 苦寒한 약재로, 淸熱燥濕瀉火解毒止血安胎의 효능이 있으며, 人蔘은 甘 微苦 微溫한 약재로 大補元氣 補脾益肺 生津止渴 安神增智하는 효능이 있으며, 乾薑은 辛溫한 약재로 溫經散寒 止血의 효능이 있으며, 甘草(炙)는 甘平하고 補中益氣의 효능이 있으며, 黃連은 苦寒하며 淸熱燥濕 瀉火解毒의 효능이 있다 141- 143. GERD에 대한 국내의 한약치료 관련 임상 연구로 식도 열공 탈장(hiatal hernia)을 동반한 위식도역류성 질환 환자의 치약 치험례 144, 위운동성 장애(gastric dysmotility)가 동반된 역류성식도염 환자에 대한 平胃散加味方 및 消積健脾丸, 침구치료 등을 포함한 한방단독 치험례 145, 소양인 망음증으로 진단한 역류성식도염 치험례 146, 熱多寒少湯으로 호전된 역류성식도염 환자 치험례 147의 연구가 있었다. 여러 한약 및 한약재를 사용한 실험연구가 대부분이었으며, GERD관련 체계적문헌 고찰 연구로 二陳湯加味方의 효과에 대한 문헌적 고찰과 28, 중국 논문을 중심으로 역류성식도염의 辨證과 처방에 관한 고찰 41연구가 있었다. 半夏瀉心湯의 임상연구 동향을 분석한 Jeon 29의 연구에 따르면, 국내외 12개의 임상 논문을 분석한 결과, 기능성소화불량, 소화성 궤양, 항암요법 부작용으로 인한 구내염 등의 목적으로 활용될 수 있는 임상적 근거가 구축되어 있으며, 그 중 기능성 소화불량과 관련하여서는 RCT 수준의 연구까지 진행된 바가 있고, 소화성 궤양에 대하여 다수 증례 분석과 소규모 임상시험 연구 수준에서 가능성을 보이고 있으므로 대조군을 이용한 임상시험 연구의 필요성이 있음을 밝혔다. 半夏瀉心湯의 효과를 입증한 실험 논문으로 흰쥐의 胃排出能에 대한 半夏瀉心湯의 效能 148의 실험연구에서 半夏瀉心湯은 흰쥐의 위 배출능을 증가시키는 효과가 있으며, 이러한 작용에 cholinergic pathway와 5-HT 3 receptor가 관여하는 것으로 생각되며, 특이 위의 수용성 이완장애가 있는 기능성 소화불량증 및 心下痞에 효과적으로 기대됨을 보고하였다. 관련 증례보고는 드물었으며, 체계적 문헌 고찰을 시행한 연구는 2011년 발표된 Choi 41 등의 논문이 1편 있었다. GERD에 대한 半夏瀉心湯의 빈번한 임상 활용에도 불구하고 체계적이고 객관적인 근거자료가 부족한 실정으로, Choi 41의 연구에서 중국 논문 검색을 중심으로 진행한 체계적 문헌 고찰 이후 최근 10년간의 GERD에 半夏瀉心湯을 이용한 한약치료에 대한 동향을 살펴보기 위하여 체계적 문헌 고찰 및 메타연구를 진행하였다. 유효성을 평가하기 위해 CNKI의 데이터베이스로부터 최근 10년간의 연구동향을 살펴보기 위해 2010년1월부터 2020년 1월까지의 자료를 취합하였다. 선정된 연구는 90편의 RCT 연구로, 이를 분석한 결과는 다음과 같다.
첫째, 본 연구의 치료방법은 半夏瀉心湯의 단독 또는 가감을 중재로 하는 한약 단독 치료와 양약의 단독 치료군 비교연구가 69편, 한약과 양약 병용치료군과 양약의 단독치료군의 비교연구는 28편, 한약과 양약 병용치료군과 한약 단독치료군, 양약 단독치료군을 비교한 3-arm study의 연구는 3편이었다.
둘째, 치료기간 및 대상자수는 다양하였으며, 모든 대조군은 양약을 투여하였으며, 중재에 따라 단일제제, 2제제 복합사용, 3제제 복합사용으로 나눌 수 있는데, 단일제제 사용시 Rabeprazole, Ormeprazole, Cisapride의 순서로 다용 되는 것을 알 수 있다.
셋째, 이상반응 및 부작용에 대해서 90편의 논문 중 22편(24.44%)에서 보고하였으나, 이상반응 정도는 경미하였으며, 통계적으로도 대조군에 비해 유의한 차이가 있었다. 또한, 대부분 특별한 추가 처치 없이 시간이 경과함에 따라 호전되는 양상이었다. 이는 한약 치료가 양약치료에 비해 안전하며, 심각한 부작용이 발생하지 않음을 보여주는 근거자료가 될 것으로 사료된다.
넷째, 유효율이 가장 다빈도로 결과변수로 사용되었으며, RDQ 등의 증상평가지수, 胃鏡療效比較 등의 내시경관련 결과변수 등의 다양한 결과변수를 사용하였으며, 대상 선정 및 배제기준에서 西醫學 선정기준으로는 ≪反流性食管(炎)診斷及治療指南≫, 中醫學 선정기준으로는 ≪中醫病證診斷(療效)標准≫이 가장 많이 사용되었으며 외에도 다양한 진단기준이 사용되었다.
본 연구의 디자인 상의 특성은 다음과 같다. 첫째, GERD에 대한 半夏瀉心湯 한약의 효과를 무작위 배정을 통해 대조군과 비교 조사하였다.
둘째, 선정된 연구는 ‘胃脘痛’, ‘嘔吐’, ‘呑酸’, ‘胸痛’, ‘嘈雜’ 등의 범주로 분류하여 치료하였으며, 제시된 한약은 모두 辨證에 따라 선별된 것으로, 辨證은 총 19가지가 추출되었고, ‘肝, 膽, 脾, 胃’를 주요 病因으로 구체화하는 경향성을 보였다. 그 중 寒熱錯雜이 가장 많았으며, 肝胃鬱熱, 肝胃不和, 胃熱熾盛, 寒邪犯胃의 순서로 인용도를 보였다. 寒, 熱, 虛, 實의 病因에 따른 유사辨證을 모아 寒熱錯雜에는 脾虛濕熱, 中虛氣滯, 實, 熱에는 肝胃鬱熱, 膽熱犯胃, 肝胃不和, 肝胃氣滯, 胃熱熾盛, 食滯胃腸, 氣鬱痰阻, 瘀血阻絡, 虛, 寒에는 胃陰虧虛(不足), 脾胃虛寒, 胃失和降, 寒邪犯胃으로 요약할 수 있다. 寒熱錯雜 다음으로 肝胃鬱熱의 인용빈도가 높은데, 이는 GERD의 초기병증으로 볼 수 있으며, 脾와 肝의 관계 149로 인해 肝氣上逆함으로 胃氣가 乘降失調하여 虛弱, 瘀血, 痰飮, 濕熱, 癰疽 등을 유발할 수 있어 GERD 환자의 초기치료에 특히 중요한 것으로 사료된다. 辨證별로 그 治法을 살펴보면 肝胃不和은 疏肝利膽 和胃降逆, 脾胃濕熱은 淸熱化濕 和胃降逆, 脾胃虛弱은 益氣建脾 和胃降逆, 胃陰不足은 滋陰淸熱 和胃降逆, 脾虛痰鬱은 淸熱化痰 和胃降逆, 氣滯血瘀은 活血化瘀 和胃降逆, 脾胃虛寒은 溫中健脾 和胃降逆으로 기본적으로 和胃降逆을 바탕으로 하여 병인과 관계하여 治法을 더함을 알 수 있다. 본 연구에 포함된 연구 중에서 중재방법과 평가지표가 동일한 무작위 임상연구들을 메타분석 하였으며, 이질성 높을 경우 이질성 해소를 위하여 한약 또는 양약의 중재에 따라 하위그룹으로 재 분류하여 분석하였다. Effective rate를 비교한 연구에서 한약의 단독 치료 또는 양약의 병용치료는 양약단독 치료에 비해 통계적으로 유의한 차이가 존재하였으며(P<0.00001), 이를 통해 GERD 증상에 半夏瀉心湯 한약이 유의미한 효과가 있음을 알 수 있었다. Total integral of RDQ or TCM syndromes 및 acid reflux, heartburn, retrosternal pain, regurgitation 등의 GERD의 대표적인 증상 별 평가점수지표의 항목에 대하여 메타분석을 시행할 결과, 대부분의 연구간 이질성은 높은 편이었으나, 한약단독 또는 한약과 양약의 병용치료군이 양약단독 치료에 비해 통계적으로 차이가 있음을 확인할 수 있었다(P<0.00001). GERD의 증상 평가 도구로 위내시경을 이용한 연구들도 다수 확인할 수 있었다. 하지만 증상 개선도를 평가하는 기준에 대해 자세히 기록되어 있는 문헌 수가 적고, 문헌마다 위내시경상의 등급이 상이함과 같이 진단기준 방법이 다양하여 메타분석을 시행하기에는 한계가 있었다.
비뚤림 위험에 대한 평가에서 배정방법과 배정순서 은폐, 평가자의 눈가림, 선택적 결과보고에서 비뚤림을 최소화하기 위한 방법이 기술되어 있는 연구가 적어 비뚤림을 판단하기에 한계점이 있었고, 향후 무작위 임상연구에서는 비뚤림을 줄이기 위한 방법에 대해 좀 더 구체적이고 명확한 서술이 필요할 것으로 사료된다. 또한 실행 비뚤림의 경우 한약의 제형 및 香味의 특성상 양약치료와 확연이 구별되는 중재 어려움이 있어 연구 참여자의 눈가림을 시행하기 어려운 측면이 있다.
본 연구는 가장 근거 수준이 높은 연구인 체계적 문헌 고찰을 수행하였으며, 포함된 문헌수가 많아 다양한 방법으로 분석을 시행할 수 있다는 것이 장점이다. 하지만, CNKI위주의 제한적 검색이 이루어졌으며, 본 연구에 선정된 90편의 연구는 모두 중국어를 이용하여 중국에서 출판된 문헌으로 언어 해석의 문제로 인한 언어편향이 존재할 가능성이 있다. 또한, 분석한 연구의 질이 비교적 낮으며, 메타분석 결과 많은 항목에서 이질성이 나타난 것이 한계점이다.
분석한 연구의 질이 낮은 측면은 다음과 같다. 먼저, 90편의 연구에 대한 비뚤림 연구에 대하여 상위 기재한 바와 같이 한약제제의 특성상 눈가림 배정을 시행하기 어려워 ‘high risk’로 일반화하기에 불충분한 측면이 있다. 둘째, 각 RCT 연구에 포함된 半夏瀉心湯에 대해서도 변증 및 증상에 따라 다양한 약재들이 가감, 합방되었으므로 어떠한 mechanism으로 효과가 있는지는 설명하기 어려운 점이 있다. 셋째, 이상반응 및 부작용에 대한 보고한 연구들이 24편 있었으나, 전체 포함된 90편의 RCTs연구 중 22.23%으로 과반수를 넘지 않았다. 마지막으로, 각 연구들의 설계를 비교하였을 때 처방 및 복용량, 치료기간, 환자들의 병정기간이 상이한 점과 증상 평가 방법 및 점수 측정방법 등의 진단 기준에 대한 기술이 상세히 되어 있지 않는 점과 같이 논문들의 질이 전반적으로 낮아 메타분석의 비교 결과 신뢰도는 불명확하였다. 이에 따라 다양하게 하위그룹을 나누어 메타분석을 시행하여 한약 및 양약병용 치료 또는 한약 단독 치료가 양약 단독 치료의 대조군에 대해 통계적으로 총유효율 및 부작용 또는 이상반응 발생이 유의한 차이가 있음을 확인할 수 있었으나, 한약 단독 치료와 한약과 양약을 병용한 치료군 중 어느 집단이 총유효율이 우수하며, 부작용 또는 이상반응 발생률이 적은지를 확인하기에는 한계가 있었다.
이와 같은 한계점들을 개선하기 위하여 향후 半夏瀉心湯의 GERD에 대한 효과와 관련된 체계적 문헌 고찰 연구에서는 중국 및 국내 뿐 아니라 국외 문헌을 통해 연구의 질이 비교적 높은 연구들을 분석하여 연구의 신뢰도를 높일 뿐 아니라, 한약치료의 효과를 더욱 명확하게 입증할 수 있는 연구가 필요할 것으로 사료 된다. 또한, 수준 높은 무작위 배정 시험을 시행하기 위해서는 위약(placebo) 한약의 개발을 통한 눈가림의 구현은 필수적인 요소로, 향후 시행될 무작위배정연구에서 충분히 고려해야할 측면으로 사료된다. 더불어 다양한 방법으로 비뚤림 위험을 최소화하여 양질의 임상연구가 이루어지기 위한 노력이 필요할 것으로 사료된다. 그리고 半夏瀉心湯의 GERD에 대한 mechanism 및 한약과 양약 사이의 상호작용에 대한 추가적인 약리학적 연구의 수행이 필요할 것이며, 이는 본 연구와 유사한 체계적 문헌 고찰과 더불어 다양한 실험 및 다수의 임상연구의 축적을 통해 근거를 보완할 필요성이 있는 것으로 사료된다.
V. 결 론
본 연구는 중국 및 한국에서의 GERD환자를 대상으로 半夏瀉心湯의 효과 및 최신동향을 확인하기 위해 기존에 시행된 RCT연구를 통해 체계적 문헌 고찰을 시행하였다. 半夏瀉心湯은 GERD에 대하여 유의미한 효과가 있음을 알 수 있으며, 또한 이상반응 및 부작용은 양약치료에 비해 낮음을 확인할 수 있다. 이는 GERD에 대해 半夏瀉心湯의 임상적 효과를 입증할 뿐 아니라, 임상에서도 GERD의 한의치료를 단독으로 또는 양약과 병용하는 치료를 시행할 경우 낮은 부작용으로 높은 치료효과를 나타낼 수 있음을 시사할 수 있다. 향후 본 연구를 토대로 GERD에 대한 半夏瀉心湯 및 한약처방, 나아가 효과 입증을 통한 GERD 뿐 아니라 다양한 질환에 대해 半夏瀉心湯의 처방이 적극적으로 이루어지는 발판이 되기를 바라며, 본 연구가 임상 진료 지침의 확립에 객관적이고 체계적인 유용한 근거 자료가 될 것으로 기대한다.
참고문헌
1. 손 여원. 위식도역류질환 치료제 임상시험 가이 드라인. 식품 의약품 안전평가원. 의약품심사부 소화계약품과 2015:
2. Kang SY. A review on clinical studies of acupuncture and moxibustion therapy for gastroesophageal reflux disease in China by searching CAJ. Korean J of Acupucture 2015:12(1):1–12.   3. Choi YJ, Jung TY, Lim SC. Inhibitory Effecs of Naegwan-acupuncture (PC6) on acute reflux esophagitis Rat. Journal of Korean Acupunbture & Moxibustion Medicine Society 2013:30(2):31–41.
4. 전국 한의과대학 비계내과학교실. 비계내과학 서울: 군자출판사: 2008.
5. Jung HK, Hong SJ, Jo YJ, Jeon SW, Cho YK, Lee KJ, et al. Updated guidelines 2012 for gastroesophageal reflux disease. Korean J Gastroenterol 2012:60(4):195–218.   6. Fitoshi S. Pathophysiology로 이해하는 내과학 6 권 서울: 도서출판 정담: 2002:54–5.
7. Moon JJ, Ahn GS, Kim SH, Park JH, Kim DH, Choi DY, et al. ShangHanLunJengHae Seoul: Publication HanEuiMunHwaSa: 2010. p. 317–9.
8. Lee SI. ShinGobangchancha Seoul: Publication Gunja: 2012. p. 267–8.
9. 한의과대학방제학교수 共編著. 方劑學 서울: 대성문화사: 1993:112–3. 116-7.
10. Naito T, Itoh H, Uasunaga F, Takeyama M. Hange-shashin-to raises levls of smatostatin, motilin, and gastrin in the plasma of healthy subjects. Biol Pharm Bull 2002:25(3):327–31.   11. Jang MW, Lim SW. Experimental study for Effect of Banhasasim-tang on Mice with Reflux esophagitis. Korean J Orient Int MED 2013:34(4):362–74.
12. Hwang GY, Kim DJ, Byun JS. Effects of Yijin- tang-gamibang Extracts on Reflux Esophagitis. Korean J Oriental Psysiology & Pathology 2006:23(4):1073–9.
13. Choi BH, Kim DJ, Byun JS. Suppressive Effects of Yijintang-gamibang on Reflux Esophagitis. Korean J Oriental Psysiology & Pathology 2010:31(5):64–81.
14. Park K, Kwak MA, Kim DJ, Byun JS. Protective Effects of Yijin-tang-gamibang Aqueous Extracts on Reflux Esophagitis Mediated by Antioxidant Defense Systems. Korean J Oriental Psysiology & Pathology 2010:24(3):416–25.
15. Kim HJ, Lim SY, Kwak MA, Kim DJ, Byun JS. Effects of Yijintang-gamibang on Reflux Esophagitis Induced by Pylorus and Forestomach Ligation in Rat. Korean J Orient Int Med 2010:31(1):128–41.
16. Lee ST, Kwak MA. Effects of Individual Herbal Components of Yijintang-gamibang in the Rat Reflux Esophagitis. Korean J Orient Int Med 2013:34(2):165–77.
17. Lee YJ, Park JH, Rho SS. Effects on Rats with Reflux Esophagitis Treated with LoniceraeFlos Extract. Korean J Orient Int Med 2010:24(6):970–5.
18. Kim DJ, Rho SS. Effect on Acute reflux Esophagitis by Evodiae Fructus Aquous Extract. Kor J Herbol 2012:27(1):51–8.  19. Lee JA, Park HJ, Kim SH, Kim MJ, Kim KJ, Shin MR, et al. Evaluation of Evodiae Fructus Extract on the Chronic Acid Reflux Esophagitis in Rats. Kor J Herbol 2019:34(2):15–23.
20. Kim SH, Roh SS, Lee JA, Shin MR, Lee AR, Koo JS, et al. Improving Effects on Rats with Chronic Acid Reflux Esophagitis Treated of CoptidisRhizoma Extract. Kor J Herbol 2019:34(1):117–24.
21. Lee JY, Seo BI, Roh SS. Improving effect of ArtemisiaeCapillarisHerba extract in reflux esophagitis rats. Kor J Herbol 2016:31(6):37–44.  22. Shim MH, Kim ES, Lee YS. Suppressive Effects of UlmiPumilae Cortex Extracts on the Reflux Esophagitis in Rat. J Physiol & Pathol Korean Med 2016:30(4):257–65.  23. Song CH, Baek TH. A Comparative Study of SepiaeOs, Arcae Concha, Ostreae Concha and Esomeprazole in a Mouse Model of Reflux Esophagitis. J Korean Med 2018:39(2):92–105.   24. Lee SH, Baik TH. Comparative Study on the Effects of Pinelliaternata, Zingiber officinale and Sobanhatang on Reflux Esophagitis. J Korean Med 2019:40(2):17–34.   25. Kwon OJ, Lee AR, Roh SS. Improving Effects on Rats with Reflux Esophagitis Treated with Combined Extract of Young persimmon fruit and Citrus peel. Kor J Herbal 2016:31(1):25–31.  26. Kim MY, Shin YO, Lee JY, Lee AR, Shin SH, Kwon OJ, et al. Improving Effect of a Combined Extract of Rhei Rhizoma and Glycyrrhizae Rhizoma through Anti-oxidative Stress in Reflux Esophagitis rats. Kor J Herbol 2015:30(4):37–44.   27. Shin MK, Kim ES, Kim TR, Lim HC, Lee YS. Effects of Jwa Kum-Whan on Reflux Esophagitis in Rats. Korean J Orient Int Med 2016:37(3):495–7.
28. Kim KH, Lee JH, Cho CK, Yoo HW, Lee YW. The Literatual Study of Yijin-tang-gamibang Effects on Reflux Esophagitis. Institute of Korean medicine, Daejeon University 2013:22(1):119–28.
29. Jeon SY, Kim WB, Seok EJ, Song SY, Jeong JG, Lee SI. An analysis of clinical studies on Banha-Sasim-Tang. Herbal Fomula Science 2018:26(3):267–81.
30. Ahn SB, Lee GY, Hwang HH, Jeong MJ, Jang IH. The Effect of Banhasasim-tang in the Treatment of Chemotherapy-induced Symptoms:A systemic Review. J Int Korean Med 2019:40(4):663–74.   31. Park JW, Ko SJ, Han GJ, Yeo IK, Ryu BH, Kim JS. The effects of banha-sasim-tang on dyspeptic symptoms and gastric motility in cases of functional dyspepsia;a randomized, double-blind, placebo-controlled, and two-center trial. Evid Based Complement Alternat Med 2013:2013:265035.   32. Yoon SH, Ryu BH, Ryu KW, Kim JS. Evaluation for therapeutic effectiveness of Banshwasashim-tang in functional dyspepsia. Korean J Orient Int Med 2003:24(3):329–36.
33. Park GH, Choi SW, Park SJ, Joo JC, Park HS. Three Case Reports of Peptic Ulcer Patients Treated with Banhasasim-tang. Korean J Oriental Psysiology & Pathology 2012:26(6):940–6.
34. Han IS, Choi JH, Lim SW. A Study on the Defence Effect of Banhasasim-tang for White Rat's Acute Duodenal Injury. J Korean Oreintal Med 2002:23(3):188–9.
35. Lee GK, Cui X, Lim JP. Effect of the Concurrent Administration of Banhasasim-tang with Cimetidine on Gastric Ulcer in Rats. Korean J Oriental Psysiology & Pathology 2012:16(3):572–6.
36. Cho TK, Lee C, Lee HJ, Yim YK. The Anti-emetic Effect of Banhasasim-tang Intravenous Herbal Acupuncture in MTX-induced Rat-Pica Model. J of Korean Med 2017:38(1):34–5.   37. Shin MK, Hwang HJ, Kim SC, Byun JS. Effect of Banhasasim-tang on the Cardiac Toxicity and clinical symptom induced by Doxorubicin. Herbal formula science 2002:10(1):131–42.
38. Hwang HJ, Shin MK, Kwak MA, Lee YH, Byun JS, Kim SC. Effect of Banhasasim-tang on the Hepatic and Splenic Toxicity induced by Doxorubicin. J of Kor Oriental Oncology 2002:8(1):9–21.
39. Ju WS, Park HJ, Yun BG, Jun SY, Park SD. Effect of Banhasasimtang on carbon tetrachloride induced hepatoxicity in rats. Kor J Herbal 1999:14(2):51–9.
40. Gi SO, Lee SB, So HS, Kim HR, Lee YR, Lee GS, et al. Inhibitory Effects of Banhasasim-tang Extracts on Cisplatin-induced Nephrotoxicity in Mouse Model. Korean J Oriental Psysiology & Pathology 2018:32(5):328–32.
41. Choi GY, Sun SH, Kim BW, Lee SJ, Oh HS, Han IS, et al. Literature Review on Syndrome Differentiation and Herbal Medicine of Reflex Esophagitis - Focusing on Chinese Journals. Korean J Orient Med 2011:32(1):75–86.
42. Sun XL. The curative effect observation of BanxiaXiexin Decoction Combined with the method of reducing the pain, opening the pain and reducing the pain in the treatment of gastroesophageal reflux disease. Guide of China Medicine 2019:17(25):167.
43. Tong SM. Clinical study on the treatment of reflux esophagitis with xinkaikujiang method. Asia-Pacific Traditonal Medicine 2017:13(14):113–4.
44. Wang SQ. Literature and clinical application of Hefa in the treatment of reflux esophagitis. Dept. of Clinical Chinese Medicine Graduate School, Beijing University of Chinese medicine 2015:
45. Sun XH, Niu R, Yang JQ, Shi HX, Zhang Y, Liu T, et al. Clinical observation on 60 cases of gastroesophageal reflux disease treated by xinkaikujiang method. Global Chinese Medicine 2013:6(S1):76–7.
46. Kim SY, Park JE, Seo HJ, Lee YJ, Jang HB, Son HJ, et al. NECA's guidance for undertaking systematic reviews and meta-analyses for intervention Seoul: National Evidence-based Healthcare Collaborating Agency: 2011. p. 64.
47. Wiggins JPT, Altman DG, Sterne JAC. In : Higgines JPT, Green S, editors. Chapter S:assising risk of bias in included studies. Chochrane handbook for systematic rivies of interventions version 5.1.0 [updated March 2011]. The cochrane collaboration 2011Availabe from: http://handbook.cochrane.org/. 48. Lee JY. Meta-analysis. Korean Journal of Endocrinology 2008:23(6):361–78.  49. Sun P, Tian XD, Li YL. Study on the Effects of BanxiaXiexin Tang on Esophageal Dynamics in Gastroesophageal Reflux Disease Patients. Western Journal of Traditional Chinese Medicine 2019:11(32):98–101.
50. Huang DH, Wu YN, Chen YB, Cao J. Clinical observation on the treatment of 41 cases of gastroesophageal reflux disease of cold and heat type by Decoction of Pinellia and Xiexin. Traditional Chinese Medicine Journal 2018:17(3):57–9.
51. Tang RZ, Fu XY, Liang SQ, Chen FL, Li X, Liang WG. Treatment of Reflux Esophagitis with BanxiaXiexin Decoction. Modern Hospitals 2018:18(6):910–2.
52. Chen JM, Feng HS, Chen CX. Analysis of Cost-effectiveness of Banxiaxiexin Decoction in Treating Reflux Esophagitis and Evaluation of Adverse Drug Adverse Reaction. Pharmacy Today 2018:28(4):273–5.
53. Yang H, Liang XM. To analyze the clinical effect of BanxiaXiexin Decoction in the treatment of reflux esophagitis and the improvement of symptom score. Journal of Clinical Medical 2018:5(84):60.
54. Li Y. Analysis of the therapeutic effect of BanxiaXiexin Decoction on reflux esophagitis. Contemporary Medical Symposium 2018:16(4):211–2.
55. Liu Qian. The Clinical Value of Modified BanxiaXiexin Decoction in Treating Reflux Esophagitis. World composite medicine 2018:4(2):7–9.
56. Li D, Gu ZJ. Therapeutic effect of BanxiaXiexin Decoction on gastroesophageal reflux disease. Shaanxi Journal of Traditional Chinese Medicine 2017:38(7):903–4.
57. Gu HT. Clinical analysis of BanxiaXiexin Decoction on 58 cases of gastroesophageal reflux disease. Guide of China Medicine 2017:15(29):192–3.
58. Huang FZ. Treatment of 64 cases of reflux esophagitis with qigesan and Banxiaxiexin Decoction. Guangming Tradit Chin Med 2016:31(23):3461–2.
59. He H, Han XF. Clinical observation on BanxiaXiexin Decoction in the treatment of non-erosive reflux disease. Zhejiang J Tradit Chin Med 2016:51(1):27–8.
60. Chen J. Effect of BanxiaXiexin Decoction in the Treatment of Reflux Esophagitis. China health standard management 2016:7(36):120–3.
61. Feng YC. Therapeutic effect of BanxiaXiexin Decoction on 32 cases of reflux esophagitis. Inner Mongolia J Tradit Chin Med 2016:
62. Sun Q. Application and effect of BanxiaXiexin Decoction in the treatment of reflux esophagitis. Health way 2016:15(12):2229–30.
63. Lin L. Clinical observation on 32 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. Heilongjiang Journal of Traditional Chinese Medicine 2016:3:19.
64. Wang GQ. Efficacy Observation of Banxiaxiexin Soup Modified Treatment of Reflux Esophagitis. China & Foreign Medical Treatment 2016:1:150–1.
65. Wang HT. Effect of BanxiaXiexin Decoction on gastroesophageal reflux. The Medical Forum 2016:20(12):1670–1.
66. Wang JP, Zhou WT, Gu RY, Song GH, Liu HM. Clinical observation of BanxiaXiexin Decoction in the treatment of gastroesophageal reflux disease. Journal of Emergency in Traditional Chinese Medicine 2016:25(9):1828–9.
67. Lim MH. Clinical effect of BanxiaXiexin Decoction on gastroesophageal reflux disease. Journal of North Pharmacy 2016:13(10):93–4.
68. Tang L, Liu X, Li XY. Clinical effect of BanxiaXiexin Decoction on gastroesophageal reflux syndrome of phlegm dampness syndrome. Internal medicine 2016:11(5):778–80.
69. Xia BL. Clinical analysis of BanxiaXiexin Decoction in the treatment of reflux esophagitis. Mod Diagn Treat 2015:26(15):3404–5.
70. Dai BH, Zou LM. Clinical effects of the BanxinaXiexin decoction on gastroesophageal reflux disease. Clinical Journal of Chinese Medicine 2015:7(17):117.
71. Wang T. To observe the clinical effect of Banxiaxiexin decoction in treatment of gastroesophageal reflux disease. Inner Mongolia J Tradit Chin Med 2015:12:12–3.
72. Shou HC. Efficacy of the BanxiaXiexin decoction on gastroesophageal reflux disease. Clinical Journal of Chinese Medicine 2015:7(22):102–3.
73. Li HP. Therapeutic effect of BanxiaXiexin Decoction on gastroesophageal reflux disease. J MED Theor & Orac 2015:28(19):2636–7.
74. Guo FX. Therapeutic effect of BanxiaXiexin Decoction on reflux esophagitis of liver stomach stagnant heat type. Guide of China Medicine 2014:12(32):276–7.
75. Jiang LQ. 30 cases of gastroesophageal reflux disease treated with traditional Chinese Medicine. Chinese Medicine Modern Distance Education of China 2014:
76. Kang XQ, Kang Z, Liu L. Clinical manifestations of BanxiaXiexin Decoction in the treatment of reflux esophagitis. Guide of China Medicine 2014:12(4):183–4.
77. Chen YX. Clinical evaluation of the efficacy of BanxiaXiexin decoction on 58 cases with gastroesophageal reflux. Clinical Journal of Chinese Medicine 2014:6(12):20–1.  78. Wang JY. Influences of modified BanxiaXiexin Tang on symptoms and quality of life in patients with non-erosive reflux disease. Chinese Journal of Basic Medicine in Traditional Chinese Medicine 2014:20(11):1562–4.
79. Li JL. Clinical Observation on 113 Cases of Gastroesophageal Reflux Treated with BanxiaXiexin Decoction. Clinical Journal of Chinese Medicine (CJCM) 2014:6(3):109–10.
80. Zhou JF. Treating 30 cases of senile reflux esophagitis with the BanxiaXiexin decoction. Clinical Journal of Chinese Medicine (CJCM) 2013:5(17):92–3.
81. Liu ZY. 68 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. J Shaanxi Coll Tradit Chin Med 2013:36(3):51.
82. Zhang JW. Clinical effect of BanxiaXiexin Decoction on gastroesophageal reflux disease. Dept. of Clinical Chinese Medicine Graduate School, Beijing University of Chinese medicine 2013:
83. Ye MB. Observation of BanxiaXiexin Decoction on gastroesophageal reflux disease. Journal of Qiqihar University of Medicine 2013:34(5):671–2.
84. Chen X. Clinical curative effec of the BanxiXiexin decoction on treating 58 cases of GERD. Clinical Journal of Chinese Medicine 2013:5(15):32–3.
85. Cao WY. 32 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. Chin J Interg Trad West Med Dig 2013:21(3):155–6.
86. Wang YP, Yang H. Therapeutic effect of traditional Chinese medicine on gastroesophageal reflux disease. Chinese Journal of Trauma and Disability Medicine 2013:13(21):9–10.
87. Yang Q, Li JX, Li XH. Influences of modified BanxiaXiexin Tang on symptoms and quality of life in patients with non-erosive reflux disease. Journal of Beijing University of Traditional Chinese Medicine 2013:36(4):280–4.
88. Hou JX. 48 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. Henan Tradit Chin Med 2012:32(8):971–2.
89. Shen YL. BanxiaXiexin Tang in Treating Reflux Esophagitis Curative Effect Observation. Journal of Liaoning University of TCM 2012:14(8):180–1.
90. Chen XJ. Observation of BanxiaXiexin Decoction on gastroesophageal reflux disease. Strait Pharm J 2012:24(11):133–4.
91. Yang Q, Li JX, Li XG. Therapeutic effect of BanxiaXiexin Decoction on non-erosive reflux disease. Jilin Journal of Traditional Chinese Medicine 2012:32(9):907–10.
92. Shi YP. Clinical Observation of Banxiaxiexin Decoction in Treatment of Bile Reflux Esophagitis. Chinese Journal of Medicinal Guide 2012:15(5):823–4.
93. Jin HB. 36 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. Chinese community doctors (Medical Major) 2012:14(333):182–3.
94. Ye F. 56 cases of gastroesophageal reflux disease treated with BanxiaXiexin Decoction. Chinese Medicine Modern Distance Education of China 2011:9(3):92–3.
95. Li YF. 44 cases of gastroesophageal reflux disease treated with BanxiaXiexin Decoction. J Pract Tradit Chin Med 2011:27(11):747.
96. Tang YQ. Clinical effective observation on treating 65 cases of gastroesophageal reflux disease with BanxiaXiexin decoction. Clinical Journal of Chinese Medicine (CJCM) 2011:3(13):17–8.
97. Duan XF. Therapeutic effect of BanxiaXiexin Decoction on 72 cases of gastroesophageal reflux disease. Chin J of Clinical Rational Drug Use 2011:4(12B):69–70.
98. Xu YJ. Clinical observation on 35 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction. Inner Mongolia J Tradit Chin Med 2010:5:13.
99. Mo X. Clinical observation on the treatment of reflux esophagitis with BanxiaXiexin Decoction. Chinese Community Doctors (Medical Major) 2010:12(26):133.
100. Liu HY, Zhao ZL, Yang LG. Clinical observation of BanxiaXiexin Decoction in the treatment of reflux esophagitis. Chin F Diffic and Compl Cas 2010:9(10):764–5.
101. Liu LQ. 60 cases of gastroesophageal reflux disease treated with Xintang. Inner Mongolia J Tradit Chin Med 2010:4:9.
102. Lu Wei, Liu XW, Li Y. BanxiaXiexin Decoction in the treatment of reflux esophagitis. Chinese Medicine Modern Distance Education of China 2010:3(13):96–7.
103. Gao WW. BanxiaXiexin Decoction in the treatment of 67 cases of gastroesophageal reflux disease. Journal of Emergency in Traditional Chinese Medicine 2010:19(2):212–3.
104. Chang YJ. Clinical effect of BanxiaXiexin Decoction on reflux esophagitis. Gansu Science and Technology 2019:35(12):107–8.
105. Wang H. Clinical Study on Treatment of Cold and Heat Miscellaneous Gastroesophageal Reflux Disease with BanxiaXiexin Decoction and Western Medicine. Smart Healthcare 2019:3(5):103–4.  106. Lu J, Liang CH. Effect of BanxiaXiexin Decoction Combined with Jianfang and Rabeprazole on reflux esophagitis. Contemporary Medical Symposium 2019:17(6):182–3.
107. Zhao XY. Effect of BanxiaXiexin Decoction Combined with omeprazole in the treatment of febrile reflux esophagitis. Family medicine 2018:12:381–2.
108. Zhang XC. Clinical Observation on BanxiaXiexin Decoction Combined with Omeprazole in the Treatment of Intermingled Heat and Cold Reflux Esophagitis. Guangming Tradit Chin Med (CJGMCM) 2018:33(18):2746–7.
109. Wang ZB. Analysis of the therapeutic effect of BanxiaXiexin Decoction Combined with cisapride on reflux esophagitis. Digest World Latest Med Inf 2018:18(53):175–6.
110. Wu YB. Observation on the curative effect of integrated traditional Chinese and Western Medicine on gastroesophageal reflux disease. J Pract Tradit Chin Med 2018:34(4):467–8.
111. Sun YF. The Influence of Pinellia Heart-Draining Decoction on Efficacy and the Expressions of Ghrelin and VIP (vasoactineintrestinal peptide) in Patients with Non-erosive Reflux Disease. Henan Tradit Chin Med 2018:38(11):1639–42.
112. Su YF. Therapeutic effect of BanxiaXiexin Decoction on 43 cases of gastroesophageal reflux disease. Journal of Chengde Medical College 2018:35(1):40–2.
113. Liu HD. Clinical observation on 43 cases of Reflux Esophagitis Treated with BanxiaXiexin Decoction and Western Medicine. Chinese Journal of Ethnomedicine and Ethnopharmacy 2018:27(3):98–9.
114. Meng FZ, An XL, Xu JC. Clinical observation on treating reflux esophagitis with the BanxiaXiexin decoction plus Rabeprazole. Clinical Journal of Chinese Medicine (CJCM) 2018:7(26):87–8.
115. Zhou SN. The curative effect of BanxiaXiexin Decoction in the treatment of cold and heat mixed reflux esophagitis. Dept. of Clinical Chinese Medicine Graduate School, Liaoning University of Traditional Chinese Medicine 2017:
116. Guo KS, Zhang HY, Li N, Liu YS, Wei LW, Lu YP. Study on the effect of BanxiaXiexin Decoction Combined with proton pump inhibitor in gastroesophageal reflux disease. Modern regimen 2017:5:11.
117. Chen YF. Clinical analysis of BanxiaXiexin Decoction Combined with western medicine in the treatment of reflux esophagitis. Chinese Community Doctors (Medical Major) 2016:3:10.
118. Cao Y. Clinical study of Mosapride combined with BanxiaXiexin Decoction in the treatment of gastroesophageal reflux disease. J Pract Tradit Chin Med 2016:32(1):54–5.
119. Zhang LJ. A clinical study on treating gastroesophageal reflux disease with Mosapride plus the BanxiaXiexin decoction. Clinical Journal of Chinese Medicine 2016:8(11):50–2.
120. Ruan SR. Clinical observation on treating reflux esophagitis with the BanxiaXiexin decoction plus Cisapride. Clinical Journal of Chinese Medicine (CJCM) 2015:7(22):68–9.
121. Lin QY. Clinical observation of BanxiaXiexin Decoction Combined with western medicine in the treatment of reflux esophagitis. J Sichuan Tradit Chin Med 2015:33(7):109–11.
122. Liu SX. 49 cases of gastroesophageal reflux disease treated with BanxiaXiexin Decoction and Mosapride. Henan Tradit Chin Med 2014:32(12):2411–2.
123. Liu MG. BanXiaXieXinTang in Treating 50 Cases of Reflux Esophagitis. Western Journal of Traditional Chinese Medicine 2014:27(10):98–9.
124. Tan LH. Clinical observation on treating gastroesophageal reflux disease with BanxiaXiexin decoction. Clinical Journal of Chinese Medicine (CJCM) 2014:6(16):103–4.
125. Wang Y, Wei W. Clinical Observation of Reflux Esophagitis Treated with Modified BanxiaXiexin Decoction and Rabeprazole. World Journal of Integrated Traditional and Western Medicine 2013:8(2):200–2.
126. Huai XX, Gao CL. BanxiaXiexin Decoction Combined with rabeprazole in the treatment of reflux esophagitis. Guangming Tradit Chin Med (CJGMCM) 2013:28(6):1217–8.
127. Tan ZX. Clinical Efficacy Observation of BanxiaXiexin Decoction for Treating Gastroesophageal Reflux Disease on 43 Cases. China Pharm 2013:22(24):90–2.
128. Bai SC. Treatment of reflux esophagitis with combination of traditional Chinese and Western Medicine. Chinese community doctors (Medical Major) 2012:14(311):211.
129. Han XL. Clinical observation on the treatment of reflux esophagitis with the combination of traditional Chinese and Western Medicine. The Medical Forum 2011:15(8):758.
130. Cheng ZH. Therapeutic effect and safety analysis of BanxiaXiexin Decoction in the treatment of reflux esophagitis. China Modern Doctor 2011:19(14):65–6.
131. Gong SQ. Clinical observation on 60 cases of Reflux Esophagitis Treated with the combination of traditional Chinese and Western Medicine. Practical Clinical Journal of Integrated Traditional Chinese and Western Medicine 2010:10(5):51–2.
132. Cao CN, Zhang BP, Zhao XY. Clinical Efficacy of BanxiaXiexin Decoction and Its Effects on Anxiety and Sleep Quality of Patients with Reflux Esophagitis. Journal of Guangzhou University of Traditional Chinese Medicine 2018:35(5):780–4.
133. Cao CN. Clinical effect of cold and heat regulating therapy on reflux esophagitis and intervention on patients'psychological state. Dept. of Clinical Chinese Medicine Graduate School, Guanzhou University of Chinese Medicine 2016:
134. Pan S, Lan QQ. Clinical research on the effect of Cold and Warming Method treating on Refluz Esophagitis and the psychological state and sleep qulaity of Reflux esophagitis patients. Liaoning Journal of Traditional Chinese Medicine 2011:38(3):479–80.
135. Vakil N, van Zanten SV, Kahrilas P, Dent J, Jones R. Global Consensus Group. The Montreal definition and classification of gastroesophageal reflux disease:a global evidence-based consensus. Am J Gastroenterol 2006:101(8):1900–20.   136. Jung H, Hong SJ, Jo YJ, Jeon SW, Cho YK, Lee KJ, et al. Updated guidelines 2012 for gastroesophageal reflux disease. Korean J Gastroenterol 2012:60(4):195–218.   137. Yun HR, Jung HY, Park HJ, Bae SC. Cost-effectiveness analysis of proton pump inhibitors and ranitidine in the treatment of gastroesophageal reflux disease. Korean J Med 2002:62(5):504–12.
138. Hunt R, Armstrong D, Katelaris P, Afihene M, Bane A, Bhatia S, et al. World gastroenterology organisation global guidelines:GERD global perspective on gastroesophageal reflux disease. J Clin Gastroenterol 2017:51(6):467–78.   139. Park CH, Lee SK. Gastroesophageal Reflux Disease. Korean J Gastroenterol 2019:73(2):70–6.   140. Odsuka K. Explanation I Sumptomatical Practice of Kampo-Medicine Wonju: Euibanseolim: 2013. p. 356–555.
141. 顔 正華, 中 藥學. 中國: 人民術生出版社: 1991:134178, 594, 721, 721.
142. 黃 泰康. 常用中藥成分與藥理手冊 中國: 中國 醫藥科技出版社: 1994. p. 178.
143. 焦 樹德. 用藥心得十講 서울: 醫聖堂: 2001. p. 94.
144. Lee JE, Park JH, Cho HS, Kim JC, Oh SW, Lee SH, et al. A Case Report of Gastroesophageal Reflux Disease (GERD) with Hiatal Hernia. Korean J Orient Int Med 2005:26(1):244–51.
145. Yoon SH. A Clinical Case Report of Endoscopic Reflux Esophagitis with Gastric Dysmotility Treated with Korean Traditional Medical Therapy. Korean J Orient Int Med 2016:37(4):669–77.   146. Lim TH, Park HS. 2 Case Reports of Gastroesophageal Reflux Disease Diagnosed as SoyanginMangeum. J SasnagConsitut Med 2015:27(2):297–306.
147. Kim YH, Kim SY, Hwang MW. A Case Study of Taeumin Patient with Gastro-esophageal reflux disease (GERD) who Treated Successfully with Yeoldahanso-tang (Reduohanshao-tang). J of SasnagConsitututional Medicine 2011:23(1):132–8.
148. Lee JS. Effect of Banhasasimtang Granule on Gastric Emptying in Rats. Dept. of Clinical Chinese Medicine Graduate School, Kyunghee University 2006:
149. Ha J, Kong KH, Jee HC, Beak TH. A Bibliographycal Study on the Relation of the Spleen, Stomach and the Liver. Korean J Orient Int Med 2010:22(4):675–81.
|
|


































