I. 서 론
췌장암이란 췌장에 생긴 암세포로 이루어진 종괴로, 5년 생존율이 8%에 불과한 예후가 극히 불량한 암종이다. 조직학적으로는 췌장 선암(pancreatic ductal adenocarcinoma)이 췌장암의 90%를 차지하여 선암이 통상 췌장암으로 통용되고 있다1. 국가 암 정보센터 통계에 따르면 우리나라에서 2017년 한 해 동안 췌장암의 발생률은 8위였으나, 2013년-2017년의 5년 상대 생존율은 12.2%로 가장 낮은 수준이다2.
일반적으로 췌장암 생존기간의 중간값은 5.5개월로 제 4병기 환자에서 연명치료를 받은 환자의 생존기간은 4.2개월이며, 항암화학요법을 진행한 환자의 생존기간의 중간값은 6.3개월로 생존기간의 연장에 큰 기대를 하기 힘든 것이 사실이다3. 완치적 치료를 위해서는 수술이 유일한 방법이나 췌장 주변의 혈관 및 림프절 침범으로 진단 당시 80% 이상이 근치적 절제수술이 어려운 상태이므로 항암화학요법을 진행하게 된다4. 췌장암의 표준 현대의학적 항암화학요법 치료제는 1990년대 중반 Gemcitabine이 도입된 이후 꾸준한 연구개발이 진행되어 왔으며, 2000년대 중반 Erlotinib, 2010년경 Oxaliplatin+Irinotecan+5-fluorouracil+Leucovorin (FOLFIRINOX)요법 도입 이후 Abraxane(nab-paclitaxel)과 Liposomal irinotecan이 개발됐다. Gemcitabine +Abraxane(nab-paclitaxel) 투여군의 OS 중간값은 8.7개월로 Gemcitabine 단독 투여군의 OS 중간값인 6.6개월에서 개선된 수치로5 췌장암의 항암화학요법을 통해 암세포의 증식을 억제하거나, 일부 암세포의 사멸로 생존율을 다소 연장시키고, 통증을 줄여주어 췌장암 환자의 삶의 질을 향상시킬 수 있음이 밝혀졌다6. 하지만 위장독성, 미각저하, 피로 등 항암화학요법의 부작용은 삶의 질을 떨어뜨릴 수 있으며 한 연구에 따르면 항함화학요법 받은 환자 중 Partial Response(PR) 반응을 보인 40-46%의 환자군에서 치료 이후 신체기능, 피로, 식욕증가 삶의 질이 다소 향상되었으며 Stable Disease(SD) 반응을 보인 0-12%의 환자군만이 항암화학요법이후 삶의 질 개선을 보였다7.
췌장암은 진단 후 사망률이 높고 생존기간이 짧은 만큼 여생에 대한 삶의 질 관리는 중요하며, 췌장암 환자에게서 주 치료요법으로 제시되고 있는 항암화학요법으로 인하여 저하되는 삶의 질을 향상시키기 위한 노력은 더욱 중요하다 할 수 있다. 이에 환자들은 질병치료 및 건강증진, 부작용 완화를 위해 통합의학치료(Integrative Medicine Therapy, IMT)에 대한 높은 관심을 가지고 있으며 다양한 암 환자군에서 IMT를 통하여 증상 및 암의 진행상태가 호전되는 여러 사례가 발표되고 있다8,9.
이에 본 증례는 잔여생존 기간이 6개월 미만으로 기대되는 췌장암 4기를 진단받은 환자로서 Gemcitabine/Abraxane 항암화학요법과 동시에 통합의학치료를 병행하여 항종양효과평가 중 PR 반응을 보이고 종양표지자의 감소 및 복부통증이 완화되어 유의한 삶의 질 상승을 보인 결과를 얻었기에 보고하는 바이다.
II. 증 례
1. 환 자 : 윤◯◯, 여, 만 69세, 158 cm, 43.3 kg
2. 치료기간 : 2019년 9월-2020년 5월
3. 진단 시 조직검사 및 병기
1) 최초진단 : 2019년 9월
2) 조직검사 및 병기 : Pancreatic cancer, body and distal tail c multiple liver meta, Stage IV. adenocarcinoma.
4. 과거력 및 가족력
1) 과거력 : HTN(+). DM(+). Hemorrhoid Op (2019년 08월)
2) 가족력 : 특이사항 없음.
5. 현병력 상기환자는 2019년 4월부터 하루에 수 시간씩 지속되는 좌하복부(Left lower quadrant, LLQ) 부위 통증으로 2019년 9월 ◯◯병원에서 AJCC/IUCC (American Joint Committee on Cancer, 미국암연합회/Union Internationale Contre le Cancer, 국제항암연맹)의 TNM 병기에 따른 췌장의 체부 및 미부암 Stage 4(T4N2M1)를 진단받았으며, 조직검사 상 adenocarcinoma로 2019년도 9월부터 현재까지 Gemcitabine/Abraxane 을 통한 항암화학치료를 지속하는 중이다. 2019년 9월 10일부터 본원에 입원하여 통합의학치료를 병행하였다.
6. 주소증
1) 좌하복부와 옆구리 통증 : 진단 6개월 전부터 시작된 하루 5회 이상의 NRS 7점의 통증으로 마약성 진통제(IRCODONE 5 mg prn, TARGIN 5/2.5 mg bid)를 복용하였으나 지속적으로 통증을 호소하였다.
2) 신체활력도 저하 : 깨어 있는 시간 중 침상에 누워있는 시간이 30% 미만이었으며 누적된 항암치료로 인해 식은땀과 함께 탈력감 호소하였다. 신체활력도 ECOG Gr 1으로 측정되었다.
3) 소화불량, 식후 복통, 복부팽만감 : 항암 후 발생한 소화불량 및 복부팽만감으로 NRS 3의 괴로움을 호소하였다.
4) 항암으로 유발된 손발 저림, Chemotherapy induced peripheral neuropathy(CIPN) : 누적된 항암치료로 양 발끝이 무디고 저릿한 NRS 4의 신경통증을 호소하였다.
7. 치료 방법
1) 한방치료
(1) 알러젠(Urushiol)이 제거된 옻나무 추출물(Allergen-Removed Rhus Verniciflua Stokes, A-RVS) 연조엑스 : 혹부리 원외탕전실에서 제조하였으며 분쇄된 옻나무 목질부 총중량의 20배의 물을 부어 120도 가압상태에서 5시간 전탕한 추출액을 3 brix로 농축한 뒤 농축액을 발효시켜 섬유질을 분해 한 후 백필터로 여과하였다. 여과된 농축액에 올리고당을 섞어 60 brix까지 교반 농축하였으며 혼합액을 1 stick 당 20 g(옻나무 엑기스 2,000 mg 함유)씩 스틱 포장하여 1일 1회 식후에 복용하였다.
(2) 향사평위산(香砂平胃散, Hyangsapyeongwi-san, HPS) : 항암 후 오심. 소화불량. 식욕부진 치료를 위해 1일 3회로 증상이 있을 때 수시로 복용하였다(Table 1).
Table 1
Prescription of HPS
(3) 뜸치료(Moxibustion) : 기기구를 이용하여 關元(CV4), 中脘(CV12)에 뜸 치료를 1일 1회 30분간 시행하였다.
(4) 침치료(Acupuncture) : 항암으로 인한 손발저림 치료를 위해 3-4일 간격으로 시행하였다. 八風에 20분간 유침하였으며 0.25×30 mm (동방침)의 호침을 사용하였다.
(5) 비훈(Herbal Steam Therapy) : 본원의 원외탕전실에서 인삼 400 g으로 4 L를 탕전한 뒤 재증류를 통해 모인 증류액을 고압증기멸균기 121 ℃에서 15분 멸균 후 10 cc를 비훈액으로 만들어 1일 1회 30분간 네뷸라이저를 통해 흡입할 수 있도록 시행하였다.
2) 병행한 현대의학적 치료
(1) 항암화학요법 : Gemcitabine/Abraxane 을 4주 간격으로 시행할 계획으로 2019년 9월 9일 1차 항암화학요법을 시작하였고 2020년 5월 12일에 11차 요법을 받았다.
(2) 고주파온열치료(High-frequency heat treatment) : 하스피케어사의 Oncothermia EHY-2000, 바이오메디신사의 Celsius42 GmbH를 이용해 복부 부위를 주 1-2회 50분간 시행하였다.
(3) 미슬토 : 하스피케어사의 Abnoba Viscum qu 주사액을 0.01 mg부터 시작해 주 3회 피하로 주입하였다. 8회 시행 후 부작용을 보이지 않으면 5배 증량하여 최종적으로 1 mg을 주입하였다.
(4) 헤리 : 싸이젠코리아사의 Tymosin Alpha 1 1.6 mg을 주3회 피하로 주입하였다.
8. 치료 평가
1) 종양의 크기 및 변화는 Chest Computed Tomography (CT)를 통해 평가하였다.
2) Response Evaluation Criteria In Solid Tumors (RECIST) : 고형종양에서의 치료반응에 대한 객관적 평가기준으로 고형암 치료법을 평가하는 임상시험에서 대부분 사용되는 평가기준이다. RECIST version 1.1에 따르면 종양에 대한 치료반응은 Complete Response(CR), Partial Response(PR), Progressive Disease(PD), Stable Disease(SD)로 나누어 평가한다. 본 증례에서는 이에 근거하여 종양에 대한 치료반응을 평가하였다10.
3) Numeric Rating Scale(NRS) : NRS는 수치평가척도로써 환자의 고통정도를 숫자로 계량화하는 방법이다. 수집이 편리하고 환자의 주관적 호소를 객관적 지표로 나타낼 수 있다는 장점이 있어 자주 사용된다. 0~10점까지 숫자통증등급을 활용하여 통증 없음 0, 경도 1~4, 중간정도 5~6, 심함 7~10으로 구분하여 통증을 객관적으로 평가한다. 본 증례에서는 주증상인 복부통증, 손발저림 및 식후소화불량 위장장애에 대해 평가가 이루어졌다.
4) Eastern Cooperative Oncology Group(ECOG) : ECOG는 암환자의 움직임과 활동 정도 파악을 위해 개발된 측정도구로 환자의 상태를 0~5점으로 구분하여 환자의 의학적 상태를 포괄적으로 반영한다. Grade 0은 질병 이전의 상태로 제한 없이 활동할 수 있는 상태, Grade 1은 경미한 증상이 있으나 거의 완전한 거동이 가능한 상태, Grade 2는 낮 시간 동안 50% 미만으로 누워 지내는 상태로 자신을 돌볼 수 있고 직장 생활은 불가능한 상태, Grade 3은 낮 시간 동안 50% 이상 누워 지내는 상태로 최소한의 자신은 돌볼 수 있는 상태, Grade 4는 완전히 누워 지내는 상태로 전혀 자신을 돌볼 수 없는 상태, Grade 5는 사망 상태를 의미한다. 본 증례에서는 2019년 9월 9일부터 2020년 5월 12일까지의 변화를 평가하였다.
5) National Cancer Institute Common Terminology Criteria for Adverse Event(NCI-CTCAE) : NCI-CTCAE는 암환자에게 사용한 치료로 인한 부작용의 정도를 정량화, 표준화시킨 평가도구로 1등급에서 5등급까지로 분류하고 있다. Grade 1은 무증상이거나 증상이 경미하여 경과관찰을 요하는 상태, Grade 2는 중등도의 부작용으로 원활한 일상생활에 제약이 있는 상태, Grade 3는 당장의 생명의 위협은 없으나 중증의 상태로 일상생활이 불가한 상태이며 Grade 4는 생명의 위협이 있는 상태로 긴급한 치료가 필요한 상태이며 Grade 5는 부작용으로 인한 사망에 이른 것을 의미한다. 본 증례에서는 NCI-CTCAE version 5.0에 의하여 치료에 따른 간기능, 신장기능, 골수억제기능의 부작용을 평가하였다11.
6) 혈액검사(Blood Test) : 치료기간동안 시행된 통합의학치료의 안전성을 검사하기 위하여 본원 임상병리검사실에서 간 기능 검사 및 신장 기능검사를 시행하였고, 병용투여기간 동안의 변화를 관찰하였다. 또한 WBC 수치 등 염증반응과 종양표지자의 치료 전과 후의 변화를 관찰하였다.
9. 치료 경과
1) 종양의 변화 : ◯◯대학병원에서 촬영한 2019년 9월 5일과 2019년 11월 6일 및 2020년 3월 2일의 전산화단층촬영(Computed Tomography, CT) 상 췌장 몸통 및 꼬리 부분의 원발병변이 큰 폭으로 감소하였으며 전이된 간의 다발병변 또한 감소하여 RECIST 1.1에 근거하였을 때 부분반응(Partial Response)로 판단되었다(Fig 1, 2).
Fig. 1
Comparison of computed tomography (CT) images before and after treatment.
A (2019/9/5) :
1. Pancreatic cancer, body and distal tail. (3.7×3.7×3.3 cm)
2. Multiple liver meta. whole segments of both lobes except caudate lobe.
B (2019/11/6) :
1. Markedly improving pancreas body tail cancer. (2.5×3.8×1.2 cm)
2. Markedly improving multiple hepatic metastasis at both lobe.
C (2020/3/2) :
1. More decreased extent of pancreas body/tail cancer. (3.3×0.8 cm on axial image)
2. Equivocal size of multiple hepatic metastasis in both lobes.

2) 독성부작용 : NCI-CTCAE version 5.0으로 평가했을 때 통합의학적 치료로 인한 부작용은 발생하지 않았다. 치료기간 중 AST, ALT 등의 간 기능 수치는 정상범위를 유지하여 간 독성은 발생하지 않았으며 BUN, Creatinine 수치도 정상범위로 신독성은 발생하지 않았다. 또한 CRP도 정상범위로 염증반응을 보이지 않았다. 골수기능에 대해서는 2020년 3월 23일 검사 상 발열은 없었으나 WBC 1430, Plt 9000으로 NCI-CTCAE Thrombocytopenia, Leukopenia Grade3에 해당하는 수치를 보여 골수세포 성장촉진효과가 있는 Leucostim 150 mcg을 주사하였으며, 이후 정상수치를 보여 항암을 지속하였다(Table 2).
Table 2
Laboratory Findings
| 2019.09.05 | 2019.10.28 | 2019.12.30 | 2020.03.23 | |
|---|---|---|---|---|
| WBC (*103/μL) | 12.91 | 4.34 | 5.65 | 1.43 |
| RBC (*106/μL) | 4.5 | 3.15 | 3.92 | 3.32 |
| Plt (*103/μL) | 193 | 120 | 318 | 90 |
| Albumin (g/dL) | 3.9 | 3.9 | 4.1 | 3.9 |
| Total bilirubin | 1 | 0.51 | 0.38 | 0.41 |
| AST (U/L) | 32 | 14 | 22 | 15 |
| ALT (U/L) | 65 | 16 | 20 | 13 |
| ALP (U/l) | 276 | 69 | 111 | 99 |
| BUN (mg/dL) | 12 | 17.5 | 12.1 | 8.8 |
| Creatinine (mg/dL) | 0.51 | 0.6 | 0.56 | 0.52 |
| CRP (mg/dL) | 0.96 | 0.34 | 0.53 | 0.22 |
| CEA (ng/mL) | 32.51 | · | 7.2 | 5 |
| Ca19-9 (U/mL) | >12000 | · | 276 | 300 |
3) 종양표지자 감소 : 종양표지자는 종양세포에서 생성되어 분비되거나 종양조직에 대한 반응으로 정상조직에서 생성되는 물질로, 혈액이나 체액 또는 조직에서 발견되는데12 종양의 치료반응 평가의 보조적인 목적으로 사용할 수 있다. 췌장암의 종양표지자는 CEA, Ca19-9로 정상범위는 각각 0-6.5, 0-34이다. 본 증례의 환자에서 치료 전 후를 비교 하였을 때 CEA는 32.51에서 5로 정상 수치로 떨어졌으며, Ca19-9는 300으로 아직 정상수치보다는 높지만 치료 전 >12000인 점을 감안하였을 때 큰 폭으로 감소하였기에 통합의학치료가 긍정적 역할을 한 것으로 생각할 수 있다.
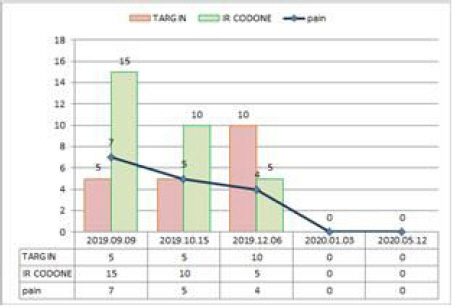
4) 증상의 변화 : 환자는 2019년 9월 내원 당시 NRS 7에 해당되는 복부통증으로 하루 TARGIN 5 mg, IR CODONE 15 mg를 복용하였으며, 치료 시작 1개월 이후에는 NRS 5의 통증으로 IRCODONE 10 mg를 복용하였다. 3개월 이후에는 TARGIN의 용량을 10 mg로 증량하였으나 IRCODONE은 5 mg로 감량하여 복용하였다. 치료 4개월 이후부터는 통증 호소가 NRS 0로 현저하게 감소하여 현재까지 진통제를 복용하지 않고 유지중이다(Fig. 2). 이 외에 항암이후 발생한 식욕저하 식후 소화불량에는 증상 호소 시 마다 향사평위산을 투여하였으며 이후 NRS 8에서 NRS 0으로 감소하였으며 누적된 항암으로 인한 말초신경병증에 침치료 후 NRS 5에서 NRS 2로 감소하였다. 복부통증 및 항암으로 인한 신체활력도 저하는 인삼 비훈 및 한약복용 후 ECOG Gr1에서 Gr0으로 개선되었다(Fig. 3).
III. 고찰 및 결론
췌장암은 다른 암과 마찬가지로 수술여부, 전이정도 등에 따라 그에 맞는 수술, 항암화학요법이 표준치료로 행해지고 있으나 그 예후가 불량하다13. 가장 효과적인 치료는 완전한 외과적인 절제뿐이나14 발견 당시 완치 목적으로 수술적 절제가 가능한 환자의 비율이 약 10% 밖에 되지 않으며 대부분의 환자들은 원격 전이 또는 진행된 국소 침윤 상태로 발견된다15.
암의 표준치료에 따른 부족한 치료 효과로 인한 한계를 보완하기 위해 전 세계적으로 한의학을 포함한 보완대체의학(Complementary and alternative medicine, CAM)에 대한 관심이 늘어나고 있으며, 특히 췌장암은 치료의 예후가 더욱 불량하므로 치료를 위한 다학제적 접근이 더욱 필요한 상황이다16,17.
통합의학이란 현대의학적 암 치료를 기본으로 하면서 과학적으로 검증된 한방요법, 심신요법 등을 병행하는 의학으로18 National Comprehensive Cancer Network 진료 가이드라인에 따르면 완화의학과의 통합의학치료는 전이성 또는 진행성 암환자의 치료에 있어 표준으로 삼고 있으며, 이로 미루어 볼 때 CAM, 특히 그 중에서도 한약제제를 포함한 통합의학치료(Integrative Medicine Therapy, IMT)가 췌장암 환자의 치료에 도움이 될 수 있을 것으로 사료된다19,20.
본 증례에서는 잔여생존 기간이 6개월 미만으로 기대되는 췌장암 4기를 진단받은 환자를 대상으로 8개월간 통합의학치료를 시행하여 종양의 부분반응(PR), 종양표지자 감소, 간⋅신기능 관련 안정성을 보임을 증명하였으며, 통합의학치료가 암성 통증 및 항암부작용을 완화하는데 유의미한 결과를 이끌어 낼 수 있음을 확인하였다.
증상개선과 종양의 퇴축을 이끌어 내기 위하여 한약치료로 옻나무 추출물 연조엑스, 향사평위산과 뜸, 침, 비훈치료 시행하였으며, 면역력 증강을 위하여 고주파, 미슬토, 자닥신요법인 현대의학적 치료를 병행하였다.
옻은 漆樹또는 漆皮로 불리우며 한의학에서 성미가 신온함하고 간, 비위, 대소장으로 귀경한다고 알려져 있으며 예로부터 破血하고 위장의 적체를 소산시키므로 주로 瘀血, 積聚, 癥瘕 및 冷心痛 등에 응용된다. 痰飮과 瘀血을 동시에 치료하면서도 보하는 성질을 가지고 있어 암치료 활용 가능성이 있다21. 실제로 기존 연구를 통해 건칠 추출물 및 성분이 암세포 증식억제, 면역증진 및 항산화 작용이 확인되었고22, 암환자에게 건칠을 투약하여 유의미한 효과를 보인 경우가 다수 보고되어있다23,24. 따라서 본 증례의 환자에게 암세포를 직접 공격하는 것을 목적으로 환자에게 옻나무 추출물을 투약하였다.
종양반응 외에도 치료기간 내에 종양표지자가 큰 폭으로 감소하였으며, 간⋅신기능 검사 및 CTCEA 기준을 적용한 부작용 평가에 있어서도 치료기간 중 한번의 골수기능이 저하되었으나 적절한 처치 후 항암을 지속적으로 진행하였으며 그 외 부작용을 보이지 않아 통합의학치료의 안정성을 확인하였다.
또한 내원 당시 NRS 7에 해당하는 복통으로 마약성 진통제를 복용하였으나 치료 4개월 이후부터는 통증 호소가 NRS 0으로 감소하여 현재까지 진통제 복용 없이 유지중이며 항암치료 이후 발생한 식욕저하 및 식후 소화불량에 燥濕建脾하고 行氣和胃하여 비위를 運化를 도와 소화불량의 治方으로 알려진 향사평위산을 투여하여 불편감이 NRS 8에서 NRS 0으로 감소된 것을 확인하였다.
누적된 항암으로 인한 말초신경병증에 곡지, 외관, 합곡, 족삼리, 태충, 팔풍 등의 혈위에 대한 침치료가 증례 및 대조군연구로 보고되어 있는데25,26 대체로 침치료 후 증상 개선 효과를 보였기에 본 증례의 환자에게도 팔풍혈에 취혈하였으며, 치료 후 NRS 5에서 NRS 3으로 호전되었다. 기력저하 및 탈력감을 호전시킬 목적으로 인삼 비훈을 시행하였으며 ECOG Gr1에서 Gr0으로 개선되어 한방치료를 통하여 삶의 질이 유의미하게 개선된 것을 확인 할 수 있었다.
미슬토는 숙주나무에 반생하는 식물로 ‘겨우살이’라 불리며 한의학에서는 ‘상기생’이라 불리는 약재이다. 그 성분 중 미슬토렉틴(Mistletoe lectin)은 암세포와 결합한 후 세포 내부로 침투하여 단백질 합성을 저해하고 면역체계를 자극시켜 대식세포 및 NK(Natural Killer) 세포의 활성을 증가시켜 종양세포의 성장을 억제시키는 것으로 알려져 있으며 미슬토 치료를 받은 췌장암 환자들에서 삶의 질의 향상 및 생존기간의 연장이 보고되어 있다27.
Tymosin Alpha 1은 흉선에서 추출한 면역조절 물질로 골수세포에서 NK-세포, T-세포를 증가시키고 바이러스의 자기복제를 억제하고 항산화제 역할 및 골수를 보호하는 효과가 있어 항암요법에 의한 골수 피해를 방지한다28,29.
고주파 온열치료는 고주파를 종양부위에 선택적으로 가해, 전기장을 형성하고 열을 발생시키는 치료법이다. 열 발생으로 암세포의 자연 살해(Apoptosis)를 유도하고, 종양에 공급되는 영양분을 차단하여 암세포의 증식을 억제하여 암의 재발과 전이를 방지하여 항암화학요법, 방사선요법과 같은 기본 암치료와 병행하였을 때 환자의 생존율 개선에 도움을 주는 것으로 알려져 있다. 흑색종, 두경부암, 유방암, 위장관 및 비뇨생식기의 암, 교모세포종, 육종 등 다양한 고형암에서 종양의 크기 및 생존율 증가를 위해 방사선 치료 및 항암 치료와 병행할 필요가 있다는 근거가 제시된 바 있다30,31.
본 증례는 췌장암 4기를 진단받은 환자로서 항암화학요법과 한방치료를 병행하면서 상대적으로 짧은 시간 내에 종양의 부분반응(PR) 및 증상개선을 이끌어 냈다는 점에서 의의를 가진다. 비록 현대의학과 한의학적 치료가 병용되었기 때문에 특정 약물의 작용이나 치료방법에서 각각의 약리 작용 및 효과를 명확히 구분하기는 어렵지만 통합의학적 암치료가 항암제 단독투여방법이나 항암제와 방사선 치료에 비해서 더욱 효과적 치료가 될 수 있는 가능성을 보여준 것으로 생각된다. 췌장암의 국내 한의학 연구 현황을 살펴보면 총 19편의 논문 중 임상연구논문은 9편, 고찰논문 2편, 실험논문 8편이며, 임상연구 중 증례보고가 6편으로 췌장암 환자의 수가 적지 않음에도 불구하고 한의학을 이용한 췌장암 관련 연구가 부족한 것이 현실이다32. 최근 한방 단독치료보다는 병용치료에 의해 긍정적인 사례가 많아짐을 볼 때9,33 본 증례가 의미가 있을 수 있다고 보며, 차후 더 진일보한 연구결과가 있기를 기대해 본다.