재발성 비소세포성 폐암환자의 Afatinib과 삼칠충초정 병용투여 경과관찰 1례
Abstract
Objective
The purpose of this study is to report the case of a patient with recurring non-small cell lung carcinoma (NSCLC) taking Samchilchoongcho-Jung with Afatinib.
Methods
An NSCLC patient diagnosed with multiple bone and pulmonary metastasis was taking Afatinib (20 mg/day) and suffering from stomatitis caused by the Afatinib. The patient was treated with Samchilchoongcho-Jung (1,500 mg/day) for 3 months. The tumor size was measured with computed tomography, and laboratory findings, including tumor markers (CEA, Cyfra 21-1), were also followed up. Stomatitis was measured by a numeric rating scale, and adverse events were evaluated using the National Cancer Institute Common Terminology Criteria for Adverse Events (NCI-CTCAE), version 4.0.
Results
After combined treatment, stable disease was shown on computed tomography. The tumor marker levels of CEA and Cyfra 21-1 were decreased, and the stomatitis significantly improved. NCI-CTCAE 4.0 showed no adverse events.
Conclusion
This case study suggests that Samchilchoongcho-Jung may have a synergic effect, in conjunction with Afatinib, on the treatment of patients with recurring NSCLC.
Keywords: non-small cell lung carcinoma, Afatinib, Samchilchoongcho-Jung, epidermal growth factor receptor
I. 서 론
폐암은 전 세계적으로 가장 흔한 악성 종양 중 하나로서 2017년 미국에서 집계된 통계에 따르면 남성에서 2위, 여성에서 2위로 발생률이 높으며, 남녀 모두에서 암으로 인한 사망률 1위를 차지하고 있다 1. 폐암은 크게 소세포성과 비소세포성으로 나뉘는데, 비소세포성 폐암은 전체 폐암의 대략 83%를 차지하고 5년 생존율이 21%로 고형암 중에서도 예후가 가장 나쁜 암이다 2. 비소세포성 폐암은 40% 이상이 진단 시 전이성 병기(stage IV)로 발견되어 일부 환자에게서만 수술치료가 가능하며, 수술이 불가능한 경우 화학항암치료를 받더라도 5년 생존율이 15.7-17.4%에 불과할 정도로 매우 불량하여 기존의 수술, 방사선요법, 항암화학요법과 이들의 병용요법으로는 치료의 한계를 보여주고 있다 3. 2000년대부터는 폐암의 발병기전에 대한 이해가 넓어지면서 epidermal growth factor receptor (EGFR)나 anaplastic lymphoma kinase(ALK), ROS proto-oncogene 1 receptor tyrosine kinase(ROS1), Programmed cell death protein 1(PD-1)과 같은 유전자의 돌연변이 유무에 따라 비소세포성 폐암을 몇 가지 아형(subtype)으로 구분할 수 있게 되었고, 이를 이용한 표적치료제가 등장하여 폐암 치료에 획기적인 변화가 있었다 4. 특히, EGFR-TKI 제제인 Gefitinib과 Erlotinib은 무작위 대조군 3상 임상시험에서 기존 백금기반 화항항암요법과 비교했을 때 무진행생존기간(progression-free survival, PFS)을 연장하고 삶의 질을 향상시켰다는 연구결과들이 보고되었다 5,6. 또한 Afatinib은 EGFR만 차단하는 1세대 표적치료제인 Gefitinb, Erlotinib에서 더 나아가 EGFR(ErbB1), HER2(ErbB2), ErbB4 등 3가지 ErbB family 모두를 차단하는 2세대 표적항암제로서 기존 표준화학요법 대비 Afatinib의 유의한 전체 생존기간(Overall Survival, OS) 향상이 보고되었다 7. 그러나 이러한 뛰어난 치료성적에도 불구하고 EGFR-TKI 제제들은 대개 9-13개월 정도가 지나면 2차 내성에 따른 질병의 진행을 경험하게 되기 때문에 EGFR-TKI 유지요법에서 시간경과 후에 발생할 수 있는 항암제 내성의 출현을 극복하는 연구가 치료율 향상에 있어 매우 중요하다 4. 한의학적 치료는 서양의학의 통상 암 치료와 병행하였을 때 부작용의 감소, 삶의 질 개선과 더불어 면역작용을 높여 시너지 효과를 내어 최종적으로 생존율을 향상시킬 수 있는 가능성을 가지고 있다. 폐암치료에 대한 한의학적 연구들을 살펴보면 단일약물로는 동충하초, 길경, 산두근, 어성초 등이, 복합약물처방으로는 길경탕, 인삼사폐탕, 경옥고, 보중익기탕, 사백산, 정력대조사폐탕 등이 연구되어 있다 8. 정 등은 삼칠, 동충하초, 산자고, 인삼 등으로 구성된 항암플러스가 진행성 비소세포성 폐암환자에 투여한 결과 암의 성장을 억제하고 삶의 질을 재선하는데 일정 정도 기여했음을 보고하였고 9, 권 등은 비소세포폐암에 있어서 최근 표적치료제로 흔히 사용되는 Pemetrexed, Erlotinib과 알러젠이 제거된 옻나무 추출물 위주의 한의치료를 병용하여 항암제의 적용기간이 연장되고 증상개선에 기여하였음을 보고하였다 10. Li 등이 보고한 체계적 문헌고찰에서는 진행성 비소세포성 폐암을 위한 항암화학요법과 결합된 한약의 효능을 평가하였는데, 한약이 비소세포성 폐암환자들에게 있어 화학항암요법의 독성을 감소시키고, 1년 생존율을 유의하게 연장시키고, 즉각적인 종양반응을 증진시키며, 신체활동지수(Karnofsky Performance Status Scale)를 증진시켰음을 보고하였다 11. 본 증례에서는 Afatinib(상품명 Giotrif)을 복용하는 전이성 비소세포성 폐암 환자에게 삼칠충초정을 병용투여하였는데, 삼칠충초정은 항종양, 신생혈관형성 억제 등의 효능을 지닌 항암플러스를 폐암치료 한약제제로 발전시킨 것으로 삼칠근, 동충하초, 인삼, 유향의 4가지 약제로 구성되어 있고, A549 폐암세포를 이용한 xenograft 동물모델실험 등에서 항폐암효과가 있음이 보고되어있다 12. 현재까지 표적치료제로 사용되는 Afatinib과 한의치료 병용에 대해 보고된 논문은 Afatinib과 감초사심탕의 병용투여 했을 때 호전을 보인 증례연구 13 이외에는 거의 없는 실정이다. 이에 본 연구에서는 Afatinib과 삼칠충초정 위주의 한의치료를 병용하여 일정 기간 동안 항종양 효과 평가 중 불변(Stable Disease, SD)을 보이고 증상 호전 및 삶의 질 개선이 나타난 재발성 비소세포성 폐암 환자를 경험하였기에 보고하는 바이다.
II. 증 례
본 증례연구를 위하여 환자동의서 및 대전대학교 둔산한방병원 기관생명윤리위원회(Institutional Review Board, IRB)의 심의면제(DJDSKH-17-E-02)를 획득하였다.
환 자 : 문○○, 만 61세, 여자 병용치료 기간 : 2016년 5월 23일~2016년 9월 8일 -
진단시 조직검사 및 병기
1) 최초 진단시(2014년 1월) : Non-small cell lung carcinoma(NSCLC), stage Ib(T2aN0M0). 선암(adenocarcinoma, papillary patter, moderately differentiated), Immunochemistry 상 EGFR mutation(+), KRAS(-), ALK(-) 2) 전이 진단시(2015년 3월) : Multiple bone metastasis, stage IV. 9th thoracic vertebrae(T9), 4th lumbar vertebra(L4), right 6th, 8th rib, sacrum, right ilium, right acetabulum 3) 재발 진단시(2016년 1월) : Pulmonary metastasis, stage IV. multiple nodules in both lung, left supraclavicular lymph node enlargement
-
4. 과거력 및 가족력
-
현병력
상기 환자는 2014년 1월 15일 건강검진 상 시행한 chest X-ray에서 이상소견 보여 ○○병원에서 흉부 컴퓨터 단층영상검사(Computed Tomography, CT) 시행한 결과 우폐 상엽부위에 약 3 cm의 mass가 발견되었다. △△병원으로 전원하여 2014년 2월 4일에 양전자 단층촬영(Fusion Torso F-18 FDG) 시행하였고, 우폐 상엽부위의 4.1×3.9×3.5 cm 크기의 비소세포성 폐암 진단 후, 2014년 2월 20일에 폐엽절제술(Rt. upper lobectomy with mediastinal lymph node dissection)을 시행 받았다. 이후 2014년 3월 29일부터 2014년 7월 7일까지 Navelbine/Cisplatin(NP) 방안으로 6 cycle의 화학항암치료를 받았다. 수술 및 항암 치료 후 추적검사를 하던 중 2015년 3월경 전신 뼈 스캔 검사(whole body bone scan, WBBS) 상 T9, L4, 6th, 8th Rt. rib, sacrum, Rt. ilium, Rt. acetabulum에 전이 판정 받았고, 2015년 3월 25일부터 2015년 4월 10일까지 lumbar spine 및 pelvic bone에 방사선치료(30 Gy/13 Fx) 13차례를 받았다. 이후 2016년 1월 4일 chest CT 상 양쪽 폐에 전이 및 재발성 다발성의 작은 결절들이 발견되어 2016년 1월 25일부터 Afatinib을 복용하던 중 한⋅양방 병용치료를 위하여 2016년 5월 23일 본원에 방문하였다.
-
주소증 및 변증소견
1) 구내염(stomatitis) : Afatinib 복용 이후인 2016년 2월경부터 입 안이 헐고 붓는 통증이 발생하였다. 2016년 5월 23일 내원시 NRS (Numeric rating scale) 5의 통증을 호소하였다. 2) 식사량(밥 1/2공기), 식욕 부진, 소화 양호, 대변(1회/일, 정상변, 잔뇨감 없음), 소변(5-6회/일, 정상뇨, 야간뇨 2-3회, 잔뇨감 없음), 수면 (4-5시간/일, 천면 경향), 舌質淡紅, 苔薄白, 齒痕, 脈沈弱, 辨證(肺腎兩虛)
-
복용약물
1) 지오트립정 20 mg(1-0-0) : Afatinib dimaleate 29.56 mg, 표적치료 항암제 2) 삼칠충초정 250 mg(2-2-2) : Panax notoginseng Radix 81 mg, Cordyceps militaris 61.5 mg, Panax ginseng C.A. Meyer 61.5 mg, Boswellia carterii BIRDWOOD 46 mg, 항폐암 한약제제
-
평가도구
1) NRS : NRS는 수치평가척도로써 환자의 통증 정도를 숫자로 계량화하는 방법이다. 수집이 편리하고 환자의 주관적 호소를 객관적 지표로 나타낼 수 있다는 장점이 있어 자주 사용된다. 0~10점까지 숫자 통증 등급을 활용하여 통증 없음(0), 경도(1~4), 중간 정도(5~6), 심함(7~10)으로 구분하여 통증을 객관적으로 평가한다. 이 증례에서는 주 증상인 구내염에 대해 평가가 이루어졌다. 2) Response Evaluation Criteria In Solid Tumors (RECIST) : RECIST는 고형 종양에서의 치료반응에 대한 객관적 평가기준으로, 고형 암 치료법을 평가하는 대부분의 임상시험에서 사용되고 있다. 본 증례에서는 RECIST 1.1에 근거하여 종양에 대한 치료반응을 평가하였다14. 3) National Cancer Institute Common Terminology Criteria for Adverse Event(NCI-CTCAE) : NCI-CTCAE는 암환자에게 약이나 의료용 기기를 사용했을 때 부작용의 정도를 정량화, 표준화시킨 평가도구로, NCI-CTCAE version 4.0에 의하여 삼칠충초정의 부작용을 평가하였다15.
-
치료경과
1) 종양의 변화 : 환자는 2016년 1월 4일 chest CT 상 양쪽 폐에 전이 및 재발성 다발성의 작은 결절들이 발견되어 2016년 1월 25일부터 Afatinib을 복용하고 있었고, 본원에 내원하기 전에 검사한 2016년 5월 6일 chest CT상 이미 양쪽 폐에 전이, 재발로 의심되는 다발성의 작은 결절들이 거의 사라져 보이지 않았고 Lt. supraclavicular lymph node 크기도 이전 CT (2016년 1월 4일)보다 감소되어 있었으며, 6th, 8th Rt. rib과 T9의 병변은 변화가 없는 상태였다. 삼칠충초정과 Afatinib 병용투여 이후인 2016년 8월 27일, 2016년 11월 19일 CT에서는 감소된 Lt. supraclavicular lymph node의 크기가 더 커지지 않고 그대로 유지되고 있었고, 6th, 8th Rt. rib과 T9의 병변 또한 변화 없이 유지되고 있었다(Fig. 1). 따라서 RECIST(Response Evaluation Criteria In Solid Tumors) 1.1에 근거하였을 때 불변(SD)의 결과를 확인할 수 있었다14. 종양표지자인 CEA(carcinoembryonic antigen) 와 Cyfra 21-1(cytokeratin 19-fragments)은 2015년 11월 18일 검사시 각각 10.48과 3.6 ng/ml로 상승되어 있었으나 병용투여 시작점인 2016년 5월 24일 각각 정상범위 이내인 1.71과 1.7 ng/ml로 감소되어있었고, 병용투여 이후인 2016년 8월 31일에는 각각 1.06과 0.9 ng/ml로 더 감소하였다(Table 1).
Fig. 1
Comparison of chest computed tomography.
A : Multiple pulmonary metastasis nearly disappeared and Lt. supraclavicular LNs decreased in size compared with previous CT (2016/01/04). No significant change of metastatic lesion at right 6th, 8th ribs and T9 (2016/05/06).
B : The tumors showed no interval changes (2016/08/27).
C : The tumors showed no interval changes (2016/11/19).
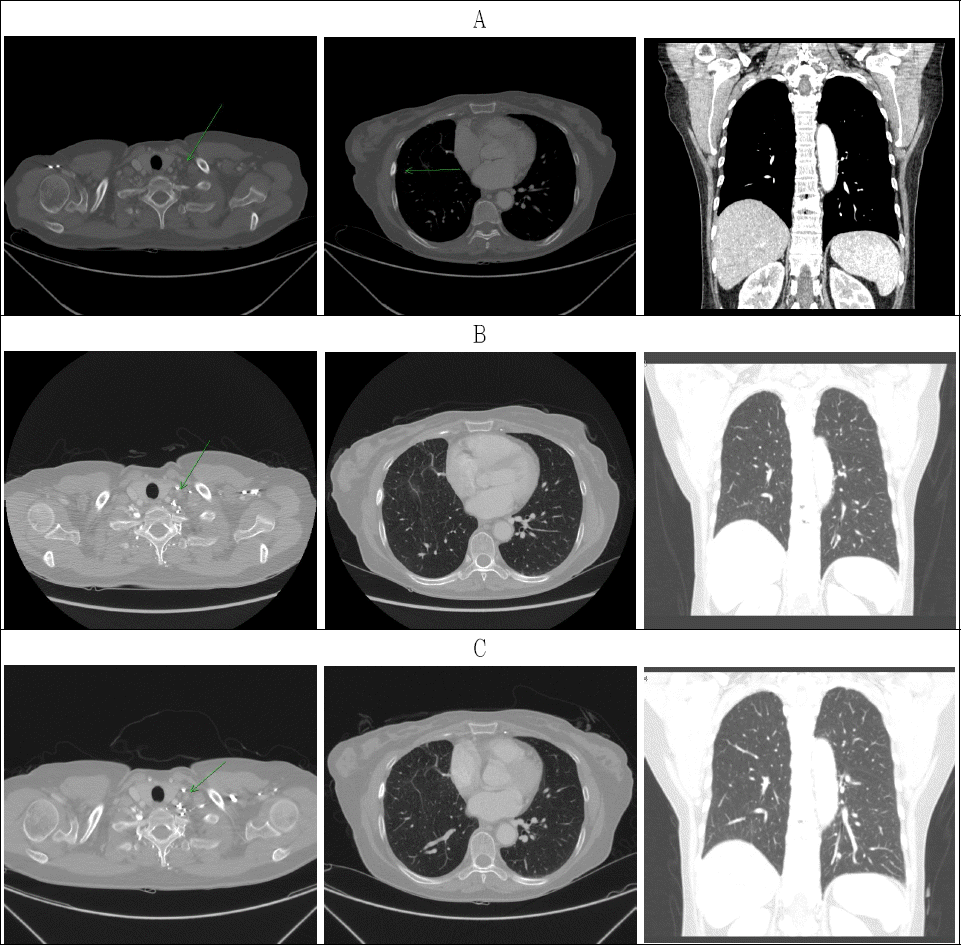
Table 1
|
2015/11/18 |
2016/05/24 |
2016/08/31 |
|
WBC (*103/μl) |
4.5 |
4.6 |
5.1 |
|
RBC (*106/μl) |
3.85↓ |
3.81↓ |
3.71↓ |
|
Hb (g/dl) |
11.0↓ |
10.6↓ |
10.5↓ |
|
Platelet (*103/μl) |
19.0 |
20.3 |
21.9 |
|
Albumin (g/dl) |
4.4 |
4.6 |
4.2 |
|
Total bilirubin (mg/dl) |
0.4 |
0.4 |
0.5 |
|
AST (U/l) |
22 |
24 |
23 |
|
ALT (U/l) |
15 |
17 |
18 |
|
ALP (U/l) |
83 |
50 |
43 |
|
γ-GTP (U/l) |
15 |
14 |
15 |
|
BUN (mg/dl) |
20.8↑ |
14.4 |
17 |
|
Creatinine (mg/dl) |
0.84 |
0.95 |
1.03 |
|
INR |
1.00 |
0.98 |
1.00 |
|
CEA (ng/ml) |
10.48↑ |
1.71 |
1.06 |
|
Cyfra 21-1 (ng/ml) |
3.6↑ |
1.7 |
0.9 |
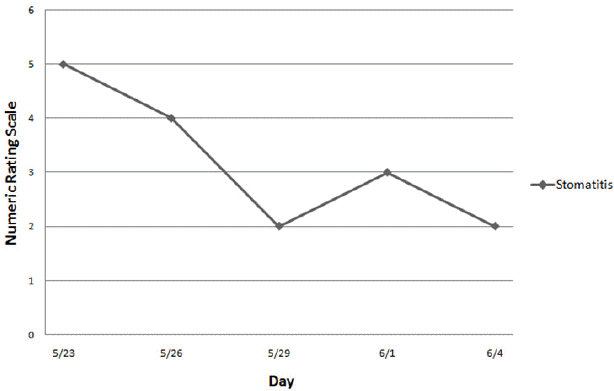
2) 독성이나 부작용 : 치료 기간 중 WBC(White blood cell) 등 염증관련 수치가 정상범위 내에 있었고, 간기능 수치와 BUN(blood urea nitrogen), Creatinine 수치도 정상범위를 유지하여 어떠한 간독성이나 신독성도 나타내지 않았다(Table 1). 또한 NCI-CTCAE version 4.0으로 평가했을 때 Afatinib과 삼칠충초정 병용투여 중 어떠한 부작용도 발생하지 않았다15. 3) 삶의 질 : 2016년 5월 23일 내원 당시 환자는 Afatinib 복용의 부작용으로 인한 구내염(NRS 5) 및 식욕 부진과 피로, 수면불량 등의 제반 컨디션 저하로 일상생활의 불편함을 호소하고 있었다(Eastern Cooperative Oncology Group(ECOG) performance status 2). 삼칠충초정 위주의 한의치료 병행 후, 주소증인 구내염은 12일만에 NRS 5에서 2로 개선되어 그 상태가 유지되었고(Fig. 2), 전반적인 컨디션도 호전되어 일상생활의 불편감이 해소되었다(ECOG 1).
Fig. 2
Changes of numeric rating scale on clinical symptom.
Numeric rating scale of stomatitis was improved significantly after Samchilchoongcho-Jung treatment (12 days).
III. 고 찰
폐암은 전 세계적으로 발생빈도가 증가하는 추세에 있으며, 우리나라의 경우 2016년에 발표된 중앙암등록본부 자료에 의하면 2014년 전체 암 발생의 11.1%로 4위를 차지했고, 남성에서 2위, 여성에서 5위를 차지했다 16. 전체 폐암의 83%를 차지하는 비소세포성 폐암은 40% 이상이 진단시 전이성 병기(stage IV)로 발견되어 일부 환자에서만 수술치료가 가능하며, 수술이 불가능한 비소세포성 폐암의 치료에 있어서 항암화학요법과 방사선 요법이 적용되는데, 항암화학요법에 사용되는 항암제는 암세포뿐만 아니라 정상세포에도 작용하여 세포독성이나 성장 억제효과를 나타내고, 오심, 구토, 탈모, 신경계 부작용, 감염 등 전신적인 부작용을 나타내어 삶의 질을 저하시킨다. 따라서 최근에는 암세포의 발생과 활동에 관여하는 특이 분자의 변이에 대한 이해를 바탕으로 이것을 치료목표로 삼는 표적치료에 대한 연구가 활발하게 진행되고 있다. 비소세포성 폐암에 사용되는 대표적인 표적치료제로는 Gefitinib(상품명 Iressa), Erlotinib(상품명 Tarceva), Pemetrexed(상품명 Alimta) 등이 있다. 본 증례에서 사용된 Afatinib은 EGFR만 차단하는 1세대 약물과 달리 EGFR(ErbB1), HER2(ErbB2), ErbB4 등 3가지 ErbB family 모두를 차단하는 2세대 표적항암제로서 T790M을 경유한 EGFR-TKI(Gefitinib 또는 Erlotinib)에 대한 획득내성을 보이는 비소세포성 폐암에 대한 치료제로써 개발된 Irreversible EGFR-TKI이다 17. LUX-Lung 3과 LUX-Lung 6에서 기존 표준화학요법 대비 Afatinib의 유의한 전체 생존기간(Overall Survival, OS) 향상이 보고되었고 7, 편평세포폐암 환자를 대상으로 한 LUX-Lung 8 결과, erlotinib 대비 OS과 PFS를 유의하게 개선하였으며 18, Gefitinib과 효능을 직접 비교한 연구인 LUX-Lung 7에 따르면 Afatinib이 Gefitinib 대비 폐암 진행 위험을 27%까지 유의하게 감소시키고, PFS 또한 우위를 입증했다 19. 그러나 Gefitinib, Erlotinib, Afatinib과 같은 EGFR-TKI 제제는 뛰어나 치료성적에도 불구하고 대개 9-13개월 정도가 지나면 2차 내성이 생기고 median PFS time이 9-12개월에 불과하며, 설사나 피부발진, 손발톱 주위염, 구내염, 구역, 구토 등의 부작용이 있다 17-19. 따라서 시간경과 후에 발생할 수 있는 표적치료제 내성의 출현 및 부작용을 극복하는 연구가 치료율 향상에 있어 매우 중요하게 되었다. 한의학적 치료는 서양의학의 통상 암 치료와 병행하였을 때 부작용 감소, 삶의 질 개선 뿐만 아니라 궁극적으로는 종양퇴축 및 생존율 향상에 시너지 효과를 낼 수 있는 가능성을 가지고 있다. 현재까지 이루어진 한의학적 연구들을 살펴보면 폐암치료에 사용되고 있는 한방약물들은 대부분 다중 표적치료에 해당된다고 할 수 있다. 본 증례에서 사용된 삼칠충초정은 기존의 항암플러스를 폐암치료 한약제제로 발전시킨 것으로 삼칠근, 동충하초, 인삼, 유향의 4가지 약제로 구성되어 있고, xenograft 동물모델에서 항폐암효과가 있음이 보고되어 있다 12. 모태가 된 항암플러스의 경우 인간 비소세포성 폐암세포주에서 성장을 억제하고 20, 진행성 비소세포성 폐암환자에 투여한 결과 암의 성장을 억제하고 삶의 질을 개선하는데 일정 정도 기여했음이 보고되었다 9. 삼칠근의 notoginsenoside R1 성분은 인간 결장암세포주의 전이를 억제하고, trilinolein은 A549 비소세포성 폐암세포주의 증식을 억제함이 보고되었다 21,22. 또한 동충하초는 p53과 p21 농도를 증가시킴으로써 비소세포성 폐암세포주의 성장을 억제하고, cordycepin은 비소세포성 폐암세포주에서 caspase-8의 활성을 억제하는 c-FLIPL를 저해하여 apoptosis를 유발한다 23,24. 인삼의 Rg3 성분은 nuclear factor-κB pathway를 조절함으로써 비소세포성 폐암세포주가 γ-radiation에 민감하게 하고 25. 유향의 boswellic acid 성분은 in vitro에서 NF-κB를 억제하여 염증을 억제하고, caspase를 활성화시키고 Bax 발현을 증가시켜 apoptosis를 유발한다고 보고되었다 26. 상기 환자를 살펴보면 2014년 2월에 stage Ib (T2aN0M0)의 비소세포성 폐암을 진단받고 폐엽절제술 및 화학항암요법(NP)을 시행했으나, 2015년 3월경 다발성 뼈전이로 방사선치료를 받았고, 2016년 1월 양 폐엽에 재발성의 다발성 작은 결절들이 발견되어 second line의 치료로 Afatinib을 복용하던 중이었다. 2016년 5월 23일 내원 당시 Afatinib 복용의 부작용으로 인한 구내염(NRS 5) 및 식욕부진, 피로, 수면 불량 등의 제반 컨디션 저하를 호소하고 있었다. 삼칠충초정 위주의 한의치료 병행 후, 치료 초기 3주 이내에 구내염이 NRS 5에서 2로 개선되었고, 제반 컨디션이 호전되어 일상생활에 불편감이 해소되었다( Fig. 2). 병용치료 기간 중 혈액검사상 종양표지자인 CEA와 Cyfra 21-1가 감소된 상태를 유지하였으며, 간독성이나 신독성은 나타나지 않았다( Table 1). 그리고 병용치료 이후인 2016년 8월 27일, 2016년 11월 19일 CT에서 감소된 Lt. supraclavicular lymph node의 크기 및 6th, 8th Rt. rib과 T9의 전이 병변이 변화 없이 유지되고 있어 RECIST 1.1에 근거하였을 때 불변(SD)에 준하는 결과는 확인할 수 있었다( Fig. 1), 2017년 2월 초 최종 내원시까지 환자의 제반상태가 양호하였고 추가로 진행된 2017년 1월 CT상에서도 불변 상태를 유지하였음을 유선상담을 통해 확인할 수 있었다. 다만, 본 증례에서 상기환자가 2016년 1월 25일부터 Afatinib을 복용하고 있었고, 본원에 내원하기 전에 검사한 2016년 5월 6일 chest CT상 이미 양쪽 폐에 전이, 재발로 의심되는 다발성의 작은 결절들이 거의 사라져 보이지 않았다는 점과 종양표지자인 CEA와 Cyfra 21-1이 병용투여 시작점인 2016년 5월 24일에 이미 각각 정상범위 이내인 1.71과 1.70 ng/ml로 감소되어 있었다는 점을 보았을 때 종양에 대한 효과가 Afatinib 단독의 효과만일 가능성을 배제할 수 없다. 하지만 병용투여 이후인 2016년 8월 31일 혈액검사상 CEA와 Cyfra 21-1가 각각 1.06과 0.9 ng/ml로 정상범위 내를 유지하였고, Afatinib 복용의 부작용으로 인한 구내염 및 제반 컨디션 저하의 개선을 감안하였을 때 삼칠충초정의 병용투여가 종양크기의 불변 및 삶의 질 개선에 일정 부분 기여하였다고 할 수 있을 것이다. 본 증례는 예후가 좋지 않은 재발성 비소세포성 폐암 환자임에도 불구하고 표적치료약물인 Afatinib과 폐암치료 한약제제인 삼칠충초정을 병용함으로써 약 13개월간의 불변(SD)의 효과 및 증상 호전과 환자의 활동도 개선을 보여 보고하는 바이다. 다만 이는 대조군이 없는 단 1례에 불과하고 Afatinib 단독의 효과만일 가능성도 배제할 수 없는 한계를 지닌다. 그럼에도 불구하고 Afatinib 단독 투여시 PFS가 약 11개월 정도이고 7, 또 수반되는 부작용과 내성 등을 지녔음을 감안할 때 한양방 병용투여를 통해 종양크기 불변 및 삶의 질 개선과 내성억제 가능성 등을 보인 점은 일정 부분 의의가 있다고 할 수 있다. 향후 폐암치료에 있어 한양방 치료를 병행함으로써 기대되는 효과 평가를 위해서는 삼칠충초정과 Afatinib의 병용투여에 대한 추가적인 임상연구가 필요할 것으로 판단된다.
참고문헌
1. Siegel RL, Miller KD, Jemal A. Cancer Statistics 2017. CA Cancer J Clin 2017:67(1):7–30.   2. Miller KD, Siegel RL, Lin CC, Mariotto AB, Kramer JL, Rowland JH, et al. Cancer treatment and survivorship statistics. 2016 CA Cancer J Clin 2016:66(4):271–89.   3. Boolell V, Alamgeer M, Watkins DN, Ganju V. The Evolution of Therapies in Non-Small Cell Lung Cancer. Cancers(Basel) 2015:7(3):1815–46.    4. Xu M, Xie Y, Ni S, Liu H. The latest therapeutic strategies after resistance to first generation epidermal growth factor receptor tyrosine kinase inhibitors in patients with non-small cell lung cancer. Ann Transl Med 2015:3(7):96.   5. Mitsudomi T, Morita S, Yatabe Y, Negoro S, Okamoto I, Tsurutani J. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancerharbouring mutations of the epidermal growth factor receptor(WJTOG3405): an open label, randomised phase 3 trial. Lancet Oncol 2010:11(2):121–8.   6. Rosell R, Carcereny E, Gervais R, Vergnenegre A, Massuti B, Felip E, et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer (EURTAC): a multicentre, open-label, randomised phase 3 trial. Lancet Oncol 2012:13(3):239–46.   7. Yang JC, Wu YL, Schuler M, Sebastian M, Popat S, Yamamoto N, et al. Afatinib versus cisplatin-based chemotherapy for EGFR mutation-positive lung adenocarcinoma(LUX-Lung 3 and LUX-Lung 6): analysis of overall survival data from two randomised, phase 3 trials. Lancet Oncol 2015:16(2):141–51.   8. Park SC, Yoo HS, Cho CK, Lee YW. Recent Experimental Tendency for Herbal Medicines Treating Lung Cancer in South Korea. J of Kor Traditional Oncology 2008:13(1):43–54.
9. Zheng HM, Yoon JW, Lee YW, Cho CK, Oh DS, Yoo HS. Case Series of Advanced Non-small Cell Lung Cancer Patients Treated with Han-Am-Plus. Korean J Orient Int Med 2011:32(1):113–20.
10. Kwon EM, Jerng UM, Kim KS, Lee SK, Choi WC, Yoon SW. Two Cases of Non-small Cell Lung Cancer Patients Treated with Allergen Removed Rhus Verniciflua Stokes Based Traditional Korean Medicine and Chemotherapy. J of Kor Traditional Oncology 2009:14(1):13–20.
11. Li SG, Chen HY, Ou-Yang CS, Wang XX, Yang ZJ, Tong Y, et al. The efficacy of Chinese herbal medicine as an adjunctive therapy for advanced non-small cell lung cancer: a systematic review and meta-analysis. PLoS One 2013:8(2):e57604.  12. Kang HJ, Park SJ, Park YM, Yoo HS, Kang IC. Inhibitory effects of HangAmDan-B1 (HAD-B1) on A549 lung cancer cell proliferation and tumor growth in a xenograft model. Academia Journal of Scientific Research 2016:4(7):187–93.
13. Chang SH. Letter to Editor : Gamchosasim-tang, Sawi-tang and Giotrif Combination Therapy for Metastatic Non-Small-Cell Lung Adenocarcinoma; A Regression Case. J of Kor Traditional Oncology 2015:20(2):1–4.  14. Eisenhauer EA, Therasse P, Bogaerts J, Schwartz LH, Sargent D, Ford R. New response evaluation criteria in solid tumours: Revised RECIST guideline(version 1.1). Eur J Cancer 2009:45(2):228–47.   16. Ministry of health &wellfare, Korea central cancer registry, National cancer center. Annual report of cancer statistics in Korea in 2014 2016:
17. Li D, Ambrogio L, Shimamura T, Kubo S, Takahashi M, Chirieac LR, et al. BIBW2992, an irreversible EGFR/HER2 inhibitor highly effective in preclinicallung cancer models. Oncogene 2008:27(34):4702–11.    18. Soria JC, Felip E, Cobo M, Lu S, Syrigos K, Lee KH, et al. Afatinib versus erlotinib as second-line treatment of patients with advanced squamous cell carcinoma of the lung(LUX-Lung 8): an open-label randomised controlled phase 3 trial. Lancet Oncol 2015:16(8):897–907.   19. Park K, Tan EH, O’Byrne K, Zhang L, Boyer M, Mok T, et al. Afatinib versus gefitinib as first-line treatment of patients with EGFR mutation-positive non-small-cell lung cancer (LUX-Lung 7): a phase 2B, open-label, randomised controlled trial. Lancet Oncol 2016:17(5):577–89.   20. Lee CY, Hsieh SL, Hsieh S, Tsai CC, Hsieh LC, Kuo YH, et al. Inhibition of human colorectal cancer metastasis by notoginsenoside R1, an important compound from Panax notoginseng. Oncol Rep 2017:37(1):399–407.   21. Chou PY, Huang GJ, Pan CH, Chien YC, Chen YY, Wu CH, et al. Trilinolein inhibits proliferation of human non-small cell lung carcinoma A549 through the modulation of PI3K/Akt pathway. Am J Chin Med 2011:39(4):803–15.   22. Bizarro A, Ferreira IC, Soković M, van Griensven LJ, Sousa D, Vasconcelos MH, et al. Cordyceps militaris(L.). Link Fruiting Body Reduces the Growth of a Non-Small Cell Lung Cancer Cell Line by Increasing Cellular Levels of p53 and p21. Molecules 2015:20(8):13927–40.   23. Yu X, Ling J, Liu X, Guo S, Lin Y, Liu X, et al. Cordycepin induces autophagy-mediated c-FLIPL degradation and leads to apoptosis in human non-small cell lung cancer cells. Oncotarget 2017:8(4):6691–9.  24. Wang L, Li X, Song YM, Wang B, Zhang FR, Yang R, et al. Ginsenoside Rg3 sensitizes human non-small cell lung cancer cells to γ-radiation by targeting the nuclear factor-κB pathway. Mol Med Rep 2015:12(1):609–14.   25. Khan MA, Ali R, Parveen R, Najmi AK, Ahmad S. Pharmacological evidences for cytotoxic and antitumor properties of Boswellic acids from Boswellia serrata. J Ethnopharmacol 2016:191:315–23.   26. Choi YJ, Shin DY, Lee YW, Cho CK, Kim GY, Kim WJ, et al. Inhibition of cell motility and invasion by HangAmDan-B in NCI-H460 human non-small cell lung cancer cells. Oncology Reports 2011:26(6):1601–9. 
|
|













