Ⅰ. 서 론
오자연종환(五子衍宗丸, Ojayeonjong-hwan, OJYJH)의 기원에 대한 견해로는 唐朝 ≪道藏 懸解錄≫에 수록된 守仙五子丸, 元代 ≪丹溪心法≫에 수록된 유사 처방을 근원으로 보기도 하지만, 명나라 시대의 장시철(張時徹)이 저술한 ≪攝生衆妙方≫에 “男服此藥, 添精補髓, 疏利腎氣, 不問下焦虛實寒熱, 服之自能平秘. 舊稱古今第一種子方”의 효능으로 처음 수록된 처방으로 보는 견해가 주류를 이루고 있다1.
오자연종환에 대한 선행 연구로는 생식관련 연구가 가장 많고 그 다음으로는 중추 신경계 계통 연구가 많았다. 생식관련 실험 연구로는 cyclophosphamide으로 유발시킨 수컷 생쥐의 생식 독성을 감소시키는 효과의 감소 효과2, Hydrogen peroxide에 의해 유도된 남성 생식 세포 GC-1 cell에서의 ROS 생성을 유의하게 억제 효능3, 성 성선기능 저하증의 노화 쥐 모델에서 SOD의 추치 증가와 더불어 8-OHdG (8-hydroxy-2’-deoxyguanosine)의 수치 감소 및 고환 조직에서 안드로겐 수용체 발현을 증가시키는 효과4에 관한 연구가 있다. 또한 FSH, Inhibin B, Androgen binding protein 등의 단백분비를 촉진하여 정자의 발생 능력을 증가시키는 효능에 관한 연구5, NLRP3/ASC/Caspase-1 신호 경로에 영향을 주어 고환염에 대한 항염증 작용에 관한 연구6, 부분 요도 폐쇄로 인한 배뇨근 과활동성에 대한 항염증, 항산화 효과7 등이 보고되어 있다. 생식관련 임상연구로는 남성의 少弱精子症 또는 무정자증(oligoasthenospermia)에 의한 불임 개선 효과에 관한 연구8, 12주간의 오자연종환 복용만으로 총 정자수의 증가와 자연 수태율의 향상 효과가 있음을 밝힌 연구가 있으며9, 64명의 남성 불임 환자의 정자의 질을 높일 뿐만 아니라 불임관련 증상도 현저한 개선 효과가 있음을 나타냈으며10, 희소무력정자증(Oligoasthenozoospermia) 환자에서 정자 농도, 운동성, 정액량이 증가하였고, 정자 DNA 분절지수는 감소하여 정자의 질을 높이는 효과가 있음을 연구11한 논문 등이 보고되어 있다.
중추 신경계 관련 실험 연구로는 D galactose로 유발된 쥐 모델에서 학습 및 기억력 향상 효과가 있음을 확인한 연구12, 자가면역성 척추염의 염증매개 인자(IL-6, IL-17, TNF-α, IFN-γ, NF-κB)의 발현을 억제하는 효과가 있음을 확인한 연구13, 신경관 기형 세포의 세포주기에 영향을 미쳐 신경관 기형을 예방하는 효과가 있음을 확인한 연구14 등이 보고되었고, 임상연구로는 신허형 파킨슨병의 경도 인지 장애 개선하여 MMSE(Mini-Mental State Examination), MoCA(Montreal Cognitive Assessment) 점수를 높였고, 동반된 제반 증상을 개선하여 기억력도 향상시키는 효과가 있음을 밝힌 연구15와, Leber 유전성 시신경 위축 환자의 시력, 시야와 시각유발전위(vision evoked potential)가 개선되었고, 기전은 mitochondrial DNA mutation rate의 감소에 기인함을 확인한 연구16 등이 보고되어 있다.
본 연구는 오자연종환의 항산화 효능을 검증하기 위하여 설계되었다. 열수 및 에탄올 추출물을 대상으로 DPPH(1,1-diphenyl-2-picrylhydrazyl) 자유 라디칼 및 ABTS(2,2’-azinobis-(3-ethyl-benzothiazoline- 6-sulfonic acid)) 양이온 라디칼 소거 활성능과 FRAP(ferric reducing ability of plasma)법을 이용한 환원력을 비교하였으며, 각 추출물의 항산화력과 총 페놀 함량 사이의 연관성을 조사하였다. 이를 기초로 in vitro 세포 실험계에서 항산화 활성 효능을 재평가하기 위해 C2C12 근아세포를 이용하여, FFITC(Annexin V-fluorescein-5-isothiocyanate) 염색을 통한 apoptosis 분석, 미토콘드리아 막 전위(mitochondrial membrane potential, MMP, Δψm) 분석, 세포 내 활성산소종(ROS) 수준 측정 등을 통해 유의한 결과를 얻었기에 보고하는 바이다.
Ⅱ. 재료 및 방법
1. 추출물 제조
본 실험에서 사용된 구성 한약재들은 ⃝⃝대학교 부속 한방병원에서 구입하였으며, 구성 한약재 및 비율은 Table 1에 제시하였다. 오자연종환의 열수 추출물을 얻기 위해 한약재 100 g 당 1 L의 증류수를 가하여 3시간 동안 열수 추출하였다. 그리고 오자연종환의 에탄올 추출물을 얻기 위해 약재 100 g 당 2 L의 70% 에탄올을 가하여 초음파추출(ultra-sonification extraction)로 추출물을 제조하였다. 이를 위하여 추출 용기에 한약재와 70% 에탄올을 혼합한 후 초음파 수조(Power sonic 405, SJ BioLab, Anyang, Republic of Korea) 바닥에 닿지 않도록 하여 40 KHz 초음파를 가하여 2시간 동안 추출하였다. 오자연종환 추출물은 여과지(Whatman No. 3 filter paper, Whatman International Ltd., Maidstone, UK)로 여과한 다음 용매를 감압회전농축기(Eyela, A-1000, Tokyo Rikakikai Co., Tokyo, Japan)를 이용하여 농축하였다. 농축된 각각의 추출물은 동결건조기(FD8508, Ilshin Co., Seoul, Republic of Korea)에서 동결 건조하여 분말화 하였다. 각 추출물의 수율은 건조중량을 기준으로 환산하였다. 이후 열수 추출물(water extract of Ojayeonjong-hwan, WEO)은 멸균된 증류수에, 에탄올 추출물(ethanol extract of Ojayeonjong-hwan, EEO)은 dimethyl sulfoxide(DMSO, Sigma-Aldrich Chemical Co. St. Louis, MO, USA)에 200 mg/ml의 농도로 녹였으며 사용 전까지 -20 ℃에서 보관하였으며, 실험방법에 따라 적절하게 희석하여 사용하였다.
2. 1,1-diphenyl-2-picrylhydrazyl(DPPH) 라디칼 소거 활성 측정
DPPH 라디칼 소거 활성은 Munteanu 등 방법에 따라 측정하였다17. DPPH 라디칼에 대한 추출물의 소거 활성을 측정하기 위해, 메탄올에 용해시킨 0.4 mM의 DPPH(Sigma-Aldrich Chemical Co.) 용액 150 μl와 다양한 농도(0.15625~20 mg/ml)로 희석해 둔 각각의 오자연종환 추출물 100 μl를 첨가하고 37 ℃에서 암소에서 반응시켰다. 30분 후 microplate reader(Molecular Devices, Sunnyvale, CA, USA)를 이용하여 518 nm에서 흡광도를 측정하였다. 양성대조군으로는 trolox(Sigma-Aldrich Chemical Co.), 음성대조군으로는 0.4 mM DPPH 용액에 추출물 대신 메탄올을 첨가하여 사용하였다. 반응물에 대한 흡광도 결과는 음성대조군에 대한 추출물의 DPPH 라디칼 소거 활성도를 백분율로 나타냈으며, 다음의 식을 이용하여 계산하였다.
DPPH radical scavenging activity(%)=(1-O.D. of sample/O.D. of negative control)×100
3. 2,2’-azinobis-(3-ethyl-benzothiazoline-6-sulfonic acid) ABTS 라디칼 소거 활성 측정
ABTS 라디칼 소거 활성은 Re 등의 방법에 따라 항산화 활성을 측정하였다18. 이를 위해, 에탄올에 용해시킨 7 mM의 ABTS(Sigma-Aldrich Chemical Co.)와 2.45 mM의 potassium persulfate(Sigma-Aldrich Chemical Co.)를 1:1(v/v)의 비율로 혼합하여 암소에서 24시간 동안 반응시켜 ABTS 양이온 라디칼을 형성시켰다. 그 후, 실험 직전에 ABTS 용액의 흡광도가 734 nm에서 0.7~0.8가 되도록 희석하여 사용하였다. 그리고 0.15625~20 mg/ml의 다양한 농도의 추출물 10 μl와 희석한 ABTS 용액 190 μl를 혼합하여 6분 동안 반응시킨 후 microplate reader를 이용하여 734 nm에서 흡광도를 측정하였다. 양성대조군으로는 trolox, 음성대조군으로는 희석한 ABTS 용액을 사용하였으며 다음의 식에 따라 ABTS 양이온 라디칼 소거 활성을 계산하였다.
ABTS radical cation scavenging activity(%)= (1-O.D. of sample/O.D. of negative control)×100
4. 총 페놀성 화합물 함량 측정
오자연종환 추출물에 함유된 총 페놀성 화합물 함량(Total phenolic contents)은 Folin-Ciocalteu’s의 방법19에 의해 측정하였다. 적정 실험 농도로 희석한 각 추출물 50 μl에 2% Na2CO3 1 ml을 첨가하고 2분 동안 상온에 반응시켰다. 그 후 Folin-Ciocalteu (50%, v/v, Sigma-Aldrich Chemical Co.) 시약 50 μl를 첨가하고 혼합하여 암소에서 30분간 반응시킨 후 microplate reader를 이용하여 750 nm에서 흡광도를 측정하였다. 표준물질로 gallic acid(Sigma-Aldrich Chemical Co.)를 사용하여 표준곡선을 작성하였고 추출물의 페놀성 화합물 함량은 mg gallic acid equivalents(GAE)/g of sample dry weight(DW)로 나타내었다.
5. FRAP 활성 측정
FRAP을 이용한 환원력(reducing power)은 Pérez-Lamela 등의 제안한 방법에 따라 측정하였다20. 300 mM acetate buffer(pH 3.6), 10 mM 2,3,5-triphenyltetrazolium chloride(Sigma-Aldrich Chemical Co.) 및 20 mM FeCl3를 각각 10:1:1 (v/v/v)의 비율로 혼합하여 37 ℃에서 20분간 반응시켜 FRAP 시약을 제조하였다. 240 μl의 FRAP 시약에 각각의 추출물을 10 μl씩 첨가하여 혼합한 후 상온에서 5분간 반응시키고 593 nm에서 흡광도를 측정하였다. Gallic acid를 사용하여 표준 곡선을 작성하였으며, 환원력은 mg GAE/g of sample DW로 나타내었다.
6. 세포 배양
본 실험을 위해 사용한 C2C12 근아세포는 American Type Culture Collection(ATCC, Manassas, VA, USA)으로부터 구입하였다. C2C12 세포의 배양을 위하여, Dulbecco Modified Eagle Medium(DMEM, Welgene Inc., Daegu, Republic of Korea)에 10% fetal bovine serum(FBS, Welgene Inc.), 1% penicillin-streptomycin (Welgene Inc.)을 첨가하여 사용하였으며, 37 ℃ 및 5% CO2 조건에서 배양하였다.
7. 세포 생존율 측정
산화적 스트레스에 대한 오자연종환 에탄올 추출물(EEO)의 산화적 스트레스에 대한 보호 효과를 평가하기 위해 수용성 tetrazolium salt가 세포 내 탈수소 효소(dehydrogenase)에 의해 환원됨으로써 주황색의 formazan을 형성하여 살아있는 세포를 정량화시키는 CCK8 분석법을 이용하였다. 세포의 생존율을 측정하기 위하여 C2C12 세포를 6 well-plate에 1.5×104 cells/well의 농도로 seeding하고 24시간 동안 부착 및 배양하였다. 그 후 적정 농도의 추출물들을 1시간 전 처리하였고 500 μM 농도의 H2O2(Sigma-Aldrich Chemical Co.)를 24시간 동안 처리하였다. CCK 8 용액(Abcam Inc., Cambridge, MA, USA)은 배지의 10%에 해당하는 용량으로 각 well에 처리하고 1시간 동안 반응시킨 후 반응액을 96-well plate로 옮겨 microplate reader를 이용하여 460 nm에서 흡광도를 측정하였다. 세포의 생존율은 대조군을 기준(100%)으로 하여, 처리군의 상대적인 백분율을 나타내었다. 아울러 동일 조건에서 배양된 세포들의 형태 변화는 도립현미경(Carl Zeiss, Oberkochen, Germany) 하에서 관찰하였다.
8. 4’,6-diamidino-2-phenylindole(DAPI) 형광 염색
산화적 스트레스 또는 오자연종환 추출물 처리에 의한 C2C12 세포에서 핵의 형태적 변화를 확인하기 위해 DAPI 염색을 이용하였다. C2C12 세포에 각각의 추출물과 H2O2를 24시간 동안 처리한 후, 세포를 4% formaldehyde로 상온에서 10분 동안 고정시켰다. C2C12 세포를 phosphate buffered saline(PBS)으로 세척하고 2.5 μg/ml로 희석한 DAPI 용액(Sigma-Aldrich Chemical Co.)을 처리하여 암소에서 10분 동안 염색하였다. 그 후, 세포를 PBS로 세척 및 건조 후 mounting 용액과 cover glass로 덮었다. DAPI로 염색된 세포의 핵은 형광현미경(EVOS FL Auto 2, Thermo Fisher Scientific, Waltham, MA, USA)을 이용하여 관찰하였다.
9. 세포 주기 측정
Propidium iodide(PI)를 이용하여 각 세포의 DNA 함량에 따른 각 세포 주기 분포를 분석하였다. C2C12 세포에 각 처방전 추출물 및 H2O2를 처리하고 24시간 뒤, 세포를 수집하였다. 수집한 세포는 BD Cycletest™ Plus kit(BD Biosciences, Franklin Lakes, NJ, USA)의 trypsin 용액과 trypsin inhibitor/ribonuclease A 용액을 넣고 각각 10분 동안 상온에서 반응시키고 마지막으로 PI 용액을 넣고 4 ℃, 암소에서 10분 동안 반응시켰다. 그리고 반응시킨 세포는 flow cytometer(Accuri C6 flow cytometer, BD Biosciences)를 사용하여 분석하였다. 세포사멸의 정량적 평가를 위하여 sub-G1기에 속하는 세포의 빈도를 측정하였다.
10. Annexin V-fluorescein-5-isothiocyanate (FITC) 염색을 통한 apoptosis 분석
세포사멸 유도의 또 다른 정량적 분석을 위하여 상기에서 언급한 동일한 조건에서 배양된 세포를 수집하여 FITC Annexin V apoptosis detection kit (BD Biosciences)를 이용하여 제조사의 권장 방법에 따라 flow cytometer를 이용하여 분석하였다. 이를 위하여, 수집된 세포에 kt에 제공된 binding buffer를 혼합하고 FITC-annexin V 및 PI 용액을 첨가하여 20분 동안 염색하였다. 염색된 세포에서 발하는 형광 강도를 측정하기 위해 flow cytometer를 이용하였으며, 세포사멸이 유도된 세포는 annexin V+/PI- 및 annexin V+/PI+ 세포의 비율을 산출하였다.
11. 총 단백질 분리 및 Western blot 분석
산화적 스트레스에 대한 오자연종환 추출물의 보호 효과에 관여하는 유전자들의 발현 변화를 단백질 수준에서 평가하였다. 이를 위하여 다양한 처리 조건에서 배양된 세포를 수집하여, lysis buffer [250 mM NaCl, 25 mM Tris-Cl(pH 7.5), 5 mM ethylenediaminetetraacetic acid(EDTA, pH 8.0), 1% NP-40, 1 mM 4-(2-aminoethyl) benzene sulfonyl fluoride hydrochloride, 5 mM dithiothreitol 및 protease inhibitor cocktail]를 첨가하고 30분 동안 4 ℃에서 반응시켰다. 반응액을 14,000 rpm에서 30분 동안 원심 분리하여 총 단백질이 포함되어 있는 상층액을 수집하였다. 상층액을 대상으로 단백질 정량 시약(Bio-Rad Laboratories, Inc., Hercules, CA, USA)을 이용하여 595 nm에서 microplate reader로 단백질 농도를 측정하였다. 각 샘플 당 3 μg/μl의 농도로 단백질을 정량하고 Laemmli sample buffer(Bio-Rad Laboratories)와 1:1(v/v)로 혼합한 후 95 ℃에서 5-10분 동안 가열하고 사용하기 전까지는 -20 ℃에서 보관하였다. 분리한 동량의 단백질을 sodium dodecyl sulfate(SDS)-polyacrylamide gel을 이용하여 전기 영동하고 nitrocellulose membrane으로 전이시켰다. 단백질이 전이된 membrane은 5% skim milk와 1시간 동안 상온에서 반응시킴으로써 비 특이적 반응을 차단하였고, 이후 적정 농도로 희석한 1차 항체와 2차 항체를 차례로 적용시킨 후 enhanced chemiluminescence detection kit(ECL, Thermo Fisher Scientific)을 이용하여 단백질의 발현을 시각화 하였고 이미지 분석 장비(Fusion Solo S system, Vilber Loumat, Collégien, France)를 이용하여 분석하였다. 본 연구에 사용된 항체 정보는 Table 2에 제시하였다.
Table 2
Antibodies used in the Present Study
12. MMP(Δψm) 분석
5,5,6,6-Tetrachloro-1,1,3,3-tetraethylbenzimidazolylcarbocyanine iodide(JC-1)은 선택적으로 미토콘드리아를 염색하며, MMP가 감소함에 따라 적색 형광에서 녹색 형광으로 가역적으로 색이 변할 수 있어 MMP를 측정하기 위하여 대표적으로 사용되고 있다. C2C12 세포에 오자연종환 추출물 및 H2O2를 처리하고 24시간 뒤, 세포를 수집하였다. 수집한 세포는 5 μg/ml의 JC-1(Sigma-Aldrich Chemical Co.)으로 상온에서 20분 동안 염색하였다. 그 후 PBS로 세포를 다시 세척하고 MMP의 변화를 flow cytometer를 이용하여 분석하였다.
13. 세포 내 활성산소종(ROS) 수준 측정
H2O2 및 오자연종환 추출물의 단독 또는 동시 처리에 따른 세포 내 ROS 수준의 변화를 측정하기 위해 2’, 7’-dichlorodihydrofluorescein diacetate (DCF-DA, Sigma-Aldrich Chemical Co.)를 이용하였다. 각 추출물 및 H2O2 처리 후 10 μM의 DCF-DA를 첨가하여 20분 동안 37 ℃에서 염색하였다. 그런 다음, 세포를 수집하여 flow cytometer 및 형광현미경을 이용하여 세포 내 ROS 수준의 변화를 측정 및 관찰하였다.
Ⅲ. 결 과
1. 오자연종환 열수 및 에탄올 추출물의 수율 비교
본 연구에서 사용한 오자연종환의 열수 및 70% 에탄올 추출물의 생리활성을 비교하기 위해 얻은 각 추출물의 수율은 추출물 조제에 사용한 원료 중량에 대한 추출물의 추출액을 농축 및 동결 건조하여 얻은 건물 중량을 백분율로 나타낸 값이다. 오자연종환의 열수 및 70% 에탄올 추출물의 수율은 각각 31.8%와 27.1%이었다.
2. 오자연종환 열수 및 에탄올 추출물의 DPPH 자유 라디칼 소거 활성 비교
3. 오자연종환의 열수 및 에탄올 추출물의 ABTS 양이온 라디칼 소거 활성 비교
다음은 ABTS를 이용한 항산화능을 평가하였으며, ABTS 양이온 라디칼 소거 활성은 열수 및 에탄올 추출물의 농도 의존적으로 증가하였으며, 2,5 mg/ml의 농도에서의 WEO가 94.6%로 가장 높게 나타났다(Fig. 1). 그리고 WEO는 1.25 mg/ml 이상, EEO는 5 mg/ml 이상의 농도에서 양성대조군으로 사용한 100 μg/ml의 trolox 보다 높은 ABTS 양이온 라디칼 소거 활성을 나타냈으며, EEO의 가장 높은 농도에서 ABTS 양이온 라디칼 소거 활성은 94.2%로 비교적 높게 나타났다(Fig. 1).
4. 오자연종환 열수 및 에탄올 추출물의 총 페놀 함량 및 환원력 비교
열수 및 70% 에탄올 추출물의 총 페놀 함량을 비교하기 위해 gallic acid를 표준물질로 하여 작성한 표준 곡선을 이용하였으며, 그 결과, WEO가 205.23±3.32 mg GAE/g로 높은 환원력을 나타냈으며, EEO는 95.70±9.22 mg GAE/g로 낮은 값을 나타냈다. 아울러 FRAP 활성 측정을 통한 환원력을 측정한 결과도 마찬가지로 gallic acid를 표준물질로 하여 작성한 표준 곡선을 이용하여 나타냈다. WEO가 222.59±1.95 mg GAE/g로 높은 환원력을 나타냈으며, EEO는 80.90±0.62 mg GAE/g로 낮은 값을 나타냈다. 이상의 결과에서 알 수 있듯이 총 페놀 함량이 높은 추출물이 환원력 또한 높게 나타났음을 확인할 수 있었다.
5. C2C12 세포에서 H2O2로 유도된 산화적 스트레스에 대한 WEO의 영향
산화적 스트레스에 대한 WEO의 보호 효과를 확인하기 위해 세포 독성을 조사하였다. C2C12 근아세포에 WEO를 0.1 mg/ml에서부터 1 mg/ml까지의 다양한 농도로 처리한 후 24시간 뒤 CCK8 방법을 이용하여 세포 생존율을 측정하였다. 0.8 mg/ml 이하의 농도에서는 유의적인 세포 독성을 나타내지 않았다(Fig. 2A). 따라서 세포보호 효과를 확인하기 위한 열수 추출물의 처리농도는 세포 독성을 나타내지 않은 농도인 0.8 mg/ml을 최고 농도로 선정하여 이후 실험을 진행하였다. H2O2로 유도한 산화적 스트레스는 세포 내 산화적 손상을 유발하여 세포 사멸에 따른 세포 생존율 감소를 초래한다. 아울러 산화적 스트레스를 유도하기 위한 H2O2 처리에 따른 세포 생존율 결과는 0.5 mM 이상의 농도에서부터 유의적으로 감소하였다(Fig. 2B). H2O2를 0.5 mM 농도로 처리한 세포 생존율이 63.7±4.8%로 나타난 결과를 바탕으로 산화적 스트레스에 대한 세포보호 효과를 확인하기 위한 H2O2의 처리농도는 0.5 mM로 설정하여 측정하였다. 그 결과, 0.2, 0.4 그리고 0.8 mg/ml의 WEO를 전 처리한 군의 세포 생존율은 H2O2만 처리한 군의 세포 생존율과 비교하여 유의적인 차이가 나타나지 않아 H2O2로 유도한 세포 독성에 대해 보호 효과를 나타내지 않았음을 확인할 수 있었다(Fig. 2C).
Fig. 2
(A) Effect of WEO on the cell viability in C2C12 myoblasts. (B, C) Effect of WEO on H2O2-induced cytotoxicity in C2C12 myoblasts. (B) Cells were treated with the indicated concentrations of H2O2 for 24 h. (C) Cells were treated with indicated concentrations of H2O2 or WEO alone for 24 h or pretreated with or without WEO for 1 h before 0.5 mM H2O2 stimulation for 24 h. Cell viability was analyzed using the CCK8 assay. Data indicated the mean±S.D. (n=3). **p<0.01 and ***p<0.001, compared with untreated control cells.
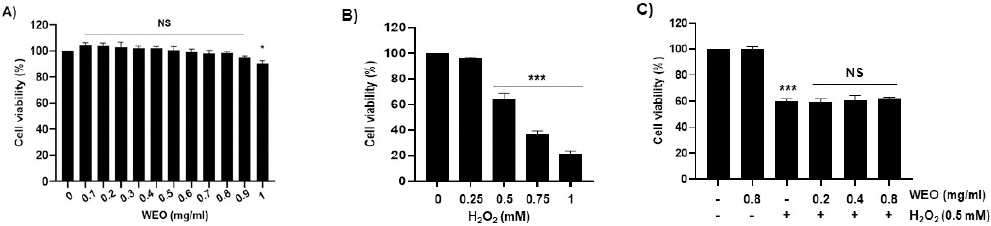
6. C2C12 세포에서 H2O2로 유도된 산화적 스트레스에 대한 EEO의 영향
산화적 스트레스에 대한 EEO의 보호효과를 확인하기에 앞서 EEO 단독처리에 따른 세포 독성을 조사하였다. EEO는 1 mg/ml 농도에서 유의적으로 세포 생존율이 감소하였음을 확인하였으며(Fig. 3A), 이후 0.2, 0.4 및 0.6 mg/ml의 농도를 전처리하여 EEO의 보호효과를 조사하였다. Fig. 3B의 결과에서 볼 수 있듯이, H2O2에 의해 감소한 세포 생존율은 0.2 mg/ml의 EEO에서는 유의적인 차이를 나타내지 않았지만 0.4와 0.6 mg/ml의 EEO에 의해서 유의적으로 증가하였다. 마찬가지로 H2O2에 의해 감소한 세포 밀집도가 EEO에 의해 회복되었음을 관찰할 수 있었고, H2O2 처리에 따른 염색질 응축 현상도 부분적으로 감소하였다(Fig. 3C와 3D). 따라서 EEO의 전 처리에 의해 H2O2로 유도한 세포 생존율 감소 및 세포의 형태적 변화가 회복되어 C2C12 세포에서의 산화적 스트레스에 대한 보호효과를 가지는 것으로 사료된다.
Fig. 3
Effect of EEO on oxidative stress (H2O2)-induced cytotoxicity in C2C12 myoblasts.
Cells were treated with the indicated concentrations of EEO or 0.5 mM H2O2 for 24 h or pretreated with or without EEO for 1 h before 0.5 mM H2O2 stimulation for 24 h.
(A and B) Cell viability was analyzed using the CCK 8 assay. Data indicated the mean±S.D. (n=3). *** p<0.001, compared with untreated control cells; ## p<0.01 and ### p<0.001, compared with H2O2 -treated cells.
(C) The morphology of the cells was visualized under an inverted-phase contrast microscope (×400).
(D) The DAPI-stained nuclei were observed using a fluorescence microscope (Scale bar=10 μm). (C and D) Representative images were presented.

7. C2C12 세포에서 H2O2로 유도된 세포 주기의 변화에 대한 EEO의 영향
H2O2로 유도한 산화적 스트레스에 의해 나타난 세포 주기 변화 관찰을 위해 flow cytometry 분석을 진행하였다. Fig. 4 및 Table 3에 제시한 바와 같이, H2O2의 처리에 의해 G2/M 및 sub-G1의 세포의 빈도가 유의적으로 증가하였다. 반면, EEO를 전처리한 경우에는 EEO의 농도 의존적으로 G2/M 및 sub-G1의 세포의 빈도가 감소하였고 특히, EEO의 고농도인 0.6 mg/ml에서는 유의적으로 감소하였음을 확인하였다.
Fig. 4
Effect of EEO on changes in cell cycle distribution of H2O2-treated C2C12 myoblasts.
Cells were treated with or without the indicated concentrations of EEO for 1 h before treatment with 0.5 mM H2O2 for 24 h. After staining the cells with PI solution, flow cytometry analysis was performed.
(A) Representative histograms of flow cytometry were presented.
(B) The average percentages of cells in each phase of the cell cycle, except for cells belonging to the sub-G1 phase, were displayed.
(C) The frequencies of cells belong to the sub-G1 phase were calculated. The results were expressed as the mean±SD obtained from three independent experiments. *** p<0.001, compared with untreated control cells; ## p<0.01, compared with H2O2-treated cells.
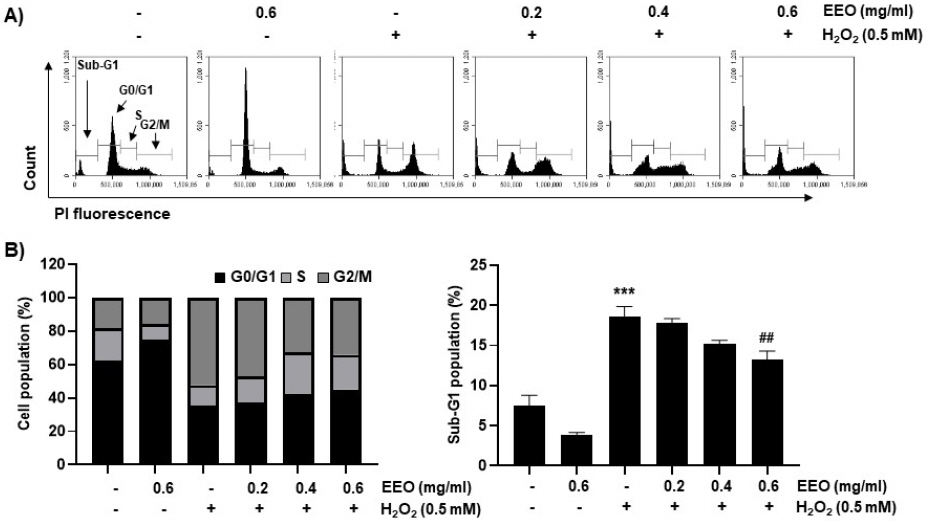
Table 3
Effect of EEO on H2O2-induced Changes of Cell Cycle Distribution in C2C12 Myoblasts
8. C2C12 세포에서 annexin V를 이용한 H2O2 유도 세포사멸에 미치는 EEO의 영향 평가
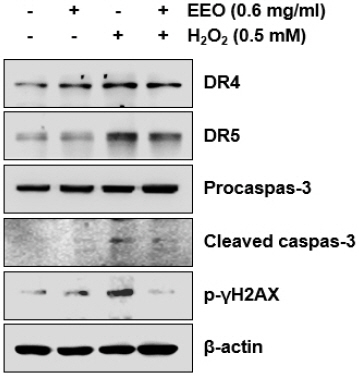
H2O2로 유도한 산화적 스트레스로 유도한 세포사멸에 대해 EEO가 억제 효과를 나타내는지 조사하기 위해 annexin V 염색을 이용한 flow cytometry 분석 통해 세포사멸 유발을 정량적으로 측정하였다. 그 결과, H2O2 처리에 의해 증가한 세포사멸은 EEO의 농도 의존적으로 감소하였음을 관찰할 수 있었다(Fig. 5). 특히, 0.4 및 0.6 mg/ml의 EEO를 전처리하였을 때는 H2O2 처리하여 측정한 결과에 비해 각각 13.7% 및 11%로 나타나 유의적으로 감소하였음을 확인하였다. 게다가 H2O2에 의해 증가한 DR4와 5, 그리고 cleaved caspase-3의 발현이 EEO(0.6 mg/ml)의 전처리에 의해 감소하였음을 확인하였고 DNA 손상의 마커인 γH2A.X의 인산화된 형태는 H2O2 처리에 의해서는 증가되었으나 EEO의 전처리에 의해서는 감소하였다(Fig. 6). 이상의 결과에서는 H2O2로 유도한 C2C12 세포의 세포사멸을 EEO가 효과적으로 억제함으로써 EEO가 산화적 스트레스로부터 세포보호 효과를 나타낸다는 것을 시사한다.
Fig. 5
Inhibition of H2O2-induced apoptosis by EEO in C2C12 myoblasts.
Cells were treated with or without the indicated concentrations of EEO for 1 h before treatment with 0.5 mM H2O2 for 24 h.
(A) After staining with annexin V-FITC and PI, representative profiles by the results of flow cytometry were presented.
(B) The percentage of apoptotic cells was determined by expressing the numbers of annexin V+ cells as a percentage of all cells. Data indicated the mean±S.D. (n=3). *** p<0.001, compared with untreated control cells; # p<0.05 and ## p<0.01 compared with H2O2-treated cells.
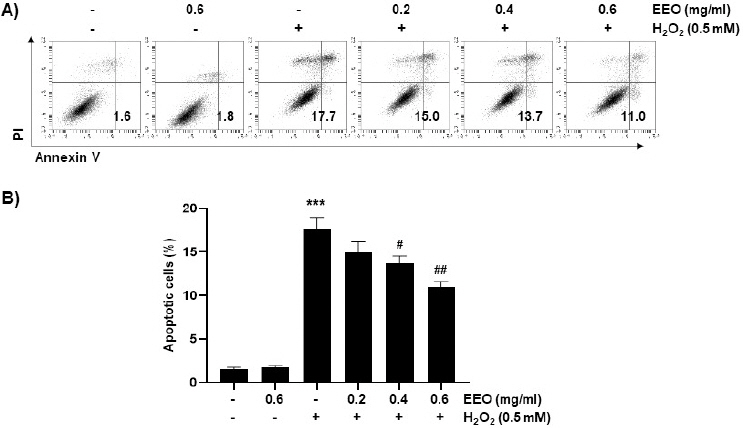
Fig. 6
Effects of EEO on the expression levels of H2O2-induced apoptosis-related proteins in C2C12 myoblasts.
Cells were treated with or without the 0.6 mg/ml EEO for 1 h before treatment with 0.5 mM H2O2 for 24 h. Total protein was isolated from cells, and the equal amounts of proteins were separated using SDS-polyacrylamide gels. Then, the separated protein according to molecular weight was transferred onto the membranes. The membranes were reacted with the anti-DR 4 and 5, anti- caspase-3, anti-p-γH2A.X, and visualized using an ECL detection system. β-actin was used as an internal control.
9. C2C12 세포에서 H2O2에 의한 미토콘드리아 기능 손상에 미치는 EEO의 영향
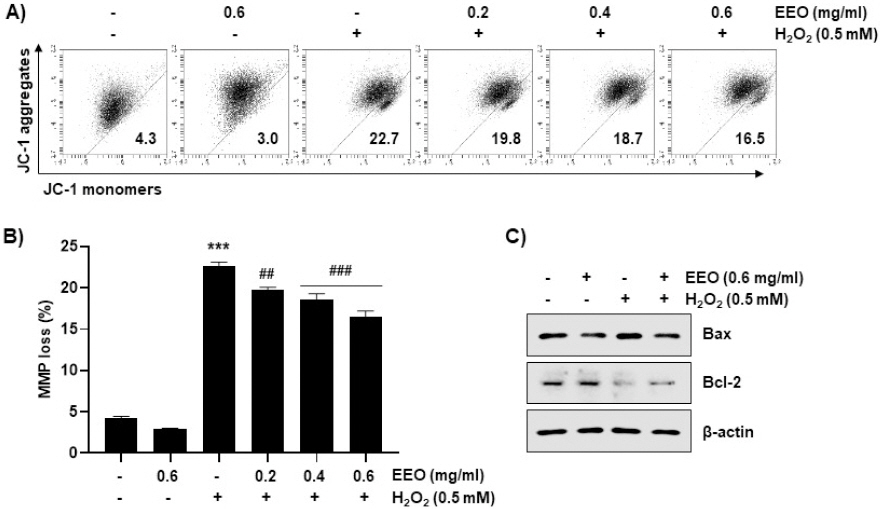
JC-1 염색을 이용한 flow cytometry 분석을 통해 산화적 스트레스에 의한 MMP(Δψm) 손실에서 EEO의 영향을 조사하였다. C2C12 세포에서 H2O2 처리에 의해 MMP(Δψm) 손실이 22.7%로 증가하였으며, 0.2, 0.4 및 0.6 mg/ml의 EEO 전처리 군에서는 각각 19.8, 18.7 및 16.5%로 나타나 EEO의 농도 의존적으로 감소하였음을 확인하였다(Fig. 7A와 7B). 그리고 Fig. 7C에 제시한 바와 같이, H2O2를 처리한 군에서 발현이 증가한 Bax 및 감소한 Bcl-2는 EEO의 전처리 군에서 대조군 수준으로 발현이 감소하였으며, Bcl-2의 경우 부분적으로 회복되었음을 관찰하였다. 따라서, 산화적 스트레스 조건에서 EEO에 의한 미토콘드리아 기능 손상 회복은 세포사멸의 유도억제와 연관성이 있음을 시사한다.
Fig. 7
Inhibition of H2O2-induced mitochondrial dysfunction by EEO in C2C12 myoblasts.
Cells were treated with or without the indicated concentrations of EEO and exposed to 0.5 mM H2O2 for 24 h. MMP was measured by flow cytometry after JC-1 staining. (A) Representative profiles of flow cytometry were shown. (B) Ratios of JC-1 aggregates to monomers were expressed. Data indicated the mean±S.D. (n=3). *** p<0.001, compared with untreated control cells; ## p<0.01 and ### p<0.001 compared with H2O2-treated cells. (C) The expressions of Bax and Bcl-2 were evaluated by immunoblotting using the indicated antibodies.
10. C2C12 세포에서 H2O2에 의해 증가된 ROS 수준에 대한 EEO의 영향
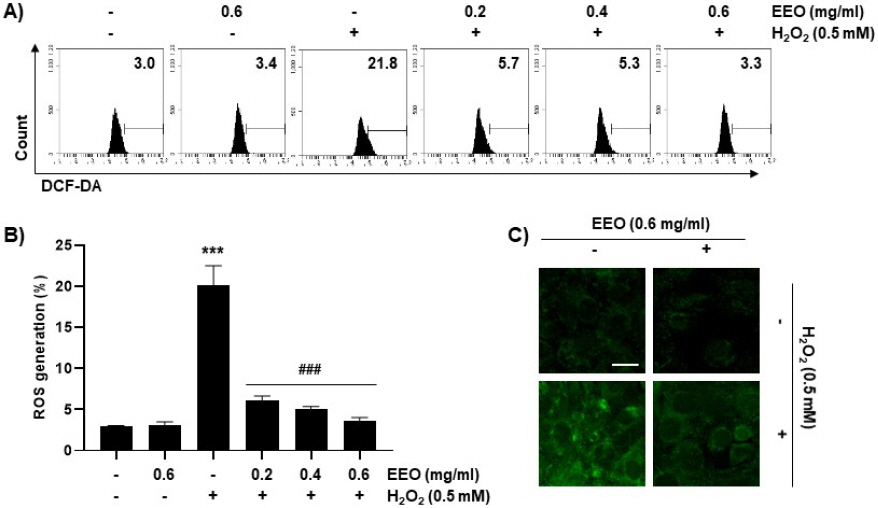
본 연구에서는 이상에서 관찰한 산화적 스트레스에 대한 EEO의 C2C12 세포보호 효과가 ROS 수준 변화와 관련이 있는지 조사하였다. Fig. 8A와 8B에 제시한 바와 같이, C2C12 세포에서 H2O2 처리에 의하여 ROS 수준이 21.8%로 나타나 대조군(3.0%)에 비해 약 7.3배 증가하였으며, EEO의 세 농도 모두 각각 5.7%, 5.3% 및 3.3%로 나타나 유의적으로 감소하였음을 확인하였다. DCF-DA의 형광 발광을 형광현미경을 통해 직접 관찰한 결과에서도 마찬가지로 H2O2에 의해 증가한 초록색의 DCF-DA 형광 발광이 EEO에 의해서는 대조군 수준으로 감소하였다(Fig. 8C). 결과적으로 H2O2 처리에 따른 산화적 스트레스에 대한 EEO의 세포사멸 억제 효과는 ROS 차단과 연관성이 있음을 의미한다.
Fig. 8
Effects of EEO on H2O2-induced ROS generation in C2C12 myoblasts.
Cells were treated with or without the indicated concentrations of EEG and exposed to 0.5 mM H2O2 for 24 h. (A) ROS levels were measured by flow cytometry after DCF-DA staining. (B) The fluorescences of DFC-DA were observed using a fluorescence microscope (Scale bar=10 μm).
Ⅳ. 고 찰
산화적 스트레스(oxidative stress)는 신체가 다양한 유해 자극에 노출되었을 때 활성산소종(reactive oxygen/nitrogen species, ROS) 또는 활성질소종(reactive nitrogen species)과 같은 고활성 분자의 과잉 생산과 체내 산화 및 항산화 시스템의 불균형으로 인해 발생하는 세포 및 조직의 생리적, 병리학적 반응을 의미하며, ROS는 일반적인 산소(O2)에 비하여 화학적반응성이 높은 산소를 가지는 분자로, 과산화물음이온(superoxideanion, O2-), 과산화수소(hydrogen peroxide, H2O2), 하이드록실 라디칼(hydroxyl radical, OH⋅) 등을 포함하고 있다21-23. 적절한 수준의 ROS는 정상적인 세포 기능을 유지하기위한 신호 전달 분자로 작용한다. 그렇지만 ROS는 불안정하고 반응성이 높아, 스트레스, 음주, 흡연, 자외선 및 유해 화학물질 노출 등의 요인은 pro-oxidant 및 anti-oxidant system 사이의 균형 장애를 유발하거나, 항산화 시스템의 기능이 저하되어 체내 산화-환원 조절 장애를 유발하게 되는데, 이 과정에서 ROS는 과도하게 생성되며, 이는 산화적 스트레스(oxidative stress)를 유발한다24-26. 지속적인 산화적 스트레스의 자극은 세포막, 핵산, 지질 및 단백질을 포함한 세포 구조물을 손상시키고, 이는 조직에 비 가역적인 변화를 유도하여 노화를 촉진시킬 뿐 아니라, 암, 치매, 관절염, 자가 면역 질환 등의 여러 가지 질환을 유발하거나 촉진시키는 것으로 알려져 있다27. 따라서 산화적 스트레스로부터 세포사멸을 보호하기 위한 항산화제의 발견 및 관련 기전 연구는 질병의 예방과 치료 차원에서 매우 중요한 관심 분야이다.
오자연종환은 枸杞子 兎絲子 覆盆子 車前子 五味子로 구성되어 있다. 오자연종환 기본방의 5가지 약재의 性味와 歸經 및 效能을 각각을 살펴보면, 菟絲子는 平하고 味甘, 辛하고 肝, 腎, 脾으로 귀경하며, 補肝益腎, 益精明目, 固精縮尿하는 작용이 있으며, 五味子는 溫하며, 味는 酸甘하며 肺, 心, 腎으로 귀경하며, 收斂固澀, 益氣生津, 補腎寧心하는 작용이 있고, 車前子는 性寒, 味甘하며 肺, 膀胱, 腎, 小腸, 肝에 귀경하며, 清熱祛痰, 利尿通淋, 滲濕止瀉, 明目 등의 효능이 있으며, 오자연종환 기본 약재 중 유일하게 寒性에 속하는 약재이다. 覆盆子는 溫하며 味는 甘, 酸하고, 肝, 腎, 膀胱에 귀경하고 益腎固精縮尿, 養肝明目하는 작용이 있다28. 補中寓瀉, 補而不膩하고 補腎益精의 작용이 있어 남성의 少弱精子症 또는 무정자증(oligoasthenospermia)에 의한 불임에 주로 효과적임이 알려져 있다8. 이에 오자연종환에 대한 선행 연구로는 주로 남성 생식 세포 GC-1 cell에서의 항산화 효과3, 안드로겐 수용체 발현을 증가4, 생식 능력의 증가5, 정자의 질적 향상11 등의 생식관련 연구가 활발하게 이루어졌다. 또한 기억력 향상12, 다발성 경화증의 개선13등 중추 신경계 계통 연구가 생식관련 연구와 더불어 주를 이루고 있으나, 이에 비해 항산화 효과 관련 연구는 드문 실정이다.
노화 예방 및 노년층의 건강한 삶은 노령화 사회에 접어든 우리나라에서 한의계가 담당해야 할 주요 영역이다. 본 연구는 이런 시대의 요구에 부응하기 위한 항노화, 항산화 효능을 가진 한약제제 개발을 위한 기초 연구로 설계되었다. 이를 위하여 오자연종환 처방전의 열수 및 에탄올 추출물을 대상으로 DPPH 자유 라디칼 및 ABTS 양이온 라디칼 소거 활성능과 FRAP법을 이용한 환원력을 비교하였으며, 각 추출물의 항산화력과 총 페놀 함량 사이의 연관성을 조사하였다.
본 연구에서는 DPPH 및 ABTS 라디칼 소거 활성능과 FRAP 활성의 측정법을 이용하여 오자연종환 추출물의 항산화 활성을 먼저 조사하였다. 본 연구의 결과에 의하면, DPPH 자유 라디칼과 항산화 활성이 있는 물질이 반응하여 짙은 보라색이 노란색으로 변하여 흡광도가 감소하는 원리를 이용하는 DPPH 자유 라디칼 소거 활성능 조사17에서 열수 및 70 에탄올 추출물 모두 농도의 증가에 따라 DPPH 자유 라디칼 소거 활성능이 유의적으로 증가하였으며, 열수 추출물보다는 에탄올 추출물의 DPPH 라디칼 소거 활성능이 우수하였다. 이 결과를 토대로, ABTS를 이용한 각 추출물의 항산화능을 평가하였다. ABTS를 이용한 항산화능 평가는 ABTS와 potassium persulfate와 반응함으로써 생성된 양이온 라디칼이 항산화물질에 의해 소거되면서 ABTS·+의 청록색이 탈색되는 정도를 흡광도로 측정하는 방법이다18. 본 연구의 결과에 의하면 ABTS를 이용한 항산화능 평가에서도 열수 추출물에 비하여 에탄올 추출물이 상대적으로 우수한 항산화능을 보여주었다. 한편, 페놀 복합물(phenolic compound)은 phenolic hydroxyl기를 가짐으로써 자유 라디칼을 소거하는 데 중요한 역할을 하여 대표적인 항산화 물질로 알려져 있다29. 따라서 총 페놀 함량 분석은 항산화 활성을 평가하는 간접적인 지표가 될 수 있다19. 그러나 본 연구의 결과에서는 DPPH 및 ABTS 라디칼 소거 활성능의 결과 각 추출물의 총 페놀 함량과는 큰 유의성을 찾기는 어려웠다. 그러나 FRAP 활성 측정을 통한 환원력20을 조사한 결과에서는 총 페놀 함량의 증가에 따라 환원력이 우수함을 알 수 있었다. 이상의 결과를 종합하면, 비록 각 추출물의 총 페놀 함량과 직접적인 상관성은 없었지만, 열수 추출물에 비하여 에탄올 추출물이 상대적으로 항산화력이 우수함을 알 수 있었다.
이상의 결과를 바탕으로 in vitro 세포 모델 수준에서 각 추출물의 항산화력에 대한 비교하기 위하여 C2C12 근아세포를 이용하였다. C2C12 근아세포는 성체 마우스 골격근 조직의 전구 세포로서 골격근의 운동 유발 변화를 모방할 수 있다는 사실이 밝혀진 이래 다양한 산화 스트레스에 대한 시험관 내 모델에서 널리 사용되고 있는 세포주이다30. 과도한 ROS의 생성에 따른 산화적 스트레스는 세포 내 다양한 소기관과 거대분자에 손상을 유도하기 때문에 지속적인 산화적 스트레스를 회복하지 못하면 결국 세포사멸을 유도하여 조직 및 장기 손상을 초래한다31. 특히, 산화적 스트레스에 민감한 미토콘드리아의 기능 손상은 세포자살 경로의 활성화를 위한 개시 신호로 작용한다32. 또한, ROS의 축적에 따른 산화적으로 손상된 DNA는 유전적 돌연변이를 유도하여 세포의 항상성 소실을 유도하여 세포사멸에 기여한다. 그러나 다양한 세포 내 신호 분자와 항산화 효소 시스템은 산화적 스트레스에 대한 방어를 위해 세포에서 산화 환원 항상성의 유지에 관여한다. 따라서 ROS 유도 산화적 스트레스의 완화 또는 제어를 위한 항산화제의 적용은 다양한 질환의 예방과 치료에 가장 기본적인 요구사항이다33. 따라서 C2C12 근아세포 모델을 이용한 각 추출물의 항산화 활성을 비교하기 위한 조전의 설정을 위하여 각 추출물이 C2C12 근아세포의 증식에 미치는 영향을 조사하였다. 그리고 산화적 스트레스를 모방하기 위한 H2O2의 처리농도를 설정하여, 각 추출물이 H2O2에 의한 산화적 스트레스 유도 세포 독성 보호 효과를 조사하였다. 본 연구의 CCK8 분석 결과에 의하면, 0.5 mM의 H2O2에 노출된 C2C12 근아세포는 약 60% 전후의 세포 생존율을 보였으며, H2O2 처리에 의한 C2C12 근아세포의 생존율 감소는 세포주기 진행의 G2/M 기에서의 정지에 의한 세포사멸과 직접적인 연관성이 있음을 알 수 있었으며, 이는 C2C12 근아세포를 이용한 선행 연구들의 결과와 잘 일치되었다34-37.
본 연구의 결과에 의하면 오자연종환 열수 추출물(WEO)은 0.8 mg/ml 처리 농도까지 C2C12 근아세포에서 유의적인 세포 독성을 나타내지 않았지만, H2O2에 의한 세포 생존율의 보호에는 유의적인 효능을 보여주지 못하였다. 반면에, 오자연종환의 에탄올 추출물(EEO)은 H2O2가 처리된 C2C12 근아세포에서 관찰되는 세포 생존율의 저하, 세포사멸의 유도 및 세포주기 정지를 모두 유의적으로 억제하였다. 또한, EEO가 존재하는 조건에서는 H2O2 유도 미토콘드리아의 기능 손상과 연계된 ROS의 생성을 유의적으로 억제되었으며, 세포사멸 조절 유단백질의 발현 변화와 DNA 손상 마크 단백질(γH2A.X)38의 증가 또한 감소하였다.
프로그램된 세포사멸(programmed cell death) 중의 하나인 세포사멸(apoptosis) 유도는 다세포 유기체에서 세포 항상성과 조직 발달을 유지하기 위한 필수 기전이다39. 세포사멸은 크게 DR-매개 외인적 경로(DR-mediated extrinsic pathway)와 미토콘드리아 매개 내인적 경로(mitochondria-mediated intrinsic pathway)로 대별된다. 이 두 경로는 다양한 세포 내 세포사멸 조절제 및 신호전달 경로에 의해 조절되며, 이는 주요 단계를 조절함으로써 전환될 수 있다40. 본 연구의 결과에 의하면 오자연종환 에탄올 추출물(EEO)은 H2O2 처리에 의하여 증가된 DR4 및 DR5의 발현 증가를 억제시켰으며, 이는 EEO가 외인적 경로의 활성화에 따른 세포사멸을 차단할 수 있음을 의미하는 결과이며, 이는 DNA 손상 차단과도 관련이 있었다. 아울러 EEO가 존재하는 조건에서는 H2O2에 의하여 증가된 활성형 caspase-3의 발현을 감소시켜, 세포사멸의 가장 큰 특징 중의 하나인 caspase cascade의 활성을 억제할 수 있음을 보여주었다. 또한, EEO는 MMP의 소실을 유의적으로 차단하여 미토콘드리아의 항상성을 유지시켰음을 알 수 있으며, 이는 ROS 생성의 차단에 의한 결과로 해석될 수 있다.
한편, 미토콘드리아 막 탈분극(mitochondrial membrane depolarization)은 미토콘드리아가 손상되었을 때 나타나는 전형적인 특징이며, MMP의 손실은 미토콘드리아 완전성이 파괴되었음을 나타내는 지표이다39,41. 이는 세포사멸 경로 중 내인성 경로가 시작되는 전형적인 과정이며, 세포사멸을 억제하는 단백질과 촉직하는 단백질로 구성된 Bcl-2 계열의 구성원에 의해 엄격하게 조절된다42,43. Bcl-2 계열 단백질은 미토콘드리아 외막의 투과성을 조절함으로써 미토콘드리아에서 세포질로의 cytochrome c와 같은 세포사멸 촉진인자들을 방출을 조절함으로써 내인성 세포사멸 유도 여부를 결정한다42,44. 본 연구의 결과에 의하면, EEO는 H2O2에 의한 Bax 단백질의 발현을 감소시킨 반면, 억제된 Bcl-2 단백질의 발현은 다소 회복시켰다. Bax는 세포사멸을 촉진하는 대표적인 단백질이며, Bcl-2는 세포사멸의 억제에 기여한다43,45. 따라서 C2C12 근아세포에서 EEO에 의한 Bax/Bcl-2의 상대적 발현 감소가 H2O2에 의한 세포사멸 차단에 결정적인 역할을 한 것으로 추정되는 이는 ROS 생성 의존적인 것으로 추정된다.
이상의 결과를 종합해 보면 오자연종환 추출물은 항산화 활성을 가지지만, 열수 추출물보다는 에탄올 추출물에서 더 우수함을 알 수 있었다. 또한, 오자연종환 에탄올 추출물에 의한 H2O2 유도 세포독성의 보호 효과는 ROS의 생성 차단에 의한 항산화 활성에 의한 것임을 보여주었다.
오자연종환의 기존 연구들이 중추 신경계 계통 연구가 생식관련 연구와 더불어 주를 이루고 있으나, 이에 비해 항산화 효과 관련 연구는 드문 실정이었다. 본 연구를 통해 오자연종환이 항산화력이 우수한 처방임을 입증하였으며, 최근 많은 선행 연구들에서, 전통적으로 다양한 질환의 예방과 치료에 사용되어온 복합 처방전 및 한약재 추출물의 약리학적 효능이 항산화 활성과 밀접한 연관성이 있는 것으로 보고되고 있다. 이에 항산화 작용뿐만 아니라 이를 바탕으로 산화적 스트레스와 연관된 다양한 질환의 예방과 치료에 오자연종환을 포함한 선행적으로 연구된 복합 처방전 및 한약재 추출물이 효과적으로 활용될 수 있기를 바란다. 또한 본 연구를 바탕으로 오자연종환의 다양한 효과를 입증할 수 있는 여러 연구들이 시행되기를 기대하며, 향후 항산화 작용에 대한 한의학적 연구에 중요한 토대가 될 수 있기를 기대하는 바이다.
Ⅴ. 결 론
본 연구에서는 가감방, 오자연종환 및 진심유생환 추출물의 항산화 활성을 비교하였으며, 다음과 같은 결과를 도출하였다. DPPH 자유 라디칼 및 ABTS 양이온 라디칼 소거 활성도 평가에서 오자연종환 열수(WEO) 및 70% 에탄올 추출물(EEO)은 우수한 라디칼 소거능을 보여주었으며, FRAP법을 이용한 환원력의 결과에서도 비교적 우수한 항산화력을 보였으며, 이는 추출물에 함유된 총 페놀 함량 의존적으로 나타났다. C2C12 근아세포에서 H2O2로 유도된 산화적 스트레스에 대한 보호 효과에 대해 WEO는 유의적인 효과가 없었지만, EEO는 처리농도 의존적으로 H2O2에 의한 세포 독성을 억제하였으며, 세포독성 보호 효과는 H2O2에 의한 세포사멸 유도 및 세포주기 정지의 억제와 연관성이 있었다. 또한 세포사멸 억제 효과는 미토콘드리아 및 DNA 손상의 억제와 연관성이 있음을 확인할 수 있었다. 이러한 C2C12 근아세포에서 H2O2로 유도된 산화적 스트레스 보호 효과는 ROS 생성에 억제와 직접적인 연관성이 있음을 확인하였다.
결론적으로 오자연종환은 산화적 스트레스에 대한 보호 잠재력으로 가지고 있으며, 여러 가지 평가를 통해 항산화력이 우수함을 확인하였다. 아울러 C2C12 근아세포에서 H2O2로 유도된 산화적 스트레스에 대한 보호 효과는 열수 추출물보다 에탄올 추출물에서 우수하였다.












