만성 위염에 대한 이중탕(理中湯)의 효과 : 체계적 문헌 고찰 및 메타 분석
ABSTRACT
Objective:
This study assessed the effectiveness of using Yijung-tang to treat chronic gastritis through a systematic review and meta-analysis of randomized controlled trials (RCTs).
Methods:
The search was conducted using keywords such as “gastritis”, “Lizhong”, “Yijung”, and “Chronic gastritis” on July 31, 2023. A meta-analysis was conducted according to outcome measurements, such as total effective rate (TER), Traditional chinese medicine symptom score (TSS), gastric hormones, and symptom relief time, using the Review Manager website.
Results:
A total of 11 RCT studies were selected. The treatment group (Yijung-tang-gagam or Yijung-tang-gagam+ Western medicine) showed significant improvement effects in terms of TER, TSS, serum gastrointestinal hormones (motilin (MTL), gastrin (GAS), and somatostatin (SS)), and symptom relief time compared to the control group (Western medicine). TER-RR : 1.20, 95% CI : 1.11 to 1.30, P≤0.00001, RR : 1.21, 95% CI : 1.14 to 1.28, P≤0.00001; MTL-MD : 35.99, 95% CI : 30.79 to 41.20, P≤0.00001); GAS-MD : 103.33, 95% CI : 97.62 to 109.04, P≤0.00001); SS : MD : -37.19, 95% CI : -41.75 to -32.64, P≤0.00001; symptom relief time (nausea)-MD : -1.96, 95% CI : -2.47 to -1.45, P≤0.00001; symptom relief time (colic)-MD : -1.75, 95% CI : -2.31 to -1.18, P≤0.00001.
Conclusion:
This study suggests that Yijung-tang is effective against chronic gastritis. However, the number of studies was insufficient, and the diagnosis and evaluation criteria were not standardized. Furthermore, because of the low quality of the included studies, more clinical studies need to be conducted to increase the possibility of clinical use.
Keywords: Chronic gastritis, Yijung-tang, Lizhong, meta-analysis
I. 서 론
위염은 조직학적으로 위 점막에 염증세포의 침윤이 있는 상태를 말하며 1 성인의 10-40%가 경험할 만큼 임상에서 빈번하게 볼 수 있는 소화기계 질환이다 2. 만성 위염(Chronic gastritis, CG)은 여러 가지 병인의 반복적인 침습에 의해 위 점막에 만성적인 염증 세포침윤이 나타난 것으로 3 1947년 Schindler가 내시경상 관찰되는 소견과 조직학적 소견을 바탕으로 만성 위염을 만성 표재성 위염과 만성 위축성 위염으로 분류하였고 그 이후로 Sydney system, Kyoto 분류 등 여러 연구자들에 의해 다양한 분류 기준이 제시되었다 4. 만성 위염의 발병 원인은 Helicobacter pylori(H. pylori) 감염, 스트레스, 술, 담배 등으로 다양하며 1 만성 위염이 장기간 지속 시 위궤양, 위장관 출혈, 위암 등과 같은 질환으로 이어질 수 있어 적극적인 치료가 필요하다 5. 치료는 대부분 점막손상을 일으키는 공격인자를 억제하거나 점막을 방어하는 방어인자를 증강시킴으로써 이루어진다 6. 만성 위염은 식욕부진, 메스꺼움, 복부팽만감, 탈력감, 피로, 쇠약증상 등 다양한 증상이 나타날 수 있으며 한의학에서는 그 증후에 따라 胃脘痛(위완통), 呑酸(탄산), 痞滿(비만), 納呆(납매), 噯氣(애기), 惡心嘔吐(오심구토), 嘈雜(조잡) 등의 범주로 치료하고 있다 7. 이중탕(理中湯)은 ≪傷寒論≫ 8에 처음 수록된 처방으로 溫中散寒시키고, 補氣健脾하는 처방으로 9,10 항산화효과 11 알콜성 위염 보호 효과 12, 항알러지 효과 13,14, 진통 및 지사 효과 15, 염증반응 억제 효과 16등이 보고되고 있다. 이에 본 연구는 脾胃陽虛한 증상을 치료하고 항염증 작용이 보고된 바 있는 이중탕이 만성 위염에 효과가 있으리라 보고 치료에 적용하는 근거를 마련하기 위해 체계적 문헌 고찰 및 메타분석을 시행하였다.
II. 대상 및 방법
1. 검색원 및 검색방법
국외 데이터베이스로는 중문 데이터베이스인 CNKI(China National Knowledge Infrastructure), 영문 데이터베이스인 PubMed, The Cochrane library를 사용하였고, 국내 데이터베이스는 RISS(Research Information Service System), Science On, OASIS (Oriental Medicine Advanced Searching Integrated System), DBPia를 사용하였다.
검색어는 ‘Gastritis’, ‘胃炎’, ‘慢性胃炎’, ‘理中湯’, ‘理中汤’, ‘yijung-tang’, ‘lizhong’ 등을 조합하여 검색을 시행하였다(Supplementary 1). 검색은 2023년 7월 31일에 시행하였으며, 문헌의 언어 및 출판시기에는 제한을 두지 않았다.
2. 연구 대상 선정 기준
1) 연구 유형
무작위 대조군 연구(Randomized Controlled Trials, RCTs)만 포함하였다. 출판연도, 출판언어에는 제한을 두지 않았다. 사람을 아닌 동물을 대상으로 한 실험논문, 학위논문, 프로토콜 논문, 문헌고찰, 인터넷 자료 등은 모두 배제하였다.
2) 연구 대상
만성 위염을 진단받은 환자를 대상으로 하였다. 만성 위염의 하위분류인 만성 위축성 위염, 만성 비위축성 위염 등을 진단받은 환자를 포함하였다. 다른 소화기계 질환과 합병된 경우에는 연구 대상에서 배제하였다. 국적, 연령, 성별에는 제한을 두지 않았다.
3) 실험군 및 대조군
실험군의 중재로 이중탕을 사용하였으며 이중탕에 다른 약재를 가감하여 사용한 연구를 모두 포함하였다. 이중탕의 구성 약재인 인삼, 건강, 백출, 감초가 모두 포함된 연구만 포함하였다. 이중탕과 다른 한약을 합방한 처방을 사용한 연구는 제외하였다. 대조군은 서양의학적 치료만 받은 군으로 하였다. 실험군과 대조군 모두 침, 뜸 등 다른 한방 치료를 병용한 연구는 제외하였다.
4) 결과 지표
만성 위염의 치료 효과를 평가할 수 있는 지표를 모두 포함하였다. 평가 도구로 총 유효율(Total Effective Rate, TER), 중의임상징후점수(TCM System Score, TSS), 혈청 위장관 호르몬(Motilin, Gastrin, Somatostatin) 등을 포함하였다.
3. 문헌선별
두 명의 연구자(KYS, LYS)가 독립적으로 논문을 검색하고, 1차적으로 제목과 초록을 보고 연구 대상 질병 및 중재와 관련 없는 논문을 배제하였고, 2차로 선정된 논문에 대해 전체 원문을 확인하여 적합하지 않은 것을 제외하였다. 두 연구자의 의견이 불일치할 경우 제3연구자(KKM, JMH)의 자문을 통해 최종적으로 선별하였다. 검색된 문헌은 Endnote X9를 사용하여 관리하였으며 프로그램의 기능을 이용하여 중복된 논문을 배제하였고 수기 검토를 통해 중복 여부를 재확인하였다.
4. 자료 추출 및 분석
최종 선정된 연구에서 두 명의 연구자(KYS, LYS)가 자료 추출 서식을 합의한 후 독립적으로 자료를 추출하였다. 저자, 출판연도, 연구대상자 수, 중재 방법, 진단기준, 평가지표, 시험군과 대조군의 정보, 처방의 제형 및 구성 약물에 대한 정보, 연구 결과, 부작용 등에 대한 정보를 추출하였다. 두 연구자의 의견이 불일치할 경우 제3연구자의 자문을 통해 최종 추출하였다.
5. 문헌의 질 평가
무작위 대조군 연구의 질을 평가하기 위한 도구 중 대표적으로 사용되는 코크란 연합의 질 평가 방법을 이용하였다. 코크란 연합은 문헌의 평가를 위하여 무작위 배정순서 생성, 배정순서 은폐, 참여자와 연구자의 눈가림, 결과 평가자의 눈가림, 불완전한 결과처리, 선택적 결과보고, 기타 비뚤림 요소의 7가지 문항을 평가 기준으로 사용하였다. 비뚤림 위험은 ‘높음(High)’, ‘낮음(Low)’, ‘알 수 없음(Unclear)’으로 구분하여 평가하였다 52.
6. 통계 분석
선정된 연구 결과의 분석 및 합성은 Review Manager(Revman) web을 사용하였다. 동일한 결과변수 내에서 치료군과 대조군의 메타분석을 시행하였다. 이분형 변수에 해당하는 경우에는 상대위험도(Risk ratio, RR)과 95% 신뢰구간으로 정리하였고, 연속형 자료에 해당하는 경우에는 평균차이(Mean difference, MD)와 95% 신뢰구간으로 정리하였다. 연구의 통계적 이질성(Heterogeneity)의 기준은 I 2 test를 사용하여 평가하였다. I 2 값 50% 기준으로 그 이상일 경우에는 통계학적으로 이질성이 높다고 판단하였다 17.
III. 연구 결과
1. 문헌 검색 및 선정 결과
검색을 통해 총 158편의 논문이 검색되었다. 이중 중복논문을 제외한 총 158편의 논문의 제목과 초록을 검토하여 무작위 대조군 연구가 아닌 연구, 이중탕을 중재로 사용하지 않은 연구, 만성 위염 환자에 대한 연구가 아닌 연구 등을 제외하고 1차적으로 16편의 논문이 선정되었다. 16개의 논문 전문을 검토하여 이중탕의 기본 구성 약재가 포함되지 않은 논문 2편, 구성 약재를 밝히지 않은 논문 1편, 한약 치료 외에 침, 뜸 등 다른 한방치료가 포함된 논문 1편, 전문을 확인할 수 없는 논문 1편을 제외하고 총 11편의 논문이 선정되었다( Fig. 1).
Fig. 1
Flow chart of selection process. 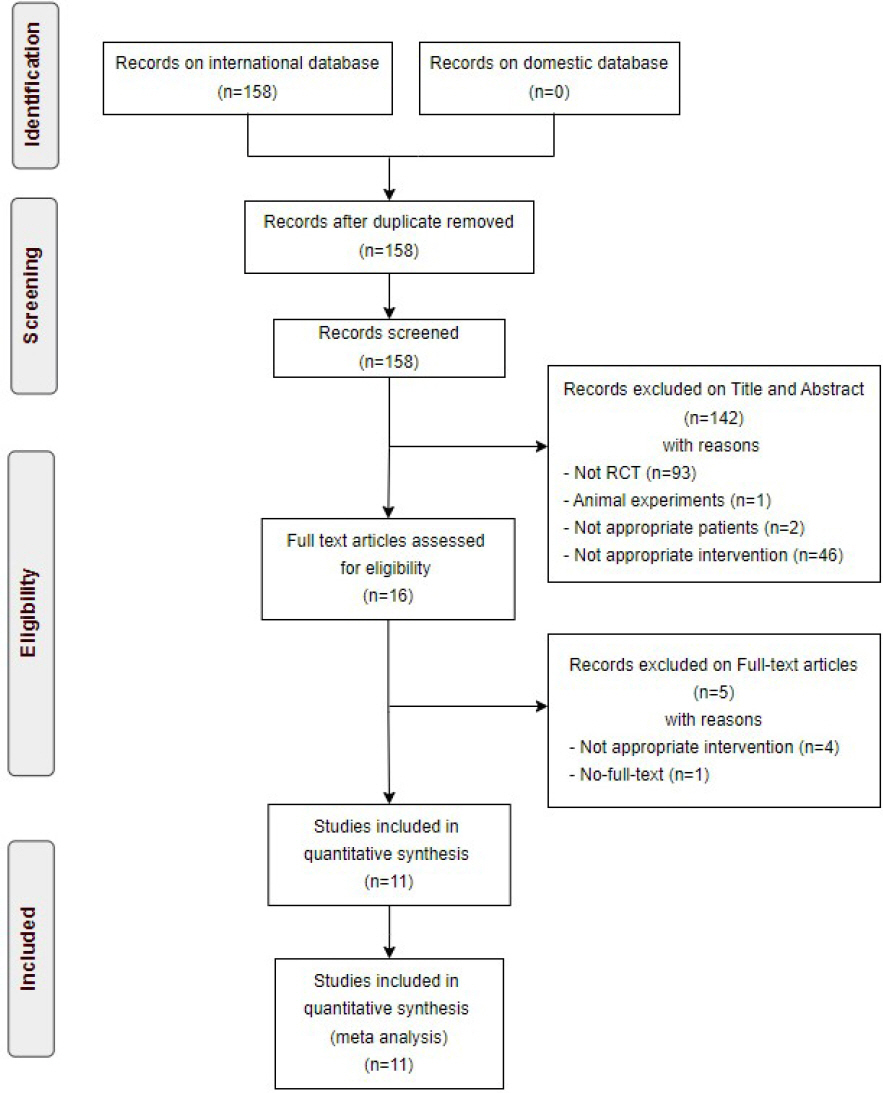
Table 1
Summary of 11 Included Studies
|
First author (year) |
Sample size 1) I
2) C |
Sex (M : F) 1) I
2) C |
Intervention (I) |
Control group intervention (C) |
Treatment period |
Outcome measurement |
Results |
Adverse reaction |
|
XU (2023) |
1) 60 2) 60 |
1) 33:27 2) 32:28 |
YJT′(Bid) |
WM 1. Aluminum Magnesium Carbonate Chewable Tablets (Tid) |
3 weeks |
1. TER 2. TSS 3-1. MTL 3-2. GAS 3-3. SS |
1. (I) 95.00>(C) 78.33* 2. (I)<(C)* 3-1. (I)>(C)* 3-2. (I)>(C)* 3-3. (I)<(C)*
|
(I) 1. Abdominal bloating (1)
2. Diarrhea (1) (C) 1. Abdominal bloating (1)
2. Diarrhea(1)
3. Constipation (1) (I) 3.33<(C)
5.00†
|
|
|
CHEN (2021) |
1) 53 2) 53 |
1) 27:26 2) 29:24 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Omeprazole enteric coated capsules (Bid)
2. Sucralfate tablets (Tid) 3. Domperidone (Tid)
4. Patients with H.pylori infection - Amoxicillin capsule (Bid) |
4 weeks |
1. TER
2. TSS 3-1. TNF-α 3-2. CRP 3-3 IL-8 |
1. (I) 94.33>(C) 69.81*
2. (I)<(C)* 3-1. (I)<(C)* 3-2. (I)<(C)* 3-3. (I)<(C)*
|
(I) 1. Nausea and vomiting (1)
2. Abdominal pain and diarrhea (1) 3. Rash (1) (C) 1. Nausea and vomiting (2)
2. Abdominal pain and diarrhea (1) 3. Rash (1) (I)
5.66<(C) 7.55†
|
|
|
DUAN (2021) |
1) 40 2) 40 |
1) 27:13 2) 25:15 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Aluminum Magnesium Carbonate Chewable Tablets (Tid) |
3 weeks |
1. TER
2. TSS 3-1. MTL 3-2. GAS 3-3. SS |
1. (I) 100>(C) 82.50*
2. (I)<(C)* 3-1. (I)>(C)* 3-2. (I)>(C)* 3-3. (I)<(C)*
|
(I) 1. Dizziness (1) (C) 1. Dizziness (1)
2. Dry mouth (1) (I)
2.50<(C)
5.00†
|
|
|
Zhang (2020) |
1) 25 2) 25 |
1) 12:!3 2) 14:11 |
YJT′(Bid) |
WM 1. rabeprazole sodium enteric-coated capsules (Qd)
2. Patients with H.pylori infection - Amoxicillin capsule (Bid), Clarithromycin extended-release tablets (Bid) |
6 weeks |
1. TER
2. TSS 3. Symptom relief time |
1. (I) 100>(C) 84.00*
2. (I)<(C)* 3. (I)<(C)*
|
NR |
|
|
WEI (2020) |
1) 41 2) 41 |
NR |
YJT′(Bid)+WM (Same as control group) |
WM 1. aluminum magnesium carbonate medicine (Tid) |
1 week |
1. TER
2. TSS |
1. (I) 97.56>(C) 80.49*
2. (I)<(C)*
|
NR |
|
|
Ding (2018) |
1) 41 2) 41 |
1) 26:15 2) 25:16 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Aluminum magnesium carbonate chewable tablets (Tid) |
3 weeks |
1. TER
2. TSS |
1. (I) 97.6>(C) 82.9*
2. (I)<(C)*
|
NR |
|
|
QU (2019) |
1) 35 2) 34 |
1) 18:17 2) 19:15 |
YJT′(Bid) |
WM 1. Omeprazole (Bid)
2. Patients with H.pylori infection - Amoxicillin capsule (Bid), Clarithromycin extended-release tablets (Qd) |
6 weeks |
1. TER
2. TSS 3. Symptom relief time |
1. (I) 97.14>(C) 79.41*
2. (I)<(C)* 3. (I)<(C)*
|
(I) 1. Dizziness (1)
2. Dry mouth (1) (C) 1. Dizziness (1) (I)
5.71>(C)
2.94†
|
|
|
Yang (2021) |
1) 46 2) 46 |
1) 26:20 2) 25:21 |
YJT′(Bid) |
WM 1. Omeprazole (Bid) |
4 weeks |
1. TER
2. TSS |
1. (I) 97.83>(C) 82.61*
2. (I)<(C)*
|
(I) 1. Nausea (1)
2. Dizziness (0) 3. Dry mouth (0) (C) 1. Nausea (0)
2. Dizziness (2) 3. Dry mouth (2) (I)
2.17<(C) 8.70†
|
|
|
Chen (2020) |
1) 25 2) 25 |
1) 13:!2 2) 12:13 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Aluminum Magnesium Carbonate Chewable Tablets (Tid) |
4 weeks |
1. TER
2. TSS |
1. (I) 96.00>(C) 68.00*
2. (I)<(C)*
|
NR |
|
|
Yao (2017) |
1) 54 2) 54 |
1) 28:26 2) 29:25 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Regulatory proton pump inhibitors
2. acid suppressants 3. antibiotics
4. Teprenone capsules (Tid) |
12 weeks |
1. TER
2. TSS 3-1. MDA 3-2. SOD 3-3. NO 4-1. MTL 4-2. GAS 4-3. SS |
1. (I) 96.30>(C) 83.33*
2. (I)<(C)* 3-1. (I)<(C)* 3-2. (I)>(C)* 3-3. (I)>(C)* 4-1. (I)<(C)* 4-2. (I)<(C)* 4-3. (I)<(C)*
|
(I) 1. Mild fever (1)
2. Dizziness (2) (C) 1. Rash (1)
2. Abdominal bloating (1) (I)
5.56>(C) 3.70†
|
|
|
Shen (2015) |
1) 60 2) 60 |
1) 34:26 2) 32:18 |
YJT′(Bid)+WM (Same as control group) |
WM 1. Aluminum Magnesium Carbonate Chewable Tablets (Tid) |
3 weeks |
1. TER |
1. (I) 98.33>(C) 83.33*
|
NR |
1) 선정된 연구의 특성
선정된 11편의 18-28 연구는 이중탕을 기본으로 한 가감방의 만성 위염에 대한 치료 효과를 양약과 비교한 연구이다. 모두 중국에서 출판된 무작위대조연구로 2015년에서 2023년 사이에 출판되었다.
2) 진단기준
진단기준으로는 ≪慢性胃炎中医诊疗专家共识意见(2017)≫ 29을 사용한 연구 18,19, ≪中国慢性胃炎共识意见≫ 30을 사용한 연구 20,23,28, ≪中医内科学≫ 31을 사용한 연구 20,25,28 등 다양하였으며 진단기준이 명확하지 않은 연구는 3편 21,22,24, 진단기준에 대해 언급하지 않은 연구는 1편 26이었다.
3) 연구대상
(1) 연구대상자의 수 및 치료기간
연구대상자는 총 959명으로 각 연구마다 50명에서 120명까지 다양하였다. 대조군은 479명, 실험군은 480명 이었으며 연구대상자의 성별에 대한 언급이 없는 연구 1편 22을 제외하고는 남성 연구대상자는 대조군 242명, 실험군 244명으로 총 486명, 여성 연구대상자는 대조군 196명, 실험군 195명으로 총 391명 이었다. (2) 실험군 및 대조군
선별된 논문의 실험군은 모두 이중탕을 중재로 사용하였으며 증상이나 변증에 따라 기본 처방에 약재를 가감하였다. 이중탕가감방 단독 치료군 4편 18,21,24,25, 이중탕가감방과 양약 병용군 7편 19,20,22,23,26-28이며 증상별 가감 약재가 모두 기재되어 있었다. Table 2, Table 3에 각 문헌에서 사용한 처방구성을 정리하였다. 대조군은 양약만을 중재로 사용하였다.
Table 2
Composition of Yijung-tang used in 11 Included Studies
|
First author (year) |
Basic medical herbs (1 dose) |
Additional medical herbs |
|
XU (2023) |
Codonopsis Pilosulae Radix (党参) 30 g
Atractylodis Rhizoma (白朮) 15 g
Zingiberis Rhizoma (乾薑) 10 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g |
Astragali Radix (黄芪) 25 g
Wolfiporiae Sclerotium (茯苓) 15 g
Paeoniae Radix Alba (白芍) 10 g
Citrus reticulata Blanco (陈皮) 10 g
Aucklandiae Radix (木香) 15 g |
|
|
CHEN (2021) |
Codonopsis Pilosulae Radix (党参) 30 g
Zingiberis Rhizoma (乾薑) 10 g
Atractylodis Rhizoma (白朮) 15 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g |
Citrus reticulata Blanco (陈皮) 10 g
Wolfiporiae Sclerotium (茯苓) 15 g
Aucklandiae Radix (木香) 15 g
Astragali Radix (黄芪) 25 g
Paeoniae Radix Alba (白芍) 10 g |
|
|
DUAN (2021) |
Codonopsis Pilosulae Radix (党参) 30 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g
Zingiberis Rhizoma (乾薑) 10 g
Atractylodis Rhizoma (白朮) 15 g |
Astragali Radix (黄芪) 25 g
Paeoniae Radix Alba (白芍) 10 g
Citrus reticulata Blanco (陈皮) 10 g
Aucklandiae Radix (木香) 15 g
Wolfiporiae Sclerotium (茯苓) 15 g |
|
|
Zhang (2020) |
Codonopsis Pilosulae Radix (党参) 10 g
Glycyrrhizae Radix et Rhizoma (甘草) 6 g
Atractylodis Rhizoma (白朮) 10 g
Zingiberis Rhizoma (乾薑) 6 g |
Astragali Radix (黄芪) 15 g
Cinnamomi Ramulus (桂枝) 10 g
Corydalis Tuber (延胡索) 15 g
Atractylodes chinensis (蒼朮) 10 g
Amomum villosum Lour. (砂仁) 3 g
Selaginellae Herba (佛手) 10 g
Citrus reticulata Blanco (陈皮) 10 g
Oryzae Fructus Germinatus (穀芽) 15 g
Hordeum vulgare L. (麦芽) 15 g
Gallus gallus domesticus Brisson (雞內金) 10 g |
|
|
WEI (2020) |
Codonopsis Pilosulae Radix (党参) 30 g
Atractylodis Rhizoma (白朮) 15 g
Zingiberis Rhizoma (乾薑) 10 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g |
Astragali Radix (黄芪) 10 g
Aucklandiae Radix (木香) 15 g
Wolfiporiae Sclerotium (茯苓) 15 g
Citrus reticulata Blanco (陈皮) 10 g
Paeoniae Radix Alba (白芍) 10 g |
|
|
Ding (2018) |
Glycyrrhizae Radix et Rhizoma (甘草) 10 g
Zingiberis Rhizoma (乾薑) 10 g
Atractylodis Rhizoma (白朮) 15 g
Codonopsis Pilosulae Radix (党参) 30 g |
Paeoniae Radix Alba (白芍) 10 g
Citrus reticulata Blanco (陈皮) 10 g
Aucklandiae Radix (木香) 15 g
Wolfiporiae Sclerotium (茯苓) 15 g
Astragali Radix (黄芪) 25 g |
|
|
QU (2019) |
Codonopsis Pilosulae Radix (党参) 9 g
Atractylodis Rhizoma (白朮) 9 g
Zingiberis Rhizoma (乾薑) 9 g
Glycyrrhizae Radix et Rhizoma (甘草) 9 g
|
|
|
|
Yang (2021) |
Codonopsis Pilosulae Radix (党参) 30 g
Atractylodis Rhizoma (白朮) 15 g
Zingiberis Rhizoma (乾薑) 10 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g |
Astragali Radix (黄芪) 25 g
Wolfiporiae Sclerotium (茯苓) 15 g
Aucklandiae Radix (木香) 15 g
Paeoniae Radix Alba (白芍) 10 g
Citrus reticulata Blanco (陈皮) 10 g |
|
|
Chen (2020) |
Glycyrrhizae Radix et Rhizoma (甘草) 10 g
Zingiberis Rhizoma (乾薑) 10 g
Atractylodis Rhizoma (白朮) 15 g
Codonopsis Pilosulae Radix (党参) 30 g |
Paeoniae Radix Alba (白芍) 10 g
Citrus reticulata Blanco (陈皮) 10 g
Aucklandiae Radix (木香) 15 g
Wolfiporiae Sclerotium (茯苓) 15 g
Astragali Radix (黄芪) 25 g |
|
|
Yao (2017) |
Glycyrrhizae Radix et Rhizoma (甘草) 12 g
Codonopsis Pilosulae Radix (党参) 12 g
Zingiberis Rhizoma (乾薑) 12 g
Atractylodis Rhizoma (白朮) 12 g |
Ponciri Fructus Immaturus (枳實) 9 g
Cinnamomi Ramulus (桂枝) 9 g
Curcumae Rhizoma (莪朮) 9 g
Ammomi Fructus Rotundus (白蔻) 9 g
Wolfiporiae Sclerotium (茯苓) 15 g |
|
|
Shen (2015) |
Codonopsis Pilosulae Radix (党参) 30 g
Zingiberis Rhizoma (乾薑) 10 g
Atractylodis Rhizoma (白朮) 15 g
Glycyrrhizae Radix et Rhizoma (甘草) 10 g |
Citrus reticulata Blanco (陈皮) 10 g
Wolfiporiae Sclerotium (茯苓) 15 g
Aucklandiae Radix (木香) 15 g
Astragali Radix (黄芪) 25 g
Paeoniae Radix Alba (白芍) 10 g |
Table 3
Mediations Adjusted according to Symptoms used in 11 Included Studies
|
First author (year) |
Medication increase(+) or decrease(-) according to symptoms |
|
XU (2023) |
胃陰虧虛者 (Deficiency of the Eum of the stomach.) |
+ |
Liriopis seu Ophiopogonis Tuber (麥門冬) 10 g, Dendrobii Caulis (石斛) 10 g |
|
|
肝胃不和者 (Disharmony between liver and stomach) |
+ |
Bupleurum falcatum(柴胡) 10 g, Aurantii Fructus Immaturus(枳壳) 10 g |
|
|
脘冷痛 (cold and pain in the epigastrium) 喜温喜按 (Being fond of warm and diminish pain by pressing with hand) |
+ |
Zingiberis Rhizoma (乾薑) 8 g, Linderae Radix (烏藥) 9 g,熟附子 6 g |
|
|
泛酸较多者 (more pantothenic acid) |
+ |
Evodia rutaecarpa Bentham (吴茱萸) 10 g, Scapharcae seu Tegillarcae Concha(瓦楞子) 10 g |
|
|
胃痛甚者 (Severe stomachache) |
+ |
Corydalis Tuber (延胡索) 15 g, Meliae Fructus (川楝子) 10 g |
|
|
大便稀溏者 (infrequent stool) |
+ |
Wolfiporiae Sclerotium (茯苓) 10 g, Dioscorea opposita Thunb. (山藥) 15 g |
|
|
CHEN (2021) |
肝胃不和者 (Disharmony between liver and stomach) |
+ |
Bupleurum falcatum (柴胡) 6 g, Aurantii Fructus Immaturus (枳壳) 6 g |
|
|
胃阴亏虚者 (Deficiency of the Eum of the stomach.) |
+ |
Liriopis seu Ophiopogonis Tuber (麥門冬) 12 g, Dendrobii Caulis (石斛) 9 g |
|
|
泛酸者 (excess acid) |
+ |
Evodia rutaecarpa Bentham (吴茱萸) 9 g, Scapharcae seu Tegillarcae Concha (瓦楞子) 6 g |
|
|
大便稀溏者 (infrequent stool) |
+ |
Corydalis Tuber (延胡索) 9 g |
|
|
DUAN (2021) |
胃陰虧虛 (Deficiency of the Eum of the stomach.) |
+ |
Liriopis seu Ophiopogonis Tuber (麥門冬), Dendrobii Caulis (石斛) |
|
|
肝胃不和 (disharmony between liver and stomach) |
+ |
Bupleurum falcatum (柴胡), Aurantii Fructus Immaturus (枳壳) |
|
|
疼痛劇烈 (severe pain) |
+ |
Corydalis Tuber (延胡索) |
|
|
胃部泛酸 (excess acid) |
+ |
Evodia rutaecarpa Bentham (吴茱萸), Scapharcae seu Tegillarcae Concha (瓦楞子) |
|
|
Zhang (2020) |
內寒偏盛 (excessive internal cold) |
+ |
Cinnamomi Cortex (肉桂) 10 g Melia toosendan Siebold et Zuccavi (川椒) 10 g |
|
|
泛吐清水 (vomiting clear fluid.) |
+ |
Pinelliae Tuber (半夏) 10 g |
|
|
吐酸水 (Vomit acidic water) |
+ |
Sepiae Endoconcha (海螵蛸) 10 g Scapharcae seu Tegillarcae Concha (瓦楞子) 10 g |
|
|
時常出現腹痛 (Abdominal pain often occurs) |
+ |
Aucklandiae Radix (木香) 10 g |
|
|
WEI (2020) |
肝胃不和 (Disharmony between liver and stomach) |
+ |
Bupleurum falcatum (柴胡) Aurantii Fructus Immaturus (枳壳) |
|
|
胃陰虧虛 (Deficiency of the Eum of the stomach.) |
+ |
Liriopis seu Ophiopogonis Tuber (麥門冬) |
|
|
疼痛感較明顯 (Pain is more obvious) |
+ |
Corydalis Tuber (延胡索) |
|
|
胃部泛酸 (excess acid) |
+ |
Scapharcae seu Tegillarcae Concha (瓦楞子) Evodia rutaecarpa Bentham (吴茱萸) |
|
|
Ding (2018) |
肝胃不和 (Disharmony between liver and stomach) |
+ |
Aurantii Fructus Immaturus (枳壳) Bupleurum falcatum (柴胡) |
|
|
胃陰虧虛 (Deficiency of the Eum of the stomach.) |
+ |
Dendrobii Caulis (石斛) Liriopis seu Ophiopogonis Tuber (麥門冬) |
|
|
疼痛劇烈 (severe pain) |
+ |
Corydalis Tuber (延胡索) |
|
|
胃部泛酸 (excess acid) |
+ |
Scapharcae seu Tegillarcae Concha (瓦楞子) Evodia rutaecarpa Bentham (吴茱萸) |
|
|
大便稀溏 (infrequent stool) |
+ |
Granati Cortex (石榴皮) Dioscoreae Rhizoma (山藥) |
|
|
QU (2019) |
泛吐清水 (vomiting clear fluid.) |
+ |
Citrus reticulata Blanco (陈皮) 10 g Pinelliae Tuber (半夏) 10 g |
|
|
吐酸水 (Vomit acidic water) |
+ |
Perillae Caulis (紫蘇梗) Sepiae Endoconcha (海螵蛸)10 g |
|
|
上腹飽脹 (Upper abdominal fullness) |
+ |
Selaginellae Herba (佛手) 10 g Citrus wilsonii Tanaka (香橼) 10 g |
|
|
腹痛甚 (severe abdominal pain) |
+ |
Aucklandiae Radix (木香) 10 g |
|
|
Yang (2021) |
反酸 (acid reflux) |
+ |
Sepiae Endoconcha (海螵蛸) 10 g Perillae Caulis (紫蘇梗) 10 g |
|
|
上腹飽脹 (Upper abdominal fullness) |
+ |
Selaginellae Herba (佛手) 10 g |
|
|
Chen (2020) |
肝胃不和 (Disharmony between liver and stomach) |
+ |
Aurantii Fructus Immaturus (枳壳) 5 g Bupleurum falcatum (柴胡) 5 g |
|
|
胃陰虧虛 (Deficiency of the Eum of the stomach.) |
+ |
Dendrobii Caulis (石斛) 5 g Liriopis seu Ophiopogonis Tuber (麥門冬) 5 g |
|
|
疼痛劇烈 (severe pain) |
+ |
Corydalis Tuber (延胡索) 10 g |
|
|
胃部泛酸 (excess acid) |
+ |
Scapharcae seu Tegillarcae Concha (瓦楞子) 5 g Evodia rutaecarpa Bentham (吴茱萸) 10 g |
|
|
大便稀溏 (infrequent stool) |
+ |
Granati Cortex (石榴皮) 5 g Dioscoreae Rhizoma (山藥) 5 g |
|
|
Yao (2017) |
嘔吐不止 (persistent vomiting) |
+ |
Syzygii Flos (丁香) Citrus reticulata Blanco (陈皮) |
|
|
燥熱煩渴 (Hot and thirsty) |
+ |
Cinnamomi Cortex (肉桂) Aconiti Lateralis Radix Preparata (附子) |
|
|
Shen (2015) |
肝胃不和 (Disharmony between liver and stomach) |
+ |
Bupleurum falcatum (柴胡) Aurantii Fructus Immaturus (枳壳) |
|
|
泛酸 (excess acid) |
+ |
Evodia rutaecarpa Bentham (吴茱萸) Scapharcae seu Tegillarcae Concha (瓦楞子) |
|
|
胃陰虧虛 (Deficiency of the Eum of the stomach.) |
+ |
Liriopis seu Ophiopogonis Tuber (麥門冬) Dendrobii Caulis (石斛) |
|
|
疼痛嚴重 (severe pain) |
+ |
Corydalis Tuber (延胡索) |
|
|
大便稀溏 (infrequent stool) |
+ |
Dioscoreae Rhizoma (山藥) Granati Cortex (石榴皮) |
사용한 양약으로는 Aluminum Magnesium Carbonate Chewable Tablets, 오메프라졸(Omeprazole), 수크랄페이트(Sucralfate), 돔페리돈(Domperidone) 등 다양하였으며 H.pylori 감염이 동반된 경우 아목시실린(Amoxicillin), 클래리스로마이신(Clarithromycin)을 사용하였다.
4) 결과지표
치료 효과에 대한 결과지표로는 총 유효율(Total effective rate, TER), 중의임상징후점수(TCM symptom score, TSS), 혈청 위장관 호르몬, 증상 완화 시간 등이 사용되었다.
(1) 총 유효율(Total Effective rate, TER)
11편의 연구 모두에서 평가 지표로 사용하였으며, 임상증상, 위내시경상의 위점막의 변화, 조직병리학적 검사 등 여러 항목을 평가하여 치료효과를 치유(治愈), 현효(显效), 유효(有效), 무효(无效)의 4단계, 혹은 현효(显效), 유효(有效), 무효(无效)의 3단계로 평가한 뒤 유효 이상의 항목에 대한 비율을 나타낸 지표이다.
항목 평가의 기준으로 ≪中药新药临床研究指导原则≫ 32을 사용하여 치료 효과를 평가하고 총 유효율을 구한 연구가 4편 18,20,23,28, 중의임상징후점수(TSS)의 변화에 따라 치료 효과를 평가하고 총 유효율을 구한 연구가 2편 19,25, ≪慢性胃炎诊疗指南≫ 33에 따라 치료 효과를 평가하고 총 유효율을 구한 연구가 1편 27, ≪中药治疗慢性胃炎脾胃虚寒证的临床观察≫ 34에 따라 치료 효과를 평가하고 총 유효율을 구한 연구가 1편 24, 평가 기준에 대한 언급 없이 치료 효과를 평가하고 총 유효율을 지표로 사용한 연구가 3편 21,22,26 이었다. (2) 중의임상징후점수(TCM Symptom score, TSS)
중의임상징후점수(TSS)는 주요 증상의 중증도를 점수로 나타낸 것으로 점수가 높을수록 증상이 심한 것을 의미한다. 총 10편 18-27의 연구에서 중의임상징후점수를 평가지표로 사용하였다. (3) 혈청 위장관 호르몬
십이지장과 공장의 점막에 있는 장크롬친화세포에서 합성되어 공복시에 주기적으로 혈중으로 분비되며 위장관 수축기능에 관여하는 기능을 하는 모틸린(Motilin, MTL) 35, 위장관 점막의 G세포에서 분비되어 위산과 펩시노겐의 분비를 촉진하며 식도괄약근의 수축을 자극하고 장의 운동성을 증대시키는 기능을 하는 가스트린(Gastrin, GAS) 36, 위산과 가스트린의 분비를 억제하는 소마토스타틴(Somatostatin, SS) 37이 평가지표로 사용되었으며 3편의 연구 19,20,27에서 결과 지표로 사용되었다. (4) 혈청염증인자
혈청염증인자로는 생체 내의 손상, 염증반응이 있을 때 상승하는 사이토카인인 종양괴사인자알파(tumornecrosis factor alpha, TNF-α) 38, 염증세포에서 분비되는 TNF-α 등에 의하여 활성화되는 비특이적인 염증 반응 물질인 C-반응성단백(C-reactive protein, CRP) 39, 염증발생 시 중성구의 보충과 활성화에 기여하는 염증성 cytokine인 인터류킨8 (interleukin 8, IL-8) 40이 있으며 1편 19의 연구에서 결과 지표로 사용하였다. (5) 증상완화시간
증상이 완화되기까지 소요되는 시간을 비교한 것으로 그 시간이 짧을수록 치료 효과가 우수한 것으로 평가하였다. 총 2편 21,24의 연구에서 결과 지표로 사용하였다. (6) 이상반응
7편 18-20,22,24,25,27의 연구에서 치료 후 이상반응에 대해 언급하였으며 4편 21,23,26,28의 연구에서 이상반응에 대해 언급하지 않았다. 보고된 이상반응으로는 복부팽만, 설사, 오심구토, 발진 등 다양하였으며 실험군과 대조군 모두에서 이상반응이 보고된 연구는 총 6편 18-20,24,25,27, 두 군에서 모두 이상반응이 나타나지 않았다고 보고한 연구는 1편 22이었다. 7편 18-20,22,24,25,27의 연구 모두에서 이상반응 발생에 두 군 간 통계적으로 유의미한 차이는 없었다(P>0.05).
3. 비뚤림 위험 평가
선정된 11편의 연구에 대하여 Cochrance Risk of Bias(RoB)를 적용하여 비뚤림 위험을 평가하였다. 결과는 다음과 같다( Fig. 2).
Fig. 2
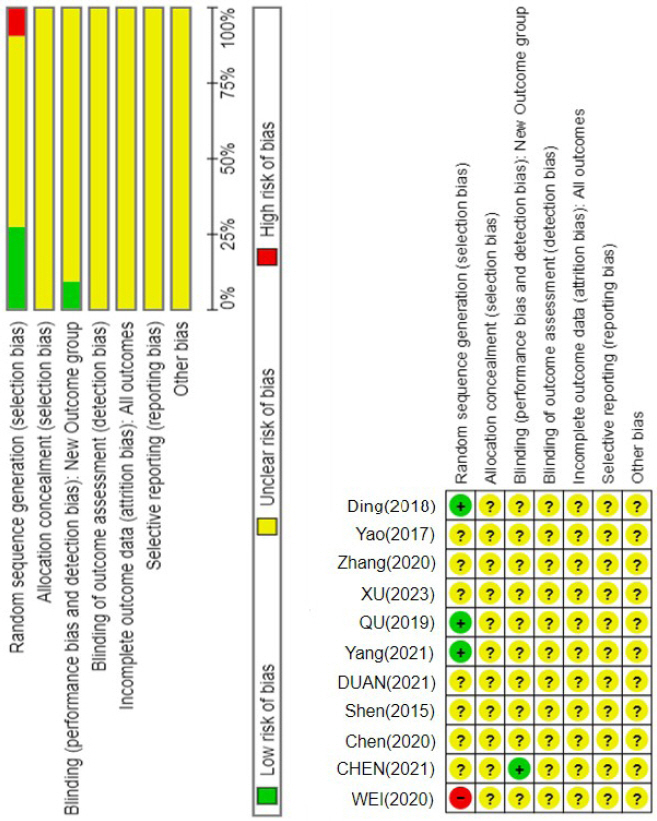
1) 무작위배정 순서 생성
11편의 연구 중 난수표를 이용하여 무작위로 순서를 배정한 연구 3편 23-25은 Low risk로 평가하였다. 단순히 무작위로만 배정하였다고 언급한 연구 5편 18,19,21,27,28, 배정에 대한 언급이 없는 연구 2편 20,26은 Unclear risk로 평가하였다. 임의로 나누었다고 언급한 연구 1편 22에 대해서는 High risk로 평가하였다.
2) 배정 순서 은폐
11편 18-28의 연구 모두 배정순서에 대한 언급이 없어 Unclear risk로 평가하였다.
3) 연구 참여자, 연구자에 대한 눈가림
이중 맹검을 시행하였다는 연구 1편 19을 Low risk로 평가하였다. 나머지 10편 18,20-28의 연구에서 연구 참여자, 연구자에 대한 눈가림에 대한 언급이 없어 Unclear risk로 평가하였다.
4) 결과 평가에 대한 눈가림
모든 연구에서 결과 평가의 눈가림에 대하여 언급하지 않았으므로 Unclear risk로 평가하였다.
5) 불충분한 결과보고
모든 연구에서 결측치에 대한 직접적인 언급은 없었으며 연구에서 배제된 대상의 중도 탈락 혹은 연구 참여 철회의 이유가 중재로 인한 것이 아님을 명확하게 명시한 연구가 없어 Unclear risk로 평가하였다.
6) 선택적 보고
모든 연구에서 프로토콜에 대한 언급이 없었으며 프로토콜의 비뚤림 정도를 판단할 근거가 불충분하여 Unclear risk로 평가하였다.
7) 그 외 비뚤림
모든 연구에서 추가 비뚤림 가능성이 있으나 비뚤림의 위험에 대한 평가 근거가 충분하지 못하여 Unclear risk로 평가하였다.
4. 메타분석 결과
선정된 문헌을 결과지표에 의거하여 분석하였다.
1) 총 유효율(TER)
Fig. 3-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
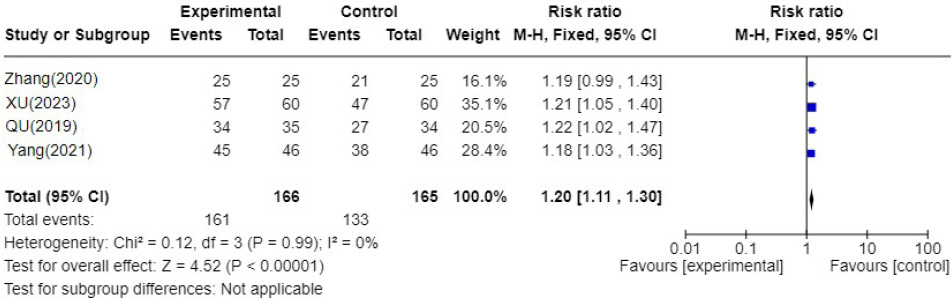
총 4편 18,21,24,25의 연구가 포함되었고 이중탕가감방으로 치료한 군은 양약 단독 치료군에 비하여 유효율이 1.20배 높아 통계적으로 유의미한 결과를 보였다. 문헌간의 통계적 이질성은 I 2=0%로 낮았다(N=4, RR : 1.20, 95% CI 1.11 to 1.30, P=<0.00001). (2) 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 3-2)
Fig. 3-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

총 7편 19,20,22,23,26-28의 연구가 포함되었고 이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비하여 유효율이 1.21배 높아 통계적으로 유의미한 결과를 보였다. 문헌간의 통계적 이질성은 I 2=0%로 낮았다(N=7, RR : 1.21, 95% CI 1.14 to 1.28, P=<0.00001).
2) 중의 임상 징후 점수(TSS)
10편의 연구 18-27에서 주요 증상별 실험군과 대조군의 점수를 비교하였으며 그 중 1편의 연구 27만 항목의 총점에 대하여 비교하였다. 10편의 연구 중 9편 18,20-27의 연구에서 증상별 점수를 0~3점으로 평가하였으며 0점은 증상 없음, 1점은 경증, 2점은 중등도, 3점은 중증을 나타낸다. 나머지 1편 19의 연구에서는 점수를 각각 0점, 2점, 4점, 6점으로 평가하였다. 평가 점수의 단위가 동일한 9편 18,20-27의 연구에 대하여 메타분석을 시행하였다. TSS의 평가 항목은 식욕저하(食少納呆), 오심구토(噁心嘔吐), 설사(便溏), 위완창통(胃脘脹痛) 등 다양하였으며 각 연구에서 공통적으로 나타나는 증상에 대하여 메타분석을 시행하였다.
(1) 식욕저하
평가 점수 단위가 동일한 9편 18,20-27의 연구 중 TSS의 평가항목으로 ‘食少纳呆’, ‘食欲不振’이 있는 연구를 8편 18,20-26을 포함하였다.
Fig. 4-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
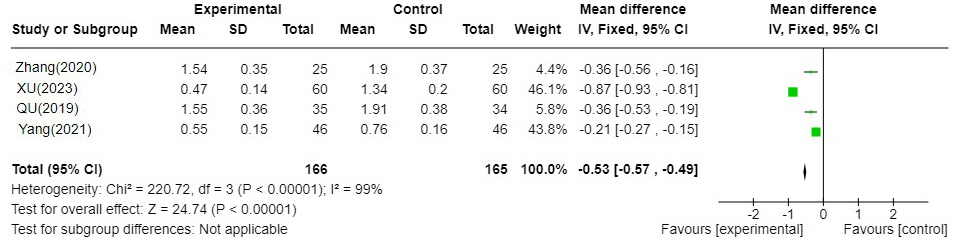
총 4편 18,21,24,25의 연구가 포함되었고 이중탕가감방 치료군이 양약 단독 치료군에 비해 식욕저하에 대한 TSS가 0.53 낮게 분석되었다. I 2=99%로 문헌간 통계적 이질성은 높았다(N=4, MD : -0.53, 95% CI -0.57 to -0.49, P=<0.00001). ② 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 4-2)
Fig. 4-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
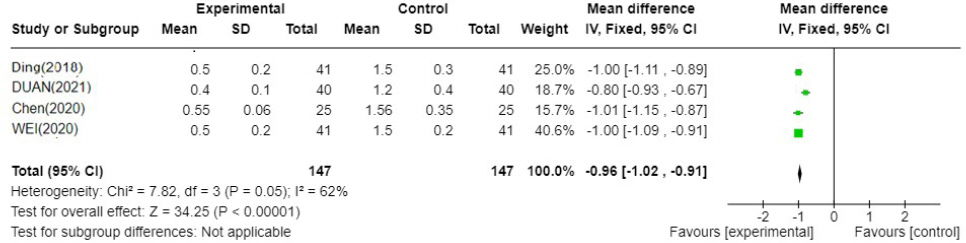
총 4편 20,22,23,26,27의 연구가 포함되었고 이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비하여 식욕저하에 대한 TSS가 0.96 낮게 분석되었다. I 2=62%로 문헌간 통계적 이질성은 높았다(N=4, MD : -0.96, 95% CI : -1.02 to -0.91, P=<0.00001). (2) 설 사
평가 점수 단위가 동일한 9편 18,20-27의 연구 중 便溏, 大便溏稀, 大便稀溏이 TSS의 평가항목으로 있는 9편 18,20-27의 연구를 분석하였다.
Fig. 5-1
Forest plot of comparison. YJT′, VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
총 4편 18,21,24,25의 연구가 포함되었고 이중탕가감방, 이중탕가감방과 양약 병용한 치료군이 양약 단독 치료군에 비하여 설사에 대한 TSS가 0.39 낮게 분석되었다. I 2=98%로 문헌간 통계적 이질성은 높았다(N=4, MD : -0.39, 95% CI -0.43 to -0.35, P=<0.00001). ② 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 5-2)
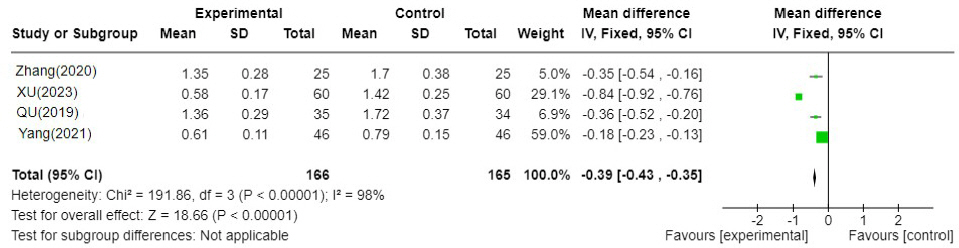
Fig. 5-2
Forest plot of comparison. YJT′+WM, VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

총 5편 20,22,23,26,27의 연구가 포함되었고 이중탕가감방, 이중탕가감방과 양약 병용한 치료군이 양약 단독 치료군에 비하여 설사에 대한 TSS가 0.29 낮게 분석되었다. I 2=99%로 문헌간 통계적 이질성은 높았다(N=5, MD : -0.29, 95% CI -0.32 to -0.26, P=<0.00001). (3) 오심구토
평가 점수 단위가 동일한 9편 18,20-27의 연구 중 噁心嘔吐, 噁心乾嘔가 TSS의 평가항목으로 있는 8편 18,20-26의 연구를 분석하였다.
Fig. 6-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
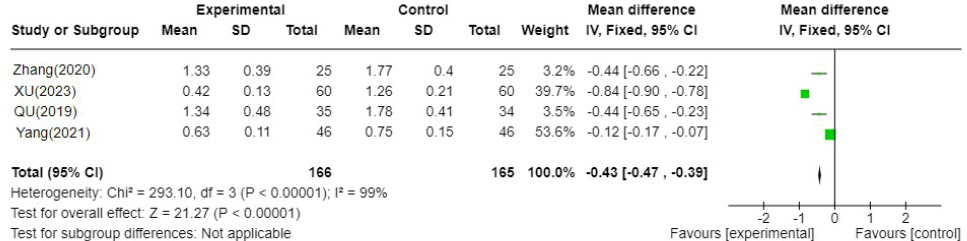
총 4편 18,21,24,25의 연구가 포함되었고 이중탕가감방 치료군이 양약 단독 치료군에 비하여 오심구토에 대한 TSS가 0.43 낮게 분석되었다. I 2=99%로 문헌간 통계적 이질성은 높았다(N=4, MD : -0.43, 95% CI -0.47 to -0.39, P=<0.00001). ② 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 6-2)
Fig. 6-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
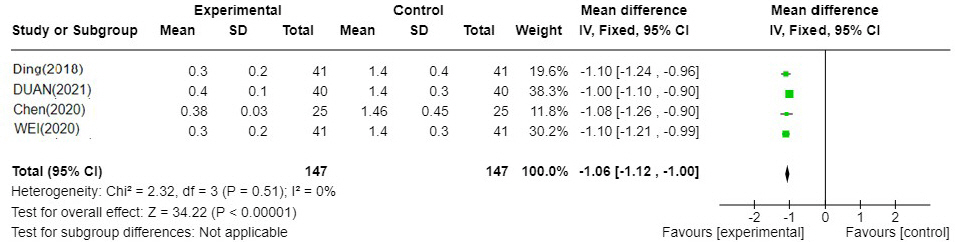
총 4편 20,22,23,26의 연구가 포함되었고 이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비하여 오심구토에 대한 TSS가 1.06 낮게 분석되었으며 I 2=0%로 문헌간 통계적 이질성이 낮아 통계적으로 유의미한 결과를 보였다(N=4, MD : -1.06, 95% CI -1.12 to -1.00, P=<0.00001). (4) 창 만
평가 점수 단위가 동일한 9편 18,20-27의 연구 중 ‘胃脘脹痛’, ‘胃脹’, ‘胃脘脹滿’이 TSS의 평가항목으로 있는 8편 18,20-24,26,27의 연구를 분석하였다.
Fig. 7-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
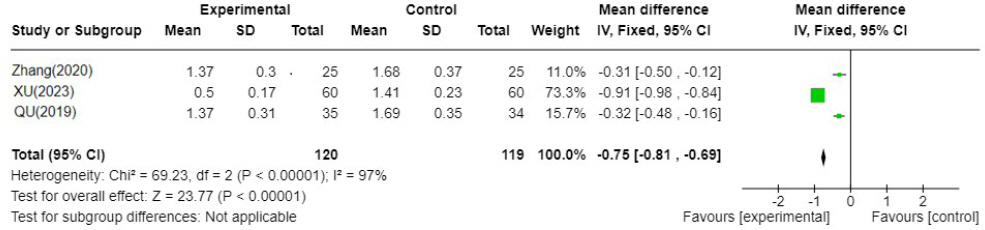
총 3편 18,21,24의 연구가 포함되었고 이중탕가감방 치료군이 양약 단독 치료군에 비해 창만에 대한 TSS가 0.75 낮게 분석되었다. I 2=97%로 문헌간 통계적 이질성은 높았다(N=3, MD : -0.75, 95% CI : -0.81 to -0.69, P=<0.00001). ② 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 7-2)
Fig. 7-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

총 5편 20,22,23,26,27의 연구가 포함되었고 이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비해 창만에 대한 TSS가 0.75 낮게 분석되었다. I 2=94%로 문헌간 통계적 이질성은 높았다(N=5, MD : -0.75, 95% CI : -0.81 to -0.69, P=<0.00001). (5) 위완통
평가 점수 단위가 동일한 9편 18,20-27의 연구 중 ‘胃痛’, ‘胃脘疼痛’, ‘胃脘隐痛’이 TSS의 평가항목으로 있는 7편 18,20,22,23,25-27의 연구를 분석하였다.
Fig. 8-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
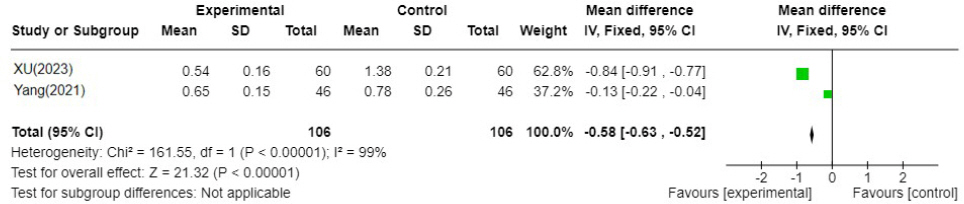
2편 18,25의 연구가 포함되었고 이중탕가감방 치료군이 양약 단독 치료군에 비해 위완통에 대한 TSS가 0.58 낮게 분석되었다. I 2=99%로 문헌간 통계적 이질성은 높았다(N=2, MD : -0.58, 95% CI : -0.63 to -0.52, P=<0.00001). ② 이중탕가감방과 양약 병용 치료군 VS 양약 단독 치료군( Fig. 8-2)
Fig. 8-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
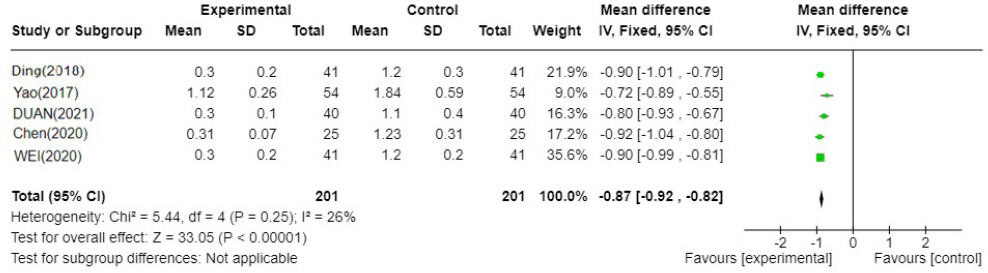
총 5편 20,22,23,26,27의 연구가 포함되었고 이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비해 위완통에 대한 TSS가 0.87 낮게 분석되었으며 I 2=26%로 문헌간 통계적 이질성이 낮아 통계적으로 유의미한 결과를 보였다(N=5, MD : -0.87, 95% CI : -0.92 to -0.82, P=<0.00001).
3) 혈청 위장관 호르몬
3편 18,20,27의 연구에서 평가 지표로 사용되었다. 2편 18,20의 연구에서는 MTL의 증가, GAS의 증가, SS의 감소를 유의미하다고 평가하였으며 1편 27의 연구에서는 MTL의 감소, GAS의 감소, SS의 감소를 유의미하다고 평가하여 평가 지표의 변화에 따른 의미가 같은 연구인 2편 18,20의 연구에 대해서만 분석을 시행하였다. 2편의 연구 모두 이중탕가감방과 양약 병용 요법과 양약 단독 치료군을 비교한 연구였다.
Fig. 9-1
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비해 치료 후 MTL이 35.99 높게 분석되었으며 문헌간 통계적 이질성이 I2=0%로 낮아 통계적으로 유의미한 결과를 보였다(N=2, MD : 35.99, 95% CI : 30.79 to 41.20, P=<0.00001).
Fig. 9-2
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
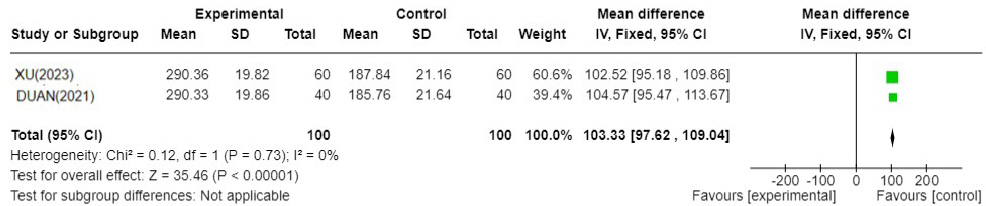
이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비해 치료 후 GAS이 103.33 높게 분석되었으며 문헌간 통계적 이질성이 I2=0%로 낮아 통계적으로 유의미한 결과를 보였다(N=2, MD : 103.33, 95% CI : 97.62 to 109.04, P=<0.00001).
(3) SS
이중탕가감방과 양약 병용 치료군이 양약 단독 치료군에 비해 치료 후 37.19 낮게 분석되었으며 문헌간 통계적 이질성이 I2=0%로 낮아 통계적으로 유의미한 결과를 보였다(N=2, MD : -37.19, 95% CI : -41.75 to -32.64, P=<0.00001)
Fig. 9-3
Forest plot of comparison. YJT′+WM VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

4) 혈청염증인자는 1편 19의 연구에서만 평가지표로 사용되어 메타분석을 시행하지 않았다. 5) 증상 완화 시간
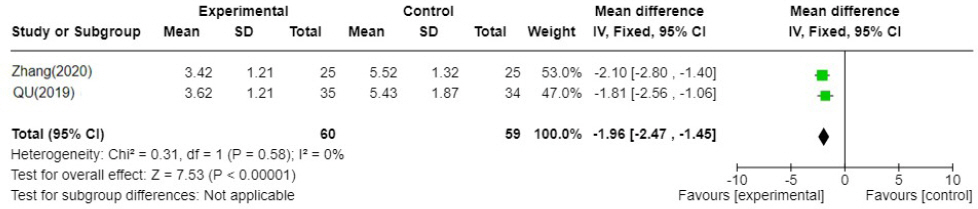
2편 21,24의 연구에서 평가 기준으로 사용되었으며 모두 이중탕가감방과 양약 단독 치료군을 비교한 연구이다. 세 가지 증상에 대한 완화시간(단위 : 일)을 평가하였으며 증상별 메타분석을 시행하였다. (1) 오 심
이중탕가감방 치료군이 양약 단독 치료군에 비해 오심 증상 완화시간이 1.96일 빠른 것으로 분석되었으며 문헌간 통계적 이질성이 I2=0%로 낮아 통계적으로 유의미한 결과를 보였다(N=2, MD : -1.96, 95% CI : -2.47 to -1.45, P=<0.00001).
Fig. 10-1
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
(2) 설 사
이중탕가감방 치료군이 양약 단독 치료군에 비해 설사 증상 완화시간이 3.24일 빠른 것으로 분석되었다. 문헌간 통계적 이질성은 I2=98%로 높았다(N=2, MD : -3.24, 95% CI : -3.59 to -2.89, P=<0.00001).
Fig. 10-2
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine

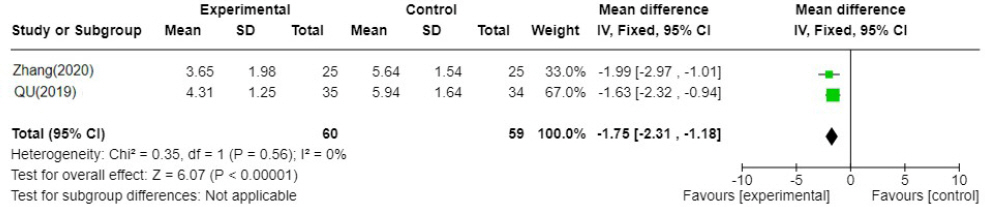
(3) 복 통
이중탕가감방 치료군이 양약 단독 치료군에 비해 복통 증상 완화시간이 1.75일 빠른 것으로 분석되었으며 문헌간 통계적 이질성 또한 I2=0%로 통계적으로 유의미한 결과를 보였다(N=2, MD : -1.75, 95% CI : -2.31 to -1.18, P=<0.00001).
Fig. 10-3
Forest plot of comparison. YJT′VS WM.
YJT′: Yijung-tang-gagam, WM : Western medicine
IV. 고 찰
우리나라에서 만성 위염은 그 유병률이 85.9%를 차지할 정도로 흔한 질환이다 41. 그러나 내시경적 진단 및 분류에 대한 의견이 통일되지 않아 명확한 진단 기준 및 분류 기준이 존재하지 않는다 42. 임상에서는 주로 내시경상 관찰되는 육안 소견에 따라 6가지로 분류하고 있으며 위점막의 발적, 삼출물, 부종이 있는 경우는 표재성 위염으로, 위점막의 소실로 함몰 부위가 관찰된 경우는 미란성 위염으로, 점막의 퇴색 및 혈관 투시상이 현저한 경우는 위축성 위염으로, 회백색조의 편평 융기가 관찰된 경우는 화생성 위염으로, 점상 또는 반상출혈이 보이는 경우는 출혈성 위염으로, 점막주름의 두께가 1 cm 이상으로 비후된 경우는 비후성 위염으로 분류하고 있다 43. 만성 위염의 일반적인 치료에 있어서는 위점막을 보호하는 제산제와 염증 억제제 등의 약물을 사용하고 대표적인 치료제로 H2 차단제, 프로톤펌프억제제 등이 있다 6. 하지만 이러한 약물치료 후에도 약 20%의 재발률을 보이고 44 발병원인으로 가장 중요하게 생각되는 H. pylori의 감염에 의한 위염은 H. pylori 박멸을 위한 복합제제를 흔히 사용하지만 이를 박멸해야 하는지에 대한 논란이 있어 현재 정립된 치료법은 없는 상태로 6 한방 치료의 필요성이 대두되고 있다. 한의학에서는 만성 위염을 증상에 따라 변증할 수 있는데 Park 등 45의 연구에 따르면 만성 표재성 위염은 肝胃不和, 脾胃濕熱, 脾胃虛弱으로, 만성 위축성 위염은 肝胃不和, 胃陰不足, 脾胃虛弱로 변증할 수 있다. 두 유형 모두 肝鬱氣滯가 병기의 근간이 되어 脾胃氣機를 조리하면서 동시에 疏肝理氣하는 치법을 사용하였으며 대표적인 처방으로는 향사육군자탕, 시호소간산, 좌금환 등이 있다. 그 외에 여러 다른 변증 유형에서도 疏肝理氣 약물을 가미한 경우가 많았다. 이중탕은 ≪傷寒論≫ 8에 처음 기재된 처방으로 人蔘(인삼), 乾薑(건강), 白朮(백출), 甘草(감초) 네 가지 약재로 구성되어 있다. 인삼은 2015년에서 2020년 사이 항염증 효능에 대하여 단일 약재로서 가장 많이 연구되었으며 46 백출은 백출의 70% 에탄올 추출물이 염증반응을 촉진시키는 NO(nitric oxide)의 생성을 현저히 억제하며, 염증성 사이토카인의 발현을 현저히 감소시킨다는 연구가 있다 47. 건강은 약리작용으로 항염증, 면역증강 및 혈소판응집억제 작용이 있고 48 감초는 성분 중 glycyrrhizin이 항염증효과가 있다고 알려져 있다. 또한 감초의 18-β-glycyrrhetinic acid는 항궤양과 더불어 항염작용, glycyrrhetinic acid는 항염증효과, 진통⋅해열 효과가 있는 것으로 밝혀졌다 49. 증상에 따라 가미된 약재를 살펴보면 위음휴허(胃陰虧虛)한 자에게는 보음약(補陰藥)인 맥문동, 석곡을 가미하였으며 18-20,23,26,28, 간위불화(肝胃不和)한 자에게는 시호, 지각을 가미하였고 18-20,22,23,27,28, 위산이 과다한 자에게는 구역탄산(嘔逆呑酸)을 주치(主治)하는 오수유, 제산(制酸) 작용을 하는 와룡자를 가미한 18-20,22,23,26 것을 확인할 수 있다. 위(胃)의 통증이 심한 자에게는 활혈지통(活血止痛)의 효능이 있는 현호색을 가미 18-20,22,23,26,28한 것을 확인할 수 있다. Ahn 50의 연구에 따르면 이중탕이 염증 억제에 유의미한 효과가 있으며 그 기전을 확인하기 위해 시행한 실험에서 이중탕의 active compound인 liquiritin, 6-gingerol은 NO(nitric oxide) 생성 억제가 뛰어난 것으로 보고된 바 있다. 또한 LPS(lipopolysaccharides)에 의해 활성화되는 JNK, ERK, p38 MAPK의 활성 억제를 통해 항염증 효과를 나타내고 iNOS와 COX-2의 발현이 억제된다는 결과가 보고된 바 있어 이러한 항염증의 효과를 토대로 만성 위염에 임상적으로 유의미한 효과가 있을 것으로 보고 본 연구를 시행하였다. 본 연구에서는 만성 위염에 대한 이중탕의 효과를 확인하기 위하여 국내⋅외 검색엔진을 활용하여 선별된 11편의 RCT 연구에 대해 체계적 문헌 고찰 및 메타분석을 진행하였다. 분석을 시행한 11편의 연구는 모두 중국에서 출판되었으며. 연구는 실험군의 중재에 따라 이중탕가감방 치료군과 양약 단독 치료군을 비교한 연구, 이중탕가감방과 양약을 병용한 치료군과 양약 단독 치료군을 비교한 연구로 나눌 수 있다. 메타 분석은 선별된 11편의 RCT 연구의 결과 지표와 중재별로 비교하여 진행하였다.
총 유효율을 메타 분석한 결과, 이중탕가감방을 사용한 치료군과 양약 단독 치료군을 비교하였을 때 총 유효율이 1.20배, 이중탕가감방과 양약 병용 치료군과 양약 단독 치료군에서는 1.21배로 모두 유의미한 결과를 보였으며 문헌간 이질성은 모두 I2=0%로 낮았다. 그러나 치료 효과를 평가하는 기준이 동일하지 않아 추후 동일한 평가기준으로 그 결과지표를 발표한 연구들에 대한 분석이 필요할 것으로 보인다.
중의 임상 징후 점수(TSS)를 지표로 사용한 연구들은 만성 위염의 대표적인 증상인 식욕저하, 오심구토, 설사, 창만, 위완통의 각각의 점수에 대해 메타 분석을 시행하였다.
식욕저하 증상에서는 이중탕가감방을 사용한 치료군은 양약 단독 치료군에 비해 치료 후의 점수가 0.53 낮게 분석되었으며 이중탕가감방과 양약 병용 치료군과 양약 단독 치료와의 비교에서는 이중탕가감방과 양약 병용 치료군이 점수가 0.53 낮게 분석되었다. 그러나 각각의 분석에서 I2=99%, I2=62%로 문헌간의 통계적 이질성이 높았다.
설사 증상에서는 이중탕가감방 치료군은 양약 단독 치료군에 비해 치료 후 TSS 점수가 0.39 낮게, 이중탕가감방과 양약 병용 치료군은 양약 단독 치료군에 비해 0.29 낮게 분석되었다. 그러나 각각 I2=98%, I2=99%로 문헌간의 통계적 이질성이 높았다.
오심구토 증상에서는 이중탕가감방을 사용한 치료군은 양약 단독 치료군에 비해 치료 후 TSS 점수가 0.43 낮게 분석되었으며 이중탕가감방과 양약 병용 치료군은 양약 단독 치료군에 비해 1.06 낮게 분석되었다. 그러나 이중탕가감방을 사용한 치료군과 양약 단독 치료군에 대한 분석에서는 문헌간의 통계적 이질성이 I2=99%로 높았다.
창만 증상에서는 이중탕가감방 치료군이 양약 단독 치료군에 비해 치료 후의 TSS 점수가 0.75 낮게, 이중탕가감방과 양약 병용 치료군은 양약 단독 치료군에 비해 0.75 낮게 분석되었다. 그러나 각각 I2=97%, I2=94%로 문헌간 통계적 이질성은 높은 것으로 나타났다.
위완통 증상에서는 이중탕가감방 치료군이 양약 단독 치료군에 비해 치료 후 TSS 점수가 0.58 낮게, 이중탕가감방과 양약 병용 치료군은 양약 단독 치료군에 비해 0.87 낮게 분석되었다. 그러나 이중탕가감방 치료군과 양약 단독 치료군을 비교한 연구에서는 I2=99로 문헌간 통계적 이질성이 높았다.
TSS는 각각의 증상마다 치료 후의 점수가 양약 단독군에 비하여 이중탕가감방 치료군, 이중탕가감방과 양약 병용 치료군에서 유의미하게 낮게 평가 되어 이중탕이 만성 위염의 치료에 있어서 양약 단독 군에 비하여 치료 효과가 우수하다는 것을 알 수 있으나 치료 후의 점수만으로 분석하였기 때문에 치료 전과 치료 후의 점수 차이에 대한 비교가 이루어지지 않은 것이 한계점이다. 또한 증상에 대한 점수가 개인의 주관적인 평가에 따라 측정되므로 결과지표의 평가 방법으로 인해 문헌간의 이질성이 높으며 각각의 증상에 대해 비슷한 범주의 증상을 함께 분석을 시행하였기 때문에 그 증상이 의미하는 바가 완전히 동일하다고 볼 수는 없으므로 문헌간의 이질성이 높다고 볼 수 있다.
혈청 위장관 호르몬을 메타 분석한 결과 이중탕가감방과 양약을 병용한 치료군이 양약 단독 치료군에 비해 치료 후 MTL이 35.99 pg/mL 높게 분석되었으며 GAS 또한 103.33 pg/mL 높게 분석되었다. SS은 37.19 pg/mL 낮게 분석되었으며 모두 I2=0%로 문헌간 통계적인 이질성이 낮아 유의미한 결과로 볼 수 있다. 또한 혈청학적 검사이므로 결과 지표의 평가 방법으로 인한 이질성은 낮다고 볼 수 있다. 그러나 분석에 사용된 연구가 2편으로 매우 적어 추후 혈청 위장관 호르몬을 평가지표로 사용한 연구 진행이 필요할 것으로 사료된다.
증상 완화 시간은 오심, 복통, 설사 증상에 대해 증상별로 메타 분석을 시행하였다. 오심 증상 완환 시간은 이중탕가감방 치료군이 양약 단독 치료군에 비해 1.96일 빠른 것으로 분석되었으며 복통 증상 완화 시간은 이중탕가감방 치료군이 양약 단독 치료군에 비해 1.75일 빠른 것으로 분석되었다. 두 증상에서 모두 I2=0%으로 문헌간 통계적 이질성이 낮았다. 설사의 증상 완화 시간은 이중탕가감방 치료군이 양약 단독 치료군에 비해 3.24일 빠른 것으로 분석되었으나 I2=98%로 문헌 간 이질성이 높았다.
결과적으로 만성 위염에서의 이중탕 치료는 양약 단독 치료군에 비해 TER, TSS, 혈청 위장관 호르몬, 증상 완화 시간에 있어서 유의미한 치료 효과가 있음을 알 수 있다.
본 연구의 한계점은 다음과 같다. 첫째, 선정된 연구 대상 논문이 총 11편으로 그 수가 적으며 연구대상자의 수 또한 총 959명으로 적다. 추후 충분한 대상자를 확보하여 연구를 시행한다면 보다 그 효과를 명확하게 확인할 수 있을 것으로 사료된다. 둘째, 만성 위염의 진단기준 및 치료 효과에 대한 결과지표의 평가 방법이 일정하지 않고 결과지표의 객관성이 부족하여 문헌간의 이질성이 높다. 국제적으로 만성 위염의 원인, 진단 및 분류에 대한 명확한 기준의 부재로 이러한 한계가 더욱 빈번한 것으로 보이며 이에 대한 보완이 필요할 것으로 사료된다. 셋째, 이중탕 원방만을 중재로 사용한 연구가 없어 이중탕 단독의 치료 효과가 명확하지 않다. 증상에 따른 약재의 가감이 이루어졌으나 그 표본수가 명확하지 않고 가감에 따른 효과를 별도로 확인한 연구가 없어 이중탕 원방을 중재로 활용한 연구 및 가감 약재에 대한 추가적인 연구가 필요하다. 넷째, 상한론에 기재된 ‘인삼’이 현대의 인삼과 동일한 것인지에 대한 논란이 있어 처방을 임상에서 활용할 때 약재의 차이에 따라 그 효과가 다르게 나타날 수 있을 것이라 사료된다. Yang 등의 연구 51에 따르면 상한론에서의 ‘인삼’은 ‘만삼’에 가까우며 이러한 이유로 11편의 연구 모두에서 ‘인삼’이 아닌 ‘만삼’을 사용한 것으로 추측되나 만삼을 사용한 이유에 대해 명확한 언급은 없어 추가적인 연구를 통하여 이를 명확할 필요가 있다. 다섯째, 비뚤림 위험으로 연구의 질이 낮다. 포함된 연구의 대부분이 비뚤림 위험을 평가하는 항목에 대해 명확하게 언급하지 않아 불확실하다 평가되었으며 모두 중국에서 중국어로 출판되었다는 점에서 위치 및 언어 비뚤림 등의 비뚤림 또한 배제할 수 없다. 이러한 한계점에도 불구하고 본 연구를 통해 만성 위염에서 이중탕이 유의미한 치료 효과가 있음을 확인하였다. 이상반응에 있어서도 총 6편의 연구에서 치료 후 나타난 이상 반응이 통계적으로 유의미하지 않아(P>0.05) 만성 위염에 있어서 이중탕을 치료로 적용하는 것의 안전성을 확인할 수 있었다. 본 연구는 향후 임상에서 이중탕을 만성 위염의 치료로 적용하는 것의 근거를 마련했다는 점에서 그 의의가 있다. 제시된 한계점을 보완하여 보다 체계적인 연구를 통해 그 활용 가치를 높일 수 있을 것이라 생각된다.
V. 결 론
본 연구는 11편의 RCT를 분석하여 만성 위염에 대한 이중탕의 치료 효과를 확인하였다. 분석 결과 이중탕을 중재로 한 치료군이 양약을 중재로 한 치료군에 비해 TER, TSS, 증상 완화 시간, 혈청 위장관 호르몬(MTL, GAS, SS)에서 유의미한 개선 효과를 보여 만성 위염에 대한 이중탕의 치료 효과를 확인할 수 있었다. 그러나 TSS, 증상 완화 시간에 있어서는 문헌 간 이질성이 높아 통계적으로 유의미하지는 못하였고 연구의 수가 불충분한 점, 진단 및 평가기준이 표준화되지 않았다는 점, 단독 효과를 명확하게 알기 어렵다는 점, 비뚤림 위험으로 연구의 질이 낮다는 한계점이 있어 보다 체계적인 연구 설계 및 시행을 통해 보완할 필요가 있다.
참고문헌
1. Lee HW, Kang SH, Park GE, Lee KH, Hong YS, Lee K, et al. Survey on the Endoscopic Diagnosis of Chronic Gastritis. Korean Journal of Helicobacter Upper Gastrointestinal Research 2014:14(3):194–8.  2. Yang SY, Lee OY, Bak YT, Bak YT, Jun DW, Lee SP, et al. Prevalence of gastroesophageal reflux disease symptoms and uninvestigated dyspepsia in Korea:a population-based study. Dig Dis Sci 2008:53(1):188–93.    3. Fang JY, Liu WZ, Li ZS, Du YQ, Ji XL, Ge ZZ, et al. Consensus on standard management of choronic gastritis in China. Chinese Journal of Gastroenterology 2013:18(01):24–36.
4. Yim SK, Seol SY. History of Various Classifications of Gastritis. Korean J Helicobacter Up Gastrointest Res 2023:23(2):84–8.   5. Kim YI, Kim YW, Choi IJ, Kim CG, Lee JY, Cho SJ, et al. Association between chronic gastritis and gastric cancer:A multicenter retrospective cohort study. J Gastroenterol Hepatol 2019:34(3):544–51.  6. Song YK, Jin SK, Han ES, Ahn MR, Jung JY, Lee HE, et al. Guideline for the Clinical Trials Evaluation for Gastritis. Yakhak Hoeji 2011:55(4):345–51.
7. Fang JY, Liu WZ, Li ZS, Ji XL, Ge ZZ, Li YQ, et al. Consensus on standard management of choronic gastritis in china. Chin J Gastroenterology 2013:18(1):24–36.
8. Ko MG, Jang MK. Hyundae-Sanghanron. Seoul:Haneuimunhwasa 2000:647–9.
9. Hur J. Donguibogam. Seoul:Namsandang 2007:382.
10. College of Oriental Medicine, Professors of Prescriptionology. Prescriptionology Seoul: Yeongrimsa: 2003. p. 232–3.
11. Seo CS, Kim OS, Kim YJ, Shin HK. Quantification Analysis and Antioxidant Activity of Leejung-tang. Official Journal of The Korean Medicine Society For The Herbal Formula Study 2013:21(1):177–85.  12. Shin IS, Lee MY, Lim HS, Seo CS, Ha HK, Shin HK. Gastroprotective effects of Leejung-tang, an oriental traditional herbal formula, on ethanol-induced acute gastric injury in rats. African journal of traditional, complementary, and alternative medicines 2013:10(2):324–30.  13. Seo HY, Han JK, Kim YH. The effect of Li Zhong tang on the suppression of The differentiation by IFN-γresponse in IgE Hyperproduction and atopic dermatitis-like shin lesions induced NC/Nga mouse. J Korean Oriental Pediatrics 2009:23(1):1–22.
14. Seo HY, Han JK, Kim YH. Therapeutic Effects of Yijung-tang on atopic dermatitis-like skin lesions of NC/Nga mouse induced by mite antigen. J Korean Oriental Pediatrics 2011:25(1):1–27.  15. Koh KS, Kang SK, Choe YT. Studies on the effects of aqua-acupuncture with Yi-Jung-tang extracts on the analgesia, anti-laxative and uropepsin value. J Korean Oriental Med 1984:5(1):62–71.
16. Lee JA, Ha HK, Jung DY, Lee HY, Lee JK, Huang DS, et al. Comparative study of 25 herbal formulas on anti-inflammatory effect. J Oriental Obstetrics &Gynecol 2010:23(3):101–11.
17. Lee JY. Meta-anallysis. J Korean Endocrinolog 2008:23(6):361–78.
18. Ming XU. Clinical Effect Research of Modified Center-Rectifying Decoction on with Spleen and Stomach Asthenia of Chronic Gastritis. Smart Healthcare 2023:9(1):182–5.
19. Chen Q, Ye W, Wang Q. Clinical Effect and Incidence of Adverse Reactions of Lizhong Decoction in the Treatment of Chronic Gastritis with Spleen Stomach Weakness(Cold). Chinese and Foreign Medical Research 2021:19(6):102–4.
20. Duan D. Clinical effects of the Lizhong decoction on spleen and stomach weakness syndrome of chronic gastritis. Clinical Journal of Chinese Medicine 2021:13(5):48–51.
21. 张 川, 孙 宏文. 理中汤加减方治疗慢性胃炎(脾胃 虚寒证) 的临床疗效[J]. 内蒙古中医药 2020:39(12):14–5.
22. Wei JT. Observation on effect of lizhong decoction in treating chronic gastritis with spleen-stomach deficiency syndrome. Journal of Shandong Medical College 2020:42(2):93–4.
23. Ding M. Effect experience of modified Lizhong decoction in treating syndrome of spleen and stomach weakness (cold) in chronic gastritis. Chinese community doctors 2018:34(25):91–2.
24. Qu F. Clinical Observation on Modified Lizhong Decoction in the Treatment of Spleen and Stomach Deficiency-cold Syndrome of Chronic Gastritis. Guangmei traditional Chinese medicine 2019:34(7):1036–8.
25. 杨录兴. 理中汤加减治疗慢性胃炎脾胃虚弱(寒) 证的临床效果. 内蒙古中医药 2021:40(10):38–9.
26. 陈妍嫣. 理中汤加减治疗慢性胃炎脾胃虚弱(寒)证 的临床效果观察. 医学食疗与健康 2020:18(11):35–7.
27. 姚 春和, 李 伟. 理中汤加味联合替普瑞酮胶囊治疗 慢性萎缩性胃炎的疗效及对血浆生长抑素, 胃泌素 含量水平的影响. 四川中医 2017:35(12):117–20.
28. Shen S. Clinical Efficacy of Lizhong Tang Combined with Western Medicine for Treating Chronic Gastritis with Spleen and Stomach Deficiency Type. Information on Traditional Chinese Medicine 2015:32(5):101–3.
29. Zhang S, Tang X, Huang S, Bian LQ. Expert consensus opinion on the diagnosis and treatment of chronic gastritis with traditional Chinese medicine (2017). Chinese Journal of Traditional Chinese Medicine 2017:32(7):3060–4.
30. Fang JY, Liu WZ, Li ZS, Du YQ, Ji XL, Ge ZZ, Li YQ, et al. Chinese consensus opinion on chronic gastritis. Chinese Journal of Gastroenterology 2013:18(1):24–36.
31. 罗仁,曹文富. 中医内科学[M]. 北京: 科学出版社 2012:36.
32. Liang MX, Gao TH. An analysis on logical problems of zang-fu viscera syndromes in “Guidance principle of clinical study on new drug of traditional Chinese medicine”. China Journal of Traditional Chinese Medicine and Pharmacy 2008:14(5):330–42.
33. Tang XD, Li ZH, Li BS, Liu SN. Guidelines for Diagnosis and Treatment of Chronic Gastritis. Chinese Medicine Modern Distance Education of China 2011:09(10):123–5.
34. Feng SJ. Clinical Observation on Chinese Medicine in Treating Chronic Gastritis of Deficiency of Spleen and Stomach. Guangmei traditional Chinese medicine 2018:33(15):2148–50.
35. Shim SG, Rhee JC, Rhee PL, Choi KW, Jeon SK, Kang TM, et al. Mechanisms of Motilin Action on Smooth Muscle of the Human Stomach. The Korean journal of gastroenterology 2002:39(1):4–12.
36. Norman AW, Litwack G. Hormones Orlando: Academic press: 1987. p. 322–54.
37. Sgouros SN, Bergele C, Viazis N, Avgerinos A. Somatostatin and its analogues in peptic ulcer bleeding:facts and pathophysiological aspects. Dig Liver Dis 2006:38(2):143–8.   38. Perkins DJ, Kniss DA. Tumor necrosis factor- alpha promotes sustained cyclooxygenase-2 expression:attenuation by dexamethasone and NSAIDs. Prostaglandins 1997:54(4):727–43.   39. McCarty M. Historical perspective on C-reactive protein. AnnN Y Acad Sci 1982:389:1–10.  40. Thelen M, Peveri P, Kernen P, von Tscharaner V, Walz A, Baggiolini M. Mechanism of neutrophil activation by NAF, a novel monocyte-derived peptide agonist. FASEB J 1988:2(11):2702–6.    41. Park HK, Kim NY, Lee SW, Park JJ, Kim JI, Lee SY, et al. The distribution of endoscopic gastritis in 23,536 health check-up subjects in Korea. The Korean Journal of Helicobacter and Upper Gastrointestinal Research 2012:12(4):237–43.
42. Lee HW, Kang SH, Park GE, Lee KH, Hong YS, Lee K, Lee JH, et al. Survey on the Endoscopic Diagnosis of Chronic Gastritis. The Korean Journal of Helicobacter and Upper Gastrointestinal Research 2014:14(3):194–8.  43. Korean Society of Gastrointestinal Endoscopy. Atlas of gastrointestinal endoscopy Seoul: Daehan Medical Books: 2010. p. 99–102.
44. Zendehdel N, Nasseri-Moghaddam S, Malekzadeh R, Massarrat S, Sotoudeh M, Siavoshi F. Helicobacter pylori reinfection rate 3 years after successful eradication. J Gastroenterol Hepatol 2005:20(3):401–4.   45. Park MS, Kim YM. Study on Syndrome Differentiation of Gastritis by Korean Standard Classification of Dsease and Cause of Death. Korean Journal of Oriental Physiology &Pathology 2017:31(5):255–63.  46. Yu BK, Lew JH. Research Trends of Anti- inflammatory Herbal Medicines and Herbal Medicines Published in Korean Journals of Oriental Medicine - Focusing on experimental papers published since 2015 -. The Korea Jounrnal of Herbology 2021:36(1):19–39.
47. Oh HK. Antioxidant and Anti-inflammatory Activities of Atractylodes japonica According to Extract Methods. Journal of the Korean Applied Science and Technology 2021:38(6):1543–52.
48. 김 호철. 한약약리학 서울: 집문당: 2001:422–7.
49. Andrea TB, Shinya S, Gary LH, Martha RH, Carl LK, Judy S, et al. Shosaikoto and other Kampo (Japanese herbal) medicines:a review of their immunomodulatory activities. J Ethnopharmacol 2000:73(1-2):1–13.   50. Ahn HR. The Ameliorating Effect of Lizhong- Tang on Antibiotic-Associated Imbalance in the Gut Microbiota in Mouse. Applied Sciences 2022:12(14):6943.  51. Yang JP, Yeo IS. A Study on the true nature of 'Chinese Jinseng'. Korean Journal of Medical History 2003:12(2):144–66.  52. In : Higgins JP, Green S, editors. Cochrane handbook for systematic reviews of interventions. Ver. 5.1.0. The Cochrane Collaboration 2011:
Appendices
【Appendix 1】
Search Terms used in Database
|
Database |
검색어 |
|
CNKI |
((SU=gastritis+胃炎+慢性胃炎) OR (TI=gastritis+胃炎+慢性胃炎) OR
(AB=gastritis+胃炎+慢性胃炎)) AND
((SU=理中+理中汤+理中湯+lizhong+yijung) OR
(TI=理中+理中汤+理中湯+lizhong+yijung) OR
(AB=理中+理中汤+理中湯+lizhong+yijung)) |
|
PubMed |
(“Gastritis[mh]" OR “Gastritis, Atrophic[mh]") AND (“yijung-tang[mh]" OR “lizhong") |
|
The Cochrane library |
#1 Gastritis |
|
#2 Gastritis, Atrophic |
|
#3 #1 or #2 |
|
#4 yijung-tang |
|
#5 lizhong |
|
#6 #4 or #5 |
|
#7 #3 and #6 |
|
RISS |
이중탕 AND 위염 |
|
Science On |
이중탕 AND 위염 |
|
OASIS |
이중탕 AND 위염 |
|
DBPia |
이중탕 AND 위염 |
|
|































