홍삼의 Dexamethasone 유도 근감소증 모델 백서에 대한 효과 연구
Abstract
Objective
As the number of sarcopenic patients worldwide is increasing, the need for the treatment of sarcopenia is increasing. Ginseng has been reported to be a major herbal supplement. We tested whether red ginseng would be effective for sarcopenia using red ginseng preparation which can be easily obtained locally in Korea.
Methods
30 rats were randomly divided into three groups: the control group (n=10) (Group C), the group with Dexamethasone -induced sarcopenia (n=10) (Group D), and the group to which red ginseng was administered group after induced sarcopenia with Dexamethasone (n=10) (Group DH). Dexamethasone was intraperitoneally administered to group D and group DH for 7 days to make sarcopenic model. After that, the red ginseng tablets prepared by Korea Ginseng Corporation were diluted in distilled water and administered orally to the DH group for 2 weeks.
Body weight and grip strength were measured 8 times during the experiment. At the end of the experiment, blood was collected by cardiac puncture. In addition, the tibialis muscle was extracted, a myofibril cross section was measured by immunohistochemical staining and MyHC (myosin heavy chain) was quantified by Western blotting.
Results
The ratio of the area on myofibril cross-section showed significant differences after administration of the red ginseng tablet.
Conclusions
Red ginseng has a significant effect on the recovery of myofibril cross-section on sarcopenia. This experiment will be helpful for future clinical studies on drug effects in sarcopennia.
Keywords: sarcopenia, dexamethasone, red ginseng, grip strength, myosin heavy chain transition
I. 서 론
인체는 나이가 들면서 많은 변화를 겪는다. 그 중 제지방체중(lean body mass)과 근육량(muscl mass)은 감소하는 다른 지표들과 비교하였을 때 더욱 유의하게 감소한다. 이는 근력감소를 일으키고, 결과적으로 노인의 재가기간증가, 독립활동의 감소, 위약, 낙상, 골절의 원인이 된다. 이러한 신체변화를 1988년 그리스어로 flesh의 의미인 ‘sarx’와 loss의 의미인 ‘penia’를 합쳐 ‘sarcopenia(근감소증)’라고 명명하기 시작하였다 1. Sarcopenia에 대한 정의나 기준은 아직 확립되어 있지 않으나 일반적으로 ‘건강한 젊은 성인의 골격근량 평균값의 2표준편차(SD, Standard deviation)이하보다 저하된 경우’로 정의한다. 최근에는 골격근량의 감소뿐 만 아니라 근력과 일상생활지수도 근감소증의 진단기준에 포함시키고 있다 2. WHO(World Health Organization, 2002)에서는 세계적으로 노인 sarcopenia 환자가 5천만 명에 이르는 것으로 추산하였으며, 40년 뒤에는 2억명에 달 할 것으로 예상하고 있다 3. 인삼(人蔘)은 두릅나무과에 속한 다년생 초본인 Panax ginseng C.A Mey의 뿌리로, 性은 微溫하고 味는 甘微苦하며 大補元氣, 固脫生津, 安神작용을 한다 4. 실험적으로 면역활성 증가 5, 심혈관질환 예방 효과 6, 항우울 및 항불안작용 7에 대해 보고되어있다. 그 밖에도 운동능력, 배뇨생식기능, 소화기능 향상 및 당뇨, 대장암, 신체증상(Somatic Symptoms)에 대한 유의한 효과가 보고된 바 있다 8. 인삼은 포제방법에 따라 채취 후 바로 건조한 것을 白蔘, 쪄서 건조한 것을 紅蔘으로 분류한다. 인삼을 蒸熟하는 과정에서 ginsenoside의 구조변화가 일어나는데, 주로 항암작용, 순환기계, 노화억제효과와 관련된 물질이 증가하는 것으로 알려져 있다. 또한 효소가 불활성화되고 자체 항산화물질이 증가하며 전분이 호화(gelatinization)된다. 이는 홍삼의 저장성을 증가시키고 내용성분 추출과 소화흡수를 용이하게 한다 9. 이러한 특징을 토대로 홍삼제품은 건강보조식품시장의 대부분을 차지하고 있으며 다양한 추출방식과 제형화가 시도되고 있다 10. Sarcopenia 치료의 필요성이 증가되는 추세에 맞추어, 한의약의 역할과 효과에 대해서 연구가 필요하다. 홍삼의 근육에 대한 효과에 대해서는 아직 근거가 부족하지만 ginsenoside Rg1을 흰 쥐에게 4주간 투여시 grip strength를 유의하게 증가시켰다는 연구가 있었으며 11, 흰 쥐에게 인삼 추출물 및 홍삼추출물을 투여하였을 경우 신장성 운동 후 근손상 회복에 유의한 효과가 있었다는 연구가 있었다 12. 이러한 연구결과들과 홍삼의 大補元氣기능, 다양한 제형화와 건강기능식품화를 통한 높은 접근성을 토대로, 홍삼이 근감소증에 효과적인 약물이 될 수 있는 지에 대해 실험하였다. Dexamethasone은 근위축을 유발할 때 Immobilization, Denervation, Disuse로 인한 근위축 모델과 다르게 Sarcopenia와 동일한 Type II 근섬유를 감소시켜 Fast to Slow로 Myosin Heavy Chain(MyHC) transition을 유발하는 것으로 알려져 있으며 13, 이를 토대로 행해진 선행 연구 14를 참고하여 glucocorticoids (Dexamethasone)로 근위축 모델을 만들었다. 주위에서 쉽게 구할 수 있는 시판 홍삼 제제를 Dexamethasone 유도 근위축 백서에 투여하여 회복에 효과가 있는지를 근감소증의 임상적 측면(골격근량, 근력)과 근섬유수준(MyHC transition)의 측면으로 살펴보았다.
II. 실험재료 및 방법
1. 실험동물 및 분류
실험동물은 14주령 수컷 SD rat 30마리를 사용하였다. 실험동물은 실험 1주 전에 구입하여 실험실 환경에 적응시켰으며, 식이 및 수분 섭취는 무제한으로 제공하였다. 동물사육실 온도는 24±0.5 ℃, 습도는 50±5%였으며 사료는 일반사료(EEGJ30060; Cargill Agri Purina, Seongnam, Korea)를 사용하였다. 일반 사료의 성분 구성은 다음과 같다( Table 1). 이후 무처치군(Control, C, n=10), Dexametasone 처치군(D, n=10), Dexamethasone 처치 후 홍삼투여군(DH, n=10) 세 군으로 각각 10마리 씩 무작위로 분류하였다.
Table 1
The Components of Normal Diet
|
Ingredient |
Proporton (%) |
|
Moisture |
12.0 |
|
Protein |
20.0 |
|
Fat |
4.5 |
|
Fiber |
8.0 |
|
Ash |
7.0 |
|
Calcium |
0.5 |
|
Phosphorus |
1.0 |
|
etc. |
47 |
|
|
Total amount |
100 |
동물 실험은 경희대학교 동물실험 윤리 규정에 따라 경희의료원 윤리위원회의 승인을 얻어 실험하였다(KHMC-IACUC 2018-19).
2. 약물 및 투여
실험동물 적응기간 후 근위축 모델을 만들기 위해 D군과 DH군에 7일간 매일 오전 10시~12시 사이에 Dexamethasone을 복강투여 하였다. 사용한 Dexamethasone의 투여용량은 선행연구를 참고하여 2 mg/kg로 결정하였다 13. 같은 기간 동안 C군에는 vehicle 포함 아무 약물도 투여하지 않았다. 홍삼은 Dexamethasone 투여가 끝난 후로부터 2주간 DH군에 투여하였다. 같은 기간 동안 C군과 D군에는 아무 약물도 투여하지 않았다. 홍삼은 ㈜한국인삼공사에서 제조한 홍삼정 타브렛을 증류수에 희석하여 구강투여하였다. 홍삼정 타브렛은 1정당 500 mg으로 홍삼농축액 비율이 97%였으며, 홍삼정 타브렛의 영양성분구성은 다음과 같다( Table 2). 실험동물의 복용용량은 1마리당 1/3 T qd(166.6 mg/day)였다. 홍삼정 타블렛의 성인 1일 권장 섭취량은 4정(2 g)으로, 60 kg 성인 기준으로 보고 500 g 실험동물의 체중비례 계산량의 10배로 계산하였다.
Table 2
The Components of Hongsam-jeong Tablet (2 g)
|
Ingredients |
per 2 g |
|
Calories |
5 kcal |
|
Total carbohydrate |
1 g |
|
Protein |
0 g |
|
Total fat |
0 g |
|
Sodium |
0 mg |
|
Marker compounds |
Ginsenosides (Rg1+Rb1+Rg3) 8 mg |
3. Body weight 측정
DH군을 기준으로 실험동물의 적응기간 3일 후(adap3), 7일간 완료 후(adap7), Dexametasone투여 4일 후(Dex4), 7일간 완료 후(Dex7), 홍삼투여 4일(H4), 7일(H7), 10일(H10), 12일 후(H12) 총 8회에 걸쳐 체중을 측정하였다. C군과 D군은 DH군 측정일과 같은 날 동시에 체중을 측정하였다.
4. Grip strength test
DH군을 기준으로 실험동물의 적응기간 6일 후(adap6), 7일간 완료 후(adap7), Dexametasone투여 4일 후(Dex4), 7일간 완료 후(Dex7), 홍삼투여 4일(H4), 7일(H7), 10일(H10), 12일 후(H12) 총 8회에 걸쳐 grip strength를 측정하였다. C군과 D군은 DH군 측정일과 같은 날 동시에 grip strength를 측정하였다.
측정은 Bioseb Grip Strength Test(BIO-GS3, BIOScience and Experimental Biology. Florida. USA)를 이용하였으며, 실험동물의 양측 전지로 실험도구의 Bar를 잡고 체중부하를 견딜 때 측정되는 수치를 기록하였다.
5. 혈액분석
각 Group은 실험이 종료되는 날 ether 마취 후 심장천자로 혈액을 채취하였다. 채취한 혈액은 생화학 검사와 complete blood count(CBC)검사 모두 (주)삼광의료재단에 의뢰하였다. 검사항목은 Myoglobin, Albumin, Total Protein, CK(Creatine kinase), AST(aspartate aminotransferase), ALT(alanine aminotransferase), BUN(blood urea nitrogen), Creatinine, WBC(white blood cell counts), RBC(red blood cell count), Hemoglobin(Hb), Hematocrit(Hct), Platelet, MCV(mean corpuscular volume), MCH(mean corpuscular hemoglobin)이었다.
6. 근육조직 적출
각 Group은 실험이 종료되는 날 안락사 시킨 후 전경골근을 적출하여 액화질소에 급속 냉동하여 -80 ℃에서 보관하였다. 우측 전경골근은 면역조직화학염색법을 통해 근섬유 단면적을 측정하는데 사용되었고, 좌측 전경골근은 Western blot을 통해 MyHC을 정량 측정하는데 사용하였다.
7. 면역조직화학염색법
선행연구의 프로토콜에 따라 실험하였다 14. 실험에 사용할 근육조직은 조직동결절편기를 사용하여 14 μm 두께로 박절한 후 슬라이드로 조직 표본을 제작하였다. 1차 항체는 laminin(L9393, Sigma-aldrich, USA), Type I(BA-F8, DSHB, USA), Type IIa: (SC-71, DSHB, USA), Type IIx(6H1, DSHB, USA), Type IIb(BF-F3, DSHB, USA)를 사용하였으며, MyHC 관련 Antibody는 2차 항체(P 0260, Dako, Denmark)에 반응시킨 후 diamino-benzidine(DAB)에 반응시켰으며, 1차 항체를 Anti-laminin를 사용한 경우 2차 항체(BA-1000, Vector stain, USA)에 반응 시킨 뒤, AB Solution(PK-6105, Vector stain, USA)에 추가로 반응 시켰다. 제작된 조직표본들은 DP Manager Software를 사용하여 촬영하였고, 촬영한 사진들은 Image J software(NIH, Bethesda, MD)를 사용하여 각 근섬유형별로 계수 및 평균 면적을 계산하였다.
8. Western blot
면역조직화학염색법과 마찬가지로 선행연구의 프로토콜을 참고하여 실험하였다 14. 촬영된 Western blot Band 이미지들은 Image J software(NIH, Bethesda, MD)를 사용하여 Band의 밀도를 측정하였다. 1차 항체는 Type I:(ab11083, abcam, UK), Type IIa:(SC-71, DSHB, USA), Type IIx(6H1, DSHB, USA), Type IIb(BF-F3, DSHB, USA)와 GAPDH(FL-335, Santa-cruz, USA)를 사용하였다. 2차 항체는 anti-rabbit(AP 307, Millipore, USA)와 anti-mouse(AP 124P, Milipre, USA)를 사용하였다.
9. 통계처리
본 논문에 제시된 자료들은 Spss 23.0 Ver 통계 프로그램(IBM Corp, Armonk, NY, USA)을 이용하여 분석하였다. 수치는 평균±표준편차(Mean±SD)로 표시하였으며 정규성 검정(Kolmogorov-Smirnov test)을 시행하여 정규분포를 따르지 않는 경우(p<0.05) 비모수 검정법인 Kruskal Wallis 검정을 시행하였으며 이후 Mann-Whitney U Test로 사후검정하였다. 정규분포를 따르는 경우 분산의 동질성 검정을 거쳐 등분산일 경우 LSD 방법을, 등분산이 아닐 경우 Dunnett의 T3 방법으로 사후검정하였다. 반복측정된 값의 경우 repeated measured ANOVA, 1회성 측정값인 경우 One way ANOVA를 시행하였다. p<0.05 일 때를 통계적으로 유의하다고 판정하였다.
III. 실험결과
본 연구는 노인질환의 대표라 할 수 있는 근감소증에 대해 홍삼이 효과적인 약물이 될 수 있는지를 실험해보고자 한 것으로, 노인성 근위축과 유사한 근위축을 일으키는 것으로 알려진 Dexamethasone을 투약하여 근감소 모델을 만들었다. 이후 홍삼을 투여하였으며 body weight, grip strength를 반복 측정하고 투여 후 혈액검사와 평균 근섬유 굵기 및 Type에 따른 근섬유 굵기, MyHC transition의 변화를 관찰하여 다음과 같은 결과를 얻었다.
1. Body weight 변화 비교
Body weight를 One way ANOVA로 분석한 결과는 다음과 같다( Table 3). 같은 측정일에서 D군이 C군에 대하여 유의한 차이가 있는 경우*, DH군이 C군과 비교하여 유의한 차이가 있는 경우 † 표시로 나타내었다. 실험동물의 적응기간동안 세 군 사이의 유의한 체중 차이는 없었다. Dexamethasone 투여 4일 후(Dex4)부터 실험종료일 까지 D군은 C군과 비교하여 유의한 차이로 체중평균이 적게 나타났다. DH군도 D군과 마찬가지로 Dexamethasone 투여 4일 후(Dex4)부터 실험 종료일까지 C군에 대하여 유의한 차이로 체중이 적었다. DH군과 D군 사이의 유의한 차이는 관찰되지 않았다.
Table 3
Body Weight Change (Mean±SD)
|
adap3 |
adap7 |
Dex4 |
Dex7 |
H4 |
H7 |
H10 |
H12 |
|
C (n=10) |
405.6±18.8 |
418.8±20.2 |
422.4±18.7 |
431.1±21.8 |
437.1±21.3 |
441.7±22.6 |
451.3±25.3 |
455.0±24.0 |
|
D (n=10) |
413.8±22.1 |
426.5±22.2 |
383.4±21.7* |
356.0±18.2* |
372.5±22.7* |
391.6±22.5* |
410.7±23.9* |
421.8±21.5* |
|
DH (n=10) |
403.1±28.5 |
417.0±29.4 |
371.7±26.0†
|
346.4±23.6†
|
359.0±20.0†
|
377.3±20.8†
|
397.2±20.9†
|
406.0±25.3†
|
Repeated measured ANOVA로 분석한 결과 D군은 C군에 비해 유의한 체중의 감소를 보였으며, DH군 또한 C군에 비해 유의하게 체중의 감소를 보였다. 그러나 DH군과 D군 사이의 유의한 차이는 없었다( Fig. 1).
Fig. 1

2. Grip strength 변화 비교
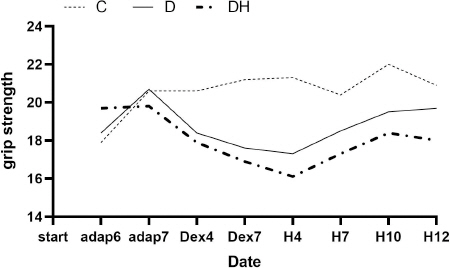
Grip strength를 One way ANOVA로 분석한 결과는 다음과 같다( Table 4). D군에서 실험동물 1마리는 실험도구의 Bar에 매달리려 하지 않아 측정이 불가능하였다(n=9). 같은 측정일에서 D군이 C군에 대하여 유의한 차이가 있는 경우*, DH군이 C군과 비교하여 유의한 차이가 있는 경우 †, DH군이 D군에 비해 유의한 차이가 있는 경우 ‡ 표시로 나타내었다. 적응 6일 후 의 grip strength test 결과는 DH군이 C군과 D군 모두와 비교하여 유의하게 높게 나타났다. 그러나 바로 다음 날 7일간의 적응 완료 후에 측정한 자료에서는 세 군에서 유의한 차이가 나타나지 않았다. Dexamethasone 투여 4일 후(Dex4)부터 홍삼 투여 10일 후(H10)까지 D군은 C군에 비해 유의한 차이로 grip strength 측정값이 작게 나타났으며, DH군은 Dexamethasone 투여 4일 후(Dex4)부터 홍삼 투여 12일 후(H12)까지 C군에 비하여 유의한 차이로 grip strength 측정값이 작았다. DH군과 D군 사이의 유의한 차이가 나타난 적은 없었다.
Table 4
Grip Strength Test (Mean±SD)
|
adap6 |
adap7 |
Dex4 |
Dex7 |
H4 |
H7 |
H10 |
H12 |
|
C (n=10) |
17.9±0.92 |
20.6±2.69 |
20.6±1.19 |
21.2±1.64 |
21.3±3.01 |
20.4±1.83 |
22.0±2.49 |
20.9±2.29 |
|
D (n=9) |
18.4±0.82 |
20.7±1.94 |
18.4±1.80*
|
17.6±1.53*
|
17.3±2.70*
|
18.5±1.65*
|
19.5±2.20*
|
19.7±2.28 |
|
DH (n=10) |
19.7±1.30†‡
|
19.8±1.83 |
17.9±1.52†
|
16.9±1.31†
|
16.1±1.07†
|
17.3±1.15†
|
18.4±1.82†
|
18.0±1.95†
|
Repeated measured ANOVA로 분석한 결과 D군은 C군에 비해 유의한 grip strength 변화를 보였으며, DH군 또한 C군에 비해 유의하게 grip strength의 변화를 보였다. 그러나 DH군과 D군 사이의 유의한 차이는 없었다( Fig. 2).
Fig. 2
3. 혈액검사 결과 비교
혈액검사 각 항목에서 각 군의 결과는 다음과 같다( Table 5). D군이 C군에 대하여 유의한 차이가 있는 경우*, DH군이 C군에 대하여 유이한 차이가 있는 경우 †, DH군이 D군에 대한 유의한 차이를 보인 경우 ‡ 표시를 하였다. D군이나 DH군에서 유의한 차이를 보인 항목은 Albumin, CK(Creatine kinase), AST(GOT), ALT(GPT), BUN, WBC, Hemoglobin(Hb), Platelet이었다.
Table 5
Group Comparison of Blood Chemistry and CBC (Mean±SD)
|
C |
D |
DH |
|
Myoglobin |
21.0±0.00 |
21.0±0.00 |
21.0±0.00 |
|
Albumin |
4.3±0.10 |
4.1±0.17*
|
4.3±0.07‡
|
|
Total protein |
6.1±0.22 |
6.0±0.26 |
6.1±0.256 |
|
CK (Creatine kinase) |
750.7±303.85 |
466.1±152.41 |
453.9±170.64†
|
|
AST (GOT) |
123.4±24.61 |
91.6±10.38*
|
88.4±7.37†
|
|
ALT (GPT) |
55.8±6.09 |
46.8±2.66*
|
44.3±5.91†
|
|
BUN |
19.1±1.73 |
17.8±2.31 |
16.1±3.01†
|
|
Creatinine |
0.4±0.04 |
0.4±0.054 |
0.4±0.06 |
|
WBC |
7.3±1.89 |
5.0±1.90*
|
5.3±2.74†
|
|
RBC |
8.8±0.25 |
8.5±0.41 |
8.8±0.33 |
|
Hemoglobin (Hb) |
15.5±0.36 |
14.9±0.50*
|
15.6±0.71‡
|
|
Hematocrit (Hct) |
53.3±1.46 |
52.3±1.85 |
54.2±2.80 |
|
Platelet |
982.8±63.00 |
946.3±95.16 |
1110.7±140.55†‡
|
|
MCV |
60.5±1.14 |
61.4±2.35 |
61.7±1.40 |
|
MCH |
17.6±0.50 |
17.6±0.53 |
17.7±0.31 |
|
MCHC |
29.1±0.66 |
28.6±0.61 |
28.7±0.63 |
혈중 Albumin과 Hemoglobin은 D군에서 C군에 비해 유의한 차이를 보이며 감소하였고, DH군에서 D군에 비해 유의한 차이를 보이며 증가하였다.
CK와 BUN은 D군과 DH군 모두 C군에 비하여 감소하였으나 DH군에서만 유의한 차이를 보였다.
AST와 ALT, WBC는 D군과 DH군 모두 C군에 비하여 유의한 감소를 나타내었으며 D군과 DH군 사이의 유의한 차이는 보이지 않았다.
Platelet은 DH군에서 C군과 D군에 비하여 유의한 차이로 증가하였다.
4. 면역조직화학염색법을 통한 근섬유 단면적 비교
C, D, DH group의 전경골근에서 각 근섬유 type별로 면역조직화학염색 후 관찰하였다.
1) 전경골근의 대표 근섬유 사진
Fig. 3은 면역조직화학염색법으로 처리한 전경골근 단면의 대표 사진을 각 근섬유 type별로 나타낸 것이다. 각 군당 백서 4마리씩 선택하여 백서 1마리당 1장씩 4배율로 관찰한 사진을 이용하여 각 근섬유 수를 계수하였다. 각 군 당 백서 1마리를 선택하여 20배율로 관찰한 사진을 백서 1마리 당 5장 씩으로 각 근섬유 평균면적을 계산하여 군 간 비교하였다.
Fig. 3
Representative images of MyHC immunohistochemistry in TA muscle sections. 
2) 근섬유 type별 계수 비교
전경골근의 한 단면적에서의 Type I, Type IIa, Type IIx, Type IIb의 수는 다음과 같다( Table 6). 각 근섬유 수는 평균±표준편차로 나타내었다.
Table 6
Cross Sectional Count of Muscle Fibers Type in Group C, D and DH
|
Type I |
Type IIa |
Type IIx |
Type IIb |
|
C (n=4) |
936.50±129.42 |
3821.00±763.70 |
270.25±36.48 |
1284.75±222.11 |
|
D (n=4) |
937.25±344.99 |
3563.50±1186.34 |
246.75±56.94 |
1964.75±670.43 |
|
DH (n=4) |
1108.50±444.09 |
3254.00±801.40 |
286.50±75.95 |
1378.00±107.58 |
Type I의 수는 DH군>D군>C군 순서로 나타났으며, 각 군간 유의한 차이는 없었다.
Type IIa의 수는 C군>D군>DH군의 순서였으며, 각 군간 유의한 차이는 없었다.
Type IIx의 수는 DH군>C군>D군의 순서였으며 각 군간 유의한 차이를 나타내지 않았다.
Type IIb의 수는 D군>DH군>C군의 순서였으며, 각 군간 유의한 차이를 나타내지는 않았다.
4) 근섬유 type별 면적 비교
전경골근의 단면에서 관찰한 각 근섬유별 평균 면적은 다음과 같다( Table 7). C군의 평균면적을 100으로 하여 D군과 DH군의 상대적인 면적을 수치화 하였으며, 그 숫자를 평균±표준편차로 나타내었다.
Table 7
Ratio of Cross Sectional Area of Muscle Fibers Type in group C, D and DH
|
Type I |
Type IIa |
Type IIx |
Type IIb |
|
C (n=5) |
100.00±40.8 |
100.00±51.6 |
100.00±34.6 |
100.00±80.7 |
|
D (n=5) |
150.48±45.8* |
182.45±79.5* |
83.65±25.4* |
120.35±107.6* |
|
DH (n=5) |
121.45±43.5†‡
|
131.88±35.7†‡
|
110.90±56.0†‡
|
228.11±117.8†‡
|
Type I의 근섬유면적 평균 순위는 C군 128.66, D군 249.16, DH군 186.34, 이었으며, 그룹 간 근섬유면적의 평균순위는 통계적으로 유의한 차이가 있었다(X2=81.072, p=0). 사후분석을 실시한 결과 typeI 근섬유 면적은 D군>DH군>C군 순으로D군과 C군, DH군과 C군, DH군과 D군 사이 모두 유의한 차이를 나타내었다.
Type IIa의 근섬유 평균순위는 C군 274.98, D군 641.38, DH군 476.69이었으며 평균순위는 통계적으로 유의한 차이가 있었다((X2=308.857, p=0). 사후분석을 실시한 결과 typeIIx 근섬유 면적은 D군>DH군>C군 순으로D군과 C군, DH군과 C군, DH군과 D군 사이 모두 유의한 차이를 나타내었다.
Type IIx의 근섬유면적 평균순위는 C군 398.59, D군 298.62, DH군 483.46이었으며 그룹 간 근섬유 면적의 평균순위는 통계적으로 의한 차이가 있었다(X2=59.484, p=0. 사후분석을 실시한 결과 typeIIx 근섬유 면적은 DH군>C군>D군 순이었으며 D군과 C군, DH군과 C군, DH군과 D군 사이 모두 유의한 차이를 나타내었다.
Type IIb의 근섬유면적 평균순위는 C군 192.22, D군 218.08, DH군 351.88이었으며 그룹 간 근섬유 면적의 평균순위는 통계적으로 의한 차이가 있었다(X 2=88.208, p=0). 사후분석을 실시한 결과 type IIb 근섬유 면적은 DH군>D군>C군 순이었으며 D군과 C군, DH군과 C군, DH군과 D군 사이 모두 유의한 차이를 나타내었다( Fig. 4).
Fig. 4
Cross sectional area of muscle fibers in the TA muscle in group C, D and DH. 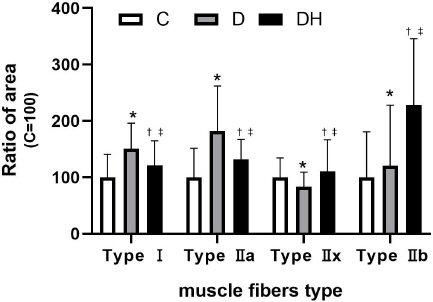
5. Western blot을 통한 MyHC 정량 측정 비교
각 군의 전경골근의 MyHC transition을 Western blot을 사용하여 측정한 결과는 다음과 같았다.
1) MyHC Band image
Fig. 5(A)는 C, D, DH군에서 MyHC 발현을 Western blot을 사용하여 촬영한 대표 band image이다.
2) MyHC 정량 비교
각 군의 MyHC 발현을 비교한 결과는 Table 8과 Fig. 5(B)에 나타내었다. 각 군당 백서 2마리씩 선택하여 Type I과 Type IIa는 총 4 sample, Type IIx와 Type IIb는 총 6 sample로 비교하였다. MHC/ GAPDH 수치를 평균±표준편차로 나타내었다.
Table 8
Protein Expression Level of MyHC Isoforms in Group C, D and DH
|
Type I (n=4) |
Type IIa (n=4) |
Type IIx (n=6) |
Type IIb (n=6) |
|
C |
96.53±42.3 |
58.13±24.8 |
48.47±12.4 |
39.49±21.6 |
|
D |
79.09±8.6 |
50.20±6.5 |
60.53±27.6 |
24.28±9.9 |
|
DH |
74.64±15.4 |
61.56±26.4 |
88.47±27.6† |
56.07±39.9 |
Fig. 5
Transition of MyHC isoforms expression in the TA muscle.
(A) representative western blotting of MyHC isoforms in group C, D and DH, (B) protein expression level of MyHC isoforms in group C, D and DH

Type I의 발현은 C군>D군>DH군 순서로 많이 나타났으며, 각 군간 유의한 차이는 없었다.
Type IIa의 발현의 정도는 DH군>C군>D군의 순서였으며, 각 군간 유의한 차이는 없었다.
Type IIx의 발현의 정도는 DH군>D군>C군의 순서였다. DH군과 C군 사이는 유의한 차이를 나타내었으며 D군과 C군 사이에 유의한 차이는 없었다.
Type IIb의 발현의 정도는 DH군>C군>D군의 순서였으며, 각 군간 유의한 차이를 나타내지는 않았다.
IV. 고 찰
본 연구는 노화된 골격근에서 근위축 이후 홍삼을 복용하는 것이 효과적인지를 알아보기 위해, rat에 Dexamethasone을 주입하여 7일간 노화와 유사한 근위축을 유발하였으며, 이후 회복기 2주 간 홍삼을 투여하였다. 임상적 측면에서 골격근량과 근력을 측정하였으며, 근섬유수준에서의 변화를 살펴보기 위해 근섬유 type별 변화를 면역조직화학염색법과 western blot을 통해 알아보았다. 골격근량의 변화는 body weight를, 근력의 변화는 grip strenght를 반복측정 하는 것으로 관찰하였다. 그 결과 홍삼투여는 근섬유수준에서 근육두께(면적) 변화에 유의한 차이를 나타내었으며 다른 지표에서는 유의한 차이를 나타내지 않았다.
Dexamethasone은 fast-twitch glycolytic muscle fibers 의 신경-근 스냅스의 변화를 일으켜 근원섬유의 조직 병변을 일으키는 것으로 알려져 있으며, 근원섬유 아형 별로 그 정도의 차이를 나타내어 MyHC transition에 순서가 발생한다 13. 골격근량은 body weight가 적응기간동안 세 군 모두 유의한 차이가 없었다. 그러나 Dexamethasone 투여시에 D군, DH군 모두에서 C군에 비해 유의하게 감소하여 근감소증모델이 잘 만들어 졌음을 확인할 수 있었다. 이후 회복기동안의 홍삼 투여는 홍삼 비투여군(D)에 비하여 골격근량 회복에 유의한 효과가 없었다.
근기능은 grip strength가 적응기간 완료후(adap7) 세 군 사이의 유의한 차이가 없다가 Dexamethasone 투여시에 D군, DH군 모두에서 C군에 비해 유의하게 감소하여 근감소증 모델이 잘 만들어 졌음을 확인할 수 있었다. 적응 6일 후의 측정값(adap6)에서 DH군에서 유의한 차이가 있었던 것은 실험동물의 측정 방식에 대한 적응과정에서 일시적으로 나타난 것으로 보인다. Body weight의 경우 Dexamethasone 투여기간 동안 계속 감소하다가 Dexamethasone 투여를 중지하자마자 다시 증가하는 추세를 보였는데, grip strength의 경우 Dexamethasone 투여 중지 4일 이후부터 다시 증가하는 추세를 보여 근기능 회복은 골격근량 회복에 비해 좀 더 천천히 이루어지는 것으로 생각된다. 근기능 회복기 동안의 홍삼투여는 홍삼 비투여군에 비하여 근기능 회복에 유의한 효과가 없었다.
골격근량과 근기능 회복에 홍삼이 유의한 효과를 보이지 않았던 점에 대해서는 사용된 홍삼제품의 유효성을 생각해 볼 수 있다. 사용된 홍삼은 시판되는 건강기능식품으로, 확인 가능한 유효성분이 표지성분인 ginsenosides Rg1, Rb1, Rg3로 일부 성분뿐이었다. 과거 시중에서 판매되는 백삼엑기스와 홍삼엑기스를 성분 분석하여 비교한 연구에서, 백삼추출물에서 더 많은 총 사포닌이 함유되어있었으며 홍삼특유 ginsenoside의 양이 백삼과 홍삼에 비슷하게 함유되어있다는 결과가 나왔다 15. 또한 시판되는 홍삼파우치 제품을 대상으로 성분 분석을 한 연구에서는 총 ginsenoside 함량은 5.5~185.7 mg/100 mL, Rg3는 1.6~46.3 mg/100 mL, Rg2는 미검출~22.0 mg/100 mL, Rg1는 미검출~4.4 mg/100 mL로 편차가 매우 큰 것으로 나타났다. 기타 Rb1, Rb2, Rc, Rd, Re, Rf, Rh1, Rh2에서도 제품별 편차는 컸으며, 이화학적 특성은 당함량 226.6~3,102.9 mg/100 mL, 당도 1.4~9.5oBx, 탁도 82.2~100.0%, pH 4.1~5.0의 범위를 나타내었다. 약 50%에서 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rg1이 미검출되었을 정도로 시판홍삼제품의 품질과 효능의 표준화는 미흡한 상태이다 16. 과거 홍삼을 투여하여 백서의 grip strength가 증가하였다는 실험에서도 홍삼 전 성분이 포함된 제품이 아닌 Rg1 일부성분을 4주간 투여하였었던 점 11을 참고하였을 때, 다른 홍삼 제품을 투여하거나 건강기능식품이 아닌 의약품으로 분류되는 홍삼을 추출하여 투여하였을 때 다른 결과가 나올 수도 있을 것이라 생각한다. 또한 본 실험에서의 홍삼 투여기간은 2주로, 4주 이상 장기간 복용하며 그 효과를 관찰하였다면 다른 결과가 나올 수도 있을 것이라 생각한다.
홍삼은 본초 분류에서 補氣藥에 속한다. 補陽藥 중 補肝腎 强筋骨 기능이 있는 것으로 분류 된 약재와 처방을 이용한 연구가 추가적으로 이루어져 추후 임상적으로 근감소증에 효과적인 약을 확인할 수 있기를 기대한다.
과거에 시행되었던 Dexamethasone 치료중인 rat에 홍삼을 투여하였을 때의 혈액성분 변화연구에서, Dexamethasone 투여군(1 mg/rat)에서 나타난 AST, ALT, creatinin의 유의한 상승을 홍삼 투여시 유의한 차이로 감소시켜 홍삼의 간보호 효과와 신장회복효능에 대해 보고 한 바 있었다. 같은 연구에서 저용량 Dexamethasone(0.5 mg/rat) 에서는 Total Protein 과 albumin이 Dexamethasone 치료시 감소되었다가 홍삼 투여시 회복되는 양상을 추가로 나타내었다 17. 본 실험에서의 혈액검사결과를 분석함에 있어서, D군에서 AST, ALT가 C군에 비해 유의하게 낮았던 점은 과거 연구와 부합되지 않으며, 혈액검사 결과가 근육기능과 직접적인 연관이 있다고 보기는 어렵다고 판단하였다. 이외의 혈액검사 항목들에 대해서도 약물용량 및 기간에 따라 다양한 결과가 도출되는 것으로 판단되며 따라서 추가적인 연구가 필요할 것으로 보인다. 이번 실험에서의 혈액 검사 결과를 통해, Dexamethasone 및 홍삼이 실험기간동안 백서에 생명을 위협할 정도의 위해나 부작용이 없었음을 추측할 수 있었다. 근섬유수준에서 살펴본 결과로는, 면역조직화학염색법을 통한 근섬유 type별 근섬유 수와 면적, western blot을 통한 정량 비교 결과가 모두 일치하지는 않았다. Dexamethasone으로 인한 Fast to Slow로 MyHC transition이 유발될 때, Type IIb→IIx→IIa→I으로 순차적으로 진행되며 transition을 유발하는 요인이 사라지면 이전 상태로 transition 되는 가역적인 특징이 있다는 과거 보고가 있었다 14. 이번 실험에서 유의한 차이를 보인 근섬유별 면적 비교를 토대로 생각해 보자면, Type I의 경우 D군이 다른 군에 비해 유의한 차이로 면적이 넓은 것은 Fast to Slow로 MyHC transition이 D군에서 가장 많이 진행되었기 때문으로 생각해 볼 수 있다. Type IIb의 면적이 DH군에서 가장 넓게 나온 점은 역순으로 진행되는 회복단계에서 Slow to Fast transition이 Type I→IIa→IIx→IIb의 순서로 가장 많이 진행되었다고 추측할 수 있다. 이러한 결과를 토대로, 근섬유 수준에서는 홍삼이 근감소증에 효과적일 수 있다는 추측이 가능하지만, 추가적인 연구가 더욱 필요할 것으로 보인다. 본 연구는 근감소증에 대한 임상적 지표와 근섬유 수준에서의 지표를 평가하여 2주간 약물의 효과를 실험하였다. 임상적지표에 있어 골격근량 뿐 만 아니라 근기능에 대한 평가도 함께 진행하였으며 근섬유 수준에서도 근섬유의 개수와 western blot 정량측정 이외에 면적을 동시에 측정하여 다각도로 MyHC transition을 관찰하였다. 이는 기존의 근감소증 연구 11와 측정 항목의 차이가 있고, dexamethasone의 근위축 효과와 근감소증과의 관련성을 MyHC transition과 연관지어 살펴본 점에서 특징이 있다 18. 약물 투여기간이 2주로 기존연구들에 비해 짧았으며 유효성 평가를 위한 약물을 선택하는 데에 있어 전문한의약재 혹은 强筋骨 약재 등 다양한 선택을 하지 않은 점이 한계이다.
향후 근감소증에 유효한 약물 연구에, 약물투여기간을 장기화 하고 다양한 약재 선택을 통하여 효과적인 약물이 밝혀지기를 기대한다.
V. 결 론
근감소증에 홍삼이 효과적인지를 알아보기 위해 Dexamethasone 유도 근위축 백서 모델을 만든 뒤 2주 간 시판홍삼을 투여하여 다음과 같은 결론을 얻었다.
골격근량은 Dexamethasone 투여 시 유의하게 감소되고 투여를 중지하면 바로 회복되는 양상을 나타낸다. 근력은 Dexamethasone 투여 시 유의하게 감소되고 투여를 중지하면 회복되는 양상을 보이나 골격근량보다는 느린 반응을 보인다. 골격근량과 근력 회복에 시판홍삼은 유의한 효과를 나타내지 않았다. 근섬유 단계에서 근섬유 수의 변화에 시판 홍삼은 유의한 효과가 없었으나 근섬유 굵기(면적) 변화에 유의한 효과를 나타내었다. Dexamethasone과 홍삼은 혈액성분분석 결과 상 심각한 위해나 부작용이 없었다. 추후 근감소증에 대한 약물 연구에 이번 실험은 도움이 될 것으로 기대한다.
감사의 글
본 연구는 경희대학교한방병원 한의약임상시험센터를 통해 ㈜다이찌산쿄의 연구비 지원을 받아 수행된 연구임.
참고문헌
1. Rosenberg IH. Sarcopenia:Origins and Clinical Relevance. J Nutr 1997:127(5):990–1.   2. Kong SA, Sung SC, Kim HS. Efficacy in methods of sarcopenia diagnosis index. KINESIOLOGY 2016:18(4):15–23.
3. Chang S, Lin P. Systematic literature review and Meta-Analysis of the association of sarcopenia with mortality. Worldviews on Evidence-Based Nursing 2016:13(2):153–62.   4. The Textbook Compilation Committee of Korean Herbology. Korean Herbology Seoul: Younglimsa: 2010. p. 573.
5. Lee BJ, Heo H, Oh SH, Lew JH. Comparison study of Korean and Chinese ginsengs on the regulation of lymphocyte proliferation and cytokine production. J Ginseng Res 2008:32(3):250–6.  6. Lee CH, Kim JH. A review on the medical potentials of ginseng and ginsenosides on cardiovascular diseases. J Ginseng Res 2014:38(3):161–6.    7. Lee SY, Rhee DK. Effects of ginseng on stress-related depression, anxiety, and the hypothalamicepituitaryeadrenal axis. J Ginseng Res 2017:41(4):589–94.    8. Choi J, Kim TH, Choi TY, Lee MS. Ginseng for Health Care:A Systematic Review of Randomized Controlled Trials in Korean Literature. PLoS ONE 2013:8(4):e59978.    9. Nam KR. The Comparative Understanding between Red Ginseng and White Ginsengs, Processed Ginsengs (panax ginseng C. A. Meyer). J Ginseng Res 2005:29(1):1–18.  10. Ryu GH. Present Status of Red Ginseng Products and Its Manufacturing Process. Food Industry and Nutrition 2003:8(2):38–42.
11. Jeong HJ, So HK, Jo AY, Kim HB, Lee SJ, Bae GU, et al. Ginsenoside Rg1 augments oxidative metabolism and anabolic response of skeletal muscle in mice. J Ginseng Res 2018:1–7.  12. Cabral de Oliveira AC, Perez AC, Merino G, Prieto JG, Alvarez AI. Protective effects of Panax ginseng on muscle injury and inflammation after eccentric exercise. Comparative Biochemistry and Physiology Part C 2001:130(3):369–77.   13. Seene T, Kaasik P, Pehme A, Alev K, Riso EM. The effect of glucocorticoids on the myosin heavy chain isoforms'turnover in skeletal muscle. Journal of Steroid Biochemistry & Molecular Biology 2003:86(2):201–6.   14. Kim YM. Dexamethasone-induced skeletal muscle atrophy in Young rats and aged rats Comparison to Myosin heavy chain Transition. Department of Gerontology Graduate School of East-West Medical Science Kyung Hee University 2018:
15. Ko SK, Lee CR, Choi YE, Im BO, Sung JH, Yoon KR. Analysis of Ginsenosides of White and Red Ginseng Concentrates. Korean journal of food science and technology 2003:35(3):536–9.
16. Choi JE, Han JS, Kang SJ, Kim KH, Kim KH, Hong SY. Saponin Contents and Physicochemical Properties of Red Ginseng Extract Pouch Products Collected from Ginseng Markets in Korea. J Korean Soc Food Sci Nutr 2010:39(11):1660–5.   17. Lin JH, Wu LS, Tsai KT, Leu SP, Jeang YF, Hsieh MT. Effect of Ginseng on the Blood Chemistry Profile of Dexamethasone-treated Male Rats. American Journal of Chinese Medicine 1995:23(2):167–72.   18. Choi YH. Effects of Schisandrae Fructus Supplementation on Apoptosis and Inflammatory Response in Gastrocnemius Muscle of Dexamethasone -Induced Muscle Atrophy Mice. Herb. Formula Sci 2017:25(3):363–74.
|
|
















